用于单细胞筛选的多级化微流控芯片及其制备方法
本发明涉及微流控芯片领域,具体涉及用于单细胞筛选的多级化微流控芯片及其制备方法。
背景技术:
1、细胞分选是把一种细胞从多细胞样品中分离出来的过程,常见的细胞分选方法包括抗体标记分离、免疫密度离心分离、免疫磁珠分离和流式细胞分离技术。其中,流式细胞分离技术因其具有通量高、设备成熟等特点,在领域内被广泛应用。但是流式细胞分离技术在使用时仍存在如下缺点:其需要昂贵的仪器装置及复杂的操作流程。
2、微流控芯片技术(microfluidics)是把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成到一块微米尺度的芯片上,可自动完成分析全过程。微流控芯片具有液体流动可控、消耗试样和试剂极少、分析速度呈十倍上百倍地提高等特点,在生物、化学、医学等领域的巨大潜力,已经发展成为一个生物、化学、医学、流体、电子、材料、机械等学科交叉的崭新研究领域。目前,微流控技术已经应用到细胞分选中,微流控领域的细胞分选方法集中在群细胞分选,而单细胞水平的监测、操控和分析平台对生物医学领域的发展至关重要,其包括细胞识别、分类、分离、培养、配对以及细胞间相互作用等;单细胞捕获和释放是单细胞水平研究的前提和重要组成部分,但是目前现有技术中尚无成熟的单细胞捕获及可寻址释放技术。传统的流体力及介电泳力操控细胞/微粒技术一般仅可实现初步的群细胞低精度分离,而不能在大量样本中准确挑选出少量目标细胞或微粒。
技术实现思路
1、本发明意在提供用于单细胞筛选的多级化微流控芯片及其制备方法,以解决现有技术中无法在低成本的微流控芯片上进行细胞/微粒捕获及少量目标可控释放与收集的问题。
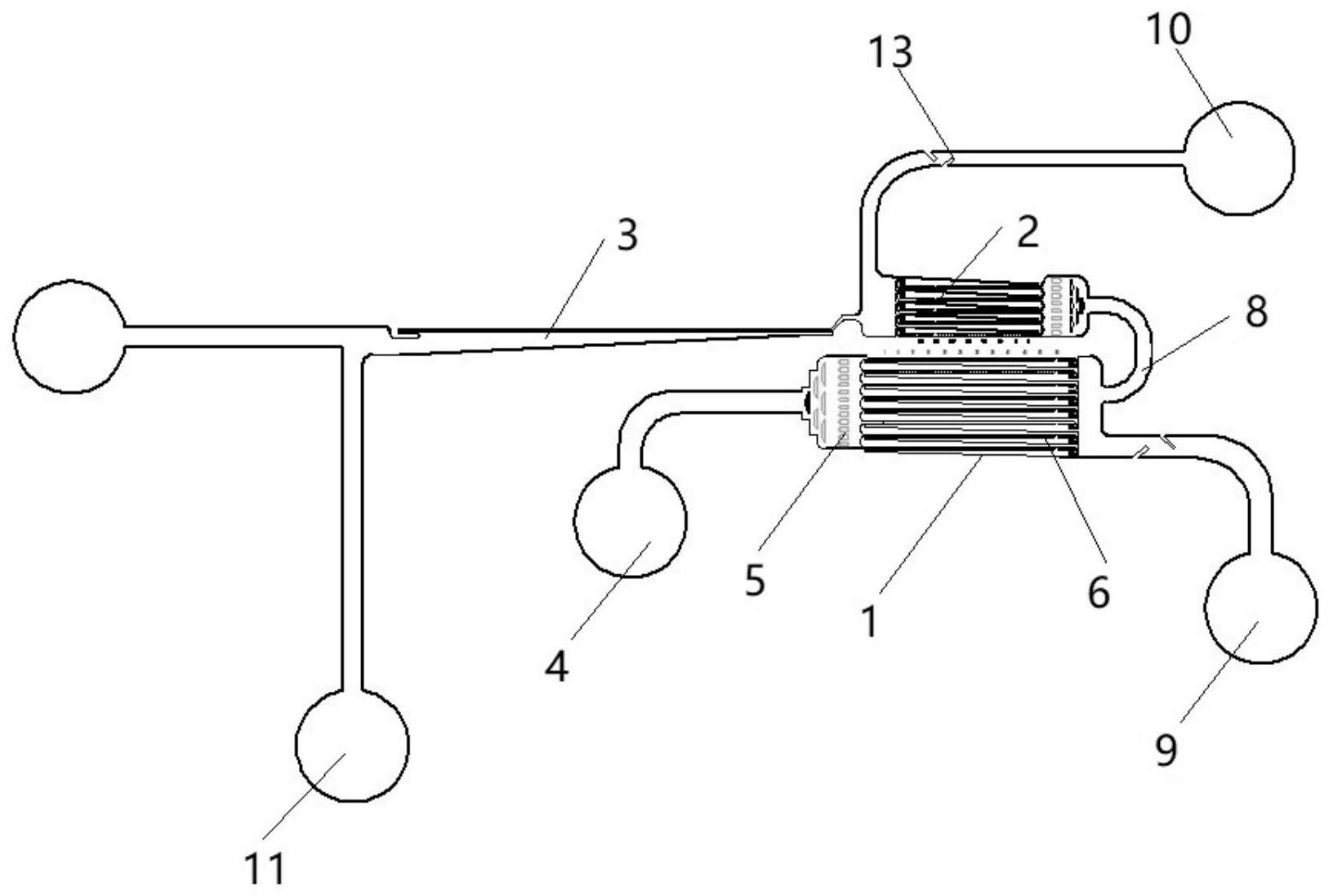
2、为达到上述目的,本发明采用如下技术方案:用于单细胞筛选的多级化微流控芯片,包括pdms结构层和与之键合的配套电极,pdms结构层内设置有用于进行细胞捕获和分选的微通道结构,微通道结构包括依次连通的多级分选单元,分选单元均包括分选腔,分选腔包括分散区、捕获区和出样区。
3、另一方面,本技术方案还提供用于单细胞筛选的多级化微流控芯片的制备方法,包括如下步骤:
4、步骤一、绘制微通道结构;
5、步骤二、设计电极阵列;
6、步骤三、利用软光刻工艺制备给予pdms的微通道结构;
7、步骤四、采用溅射-光刻法制备金电极;
8、步骤五、将电极阵列与微通道结构进行表面等离子处理并键合封装。
9、本方案的原理及优点是:实际应用时,本技术方案中,针对现有技术中难以进行细胞/微粒捕获及少量目标物可控精准释放的技术问题,对微流控芯片的结构进行了改进和升级,旨在实现单细胞分选。首先,通过设置多级捕获和分选单元,通过微陷阱阵列实现细胞/微粒的捕获,而后通过配套电极的加电实现不同分选单元内捕获的细胞/微粒的精准筛选,细胞/微粒在上一级分选单元分选后,会进入下一级分选单元进行再次的捕获和分选,通过多级、多通道的结构设计,可以实现样品的逐级富集、纯化和目标样品筛选收集的过程。通过实验验证,采用本方案的芯片可以实现可视化、可寻址式单细胞/微粒精准释放,并且能够极大的提高捕获率(即样品利用率),15微米颗粒的捕获率可达到90%以上。且本方案的多级分选可以在同一微流控芯片上实现从大量样本中分拣筛选出其中的目标细胞/微粒,具有成本低、便于操作、样本捕获率高、利用率高的优势。
10、优选的,作为一种改进,分散区内设置有若干分流微柱,若干分流微柱交错设置。
11、本技术方案中,分散区用于样品的分散,通过交错设置的分流微柱,可以对样品进入后的流向进行分散干预,使得样品被均匀的分散至各个样品通道内,提高捕获、分选的效率。
12、优选的,作为一种改进,捕获区内设置有若干样品通道,样品通道内均阵列设置有若干捕获腔室,且样品通道靠近出样区的一端均设置有挡板。
13、本技术方案中,样品通道为样品捕获/分选的流道,通过阵列、条带设置的捕获腔室,能够实现高通量的样品捕获、纯化。在研发初期,还是存在利用流体动力和微柱结构捕获单微粒/细胞的捕获率较低的问题,通过在样品通道内设置挡板,可以改变通道流阻,从而实现微粒/细胞高效捕获。
14、优选的,作为一种改进,出样区与样品通道连通,出样区连通有出样通道,出样通道内均固定有倾斜设置的截留板。
15、本技术方案中,截留板起到截留的作用,减缓出样。
16、优选的,作为一种改进,配套电极为金属电极阵列结构,且配套电极包括与多级分选单元分别对应的多级电极阵列单元。
17、本技术方案中,通过将配套电极设置为与多级分选单元分别对应的阵列电极结构,能够实现不同分选区(不同级别分选区)的精准加电控制分选,进而实现可视化的单细胞/微粒的精准释放。
18、优选的,作为一种改进,步骤三中,利用软光刻工艺制备微通道结构的具体造作为:在硅片上旋涂20μm-200μm的光刻胶,用热板软烘后曝光处理,随后放入显影液中显影,再用热板硬烘,制作出通道模板,用pdms脱模,得到微通道结构层。
19、本技术方案中,采用软光刻技术进行微通道结构的构建,技术成熟且制备而成的微通道结构能够满足本技术方案的细胞分选、富集需求。
20、优选的,作为一种改进,步骤四中,制备金电极的具体方法为:在石英玻璃上用磁控溅射仪溅射一层5-10nm的金属层,再溅射一层厚度100nm-300nm的金,并旋涂一层光刻胶,用热板进行软烘后曝光处理,随后放入显影液中显影,放入刻蚀液中刻蚀,最后用除胶液除胶,得到金电极。
21、本技术方案中,采用磁控溅射的方式结制备金电极,操作简单方便。
22、优选的,作为一种改进,步骤五中,等离子体处理时间为10-15s,键合的温度为100-150℃。
23、本技术方案中,等离子体处理的时间主要影响后期的键合效果,等离子体处理时间过长会导致键合过于紧密,样品液难以进入结构;等离子处理时间过短会导致键合不紧,容易出现漏液问题。
24、优选的,作为一种改进,对键合后的芯片进行真空脱气处理,真空脱气处理的时间>30min。
25、本技术方案中,将芯片的各个出入口均浸没在缓冲溶液中,在-1.5至-1.2psi的真空箱内脱气30min以上,能够使通道内完全填充液体,避免气泡对微流体流动的影响
技术特征:
1.用于单细胞筛选的多级化微流控芯片,其特征在于:包括pdms结构层和与之键合的配套电极,所述pdms结构层内设置有用于进行细胞捕获和分选的微通道结构,所述微通道结构包括依次连通的多级分选单元,分选单元均包括分选腔,分选腔包括分散区、捕获区和出样区。
2.根据权利要求1所述的用于单细胞筛选的多级化微流控芯片,其特征在于:所述分散区内设置有若干分流微柱,若干分流微柱交错设置。
3.根据权利要求2所述的用于单细胞筛选的多级化微流控芯片及其制备方法,其特征在于:所述捕获区内设置有若干样品通道,样品通道内均阵列设置有若干捕获腔室,且样品通道靠近出样区的一端均设置有挡板。
4.根据权利要求3所述的用于单细胞筛选的多级化微流控芯片,其特征在于:所述出样区与样品通道连通,出样区连通有出样通道,出样通道内均固定有倾斜设置的截留板。
5.根据权利要求4所述的用于单细胞筛选的多级化微流控芯片,其特征在于:所述配套电极为金属电极阵列结构,且配套电极包括与多级分选单元分别对应的多级电极阵列单元。
6.根据权利要求1-5任一所述的用于单细胞筛选的多级化微流控芯片的制备方法,其特征在于,包括如下步骤:
7.根据权利要求6所述的用于单细胞筛选的多级化微流控芯片的制备方法,其特征在于:步骤三中,利用软光刻工艺制备微通道结构的具体造作为:在硅片上旋涂20μm-200μm的光刻胶,用热板软烘后曝光处理,随后放入显影液中显影,再用热板硬烘,制作出通道模板,用pdms脱模,得到微通道结构层。
8.根据权利要求7所述的用于单细胞筛选的多级化微流控芯片的制备方法,其特征在于:步骤四中,制备金电极的具体方法为:在石英玻璃上用磁控溅射仪溅射一层5-10nm的金属层,再溅射一层厚度100nm-300nm的金,并旋涂一层光刻胶,用热板进行软烘后曝光处理,随后放入显影液中显影,放入刻蚀液中刻蚀,最后用除胶液除胶,得到金电极。
9.根据权利要求8所述的用于单细胞筛选的多级化微流控芯片的制备方法,其特征在于:步骤五中,等离子体处理时间为10-15s,键合的温度为100-150℃。
10.根据权利要求9所述的用于单细胞筛选的多级化微流控芯片的制备方法,其特征在于:对键合后的芯片进行真空脱气处理,真空脱气处理的时间>30min。
技术总结
本发明涉及微流控芯片领域,公开了用于单细胞筛选的多级化微流控芯片及其制备方法,该微流控芯片包括PDMS结构层和与之键合的配套电极,PDMS结构层内设置有用于进行细胞捕获和分选的微通道结构,微通道结构包括依次连通的多级分选单元,分选单元均包括分选腔,分选腔包括分散区、捕获区和出样区。本发明设计了微陷阱阵列用于细胞/微粒捕获,捕获区的挡板结构可以大大提高样品利用率,配套的电极阵列用于负向介电泳力释放,多出口、多流路的芯片通道结构可以实现样品逐级富集、纯化、目标样品收集及回收。
技术研发人员:胡宁,刘星,郑嘉辉,杨晨,杨军,曹文玥,郑小林
受保护的技术使用者:重庆大学
技术研发日:
技术公布日:2024/1/12
- 还没有人留言评论。精彩留言会获得点赞!