一种在烯丙酯化合物芳香环上引入二氟亚甲基的方法
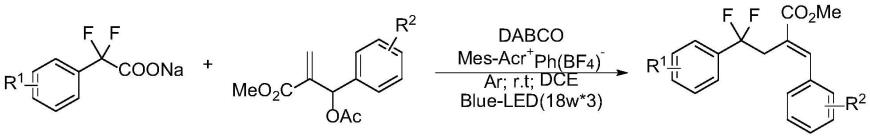
1.本发明属于有机化学合成技术领域,尤其涉及一种在烯丙酯化合物芳香环上引入二氟亚甲基的方法。
背景技术:
2.氟化合物在药物、农业化学和材料科学领域发挥着重要作用,因为将氟原子引入分子中可以明显提高相应化学分子的代谢稳定性、溶解度和亲脂性。二氟亚甲基单元的独特性质在药物化学中引起了特别关注,当在芳香环上引入二氟亚甲基可以显著提高母体化合物的代谢稳定性和口服生物利用度。它被认为是氧原子和羰基的生物异构体,可以改变相邻原子的pka值,增强了分子中的偶极矩和构象变化。
3.通常,二氟亚甲基结构部分是通过用二乙胺基三氟化硫或脱氧氟转化羰基来实现的。但这种方法具有一定的局限性,例如重要的官能团不相容性以及使用昂贵和有毒的氟化试剂,严重限制了其广泛的合成应用。为了解决这些问题,一种替代方法是将官能化的cf2基团直接引入由昂贵的过渡金属(钯或镍)催化的有机分子中。
4.因此,从环境和经济的角度,利用无毒,廉价,易于获得且对环境相对无害的原料以开发节能高效的绿色合成方法是极具有吸引力的。
技术实现要素:
5.为克服现有技术的缺点和不足,本发明的首要目的在于提供一种在烯丙酯化合物芳香环上引入二氟亚甲基的方法。
6.本发明是这样实现的,一种为烯丙酯化合物修饰二氟亚甲基的方法,该方法包括以下步骤:
7.(1)将烯丙酯化合物、二氟基化试剂、光氧化还原催化剂、添加剂依次加入反应溶剂中,在惰性气体氛围下、蓝光照射和室温条件下搅拌反应18h,得到反应液;其中,所述烯丙酯化合物的化学结构式如下式所示:
[0008][0009]
所述二氟基化试剂的化学结构式如下式所示:
[0010][0011]
(2)除去所述反应液中的反应溶剂,再通过薄层层析法纯化,得到二氟亚甲基丙烯基类化合物;
[0012]
所述二氟亚甲基丙烯基类化合物的化学结构式如下式(ⅰ)所示:
[0013][0014]
其中,r1选自氢基、甲氧基、氰基、叔丁基、三氟甲基、氟基、氯基、溴基、稠合芳基、杂芳基中的任意一种;
[0015]
r2选自氢基、甲氧基、氰基、硝基、叔丁基、氟基、溴基、氯基、二茂铁基、三甲基硅烷乙炔基、稠合芳基、杂芳基、环烷基、直链烷基中的任意一种。
[0016]
具体来说,所述烯丙酯化合物选自2-乙酰氧基(苯基)甲基丙烯酸甲酯、2-乙酰氧基(4-氟苯)甲基丙烯酸甲酯、2-乙酰氧基(3-氟苯)甲基丙烯酸甲酯、2-乙酰氧基(2-氟苯)甲基丙烯酸甲酯、2-乙酰氧基(4-氯苯)甲基丙烯酸甲酯、2-乙酰氧基(3-氯苯)甲基丙烯酸甲酯、2-乙酰氧基(2-氯苯)甲基丙烯酸甲酯、2-乙酰氧基(4-溴苯)甲基丙烯酸甲酯、2-乙酰氧基(3-溴苯)甲基丙烯酸甲酯、2-乙酰氧基(4-硝基苯)甲基丙烯酸甲酯、2-乙酰氧基(4-氰基苯)甲基丙烯酸甲酯、2-乙酰氧基(4-甲氧基苯)甲基丙烯酸甲酯、2-乙酰氧基(4-叔丁基苯)甲基丙烯酸甲酯、2-乙酰氧基(4-甲酰基苯基)甲基丙烯酸甲酯、2-乙酰氧基(萘-1-基)甲基丙烯酸甲酯、2-乙酰氧基(呋喃-2-基)甲基丙烯酸甲酯、2-乙酰氧基(苯基)甲基丙烯酸乙酯、2-氰基-1-苯基烯丙基乙酸酯、2-乙酰氧基-(2,4-二氯苯基)甲基丙烯酸薄荷醇酯以及2-乙酰氧基-(2,4-二氯苯基)甲基丙烯酸胆固醇酯中的任意一种;
[0017]
所述二氟甲基化试剂为氟基苯乙酸钠类化合物,选自2,2-二氟-2-苯乙酸钠、2,2-二氟-2-(4-氟苯基)乙酸钠、2,2-二氟-2-(4-氯苯基)乙酸钠、2,2-二氟-2-(4-溴苯基)乙酸钠、2,2-二氟-2-(3-溴苯基)乙酸钠、2,2-二氟-2-(2-溴苯基)乙酸钠、2,2-二氟-2-(4-硝基苯基)乙酸钠、2,2-二氟-2-(4-氰基苯基)乙酸钠、2,2-二氟-2-(4-甲氧基苯基)乙酸钠、2,2-二氟-2-(4-叔丁基苯基)乙酸钠、2,2-二氟-2-(4-(三氟甲基)苯基)乙酸钠、2-([1,1'-联苯]-4-基)-2,2-二氟乙酸钠、2,2-二氟-2-(萘-2-基)乙酸钠、2,2-二氟-2-(噻吩-2-基)乙酸钠以及2,2-二氟-2-(2,4,6-三甲基苯基)乙酸钠中的任意一种。
[0018]
优选地,所述杂芳基为如呋喃基或噻吩基;所述环烷基为环己基。
[0019]
优选地,在步骤(1)中,所述烯丙酯、二氟甲基化试剂、3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐、添加剂和反应溶剂的摩尔体积比为(0.24~0.48)mmol:(0.2~0.4)mmol:(0.01~0.02)mmol:(0.04~0.08)mmol:(1.5~3)ml。
[0020]
优选地,在步骤(1)中,惰性气体为氩气;在步骤(2)中,所述纯化的展开剂体系为石油醚/乙酸乙酯=9:1。
[0021]
优选地,在步骤(1)中,所述反应溶剂选自甲苯、二甲苯、二氯甲烷、乙腈、1,2-二氯乙烷、四氢呋喃、1,4二氧六环以及异丙醇中的任意一种。
[0022]
优选地,在步骤(1)中,所述添加剂选自三苯基膦、三(4-甲氧基苯基)膦、4-二甲氨基吡啶、三乙胺以及三乙烯二胺中的任意一种。
[0023]
优选地,在步骤(1)中,所述光氧化还原催化剂为3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐。
[0024]
本发明克服现有技术的不足,提供一种在烯丙酯化合物芳香环上引入二氟亚甲基的方法,本发明直接使用烯丙酯化合物作原料,选择氟基苯乙酸钠类化合物作为二氟甲基
化试剂,使用三乙烯二胺作为添加剂,无金属的3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐作为光氧化还原催化剂,在该有机光氧还原剂催化下,分别生成对应的二氟亚甲基自由基和烯丙基自由基,从而使反应在温和条件下以环境友好的方式发生,该反应过程为:
[0025][0026]
相比于现有技术的缺点和不足,本发明具有以下有益效果:
[0027]
(1)本发明制备方法中所用的烯丙酯为合成简单、转化率高的morita-baylis-hillman醇类烯丙醇简单酯化原料,适用的底物范围广泛,如烯丙酯上可以是各种取代苯基、烷基,具有制备成本低的特点;此外,本发明制备方法步骤简单,具有操作方便、绿色环保、优异的立体选择性、耐受广谱官能团的特点;
[0028]
(2)本发明方法所合成得到的二氟亚甲基丙烯基类化合物是制备相关cf2分子的通用前体,具有潜在的药物活性和生物活性,可为生物学和药学活性分子的合成及应用提供新的途径。
附图说明
[0029]
图1是本发明实施例1中化合物(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振氢谱图;
[0030]
图2是本发明实施例1中化合物(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振碳谱图;
[0031]
图3是本发明实施例1中化合物(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振氟谱图。
具体实施方式
[0032]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0033]
实施例1
[0034]
(1)在10ml史莱克管中,在氩气环境下,先将0.48mmol 2-乙酰氧基(苯基)甲基丙烯酸甲酯、0.4mmol 2,2-二氟-2-苯乙酸钠、0.02mmol 3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐,0.08mmol三乙烯二胺,加入3ml1,2-二氯乙烷,在氩气、室温和54w蓝灯照射下搅拌反应,反应方程式为:
[0035][0036]
(2)tlc监测反应完全后,用真空旋转蒸发器除去溶剂,薄层层析法分离产物,展开剂为石油醚/乙酸乙酯体系(9:1),产物为无色透明液化合物(e)-2-亚苄基-4,4-二氟-4-苯
基丁酸甲酯(化合物1),收率88%。
[0037]
对化合物(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯进行表征,结果如图1~3所示,图1是(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振氢谱;图2是(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振碳谱;图3是(e)-2-亚苄基-4,4-二氟-4-苯基丁酸甲酯的核磁共振氟谱。
[0038]
实施例2
[0039]
(1)在10ml史莱克管中,在氩气环境下,先将0.24mmol 2-乙酰氧基(4-甲酰基苯基)甲基丙烯酸甲酯、0.2mmol 2,2-二氟-2-苯乙酸钠、0.01mmol 3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐,0.08mmol三乙烯二胺,加入1.5ml 1,2-二氯乙烷,在氩气、室温和54w蓝灯照射下搅拌反应,反应方程式为:
[0040][0041]
(2)tlc监测反应完全后,用真空旋转蒸发器除去溶剂,薄层层析法分离产物,展开剂为石油醚/乙酸乙酯体系(5:1),产物为黄色固体(e)-4,4-二氟-2-(4-甲酰基亚苄基)-4-苯基丁酸甲酯,收率92%。
[0042]
实施例3
[0043]
(1)在室温条件下,将薄荷醇加入二氯甲烷溶液中,在0℃条件下加入三乙胺,搅拌0.5h。再将丙烯酰氯的二氯甲烷溶液在0℃滴入上述反应液中,室温下搅拌反应12h得到反应混合物;其中,所述薄荷醇、三乙胺、丙烯酰氯的摩尔比为1:2:1;反应方程式为反应方程式为:
[0044][0045]
(2)将反应混合物加入饱和氯化铵溶液淬灭,乙醚萃取3次,合并有机相,用无水硫酸镁干燥,减压除去溶剂,通过柱硅胶色谱法分离产物,展开剂为石油醚/乙酸乙酯体系(80:1),产物为无色液体丙烯酸薄荷醇酯,收率93%。
[0046]
(3)在室温条件下,将2,4-二氯苯甲醛、丙烯酸薄荷醇酯、三乙烯二胺溶解于四氢呋喃,在室温条件下搅拌1周,得到反应混合物;其中,所述2,4-二氯苯甲醛、丙烯酸薄荷醇酯、三乙烯二胺的摩尔比为1:1.2:0.5;反应方程式为:
[0047][0048]
(4)将反应混合物通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=30/1)纯化残
余物,得到无色液体2-羟基-(2,4-二氯苯基)甲基丙烯酸薄荷醇酯,收率89%。
[0049]
(5)在室温条件下,将2-羟基-(2,4-二氯苯基)甲基丙烯酸薄荷醇酯、乙酸酐、4-二甲氨基吡啶混合,在室温条件下搅拌1h,得到反应混合物;其中所述2-羟基-(2,4-二氯苯基)甲基丙烯酸薄荷醇酯、乙酸酐、4-二甲氨基吡啶的摩尔比为1:2:0.2
[0050][0051]
(6)将反应混合物通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=1/1)纯化残余物,得到白色固体2-乙酰氧基-(2,4-二氯苯基)甲基丙烯酸薄荷醇酯,收率85%。
[0052]
(7)二氟亚甲基丙烯基类化合物的合成
[0053]
在10ml史莱克管中,在氩气环境下,先将0.48mmol 2-乙酰氧基(2,4-二氯苯基)甲基丙烯酸薄荷醇酯、0.4mmol 2,2-二氟-2-苯乙酸钠、0.02mmol 3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐,0.08mmol三乙烯二胺,加入3ml 1,2-二氯乙烷,在氩气、室温和54w蓝灯照射下搅拌反应,反应方程式为:
[0054][0055]
(8)tlc监测反应完全后,用真空旋转蒸发器除去溶剂,薄层层析法分离产物,展开剂为石油醚/乙酸乙酯体系(9:1),产物为无色透明液化合物(e)-2-(2,4-二氯亚苄基)-4,4-二氟-4-苯基丁酸薄荷醇酯,收率90%。
[0056]
实施例4
[0057]
(1)在室温条件下,将双丙酮半乳糖加入二氯甲烷溶液中,在0℃条件下加入三乙胺,搅拌0.5h。再将丙烯酰氯的二氯甲烷溶液在0℃滴入上述反应液中,室温下搅拌反应12h得到反应混合物;其中,所述双丙酮半乳糖、三乙胺、丙烯酰氯的摩尔比为1:2:1;反应方程式为:
[0058][0059]
(2)将反应混合物加入饱和氯化铵溶液淬灭,二氯甲烷萃取3次,合并有机相,用无水硫酸镁干燥,减压除去溶剂,通过柱硅胶色谱法分离产物,展开剂为石油醚/乙酸乙酯体系(80:1),得到白色固体丙烯酸双丙酮半乳糖酯,收率87%。
[0060]
(3)在室温条件下,将2,4-二氯苯甲醛、丙烯酸双丙酮半乳糖酯、三乙烯二胺溶解于四氢呋喃,在室温条件下搅拌1周,得到反应混合物;其中,所述2,4-二氯苯甲醛、丙烯酸双丙酮半乳糖酯、三乙烯二胺的摩尔比为1:1.2:0.5;
[0061][0062]
(4)将反应混合物减压除去溶剂,通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=30/1)纯化残余物,得到白色固体2-羟基-(2,4-二氯苯基)甲基丙烯酸双丙酮半乳糖酯,收率94%。
[0063]
(5)在室温条件下,将2-羟基-(2,4-二氯苯基)甲基丙烯酸双丙酮半乳糖酯、乙酸酐、4-二甲氨基吡啶混合,在室温条件下搅拌1h,得到反应混合物;其中所述2-羟基-(2,4-二氯苯基)甲基丙烯酸双丙酮半乳糖酯、乙酸酐、4-二甲氨基吡啶的摩尔比为1:2:0.2
[0064][0065]
(6)将反应混合物通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=30/1)纯化残余物,得到无色液体2-乙酰氧基-(2,4-二氯苯基)甲基丙烯酸双丙酮半乳糖酯,收率85%。
[0066]
(7)二氟亚甲基丙烯基类化合物的合成
[0067]
在10ml史莱克管中,在氩气环境下,先将0.48mmol 2-乙酰氧基(2,4-二氯苯基)甲基丙烯酸双丙酮半乳糖酯、0.4mmol 2,2-二氟-2-苯乙酸钠、0.02mmol 3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐,0.08mmol三乙烯二胺,加入3ml 1,2-二氯乙烷,在氩气、室温和54w蓝灯照射下搅拌反应,反应方程式为:
[0068][0069]
(8)tlc监测反应完全后,用真空旋转蒸发器除去溶剂,薄层层析法分离产物,展开剂为石油醚/乙酸乙酯体系(9:1),产物为无色透明液化合物(e)-2-(2,4-二氯亚苄基)-4,4-二氟-4-苯基丁酸双丙酮半乳糖酯,收率85%。
[0070]
实施例5
[0071]
(1)在室温条件下,将胆固醇加入二氯甲烷溶液中,在0℃条件下加入三乙胺,搅拌0.5h。再将丙烯酰氯的二氯甲烷溶液在0℃滴入上述反应液中,室温下搅拌反应12h得到反应混合物;其中,所述胆固醇、三乙胺、丙烯酰氯的摩尔比为1:2:1;反应方程式为
[0072][0073]
(2)将反应混合物加入饱和氯化铵溶液淬灭,二氯甲烷萃取3次,合并有机相,用无水硫酸镁干燥,减压除去溶剂,通过柱硅胶色谱法分离产物,展开剂为石油醚/乙酸乙酯体系(80:1),产物为白色固体丙烯酸胆固醇酯,收率61%。
[0074]
(3)在室温条件下,将2,4-二氯苯甲醛、丙烯酸胆固醇酯、三乙烯二胺溶解于四氢呋喃,在室温条件下搅拌1周,得到反应混合物;其中,所述2,4-二氯苯甲醛、丙烯酸胆固醇酯、三乙烯二胺的摩尔比为1:1.2:0.5;
[0075][0076]
(4)将反应混合物减压除去溶剂,通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=30/1)纯化残余物,得到白色固体2-羟基-(2,4-二氯苯基)甲基丙烯酸胆固醇酯,收率58%
[0077]
(5)在室温条件下,将2-羟基-(2,4-二氯苯基)甲基丙烯酸胆固醇酯、乙酸酐、4-二甲氨基吡啶混合,在室温条件下搅拌1h,得到反应混合物;其中所述2-羟基-(2,4-二氯苯基)甲基丙烯酸胆固醇酯、乙酸酐、4-二甲氨基吡啶的摩尔比为1:2:0.2
[0078][0079]
(6)将反应混合物通过柱硅胶色谱法用石油醚和乙酸乙酯(pe/ea=1/1)纯化残余物,得到白色固体2-乙酰氧基-(2,4-二氯苯基)甲基丙烯酸胆固醇酯,收率85%。
[0080]
(7)二氟亚甲基丙烯基类化合物的合成
[0081]
在10ml史莱克管中,在氩气环境下,先将0.48mmol 2-(乙酰氧基-(2,4-二氯苯基)甲基)丙烯酸胆固醇酯、0.4mmol 2,2-二氟-2-苯乙酸钠、0.02mmol 3,6,-二叔丁基-9-均三甲苯基-10-苯基吖啶-10-四氟硼酸盐,0.08mmol三乙烯二胺,加入3ml 1,2-二氯乙烷,在氩气、室温和54w蓝灯照射下搅拌反应,反应方程式为:
[0082][0083]
(8)tlc监测反应完全后,用真空旋转蒸发器除去溶剂,薄层层析法分离产物,展开剂为石油醚/乙酸乙酯体系(9:1),产物为无色透明液化合物(e)-2-(2,4-二氯亚苄基)-4,4-二氟-4-苯基丁酸胆固醇酯,收率90%。
[0084]
实施例6~13
[0085]
该实施例6~13与上述实施例1基本相同,所得产物相同,差别之处在于如下表1所
示:
[0086]
表1实施差异比较
[0087]
编号反应溶剂添加剂产率实施例6甲苯三苯基膦80%实施例7二甲苯三(4-甲氧基苯基)膦82%实施例8二氯甲烷4-二甲氨基吡啶83%实施例9乙腈三乙胺86%实施例101,2-二氯乙烷三乙烯二胺81%实施例11四氢呋喃三苯基膦84%实施例121,4二氧六环三(4-甲氧基苯基)膦86%实施例13异丙醇4-二甲氨基吡啶80%
[0088]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1