血浆替代液及其制备方法与应用与流程
本发明涉及细胞培养液的配制,尤其涉及一种血浆替代液、其制备方法及应用,如,用于间充质干细胞、脐带血干细胞、软骨干细胞、脂肪干细胞等方面的培养。
背景技术:
1、目前市面上流通的间充质干细胞培养液,分为基础培养基+fbs、基础培养基+动物血替、基础培养基+人外周血血替、基础培养基+重组人蛋白类细胞因子、基础培养基+天然或人工合成的非蛋白细胞因子。其中,基础培养基+fbs、基础培养基+动物血替这类添加fbs或动物血替的培养液具有较大的人畜共患传染病感染风险,如dna、rna、朊病毒;同时,外来动物源添加因子会诱导人细胞发生异化,使细胞产生非人类的特异基因表达形式,形成特有的细胞表面分子特征或代谢分泌方式,注入人体后,细胞表面特征会引起人体产生强烈的排异和适应反应。对于基础培养基+人外周血血替,由于人外周血血源基本上来自于成年人、甚至携带潜在病原体的成年人,因此添加人外周血血替的培养液仍然存在很大的人之间共患传染病的传播风险,主要是dna或rna病毒;而且,成年人外周血相对于胎儿脐带血,除了其成分复杂和感染风险大外,还有有效成分含量低、种类少、效应弱的特点,而脐带是为胎儿提供血液的通道,其中含有的血液相对干净很多,有效成分的种类更丰富,效价也更高。对于基础培养基+重组人蛋白类细胞因子培养液,相对于上述三种培养液,具有非常不错的应用前景,主要是因为其不含有任何病毒,而且重组蛋白的种类可以随意选取、效价可以不断改进。但是,这只是理论上的设想,在实际操作中,重组蛋白种类的选取必须建立在对传统的能够刺激细胞生长增殖的任何添加剂中所有成分的充分分析和识别的基础上,特别是蛋白成分,例如需要通过复杂的综合性手段分离、纯化和识别血清或血替蛋白质混合物中的所有蛋白成分,最好是得到有效蛋白因子的一维至四维的结构特征,否则重组表达无效或无关蛋白是一种无意义的资源浪费;因此,这不仅要花费巨大的分析费用,更重要的是,以目前的技术手段,并不能够获得任何所选蛋白质的高维特征,比如蛋白质的糖基化修饰、磷酸化修饰等,甚至并不能获得很多蛋白质的纯品用于一维测序;还有一个更重要的理论限制是,以目前的技术能力,并非任何蛋白都可以放入特定宿主中进行表达,一方面是宿主种类不够多的原因,另一方面是有理由认为任何宿主都不会大量表达分子量过大的、氨基酸排列特异的、非己所需的外源蛋白质,因为这超出了宿主的生物学代谢能力和蛋白表达能力,宿主无法有效地对翻译出的蛋白质一维序列进行必要的三维或四维重现和非蛋白修饰,甚至于一维氨基酸序列都不一定能被完整翻译出来,因为这还与不同宿主有不同的基因表达和调控模式有关;即使某些外源蛋白可以由宿主分泌或表达出来,重组蛋白的提取和复性技术也是一个不小的技术挑战,人工标签的加入会改变蛋白质的三维构象,而且,天然蛋白处在一个自然进化和选择的非蛋白环境中,如血清中的无机盐种类和浓度、非蛋白质有机物种类和浓度等对维持蛋白质的活性非常重要,这往往是重组蛋白所不能拥有的溶液环境。而对于基础培养基+天然或人工合成的非蛋白细胞因子这类培养液,目前还处于设想阶段,其添加液通常是植物、微生物提取液,其中可能含有能够刺激人细胞生长繁殖的蛋白或非蛋白成分,但由于物种跨度较大,这些成分的效果往往不能与动物源成分相提并论,只是作为一种优化或改良试剂加入到人细胞或动物细胞培养实验中,还有一种可能就是化学合成非蛋白有机物如生物碱、杂环化合物或高分子聚合物等,其性能仍需理论探索和大量实验论证。
2、因此,优化天然人源蛋白类添加液的制备技术仍是当前行业发展的主流,比如,选择更有效的血源、降低传染病风险、剔除无效或无关成分、激活和富集有效成分、添加商业成熟的高活性重组蛋白等。
技术实现思路
1、有鉴于此,本发明所要解决的问题在于提供一种用于间充质干细胞培养的血浆替代液制备方法,有效解决了人源血液中传染病感染风险、部分剔除了血浆中的无效蛋白和杂质、激活了有效蛋白的效价和选定了更有效的蛋白类刺激因子。
2、本发明的技术方案如下:
3、一种用于间充质干细胞培养的血浆替代液的制备方法,包括如下步骤:
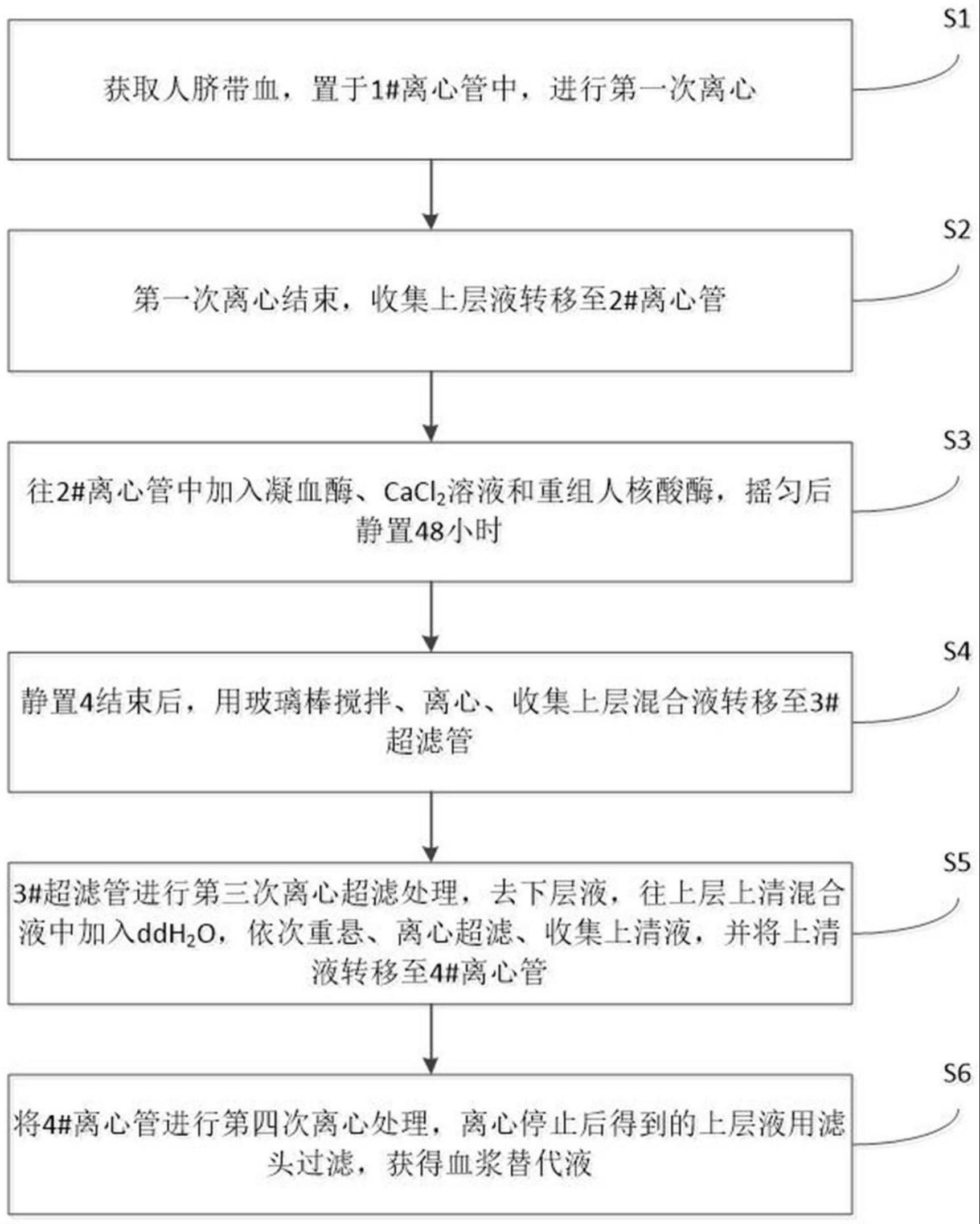
4、获取人脐带血,转移至盛有抗凝剂的第一离心管中,并进行第一次离心处理,离心停止后,收集上层液转移至第二离心管;
5、往第二离心管中加入凝血酶、cac l 2溶液和重组人核酸酶并摇动混匀,得到血浆混合液并进行静置处理;
6、静置结束后对所述血浆混合液进行第二次离心处理,离心停止后,收集第二离心管中的上层混合液转移至第三超滤管;
7、将第三超滤管进行第三次离心超滤处理,离心停止后,摒弃下层液体,并往第三超滤管的上清混合液中加入ddh2o,然后依次进行重悬、离心超滤、收集上清液,并将收集的上清液转移至第四离心管中;
8、将第四离心管进行第四次离心处理,离心停止后得到的上层液用滤头过滤,获得血浆替代液。
9、一实施例,所述血浆替代液制备方法中,所述第一离心、第二次离心及第四次离心处理时,均为4℃下5000~10000g离心5~10mi n。
10、一实施例,所述血浆替代液制备方法中,所述血浆混合液中,凝血酶的终浓度为10~100u/ml,cacl2的终浓度为50~100mm,重组人核酸酶的终浓度为10~100u/ml。
11、一实施例,所述血浆替代液制备方法中,所述血浆混合液静置处理时,还包括如下处理步骤:
12、首先,4℃下静置24小时;随后,转室温下静置24小时;这两个步骤需要交替执行至少3个循环。
13、一实施例,所述血浆替代液制备方法中,所述第三超滤管的孔径为3kd。
14、一实施例,所述血浆替代液制备方法中,往第三超滤管的上清混合液中加入ddh2o,然后依次进行重悬、离心超滤、收集上清液的步骤中,需要执行三个循环,各循环如下:
15、第一次循环,加入ddh2o时,ddh2o的加入量达到第三超滤管刻度体积的2/3,然后依次进行重悬、离心超滤、收集上清液;
16、第二次循环,加入ddh2o时,ddh2o的加入量达到第三超滤管刻度体积的1/2,然后依次进行重悬、离心超滤、收集上清液;
17、第三次循环,加入ddh2o时,ddh2o的加入量达到第三超滤管刻度体积的1/3,然后依次进行重悬、离心超滤、收集上清液。
18、一实施例,所述血浆替代液制备方法中,所述第三超滤管离心处理时,10℃下400~10000g离心1.5h。
19、一实施例,所述血浆替代液制备方法中,所述滤头孔径为0.22μm。
20、上述制备方法制得的血浆替代液,可以添加入细胞培养基础基中,诱导间充质干细胞细胞生长。
21、本发明制备得到的血浆替代液,具有如下优点:
22、1、由于制备过程中添加了凝血酶、cac l 2,增强了血浆中纤维蛋白的凝固,使脐带血浆中的原始无关蛋白浓度大大降低,血清由粘稠变得澄清;同时,钙离子是一种特殊的2价金属离子物质,是某些细胞因子的辅助因子,它可以激活细胞因子使之保持激活状态,增强了细胞因子与干细胞表面受体的结合;
23、2、加入的核酸酶可以有效地降解血浆中游离的dna或rna,降低或消除血液中病毒的含量。通过超滤和冲洗,可以进一步把血液中低于3kd的蛋白质、有机物、无机盐除去;
24、3、滤头过滤,保证了所制血浆替代液的无菌性;
25、4、干细胞培养使用时,相对于含fbs的常规干细胞培养液,得到的干细胞在细胞数目、培养代数、培养周期、细胞活率、制剂安全性、间充质干细胞干性等指标上均达到或优于传统添加fbs的培养效果;血浆替代液培养的干细胞无动物源细胞刺激因子带入,进而避免了诱发肌体产生对动物源生物材料的过敏反应。
- 还没有人留言评论。精彩留言会获得点赞!