重组胰蛋白酶在无动物源成分细胞培养体系的流感疫苗生产的应用的制作方法
本发明属于生物药物领域。具体涉及一种使用重组胰蛋白酶在无血清悬浮适应的mdck细胞中制备流感疫苗的方法。
背景技术:
1、接种流感疫苗是预防流感最有效的手段。当前广泛使用的依赖于鸡胚的流感疫苗生产技术难以有效应对不断提高的流感防控需求.使用动物细胞基质代替鸡胚培养进行流感疫苗生产成为流感疫苗技术创新的重要趋势。近年来,基于不同细胞基质的季节性流感疫苗和大流行流感疫苗在多个国家和地区获批上市,为流感流行和大流行有效防控提供了重要支撑。目前利用动物细胞培养进行流感疫苗生产的体系有含血清和无血清培养等类型,近年来,鉴于动物源性血清的潜在污染风险和成本控制问题以及不断提升的质量监管要求,采用无血清培养成为流感病毒扩增工艺的主要趋势。
2、流感病毒血凝素(ha)与病毒的感染能力有密切关系,ha为三聚体,每条单体前体(ha0)由ha1和ha2通过精氨酸(1个或多个)及二硫键连接而成,只有ha在该精氨酸位点被裂解为ha1和ha2时才具有感染性。在哺乳细胞培养中一般不含有该蛋白水解酶,无法有效将病毒粒非裂解型的ha0变成裂解型的ha1和ha2,因此在基于动物细胞培养的流感疫苗生产体系中,在流感病毒培养阶段需要添加甲苯磺酰胺-苯乙基氯甲基酮(tpck)处理的胰蛋白酶(tpck-trypsin,tt)以提高流感病毒在细胞中的复制能力。经tpck处理的胰蛋白酶,其糜胰蛋白酶活性被抑制,能够专一性地切割蛋白分子中精氨酸和赖氨酸位点,能够增强对流感病毒ha0的裂解能力,然而目前可供应的tt均为动物(猪胰脏)来源。因此,从目前的细胞基质流感疫苗生产工艺来看,尽管可通过使用无血清、无动物源成分的细胞培养基实现细胞培养阶段的无动物源性成分添加,但后续病毒培养过程中使用的动物源性tt在一定程度上增加了可能的外源性物质污染的风险。
3、国际生物制品行业发展的趋势是尽量避免使用动物源性原材料,有效降低生物制品风险。因此,本领域急需开发非动物来源的胰蛋白酶,作为病毒培养和疫苗生产的原料。
技术实现思路
1、本发明的目的是提供一种使用重组胰蛋白酶替代动物源胰蛋白酶来保证在无血清悬浮适应的mdck细胞中制备季节性流感疫苗的过程中不引入动物源成分。
2、本发明第一方面提供一种病毒的培养方法,包括步骤:
3、(1)在培养介质中,提供待感染的细胞;和
4、(2)用病毒感染所述细胞,培养并收集,从而获得扩增的目的病毒收获液;
5、其中,所述培养介质中使用的胰蛋白酶为重组胰蛋白酶。
6、在另一优选例中,所述培养介质包括培养基。
7、在另一优选例中,所述培养介质包括无血清的培养基。
8、在另一优选例中,所述培养基包括无血清的培养基。
9、在另一优选例中,所述培养介质包括不含有动物源成分的培养基。
10、在另一优选例中,所述培养基包括不含有动物源成分的培养基。
11、如本文所用,“培养介质”、“培养基”、和“培养液”可互换使用。
12、在另一优选例中,所述细胞来自动物模型。
13、在另一优选例中,所述细胞来自哺乳动物。
14、在另一优选例中,所述细胞来自人。
15、在另一优选例中,所述细胞来自非人哺乳动物。
16、在另一优选例中,所述细胞来自灵长动物。
17、在另一优选例中,所述细胞来自啮齿动物。
18、在另一优选例中,所述细胞来自食肉目动物。
19、在另一优选例中,所述细胞来自犬形亚目动物。
20、在另一优选例中,所述细胞来自:人、小鼠、大鼠、兔、猴、犬、或其组合。
21、在另一优选例中,所述细胞包括mdck细胞。
22、在另一优选例中,所述细胞为mdck细胞。
23、在另一优选例中,步骤(1)中,所述mdck细胞接种时处于对数生长期。
24、在另一优选例中,步骤(1)中,所述mdck细胞接种密度为1×106-1×107个/ml,较佳地2×106-5×106个/ml。
25、在另一优选例中,所述重组胰蛋白酶在所述培养介质中的终浓度为0.1-100μg/ml,较佳地0.5-10ug/l,更佳地1-5μg/ml。
26、在另一优选例中,步骤(2)中,所述病毒的感染复数(病毒数量:细胞数量)为0.0005-0.2,较佳地0.0008-0.12,更佳地0.001-0.1。
27、在另一优选例中,所述病毒包括流感病毒。
28、在另一优选例中,所述流感病毒选自下组:h1n1、h3n2、乙型yamagata系流感病毒疫苗株,或其组合。
29、在另一优选例中,所述病毒为流感病毒。
30、在另一优选例中,所述病毒为流感病毒,且在步骤(2)中,所述病毒的感染复数为0.0008-0.1,较佳地0.0009-0.01,更佳地0.001-0.002。
31、在另一优选例中,所述病毒包括乙型yamagata系流感病毒疫苗株。
32、在另一优选例中,所述病毒为乙型yamagata系流感病毒疫苗株。
33、在另一优选例中,所述病毒为乙型yamagata系流感病毒疫苗株,且在步骤(2)中,所述病毒的感染复数为0.008-0.5,较佳地0.009-0.03,更佳地0.01-0.02。
34、在另一优选例中,所述病毒收获液为一次或多次收获液。
35、本发明第二方面提供一种病毒疫苗的制备方法,包括步骤:
36、(1)在培养介质中,提供待感染的细胞;
37、(2)用病毒感染所述细胞,培养并收集,从而获得扩增的目的病毒收获液;和
38、(3)将步骤(2)所获得病毒纯化后配制成疫苗;
39、其中,所述培养介质中使用的胰蛋白酶为重组胰蛋白酶。
40、在另一优选例中,所述方法还包括步骤:
41、(4)将步骤(2)所得病毒纯化、灭活后配制成疫苗。
42、在另一优选例中,所述方法包括步骤:
43、(1)提供目的病毒收获液,其中,所述目的病毒收获液为用本发明第一方面所述方法获得的目的病毒收获液;和
44、(2)将所述目的病毒纯化后配制成疫苗。
45、在另一优选例中,所述方法还包括步骤:
46、(3)将步骤(1)提供的目的病毒纯化、灭活后配制成疫苗。
47、在另一优选例中,所述培养介质包括培养基。
48、在另一优选例中,所述培养介质包括无血清的培养基。
49、在另一优选例中,所述培养基包括无血清的培养基。
50、在另一优选例中,所述培养介质包括不含有动物源成分的培养基。
51、在另一优选例中,所述培养基包括不含有动物源成分的培养基。
52、如本文所用,“培养介质”、“培养基”、和“培养液”可互换使用。
53、在另一优选例中,所述细胞来自动物模型。
54、在另一优选例中,所述细胞来自哺乳动物。
55、在另一优选例中,所述细胞来自人。
56、在另一优选例中,所述细胞来自非人哺乳动物。
57、在另一优选例中,所述细胞来自灵长动物。
58、在另一优选例中,所述细胞来自啮齿动物。
59、在另一优选例中,所述细胞来自食肉目动物。
60、在另一优选例中,所述细胞来自犬形亚目动物。
61、在另一优选例中,所述细胞来自:人、小鼠、大鼠、兔、猴、犬、或其组合。
62、在另一优选例中,所述细胞包括mdck细胞。
63、在另一优选例中,所述细胞为mdck细胞。
64、在另一优选例中,步骤(1)中,所述mdck细胞接种时处于对数生长期。
65、在另一优选例中,步骤(1)中,所述mdck细胞接种密度为1×106-1×107个/ml,较佳地2×106-5×106个/ml。
66、在另一优选例中,所述重组胰蛋白酶在所述培养介质中的终浓度为0.1-100μg/ml,较佳地0.5-10ug/l,更佳地1-5μg/ml。
67、在另一优选例中,步骤(2)中,所述病毒的感染复数(病毒数量:细胞数量)为0.0005-0.2,较佳地0.0008-0.12,更佳地0.001-0.1。
68、在另一优选例中,所述病毒包括流感病毒。
69、在另一优选例中,所述流感病毒选自下组:h1n1、h3n2、乙型yamagata系流感病毒疫苗株,或其组合。
70、在另一优选例中,所述病毒为流感病毒。
71、在另一优选例中,所述病毒为流感病毒,且在步骤(2)中,所述病毒的感染复数为0.0008-0.1,较佳地0.0009-0.01,更佳地0.001-0.002。
72、在另一优选例中,所述病毒包括乙型yamagata系流感病毒疫苗株。
73、在另一优选例中,所述病毒为乙型yamagata系流感病毒疫苗株。
74、在另一优选例中,所述病毒为乙型yamagata系流感病毒疫苗株,且在步骤(2)中,所述病毒的感染复数为0.008-0.5,较佳地0.009-0.03,更佳地0.01-0.02。
75、在另一优选例中,所述病毒收获液为一次或多次收获液。
76、在另一优选例中,本发明的方法和/或用途为体外的和/或非治疗性的。
77、本发明第三方面提供一种重组胰蛋白酶的用途,所述重组胰蛋白酶用于制备用于病毒培养的培养介质。
78、在另一优选例中,所述培养介质包括培养基。
79、在另一优选例中,所述培养介质包括无血清的培养基。
80、在另一优选例中,所述培养基包括无血清的培养基。
81、在另一优选例中,所述培养介质包括不含有动物源成分的培养基。
82、在另一优选例中,所述培养基包括不含有动物源成分的培养基。
83、如本文所用,“培养介质”、“培养基”、和“培养液”可互换使用。
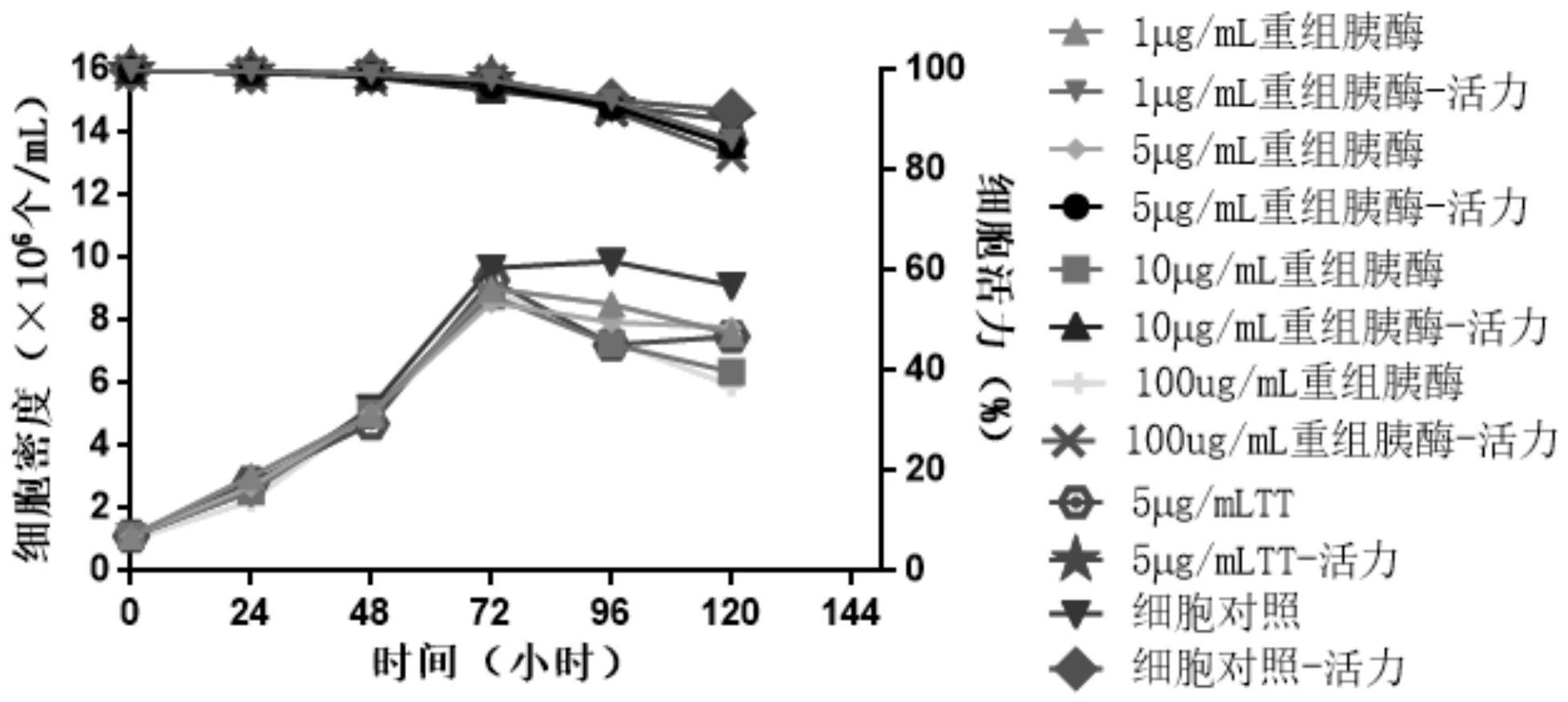
84、在一实施方式中,所述重组胰蛋白酶在优选浓度下对细胞生长无显著影响。
85、在一实施方式中,所述优选浓度包括终浓度。
86、在一实施方式中,所述优选浓度包括0.1-100μg/ml,较佳地0.5-10ug/l,更佳地1-5μg/ml。
87、在一实施方式中,所述重组胰蛋白酶具有优秀的增强病毒扩增的能力。
88、在一实施方式中,所述病毒包括流感病毒。
89、在另一优选例中,所述流感病毒包括季节性流感病毒。
90、在另一优选例中,所述流感病毒包括流感病毒的疫苗株。
91、在另一优选例中,所述季节性流感病毒包括:甲型、乙型,或其组合。
92、在另一优选例中,所述季节性流感病毒包括:h1n1、h3n2、乙型victoria系、乙型yamagata系,或其组合。
93、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!