4-氧代-4H-1-苯并吡喃衍生物的制作方法
本技术涉及4-氧代-4h-1-苯并吡喃衍生物、其制备方法、含有该衍生物的药物组合物、以及其在治疗疾病中的用途。
背景技术:
1、磷脂酰肌醇3-激酶(phosphoinositide 3-kinase,pi3ks)途径是人类癌症中最常被激活的信号通路之一,几乎介导50%的恶性肿瘤的发生。pi3k信号参与过敏性接触性皮炎、类风湿性关节炎、骨关节炎、炎症性肠病、慢性阻塞性肺疾病、银屑病、多发性硬化症、哮喘、糖尿病并发症相关疾病、心血管系统炎症并发症如急性冠状动脉综合征等多种疾病状态。
2、pi3k是一种胞内脂质磷酸激酶,催化肌醇第3位的磷酸化。pi3k是由一个催化亚基p110和一个调节亚基p85构成的异二聚体,具有sh2结构域(src homology 2domain)。通过sh2结构域,pi3k可与其它蛋白的磷酸化酪氨酸残基结合,从而被募集到质膜,使其催化亚基靠近质膜内小叶的磷脂酰肌醇。在膜脂代谢过程中,pi3k催化磷脂酰肌醇4,5-二磷酸(phosphatidylinositol 4,5-bisphosphate,pip2)的肌醇环3’-oh磷酸化生成磷脂酰肌醇3,4,5-三磷酸(phosphatidylinositol 3,4,5-trisphosphate,pip3)。这些与膜结合的pi3k为多种信号转导蛋白提供了锚定位点,进而介导多种下游信号通路,例如活化akt/pkb、mtor激酶等下游通路。
3、根据pi3k的结构特点和底物分子可将其分为ⅰ型、ⅱ型、ⅲ型3类。ⅰ型分为ia型和ib型,ia型由受体酪氨酸激活,根据催化亚基p110的不同又可分为pi3kα、pi3kβ和pi3kδ3个亚型;ib型即为pi3kγ亚型。ia型pi3k与肿瘤的发生发展密切相关,其中编译pi3kα的基因pik3ca是肿瘤中最常见的突变,这种功能获得性突变通常影响p110α的两个不同结构域,激酶结构域和螺旋结构域,其中突变热点分别影响h1047和e542/e545密码子。pik3ca突变后在异常激活pi3kα的同时,还能抑制抑癌基因pten的表达,因此,pi3kα成为抗癌药物研发中极为重要的靶点。
4、目前,已有许多pi3k抑制剂批准上市或进入临床研究。泛pi3k抑制剂,如buparlisib、pictilisb(gdc-0941)、copanlisib等,泛pi3k抑制剂可以作用于所有i型的pi3k亚型,因此副作用与毒性较大,使得它们的临床进展缓慢。选择性作用于某个pi3k亚型的抑制剂具有更小的毒副作用,已有部分选择性pi3k抑制剂获批上市。alpelisib是fda批准的第一个pi3kα抑制剂用于乳腺癌治疗。虽然该药被归类为pi3kα特异性药物,但治疗窗口有限,大部分患者需要中断剂量和/或减少剂量,并且毒副作用大,主要包括高胰岛素血症、高血糖、胃肠道毒性以及皮疹。其主要原因是pi3kα介导肌肉、肝脏和脂肪细胞中胰岛素驱动的葡萄糖摄取。通过抑制pi3kα,阻断肌肉和脂肪细胞对葡萄糖的摄取,刺激肝糖原分解,损害胰岛素信号传导,导致胰岛素抵抗并诱发高血糖。因此,诱导高胰岛素血症和高血糖可能会阻止使用足够高的剂量来完全抑制肿瘤中的pi3k信号传导。因此,降低副作用,对pi3k抑制剂的开发与癌症治疗具有重要意义。
5、在具有pi3kα突变的癌症环境中,克服在全身性pi3kα抑制后代偿产生胰岛素和/或葡萄糖毒副作用的一种方法是开发针对突变pi3kα的选择性抑制剂。这将为药物给药创造一个更高的安全窗口,以选择性地抑制癌细胞中突变pi3kα的病理信号,而不影响宿主组织中控制全身代谢的野生型pi3kα,从而限制毒性并允许更高剂量和对药物靶标的完全抑制。
6、目前pi3kα抑制剂对野生型和突变型pi3kα的抑制活性几乎等价。由于pi3kα突变位置远离活性位点,突变选择性抑制剂一直难以捉摸。因此,靶向已知突变(例如,h1047r)附近的第二个外周结合口袋的抑制剂可以提供选择性抑制pi3kα的途径。因此,靶向pi3kα突变的外周结合口袋可能反过来为药物开发提供有价值的治疗靶点。
7、发明详述
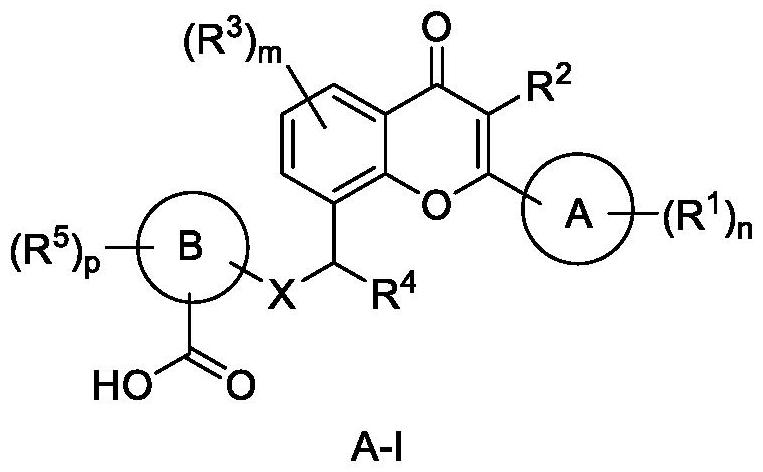
8、一方面,本技术涉及式(a-i)化合物、其立体异构体或其药学上可接受的盐,
9、
10、其中,
11、环a选自5~10元芳基或含有1~5个各自独立地选自n、o或s原子的5~10元杂芳基;
12、r1各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)、-n(c1-6烷基)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的4~8元杂环基;
13、r2选自氢、卤素、c1-6烷基或c1-6卤代烷基;
14、r3各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
15、r4选自c1-6烷基;
16、x选自nr6、o或s;
17、环b选自c3-c10环烷基、5~10元芳基、含有1~5个各自独立地选自n、o或s原子的5~10元杂环烷基、或含有1~5个各自独立地选自n、o或s原子的5~10元杂芳基;
18、r5各自独立地选自卤素、羟基、氰基、硝基、c1-6烷基、c1-6烷氧基、c1-6卤代烷基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
19、r6选自氢、c1-6烷基、卤代c1-6烷基、羟基c1-6烷基或氨基c1-6烷基;
20、n选自0~5;
21、m选自0~3;
22、p选自0~4;
23、所述式(a-i)化合物、其立体异构体或其药学上可接受的盐不包括其立体异构体或其药学上可接受的盐。
24、另一方面,本技术涉及式(a-ii)化合物、其立体异构体或其药学上可接受的盐,
25、
26、其中,
27、环a选自5~10元芳基或含有1~5个各自独立地选自n、o或s原子的5~10元杂芳基;
28、r1各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)、-n(c1-6烷基)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的4~8元杂环基;
29、r2选自氢、卤素、c1-6烷基或c1-6卤代烷基;
30、r3各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
31、r4选自c1-6烷基;
32、x1、x2、x3或x4分别独立地选自ch或n,并且x1、x2、x3或x4中的至少一个选自ch;
33、r5各自独立地选自卤素、羟基、氰基、硝基、c1-6烷基、c1-6烷氧基、c1-6卤代烷基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
34、n选自0~5;
35、m选自0~3;
36、p选自0~4;
37、所述式(a-ii)化合物、其立体异构体或其药学上可接受的盐不包括其立体异构体或其药学上可接受的盐。
38、另一方面,本技术涉及式(i)化合物、其立体异构体或其药学上可接受的盐,
39、
40、其中,
41、环a选自5~10元芳基或含有1~5个各自独立地选自n、o或s原子的5~10元杂芳基;
42、r1各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)、-n(c1-6烷基)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的4~8元杂环基;
43、r2选自氢、卤素、c1-6烷基或c1-6卤代烷基;
44、r3各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基、c1-6烷氧基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
45、r4选自c1-6烷基;
46、r5各自独立地选自卤素、羟基、氰基、硝基、c1-6烷基、c1-6烷氧基、c1-6卤代烷基、-nh2、-nh(c1-6烷基)或-n(c1-6烷基)2;
47、n选自0~5;
48、m选自0~3;
49、p选自0~4;
50、所述式(i)化合物、其立体异构体或其药学上可接受的盐不包括其立体异构体或其药学上可接受的盐。
51、在一些实施方案中,环a选自5~10元芳基或含有2~5个各自独立地选自n、o或s原子的5~10元杂芳基。
52、在一些实施方案中,环a选自5~8元芳基或含有2~5个各自独立地选自n、o或s原子的5~8元杂芳基。
53、在一些实施方案中,环a选自苯基或含有2~5个各自独立地选自n的5~8元杂芳基。
54、在一些实施方案中,环a选自苯基或含有2~3个各自独立地选自n的5~8元杂芳基。
55、在一些实施方案中,环a选自苯基或5~6元杂芳基,所述杂芳基含有1个或2个选自n、o或s的杂原子。
56、在一些实施方案中,环a选自苯基或6元杂芳基,所述杂芳基含有1个或2个选自n、o或s的杂原子。
57、在一些实施方案中,环a选自苯基或含有2个选自n原子的6元杂芳基。
58、在一些实施方案中,环a选自苯基、嘧啶基、哒嗪基或吡嗪基。
59、在一些实施方案中,环a选自苯基、
60、在一些实施方案中,环a选自苯基。
61、在一些实施方案中,r1各自独立地选自卤素、羟基、氰基、c1-4烷基、c1-4卤代烷基、c1-4烷氧基、-nh2、-nh(c1-4烷基)、-n(c1-4烷基)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的4~8元杂环基。
62、在一些实施方案中,任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的4~8元杂环基。
63、在一些实施方案中,r1各自独立地选自卤素、羟基、氰基、c1-4烷基、c1-4卤代烷基、c1-4烷氧基、-n(c1-4烷基)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的5~6元杂环基。
64、在一些实施方案中,任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~3个各自独立地选自n、o或s原子的5~6元杂环基。
65、在一些实施方案中,任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~2个选自o原子的5~6元杂环基。
66、在一些实施方案中,r1各自独立地选自f、cl、br、i、羟基、氰基、甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、-och3、-och2ch3、-och2ch2ch3、-och(ch3)2、-cf3、-ch2cf3、-n(ch3)2、-n(ch2ch3)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个含有1~2个选自o原子的5~6元杂环基。
67、在一些实施方案中,r1各自独立地选自f、cl、羟基、氰基、甲基、乙基、正丙基、-och3、-cf3、-n(ch3)2、或任意两个相邻的r1和与它们连接的碳原子一起形成一个四氢呋喃基、四氢吡喃基或1,3-二氧戊烷基。
68、在一些实施方案中,n选自0、1、2、3、4或5。
69、在一些实施方案中,n选自0、1或2。
70、在一些实施方案中,基团选自
71、
72、在一些实施方案中,r2选自氢或c1-6烷基。
73、在一些实施方案中,r2选自氢或c1-4烷基。
74、在一些实施方案中,r2选自氢。
75、在一些实施方案中,r3各自独立地选自卤素、羟基、氰基、c1-6烷基、c1-6卤代烷基或-nh2。
76、在一些实施方案中,r3各自独立地选自f、cl、羟基、c1-6烷基或-nh2。
77、在一些实施方案中,r3各自独立地选自c1-6烷基。
78、在一些实施方案中,r3各自独立地选自c1-3烷基。
79、在一些实施方案中,r3各自独立地选自甲基、乙基、正丙基或异丙基。
80、在一些实施方案中,r3选自甲基。
81、在一些实施方案中,m选自0、1或2。
82、在一些实施方案中,r4选自c1-3烷基。
83、在一些实施方案中,r4选自甲基。
84、在一些实施方案中,x1、x2、x3或x4分别独立地选自n或ch,并且x1、x2、x3或x4中的0个、1个、2个或3个选自n。
85、在一些实施方案中,x1、x2、x4选自n,并且x3选自ch。
86、在一些实施方案中,x1、x3、x4选自n,并且x2选自ch。
87、在一些实施方案中,x1、x2选自n,并且x3、x4选自ch。
88、在一些实施方案中,x1、x3选自n,并且x2、x4选自ch。
89、在一些实施方案中,x2、x3选自n,并且x1、x4选自ch。
90、在一些实施方案中,x2、x4选自n,并且x1、x3选自ch。
91、在一些实施方案中,x3、x4选自n,并且x1、x2选自ch。
92、在一些实施方案中,x1选自n,并且x2、x3、x4选自ch。
93、在一些实施方案中,x2选自n,并且x1、x3、x4选自ch。
94、在一些实施方案中,x3选自n,并且x2、x3、x4选自ch。
95、在一些实施方案中,x4选自n,并且x1、x2、x3选自ch。
96、在一些实施方案中,x1、x2、x3或x4选自ch。
97、在一些实施方案中,环b选自c5-c8环烷基、5元~6元芳基、9~10元芳基、含有1~3个各自独立地选自n或o原子的5~8元杂环烷基、或含有1~3个各自独立地选自n或o原子的5元~6元或9~10元杂芳基;
98、在一些实施方案中,环b选自5~6元芳基或含1~3个氮原子的5~6元杂芳基。
99、在一些实施方案中,环b选自苯基或含1个氮原子的6元杂芳基。
100、在一些实施方案中,环b选自苯基或吡啶基。
101、在一些实施方案中,x选自nr6或o。
102、在一些实施方案中,x选自nh。
103、在一些实施方案中,x选自o。
104、在一些实施方案中,r5各自独立地选自卤素、氰基、硝基、c1-4烷基、c1-4烷氧基或c1-4卤代烷基。
105、在一些实施方案中,r5各自独立地选自卤素。
106、在一些实施方案中,r5各自独立地选自f、cl、br或i。
107、在一些实施方案中,r6选自氢或c1-4烷基。
108、在一些实施方案中,r6选自氢或c1-3烷基。
109、在一些实施方案中,r6选自氢或甲基;
110、在一些具体实施方案中,r6选自氢。
111、在一些实施方案中,p选自0、1或2。
112、在一些实施方案中,p选自0。
113、在一些实施方案中,本技术的式(a-i)、式(a-ii)或式(i)化合物、其立体异构体或其药学上可接受的盐选自以下式(ii)、式(iii)、式(ii-a)、式(ii-b)、式(iii-a)或式(iii-b)化合物、其立体异构体或其药学上可接受的盐:
114、
115、
116、其中,环a、r1、r3和n如本技术所述。。
117、在一些实施方案种,本技术包含上述定义的变量及其实施方案,以及它们的任意组合。
118、在一些实施方案中,本技术选自以下化合物、其立体异构体或其药学上可接受的盐:
119、
120、
121、
122、在一些实施方案中,本技术选自以下化合物、其立体异构体或其药学上可接受的盐:
123、
124、
125、
126、
127、
128、
129、另一方面,本技术提供了药物组合物,其包含本技术的上述化合物、其立体异构体或其药学上可接受的盐。在一些实施方案中,本技术的药物组合物还包括药学上可接受的辅料。
130、另一方面,本技术提供了一种治疗哺乳动物中与pi3kα激酶相关的疾病的方法,所述方法包括对需要该治疗的哺乳动物,优选人类,给予治疗有效量的上述化合物、其立体异构体或其药学上可接受的盐、或其药物组合物。
131、另一方面,本技术提供了上述化合物、其立体异构体或其药学上可接受的盐、或其药物组合物在制备治疗与pi3kα激酶相关的疾病的药物中的用途。
132、另一方面,本技术提供了上述化合物、其立体异构体或其药学上可接受的盐、或其药物组合物在治疗与pi3kα激酶相关的疾病中的用途。
133、另一方面,本技术提供了治疗与pi3kα激酶相关的疾病的上述化合物、其立体异构体或其药学上可接受的盐、或其药物组合物。
134、在一些实施方案中,所述与pi3kα激酶相关的疾病选自癌症。优选地,所述癌症选自实体瘤、淋巴瘤等。
135、在一些实施方案中,所述pi3kα激酶为突变型pi3kα激酶。
136、本技术的化合物具备良好的pi3kα激酶抑制活性、细胞增殖抑制活性。
137、定义
138、除非另有说明,本技术中所用的下列术语具有下列含义。一个特定的术语在没有特别定义的情况下不应该被认为是不确定的或不清楚的,而应该按照本领域普通的含义去理解。当本文中出现商品名时,意在指代其对应的商品或其活性成分。
139、术语“被取代”是指特定原子上的任意一个或多个氢原子被取代基取代,只要特定原子的价态是正常的并且取代后的化合物是稳定的。当取代基为氧代(即=o)时,意味着两个氢原子被取代,氧代不会发生在芳香基上。
140、术语“任选”或“任选地”是指随后描述的事件或情况可以发生或不发生,该描述包括发生所述事件或情况和不发生所述事件或情况。例如,乙基“任选”被卤素取代,指乙基可以是未被取代的(-ch2ch3)、单取代的(如-ch2ch2f)、多取代的(如-chfch2f、-ch2chf2等)或完全被取代的(-cf2cf3)。本领域技术人员可理解,对于包含一个或多个取代基的任何基团,不会引入任何在空间上不可能存在和/或不能合成的取代或取代模式。
141、本文中的cm-n,是该部分具有给定范围中的整数个碳原子。例如“c1-6”是指该基团可具有1个碳原子、2个碳原子、3个碳原子、4个碳原子、5个碳原子或6个碳原子;“c1-3”是指该基团可具有1个碳原子、2个碳原子或3个碳原子。
142、本文中的“一个或多个”指一个至十个以内的整数。例如“一个或多个”指一个、两个、三个、四个、五个、六个、七个、八个、九个或十个;或者,“一个或多个”指一个、两个、三个、四个、五个或六个;或者,“一个或多个”指一个、两个或三个。
143、当任何变量(例如r)在化合物的组成或结构中出现一次以上时,其在每一种情况下的定义都是独立的。因此,例如,如果一个基团被2个r所取代,则每个r都有独立的选项。
144、当一个取代基的键交叉连接到一个环上的两个原子之间时,这种取代基可以与这个环上的任意原子相键合。例如,结构单元表示其可在环己基或者环己二烯上的任意一个位置发生取代。
145、术语“卤”或“卤素”是指氟、氯、溴和碘。
146、术语“羟基”是指-oh基团。
147、术语“氨基”是指-nh2基团。
148、术语“硝基”是指-no2基团。
149、术语“氰基”是指-cn基团。
150、术语“烷基”是指通式为cnh2n+1的烃基。该烷基可以是直链或支链的。例如,术语“c1-6烷基”指含有1至6个碳原子的烷基(例如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、1-甲基丁基、2-甲基丁基、3-甲基丁基、新戊基、己基、2-甲基戊基等)。类似地,烷氧基、烷基氨基、二烷基氨基、烷基磺酰基和烷硫基的烷基部分(即烷基)具有上述相同定义。
151、术语“烷氧基”指-o-烷基。
152、术语“环烷基”是指完全饱和的碳环。除非另有指示,该碳环通常为3至10元环。除非另有指示,所述环烷基可以是单环、双环或三环。环烷基非限制性实例包括但不限于环丙基、环丁基、环戊基、环己基、降冰片基(双环[2.2.1]庚基)、双环[2.2.2]辛基、金刚烷基等。
153、术语“杂环基”是指无芳香性的含有杂原子的环状基团,其中部分环原子是选自n、o、s(o)n(其中n为0、1或2)的杂原子,其余环原子为c。这样的环可以是饱和的或不饱和的(例如具有一个或多个双键),但是不具有完全共轭的π-电子体系。杂环基的非限制性实例包括环氧乙烷基、环硫乙烷基、环氮乙烷基、吖丁啶基、噁丁环基、噻丁环基、四氢呋喃基、吡咯烷基、噁唑烷基、四氢吡唑基、吡咯啉基、二氢呋喃基、二氢噻吩基、哌啶基、四氢吡喃基、四氢噻喃基、吗啉基、哌嗪基、二氢吡啶基、四氢吡啶基、二氢吡喃基、四氢吡喃基、二氢噻喃基、氮杂环庚烷基、氧杂环庚烷基、硫杂环庚烷基、氧杂氮杂双环[2.2.1]庚基和氮杂螺[3.3]庚基等。术语“5元或6元杂环基”是指具有5~6个环原子的杂环基。所述“杂环基”或“5元或6元杂环基”可以是非取代的或是被一个或多个选自羟基、卤素、c1~4烷基或氧代的取代基取代。
154、术语“杂环烷基”是指完全饱和的含有杂原子的环状基团。除非另有指示,该杂环烷基通常为含有1至3个独立地选自n、o、s(o)n(其中n为0、1或2)的杂原子(优选1或2个杂原子)的环。除非另有指示,所述杂环烷基可以是单环、双环或三环基。除非另有指示,所述杂环烷基包括但不限于3至12元环、3至8元环或者4至8元环。3元杂环烷基的实例包括但不限于环氧乙烷基、环硫乙烷基、环氮乙烷基,4元杂环烷基的非限制性实例包括但不限于吖丁啶基、噁丁环基、噻丁环基,5元杂环烷基的实例包括但不限于四氢呋喃基、1,3-二氧戊烷基、四氢噻吩基、吡咯烷基、异噁唑烷基、噁唑烷基、异噻唑烷基、噻唑烷基、咪唑烷基、四氢吡唑基,6元杂环烷基的实例包括但不限于哌啶基、四氢吡喃基、四氢噻喃基、吗啉基、哌嗪基、1,4-噻噁烷基、1,4-二氧六环基、硫代吗啉基、1,3-二噻烷基或1,4-二噻烷基,7元杂环烷基的实例包括但不限于氮杂环庚烷基、氧杂环庚烷基、硫杂环庚烷基。优选为具有5或6个环原子的单环杂环烷基。
155、术语“芳基”是指具有共轭的π电子体系的全碳单环或稠合多环的芳香环基团。除非另有指示,芳基可以具有6-20个碳原子,6-14个碳原子或6-12个碳原子。芳基的非限制性实例包括但不限于苯基、萘基、蒽基和1,2,3,4-四氢化萘等。
156、术语“杂芳基”是指单环或多环体系,其中含有至少一个选自n、o、s(o)n(其中n为0、1或2)的环原子,其余环原子为c,并且具有至少一个芳香环。除非另有指示,所述杂芳基可以是单环、双环或三环基。除非另有指示,所述杂芳基可以具有单个5至8元环,或包含6至14个,尤其是6至10个环原子的多个稠合环。杂芳基的非限制性实例包括但不限于吡咯基、呋喃基、噻吩基、咪唑基、噁唑基、吡唑基、吡啶基、嘧啶基、吡嗪基、喹啉基、异喹啉基、四唑基、三唑基、三嗪基、苯并呋喃基、苯并噻吩基、吲哚基、异吲哚基等。
157、术语“治疗”意为将本技术所述化合物或制剂进行给药以改善或消除疾病或与所述疾病相关的一个或多个症状,且包括:
158、(i)抑制疾病或疾病状态,即遏制其发展;
159、(ii)缓解疾病或疾病状态,即使该疾病或疾病状态消退。
160、术语“治疗有效量”意指(i)治疗本文中所述的特定疾病、病况或障碍,(ii)减轻、改善或消除本文中所述的特定疾病、病况或障碍的一种或多种症状,或(iii)预防或延迟本文中所述的特定疾病、病况或障碍的一种或多种症状发作的本技术化合物的用量。构成“治疗有效量”的本技术化合物的量取决于该化合物、疾病状态及其严重性、给药方式以及待被治疗的哺乳动物的年龄而改变,但可例行性地由本领域技术人员根据其自身的知识及本公开内容而确定。
161、术语“药学上可接受的”是针对那些化合物、材料、组合物和/或剂型而言,它们在可靠的医学判断的范围之内,适用于与人类和动物的组织接触使用,而没有过多的毒性、刺激性、过敏性反应或其它问题或并发症,与合理的利益/风险比相称。
162、作为药学上可接受的盐,例如,可以提及金属盐、铵盐、与有机碱形成的盐、与无机酸形成的盐、与有机酸形成的盐、与碱性或者酸性氨基酸形成的盐等。
163、术语“药物组合物”是指一种或多种本技术的化合物或其盐与药学上可接受的辅料组成的混合物。药物组合物的目的是有利于对有机体给予本技术的化合物。
164、术语“药学上可接受的辅料”是指对有机体无明显刺激作用,而且不会损害该活性化合物的生物活性及性能的那些辅料。合适的辅料是本领域技术人员熟知的,例如碳水化合物、蜡、水溶性和/或水可膨胀的聚合物、亲水性或疏水性材料、明胶、油、溶剂、水等。
165、词语“包括(comprise)”或“包含(comprise)”及其英文变体例如comprises或comprising应理解为开放的、非排他性的意义,即“包括但不限于”。
166、除非另外特别说明,否则单数术语涵盖复数术语,并且复数术语涵盖单数术语。除非另外特别说明,否则词语“一个”或“一种”意指“至少一个”或“至少一种”。除非另外说明,否则“或”的使用意指“和/或”。
167、本发明的化合物可以存在特定的几何或立体异构体形式。本发明设想所有的这类化合物,包括顺式和反式异构体、(-)-和(+)-对映体、(r)-和(s)-对映体、非对映异构体、(d)-异构体、(l)-异构体,及其外消旋混合物和其它混合物,例如对映异构体或非对映体富集的混合物,所有这些混合物都属于本发明的范围之内。烷基等取代基中可存在另外的不对称碳原子。所有这些异构体以及它们的混合物,均包括在本发明的范围之内。
168、除非另有说明,“(d)”或者“(+)”表示右旋,“(l)”或者“(-)”表示左旋,“(dl)”或者“(±)”表示外消旋。
169、除非另有说明,用楔形实线键和楔形虚线键表示一个立体中心的绝对构型,用直形实线键和直形虚线键表示立体中心的相对构型。
170、可以通过手性合成或手性试剂或者其他常规技术制备光学活性的(r)-和(s)-异构体以及d和l异构体。如果想得到本发明某化合物的一种对映体,可以通过不对称合成或者具有手性助剂的衍生作用来制备,其中将所得非对映体混合物分离,并且辅助基团裂开以提供纯的所需对映异构体。或者,当分子中含有碱性官能团(如氨基)或酸性官能团(如羧基)时,与适当的光学活性的酸或碱形成非对映异构体的盐,然后通过本领域所公知的常规方法进行非对映异构体拆分,然后回收得到纯的对映体。此外,对映异构体和非对映异构体的分离通常是通过使用色谱法完成的,所述色谱法采用手性固定相,并任选地与化学衍生法相结合(例如由胺生成氨基甲酸盐)。
171、本技术还包括与本文中记载的那些相同的,但一个或多个原子被原子量或质量数不同于自然中通常发现的原子量或质量数的原子置换的同位素标记的本技术化合物。可结合到本技术化合物的同位素的实例包括氢、碳、氮、氧、磷、硫、氟、碘和氯的同位素,诸如分别为2h、3h、11c、13c、14c、13n、15n、15o、17o、18o、31p、32p、35s、18f、123i、125i和36cl等。
172、某些同位素标记的本技术化合物(例如用3h及14c标记的那些)可用于化合物和/或底物组织分布分析中。氚化(即3h)和碳-14(即14c)同位素由于它们易于制备和可检测性是尤其优选的。正电子发射同位素,诸如15o、13n、11c和18f可用于正电子发射断层扫描(pet)研究以测定底物占有率。通常可以通过与公开于下文的方案和/或实施例中的那些类似的下列程序,通过同位素标记试剂取代未经同位素标记的试剂来制备同位素标记的本技术化合物。
173、此外,用较重同位素(诸如氘(即2h或d))取代可以提供某些由更高的代谢稳定性产生的治疗优点(例如增加的体内半衰期或降低的剂量需求),并且因此在某些情形下可能是优选的,其中氘取代可以是部分或完全的,部分氘取代是指至少一个氢被至少一个氘取代,完全氘取代是指基团上的所有氢均被氘取代,例如甲基(-ch3)完全被氘取代即为-cd3。
174、本技术的和化合物可以以其互变异构体形式存在,并且所有这样的形式包含于本技术的范围内。术语“互变异构体”或“互变异构体形式”是指可经由低能垒互变的不同能量的结构异构体。例如,质子互变异构体(也称为质子转移互变异构体)包括经由质子迁移的互变,如酮-烯醇及亚胺-烯胺异构化。质子互变异构体的具体实例可以是咪唑部分,其中质子可在两个环氮间迁移。
175、本技术的药物组合物可通过将本技术的化合物与适宜的药学上可接受的辅料组合而制备,例如可配制成固态、半固态、液态或气态制剂,如片剂、丸剂、胶囊剂、粉剂、颗粒剂、膏剂、乳剂、悬浮剂、栓剂、注射剂、吸入剂、凝胶剂、微球及气溶胶等。
176、给予本技术化合物或其药学上可接受的盐或其药物组合物的典型途径包括但不限于口服、直肠、局部、吸入、肠胃外、舌下、阴道内、鼻内、眼内、腹膜内、肌内、皮下、静脉内给药。
177、本技术的药物组合物可以采用本领域众所周知的方法制造,如常规的混合法、溶解法、制粒法、制糖衣药丸法、磨细法、乳化法、冷冻干燥法等。
178、本文所述的通式i化合物的所有给予方法中,每天给药的剂量为0.01到200mg/kg体重,以单独或分开剂量的形式。
179、本技术的化合物可以通过本领域技术人员所熟知的多种合成方法来制备,包括下面列举的具体实施方式、其与其它化学合成方法的结合所形成的实施方式以及本领域技术上人员所熟知的等同替换方式,优选的实施方式包括但不限于本技术的实施例。
180、本技术具体实施方式的化学反应是在合适的溶剂中完成的,所述的溶剂须适合于本技术的化学变化及其所需的试剂和物料。为了获得本技术的化合物,有时需要本领域技术人员在已有实施方式的基础上对合成步骤或者反应流程进行修改或选择。
181、在一些实施方案中,本技术的式a-i化合物可以由有机合成领域技术人员参考以下路线来制备:
182、制备路线1:
183、
184、制备路线2:
185、
186、其中,m选自f、oh、nh2或nhr6等基团;y和z各自独立地选自卤素等基团。
187、其中环a、环b、x、r1、r2、r3、r4、r5、r6、m、n和p的定义如本技术所述。
188、为了描述和公开的目的,以引用的方式将所有的专利、专利申请和其它已确定的出版物在此明确地并入本文。这些出版物仅因为它们的公开早于本技术的申请日而提供。所有关于这些文件的日期的声明或这些文件的内容的表述是基于申请者可得的信息,并且不构成任何关于这些文件的日期或这些文件的内容的正确性的承认。而且,在任何国家,在本技术中对这些出版物的任何引用并不构成关于该出版物成为本领域的公知常识的一部分的认可。
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!