吡咯并环类化合物及其制备方法和用途与流程
本发明属于医药领域,具体涉及一种用于治疗hbv感染的吡咯并环类化合物及其制备方法和用途。
背景技术:
1、乙型肝炎病毒(hepatitis b virus,hbv),简称“乙肝病毒”,能引发乙型病毒性肝炎,是全球最值得关注的病毒之一。目前,全世界有超2.5亿人携带乙肝病毒,这类患者相比正常人群,罹患重大肝病包括肝硬化、肝脏永久性疤痕以及肝衰竭和癌症的风险增加。世界卫生组织估计,每年有超过78万人死于乙肝病毒引发的疾病。根据hepatitis bfoundation数据显示,乙肝病毒占诱导肝癌发生因素的80%,而肝癌患者的五年存活率通常只有15%。
2、尽管存在有效的疫苗,但在hbv流行地区,疫苗覆盖率并不令人满意[1]。当前主要有两类药物被批准用于慢性乙型肝炎的治疗:一类是干扰素(ifn-α)及其聚乙二醇化形式(peg-ifn-α),另一类是核苷类似物(nucleoside analogs,nas)。ifn-α是一种免疫调节剂,能以非特异性的方式诱导干扰素刺激基因(interferon-stimulated genes,isgs)表达;该基因编码具有直接或间接抗病毒特性的组成型或分泌型蛋白,从而促进免疫细胞的分化或激活[2]。经过48周的皮下注射ifn-α后,hbv患者的有效率仅为25%[3]。ifn-α除应答率不高外,还存在其他不足,如需要注射给药、严重的流感样症状等不良反应,代偿性肝硬化、重症肝炎、合并自身免疫性和心理疾病患者禁忌。目前共5种核苷类似物(nas)药物获批,包括拉米夫定(lamivudine,lmv)、替比夫定(telbivudine,ldt)、阿德福韦酯(adefovirdipivoxil,adv)、替诺福韦(tenofovir,tfv)、恩替卡韦(entecavir,etv)。nas通过直接抑制hbv聚合酶活性导致病毒粒子的减少,从而中断核衣壳到感染细胞中细胞核的循环,理论上可降低cccdna的表达量。但是nas治疗后无法抑制cccdna在新感染细胞中的从头合成,这表明抗病毒治疗期间残留的病毒粒子会导致新细胞的感染和cccdna库的重建,患者一旦自行停药,可能造成病毒学反弹。因此,慢性乙肝病毒感染很少达到功能性治愈,多数患者需要终身服用药物,但长期服用nas药物易使病毒变异而产生耐药性。
3、基于当前疗法的不足,一些针对hbv复制周期或增强人体免疫反应的药物正在被开发并陆续推向临床研究阶段。其中,hbv复制过程中的核心蛋白对hbv pgrna的包装和逆转录至关重要,针对该蛋白研发的分子称为核心蛋白变构调节剂或称为衣壳组装调节剂(cpams)。根据cpams的作用机制可将其分为两类:以杂芳基二-h嘧啶(hap)为代表的i类cpams,其作用机制是增强核衣壳形成动力学,导致核衣壳的错误组装;以苯丙烯酰胺(ppas)和磺胺基苯甲酰胺(sbas)结构类型为代表的ii类cpams,其作用机制是加速核衣壳组装,并形成形态正常但缺乏病毒pgrna和hbv聚合酶包裹在内的核衣壳[4]。
4、对不同机制的核衣壳抑制剂bay41-4109(hap)和jnj-632(sba)在人的原代肝细胞中进行抗病毒研究,发现cpams不仅能抑制hbv复制,还能抑制hbv rna的转录和抗原的产生,提示cpams具有抑制病毒早期和晚期阶段的双重作用机制[5-6]。nvr3-778(sba)作为早期研发的cpams分子,表现出较强的抗hbv活性,在hepg2.2.15细胞中的ec50为0.4μm。同样,在hbv感染的人源化肝脏小鼠模型中也显示出了有效的抗hbv活性[7]。随着科学技术的进步,目前药物研发人员已经设计并筛选出体外抗hbv活性高达nm级别的分子结构如glp-26、rg7907等。
5、目前研发的抗hbv药物大多表现出良好的体外抗hbv活性,但进入临床研究后,显示疗效不高并且可能会出现一些不良反应,如alt(谷丙转氨酶)升高、停药后复发等,导致这些药物临床试验宣告失败。因此,虽然目前有较多治疗乙肝的药物和疗法,但是用于实现其治愈的新结构类型、新作用机制的分子仍是乙肝治疗领域亟需探索和研究的。
技术实现思路
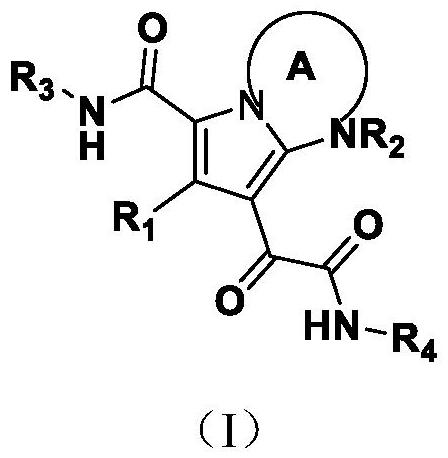
1、本发明提供了一种式(i)所示的化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体:
2、
3、其中,r1选自-h、氘、c1-8烷基、c3-8环烷基、c1-8卤代烷基、c1-8氘代烷基、c1-8烷氧基、c1-8氘代烷氧基、卤素、-cn、-oh、-nh2;
4、r2选自-h、c1-3烷基、c1-3酰基、c1-3卤代酰基;
5、r3选自取代或未取代的c6-10芳基、取代或未取代的5-10元杂芳基;所述5-10元杂芳基含有1至3个选自n、o和s的杂原子;所述c6-10芳基的取代基选自卤素、c1-8烷基、c1-8卤代烷基、c1-8卤代烷氧基、-cn;所述5-10元杂芳基的取代基选自卤素、c1-8烷基、c1-8卤代烷基、c1-8卤代烷氧基、-cn;
6、r4选自取代或未取代的c1-10烷基、取代或未取代的c3-14环烷基、取代或未取代的4-14元杂环烷基、c2-8炔基;
7、所述c1-10烷基的取代基选自-h、氘、卤素、-cn、-c(o)ora、-c(o)nrarb、-nrarb、c2-8炔基、-oh、c2-8烷氧基、c2-8烷氧烷基;或同一个碳原子上的两个取代基可以一起组成取代或未取代的c3-8环烷基、取代或未取代的5-6元杂环烷基、5-6元杂芳基;所述5-6元杂环烷基含有1-3个选自n、o和s的杂原子;所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;所述5-6元杂环烷基的取代基选自c1-8烷基、-c(o)ra;所述c3-8环烷基的取代基选自-h、氘、卤素;
8、所述c3-14环烷基包括单环、螺环、稠环和桥环;所述c3-14环烷基的取代基选自-h、氘、卤素、-c(o)nrarb、c1-8卤代烷基、-cn、c2-8炔基、-nrarb、-oh、c2-8烷氧基、c2-8烷氧烷基、-c(o)ora、-c(o)ra、5-6元杂芳基、c1-8烷基、c1-8羟基烷基;所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;
9、所述4-14元杂环烷基包括单环、螺环、稠环和桥环;所述4-14元杂环烷基含有1-4个选自n、o和s的杂原子;所述4-14元杂环烷基的取代基选自c1-8卤代烷基、卤素、-c(o)ra、c1-8烷基、-oh、c2-8烷氧基、c2-8烷氧烷基、-nrarb;
10、其中,ra和rb各自独立地选自-h、c1-8氘代烷基、c1-8烷基、c1-8卤代烷基;
11、a环为取代或未取代的4-6元杂环烷基、杂芳基;所述杂环烷基包括单环、双环或多环,其包含1-3个杂原子;优选地,所述杂原子为n、o、s,杂环烷基的成环碳原子和杂原子可以任意地氧化以形成c(o)、s(o)、c(s)或s(o)2、n-氧化物;所述杂芳基包括单环、双环或多环,其包含1-5个杂原子;优选地,所述杂原子为n、o、s,杂芳基的成环碳原子和杂原子可以任意地氧化以形成c(o)、s(o)、c(s)或s(o)2、n-氧化物。
12、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r1选自-h、氘、c1-6烷基、c1-6卤代烷基、c1-6氘代烷基、c3-6环烷基、卤素、-cn、-oh、-nh2;所述c1-6烷基包括支链或直链的c1-6烷基。
13、在一个实施方案中,r1选自c1-6烷基、c1-6卤代烷基、c1-6氘代烷基、卤素、-cn、-nh2。
14、在一个实施方案中,r1选自c1-4烷基、c1-4卤代烷基、c1-4氘代烷基、卤素、-cn、-nh2。
15、在一个实施方案中,r1选自-ch3、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、戊基、3-戊基、己基、-cf3、-ccl3、cbr3、-cl、-f、-br、-i、-cd3、氘代乙基、氘代丙基、氘代丁基、氘代戊基、氘代己基、-cn、-nh2。
16、在一个实施方案中,r1选自-ch3、-cf3、-cd3、-cl、-f、-br、-cn、-nh2。
17、在一个实施方案中,r1选自-ch3、-cd3、-cl、-cf3。
18、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r2选自-h、-ch3、乙基、丙基、异丙基、甲酰基、乙酰基、丙酰基、卤代乙酰基或卤代丙酰基。
19、在一个实施方案中,r2选自-h、-ch3、乙基、异丙基、甲酰基、乙酰基、丙酰基、氯代乙酰基、氟代乙酰基、溴代乙酰基、氯代丙酰基、氟代丙酰基、溴代丙酰基。
20、在一个实施方案中,r2选自-h、-ch3、乙基、异丙基。
21、在一个实施方案中,r2选自-h。
22、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r3选自取代或未取代的苯基、取代或未取代的吡啶基、所述苯基的取代基选自卤素、c1-8烷基、c1-8卤代烷基、c1-8卤代烷氧基、-cn;所述吡啶基的取代基选自卤素、c1-8烷基、c1-8卤代烷基、c1-8卤代烷氧基、-cn。
23、在一个实施方案中,r3选自取代或未取代的苯基、取代或未取代的吡啶基、所述苯基的取代基选自卤素、c1-6烷基、c1-6卤代烷基、c1-6卤代烷氧基、-cn;所述吡啶基的取代基选自卤素、c1-6烷基、c1-6卤代烷基、c1-6卤代烷氧基、-cn。
24、在一个实施方案中,r3选自取代或未取代的苯基、取代或未取代的吡啶基、所述苯基的取代基选自-f、-cl、-br、c1-4烷基、c1-4卤代烷基、c1-4卤代烷氧基、-cn;所述吡啶基的取代基选自-f、-cl、-br、c1-4烷基。
25、在一个实施方案中,r3选自
26、在一个实施方案中,r3选自
27、在一个实施方案中,r3选自
28、在一个实施方案中,r3选自
29、在一个实施方案中,r3选自
30、在一个实施方案中,r3选自
31、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r4选自取代或未取代的c1-8烷基、取代或未取代的c3-12环烷基、取代或未取代的4-10元杂环烷基、c2-6炔基;
32、所述c1-8烷基的取代基选自-h、氘、卤素、-cn、-c(o)ora、-c(o)nrarb、-nrarb、c2-6炔基、-oh、c2-6烷氧基、c2-6烷氧烷基;或同一个碳原子上的两个取代基可以一起组成取代或未取代的c3-6环烷基、取代或未取代的5-6元杂环烷基、5-6元杂芳基;所述5-6元杂环烷基含有1-3个选自n、o和s的杂原子;所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;所述5-6元杂环烷基的取代基选自c1-6烷基、-c(o)ra;所述c3-6环烷基的取代基选自-h、氘、卤素;
33、所述c3-12环烷基包括单环、螺环、稠环和桥环;所述c3-12环烷基的取代基选自-h、氘、卤素、-c(o)nrarb、c1-6卤代烷基、-cn、c2-6炔基、c1-6烷基、-nrarb、-oh、c2-6烷氧基、c2-6烷氧烷基、-c(o)ora、-c(o)ra、5-6元杂芳基、c1-6羟基烷基;所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;
34、所述4-10元杂环烷基包括单环、螺环、稠环和桥环;所述4-10元杂环烷基含有1-3个选自n、o和s的杂原子;所述4-14元杂环烷基的取代基选自c1-6卤代烷基、卤素、-c(o)ra、c1-6烷基、-oh、c2-6烷氧基、c2-6烷氧烷基、-nrarb;
35、其中,ra和rb各自独立地选自-h、c1-6氘代烷基、c1-6烷基、c1-6卤代烷基。
36、在一个实施方案中,r4选自取代或未取代的c1-6烷基、取代或未取代的c3-10环烷基、取代或未取代的4-10元杂环烷基、c2-4炔基;
37、所述c1-6烷基的取代基选自-h、氘、卤素、-cn、-c(o)ora、-c(o)nrarb、-nrarb、c2-4炔基、-oh、c2-4烷氧基、c2-4烷氧烷基;或同一个碳原子上的两个取代基可以一起组成取代或未取代的c3-6环烷基、取代或未取代的5-6元杂环烷基、5-6元杂芳基;所述5-6元杂环烷基含有1-3个选自n、o的杂原子;所述5-6元杂芳基含有1-3个选自n、o的杂原子;所述5-6元杂环烷基的取代基选自c1-6烷基、-c(o)ra;所述c3-6环烷基的取代基选自-h、氘、卤素;
38、所述c3-10环烷基包括单环、螺环、稠环和桥环;所述c3-10环烷基的取代基选自-h、氘、卤素、-c(o)nrarb、c1-4卤代烷基、-cn、c2-4炔基、c1-4烷基、-nrarb、-oh、c2-4烷氧基、c2-4烷氧烷基、-c(o)ora、醇类、-c(o)ra、5-6元杂芳基、c1-3羟基烷基;所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;
39、所述4-10元杂环烷基包括单环、螺环、稠环和桥环;所述4-10元杂环烷基含有1-3个选自n、o和s的杂原子;所述4-10元杂环烷基的取代基选自c1-4卤代烷基、卤素、-c(o)ra、c1-6烷基、-oh、c2-4烷氧基、c2-4烷氧烷基、-nrarb;
40、其中,ra和rb各自独立地选自-h、c1-4氘代烷基、c1-3烷基、c1-4卤代烷基。
41、在一个实施方案中,r4选自取代或未取代的c1-6烷基、取代或未取代的c3-8环烷基、c2-4炔基、
42、所述c1-6烷基的取代基选自-h、氘、-f、-cl、-br、-cn、-cooh、-c(o)och3、-nh2、-c(o)nh(ch3)、-ch3、乙炔基、-oh;
43、所述c3-8环烷基包括单环、螺环、稠环和桥环;所述c3-8环烷基的取代基选自-h、-f、-cl、-br、-c(o)nh(ch3)、-cf3、-cn、乙炔基、-nh2、-oh、-c(o)och3、-cooh、-c(o)ch3、-ch3、乙基、甲醇、羟甲基、羟乙基、羟丙基、丙醇。
44、在一个实施方案中,r4选自-ch3、乙基、丙基、异丙基、
45、在一个实施方案中,r4选自
46、在一个实施方案中,r4选自
47、在一个实施方案中,r4选自
48、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物具有式(ⅱ-1)、式(ⅱ-2)、式(ⅱ-3)、式(ⅱ-4)、(ⅱ-5)、式(ⅱ-6)、式(ⅱ-7)、式(ⅱ-8)、式(ⅱ-9)或式(ⅱ-10)所述结构:
49、
50、
51、其中,r4的定义引用前述定义。
52、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物具有式(iii-1)、式(iii-2)、式(iii-3)、式(iii-4)、(iii-5)、式(iii-6)、式(iii-7)、式(iii-8)、式(iii-9)或式(iii-10)所述结构:
53、
54、其中,r4的定义引用前述定义。
55、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物具有式(iv-1)、式(iv-2)、式(iv-3)、式(iv-4)、(iv-5)、式(iv-6)、式(iv-7)、式(iv-8)、式(iv-9)、式(iv-10)或(iv-11)所述结构:
56、
57、其中,r4的定义引用前述定义。
58、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物具有式(v-1)所述结构:
59、
60、其中,r1和r3的定义引用前述定义。
61、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物具有式(ⅵ-1)、(ⅵ-2)、(ⅵ-3)、(ⅵ-4)或(ⅵ-5)所述结构:
62、
63、其中,r1、r2、r3的定义引用前述定义。
64、作为本发明优选的技术方案,本发明还提供了式(ia)所示的化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体:
65、
66、其中,r11选自h、卤素、c1-8烷基、c1-8氘代烷基、c1-8卤代烷基;
67、r12选自未取代的或被1个或多个rc取代的c6-10芳基、未取代的或被1个或多个rd取代的5-10元杂芳基,所述5-10元杂芳基含有1-3个选自n、o和s的杂原子;每个rc、rd各自独立地选自相同或不同的卤素、c1-8烷基、c1-8卤代烷基、c1-8卤代烷氧基、-cn;
68、r13选自c1-8烷基、c1-8卤代烷基、未取代的或被1个或多个羟基或卤素取代的c3-8环烷基、r14和r15与它们连接的碳原子组合成4-8元杂环烷基或未取代的或被1个或多个卤素或羟基取代的c3-8环烷基,所述4-8元杂环烷基含有1-3个选自n、o和s的杂原子;r16选自c1-8烷基、c2-8炔基、c1-8卤代烷基、c1-8羟基烷基、-c(o)nrirj;ri和rj各自独立地选自h、c1-4烷基;
69、环b选自4-6元杂环烷基、4-6元杂环烯基、4-6元杂环酰胺基,所述4-6元杂环烷基、4-6元杂环烯基、4-6元杂环酰胺基各自独立地含有2-3个选自n、o和s的杂原子,且至少含有2个n原子。
70、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r11选自c1-6烷基、卤素。
71、在一个具体实施方案中,r11选自c1-4烷基、c5-6烷基、卤素。
72、在一个具体实施方案中,r11选自甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基、叔丁基、f、cl、br。
73、在一个具体实施方案中,r11选自甲基、cl。
74、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r12选自未取代的或被1个或多个rc取代的苯基、未取代的或被1个或多个rd取代的5-6元杂芳基,所述5-6元杂芳基含有1-3个选自n、o和s的杂原子;每个rc、rd各自独立地选自相同或不同的卤素、c1-6烷基、c1-6卤代烷基、c1-6卤代烷氧基、-cn。
75、在一个具体实施方案中,r12为未取代的或被1个或多个rc取代的苯基;每个rc各自独立地选自相同或不同的卤素、c1-6烷基、c1-6卤代烷基、c1-6卤代烷氧基、-cn。
76、在一个具体实施方案中,r12为未取代的或被1个或多个rc取代的苯基;每个rc各自独立地选自相同或不同的卤素、c1-4烷基、c1-4氟代烷基、c1-4氟代烷氧基、-cn。
77、在一个具体实施方案中,r12为未取代的或被1个、2个或3个rc取代的苯基;每个rc各自独立地选自相同或不同的f、cl、br、-cn、甲基。
78、在一个具体实施方案中,r12选自
79、在一个具体实施方案中,r12选自
80、在一个具体实施方案中,r12选自
81、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,r13选自c1-6烷基、c1-6卤代烷基、未取代的或被1个或多个羟基或卤素取代的c3-6环烷基、r14和r15与它们连接的碳原子组合成4-7元杂环烷基或未取代的或被1个或多个卤素或羟基取代的c3-6环烷基,所述4-7元杂环烷基含有1-2个选自n、o和s的杂原子;r16选自c1-6烷基、c2-6炔基、c1-6卤代烷基、c1-6羟基烷基、-c(o)nrirj;ri和rj各自独立地选自h、c1-4烷基。
82、在一个具体实施方案中,r13选自c1-4烷基、c1-4氟代烷基、未取代的或被1个或多个羟基或卤素取代的c3-6环烷基、r14和r15与它们连接的碳原子组合成4-6元杂环烷基或未取代的或被1个或多个卤素或羟基取代的c3-6环烷基,所述4-6元杂环烷基含有1-2个选自n、o和s的杂原子;r16选自c1-4烷基、c2-4炔基、c1-4卤代烷基、c1-4羟基烷基、-c(o)nrirj;ri和rj各自独立地选自h、c1-4烷基。
83、在一个具体实施方案中,r13选自环丙基、环丁基、环戊基、环己基、被1个或多个羟基取代的c3-6环烷基、r14和r15与它们连接的碳原子组合成4-6元杂环烷基或未取代的或被1个或多个f、cl或br取代的c3-6环烷基,所述4-6元杂环烷基含有1个选自n、o和s的杂原子;r16选自甲基、乙基、乙炔基、丙炔基、氟代甲基、氟代乙基、羟甲基、羟乙基、-c(o)nrirj;ri和rj各自独立地选自h、甲基、乙基。
84、在一个具体实施方案中,r13选自环戊基、被1个羟基取代的环丁基、r14和r15与它们连接的碳原子组合成氧杂环丁基或未取代的或被1个或2个f取代的环丙基或环丁基;r16选自甲基、乙炔基、-cf3、羟甲基、-c(o)nhch3。
85、在一个具体实施方案中,r13选自环戊基、
86、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,环b选自4-6元杂环烷基、4-6元杂环烯基,所述4-6元杂环烷基、4-6元杂环烯基各自独立地含有2个n原子。
87、在一个具体实施方案中,环b并吡咯组成的结构为
88、在一个具体实施方案中环b并吡咯组成的结构为
89、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述式ia具有式ia-1所示结构:
90、
91、其中,r12、r13定义如前所述。
92、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述式ia具有式ia-2所示结构:
93、
94、其中,r13定义如前所述。
95、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述式ia具有式ia-3所示结构:
96、
97、其中,r13定义如前所述。
98、在一个具体实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述式ia具有式ia-4所示结构:
99、
100、其中,r13定义如前所述。
101、在一个实施方案中,上述化合物,或其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体中,所述化合物选自下列化合物:
102、
103、
104、
105、
106、
107、
108、
109、
110、
111、
112、
113、
114、
115、
116、
117、
118、
119、
120、
121、
122、本发明的技术术语:
123、根据本领域惯例,在本文结构式中用于描述为该部分或取代基与母核或主结构的连接点的键。
124、本发明中,所述术语“任选”是指可以被后续所述部分替换,也可以不被后续所述部分替换。
125、本发明中,所述术语“取代的”意指原子或原子团在形式上置换氢而作为“取代基”连接至另一基团。除非另外指出,否则所述术语“取代的”是指在允许此类取代的情况下的任何取代程度,例如单取代、二取代、三取代、四取代或五取代。独立地选择取代基,并且取代可以在任何化学可达位置上。应当理解,指定原子上的取代受原子价限制。应当理解,指定原子上的取代产生化学上稳定的分子。
126、本发明中,单独或与其他术语组合使用的所述术语“烷基”是指可为直链或支链的饱和烃基。所述术语“c1-10烷基”是指具有1至10个碳原子的烷基。烷基在形式上对应于一个c-h键被置换为烷基与化合物其余部分的连接点的烷烃。在一些实施方案中,烷基含有1-10个碳原子、1-8个碳原子、1-6个碳原子、1-4个碳原子、1-3个碳原子或1-2个碳原子。烷基部分的实例包括但不限于化学基团,如甲基、乙基、正丙基、异丙基、正丁基、伯丁基、叔丁基、异丁基;高级同系物,如2-甲基-1-丁基、正戊基、3-戊基、正己基、1,2,2-三甲基丙基等。
127、本发明中,单独或与其他术语组合使用的所述术语“卤代”或“卤素”是指f、cl、br和i。在一些实施方案中,所述术语“卤代”是指选自f、cl或br的卤素原子。
128、本发明中,单独或与其他术语组合使用的所述术语“卤代烷基”是指被一个或多个卤素取代的烷基,其中所述术语“卤素”、“烷基”如以上所定义。
129、本发明中,单独或与其他术语组合使用的所述术语“氘代烷基”是指被一个或多个氘原子取代的烷基,其中所述术语“烷基”如以上所定义。
130、本发明中,单独或与其他术语组合使用的所述术语“羟基烷基”是指被一个或多个羟基取代的烷基,其中所述术语“烷基”如以上所定义。
131、本发明中,单独或与其他术语组合使用的所述术语“杂原子”包括s、o和n。
132、本发明中,单独或与其他术语组合使用的所述术语“芳基”是指芳香族烃基,其可以为单环或多环(例如具有2个稠合环)。所述术语“c6-10芳基”是指具有6至10个环碳原子的芳基。芳基包括例如苯基、萘基、茚满基、茚基等。在一些实施方案中,芳基具有6个碳原子。在一些实施方案中,芳基具有10个碳原子。在一些实施方案中,芳基为苯基。在一些实施方案中,芳基为萘基。
133、本发明中,单独或与其他术语组合使用的所述术语“杂芳基”是指具有至少一个选自s、o和n的杂原子环成员的单环或多环芳香族杂环,杂原子可以在其中任意环上,也可以同时在多个(例如两个或三个)环上。在一些实施方案中,杂芳基环具有1、2、3或4个独立地选自s、o和n的杂原子环成员。在一些实施方案中,杂芳基部分中的任何成环n都可以为n-氧化物。在一些实施方案中,杂芳基具有5至14个环原子,包括碳原子以及1、2、3或4个独立地选自s、o和n的杂原子环成员。在一些实施方案中,杂芳基具有5至10个环原子,包括碳原子以及1、2、3或4个独立地选自s、o和n的杂原子环成员。在一些实施方案中,杂芳基具有5至6个环原子以及1或2个独立地选自s、o和n的杂原子环成员。在一些实施方案中,杂芳基为五元或六元杂芳基环。在其他实施方案中,杂芳基为八元、九元或十元稠合双环杂芳基环。实例杂芳基包括但不限于吡啶基、嘧啶基、吡嗪基、哒嗪基、吡咯基、吡唑基、唑基、噁唑基、噻唑基、咪唑基、呋喃基、噻吩基、喹啉基、异喹啉基、萘啶基(包括1,2-萘啶、1,3-萘啶、1,4-萘啶、1,5-萘啶、1,6-萘啶、1,7-萘啶、1,8-萘啶、2,3-萘啶和2,6-萘啶)、吲哚基、苯并噻吩基、苯并呋喃基、苯并异噁唑基、咪唑并[1,2-b]噻唑基、嘌呤基等。
134、本发明中,单独或与其他术语组合使用的所述术语“环烷基”是指非芳香族烃环系统(单环、双环或多环),多环(例如双环或三环)包括稠环、螺环、桥环,包括环化的烷基。所述术语“c3-8环烷基”或“c3-14环烷基”分别是指具有3-8个或3-14个环成员碳原子的环烷基。环烷基可以包括单环或多环(例如具有2、3或4个稠合环)基团和螺环。环烷基可以具有3、4、5、6、7、8、9、10、11、12、13或14个成环碳(c3-14)。在一些实施方案中,环烷基具有3-12个环成员、3-10个环成员、3-8个环成员、3-6个环成员、3-5个环成员或3-4个环成员。在一些实施方案中,环烷基是单环。在一些实施方案中,环烷基是单环或双环。在一些实施方案中,环烷基为c3-8单环环烷基。环烷基的成环碳原子可以任选地被氧化以形成氧代或硫离子基。在一些实施方案中,环烷基为环丙基、环丁基、环戊基或环己基。环烷基的实例包括环丙基、环丁基、环戊基、环己基、环庚基等等。在一些实施方案中,环烷基为环丙基、环丁基、环戊基或环己基。
135、本发明中,单独或与其他术语组合使用的所述术语“杂环烷基”是指非芳香族环或环系统,其具有至少一个独立地选自n、s和o的杂原子环成员,并且其具有4-10个环成员、4-7个环成员或4-6个环成员,杂原子可以在其任意环上,也可以同时在多个(例如两个或三个)环上。所述术语“杂环烷基”内包括单环4元、5元、6元和7元杂环烷基。杂环烷基可以包括单环或双环(例如具有两个稠合或桥接环)环系统。在一些实施方案中,杂环烷基为具有1、2或3个独立地选自n、s和o的杂原子的单环基团。杂环烷基的成环碳原子和杂原子可以任选地氧化以形成氧代或硫离子基或其他氧化键(例如c(o)、s(o)、c(s)或s(o)2、n-氧化物等),或氮原子可以季铵化。杂环烷基可以经由成环碳原子或成环杂原子而连接。
136、本技术的化合物可以通过本领域技术人员所熟知的多种合成方法来制备,包括下面列举的具体实施方式、其与其他化学合成方法的结合所形成的实施方式以及本领域技术上人员所熟知的等同替换方式,优选的实施方式包括但不限于本技术的实施例。本技术具体实施方式的化学反应是在合适的溶剂中完成的,所述的溶剂须适合于本技术的化学变化及其所需的试剂和物料。为了获得本技术的化合物,有时需要本领域技术人员在已有实施方式的基础上对合成步骤或者反应流程进行修改或选择。
137、本领域合成路线规划中的一个重要考量因素是为反应性官能团(如本技术中的氨基)选择合适的保护基,例如,可参考chem.commun.,2019,55,7331--7334。本技术引用的所有参考文献整体上并入本技术,或者综合使用本领域已知的合成方法和本发明所述方法。每步反应所得的产物用本领域已知的分离技术得到,包括但不限于萃取、过滤、蒸馏、结晶、色谱分离等。合成所需的起始原料和化学试剂可以根据文献常规合成(如scifinder提供的)或购买。
138、在一些实施方案中,本技术通式(i)的化合物可以由有机合成领域技术人员通过以下路线,用本领域的标准方法来制备:
139、
140、步骤1:式1-a所示化合物与卤代丁二酰亚胺(如nbs)反应,得到式1-b所示化合物;
141、步骤2:式1-b所示化合物与式1-c所示化合物在碱性条件下(如nah)反应,得到式1-d所示化合物;
142、步骤3:式1-d所示化合物在碱性条件下(如lioh)反应,水解得到式1-e所示化合物;
143、步骤4:式1-e所示化合物与式1-f所示化合物,缩合反应得到式1-g所示化合物;
144、步骤5:式1-g所示化合物在碱性条件下(如csco3)反应,偶联得到式1-h所示化合物;
145、步骤6:式1-h所示化合物在酸性条件下(如tfa)反应,水解得到式1-i所示化合物;
146、步骤7:式1-i所示化合物在碱性条件下(如pyridine)反应,得到式1-j所示化合物;
147、步骤8:式1-j所示化合物与式1-k所示化合物在路易斯酸条件下(如alcl3)反应,得到式1-l所示化合物;
148、步骤9:式1-l所示化合物与式1-m所示化合物,缩合反应得到式1-n所示化合物;
149、步骤10:式1-n所示化合物在碱性条件下(如k2co3)反应,水解得到式1所示化合物;
150、其中,r3和r4的定义如本发明所述。
151、本发明还提供了一种药物组合物,其包含上述式(ⅰ)、(ⅱ-1)、(ⅱ-2)、(ⅱ-3)、(ⅱ-4)、(ⅱ-5)、(ⅱ-6)、(ⅱ-7)、(ⅱ-8)、(ⅱ-9)、(ⅱ-10)、(ⅲ-1)、(ⅲ-2)、(ⅲ-3)、(ⅲ-4)、(ⅲ-5)、(ⅲ-6)、(ⅲ-7)、(ⅲ-8)、(ⅲ-9)、(ⅲ-10)、(iv-1)、(iv-2)、(iv-3)、(iv-4)、(iv-5)、(iv-6)、(iv-7)、(iv-8)、(iv-9)、(iv-10)、(iv-11)、(v-1)、(ⅵ-1)、(ⅵ-2)、(ⅵ-3)、(ⅵ-4)、(ⅵ-5)、(ⅰa)、(ⅰa-1)、(ⅰa-2)、(ⅰa-3)或(ⅰa-4)所示的化合物、其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体和药学上可接受的辅助性成分。
152、本发明还提供了上述式(ⅰ)、(ⅱ-1)、(ⅱ-2)、(ⅱ-3)、(ⅱ-4)、(ⅱ-5)、(ⅱ-6)、(ⅱ-7)、(ⅱ-8)、(ⅱ-9)、(ⅱ-10)、(ⅲ-1)、(ⅲ-2)、(ⅲ-3)、(ⅲ-4)、(ⅲ-5)、(ⅲ-6)、(ⅲ-7)、(ⅲ-8)、(ⅲ-9)、(ⅲ-10)、(iv-1)、(iv-2)、(iv-3)、(iv-4)、(iv-5)、(iv-6、(iv-7)、(iv-8)、(iv-9)、(iv-10)、(iv-11)、(v-1)、(ⅵ-1)、(ⅵ-2)、(ⅵ-3)、(ⅵ-4)、(ⅵ-5)、(ⅰa)、(ⅰa-1)、(ⅰa-2)、(ⅰa-3)或(ⅰa-4)所示的化合物、其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体或上述的药物组合物在制备用于抗hbv感染的药物中的用途。
153、本发明还提供了抗hbv感染的方法,向有需要的患者施用上述式(ⅰ)、(ⅱ-1)、(ⅱ-2)、(ⅱ-3)、(ⅱ-4)、(ⅱ-5)、(ⅱ-6)、(ⅱ-7)、(ⅱ-8)、(ⅱ-9)、(ⅱ-10)、(ⅲ-1)、(ⅲ-2)、(ⅲ-3)、(ⅲ-4)、(ⅲ-5)、(ⅲ-6)、(ⅲ-7)、(ⅲ-8)、(ⅲ-9)、(ⅲ-10)、(iv-1)、(iv-2)、(iv-3)、(iv-4)、(iv-5)、(iv-6、(iv-7)、(iv-8)、(iv-9)、(iv-10)、(iv-11)、(v-1)、(ⅵ-1)、(ⅵ-2)、(ⅵ-3)、(ⅵ-4)、(ⅵ-5)、(ⅰa)、(ⅰa-1)、(ⅰa-2)、(ⅰa-3)或(ⅰa-4)所示的化合物、其前药、溶剂合物、晶型、药学上可接受的盐、立体异构体或互变异构体或上述的药物组合物。
154、本发明的有益效果:
155、本发明提供的化合物和药物组合物显示出良好的抗hbv感染活性,能够作为与该作用有关的疾病的预防和/或改善和/或治疗有关的药物。
- 还没有人留言评论。精彩留言会获得点赞!