烯还原酶、酶制剂、核酸、表达载体、制备方法与应用
本发明涉及蛋白修饰,特别涉及一种烯还原酶。同时,本发明还涉及一种含烯还原酶的酶制剂和编码上述烯还原酶的核酸,以及上述烯还原酶的表达载体、制备方法和应用。
背景技术:
1、手性α-芳甲基环羰基化合物,如酮、内酰胺和内酯,是合成药物、生物活性分子和天然产物的重要基础。目前的合成方法是以化学催化为主,这些方法虽然有效,但在绿色和可持续化学方面仍存在一些缺点。生物催化已成为高效、选择性和可持续合成的一种环境友好型替代方法,然而,遗憾的是,芳基取代的外环c=c双键的生物还原尚未见报道,因此,我们设想利用烯还原酶(er)催化共轭c=c双键的立体选择性还原来填补这一空白,提供一种理想的绿色合成途径。
2、具有一个或者多个手性中心的α-手性环酮类化合物是生物活性分子、药物以及天然产物合成的重要砌块,在制药和精细化工行业具有重要应用价值。α,β-不饱和共轭烯酮的不对称氢化反应是制备这类高附加值化合物的各种合成方法中最有效、最经济和最环保的方法之一,这些过程通常依靠手性配体辅助的过渡金属催化(特别是铑、钌和铱)。不对称氢化反应中常用的环状底物有两种:环外双键共轭烯酮和环内双键共轭烯酮。近年来,利用多种配体和金属催化剂,许多具有挑战性的环外双键共轭烯酮已被成功研究。
3、化学催化虽然在工业生产手性化合物中具有很多优势,但是也存在很多问题,包括催化剂价格高昂且反应过程不够绿色,反应条件苛刻,催化剂与产物分离困难等问题。相比之下,生物催化可以有效地克服这些缺点。多种生物酶催化手性化合物的合成已取得重要进展。其中,烯还原酶催化不对称反应以辅酶nad(p)h以及溶液中的质子作为氢供体,将α,β-不饱和酮还原成α,β-手性酮,理论上没有副产物产生,引起了广泛关注。
4、老黄酶是烯还原酶的一种,是一类nad(p)h依赖型的氧化还原酶,1932年warburg和christian从啤酒酵母中首次发现并报道,随后的研究表明老黄酶属于一种带有黄素单核苷酸辅基的氧化还原酶,能够不对称催化c=c键还原,理论上最多可以产生2个手性中心。其反应过程需要辅酶nad(p)h的参与,又被称为烯还原酶,可以不对称催化包括α,β不饱和醛、酮、羧酸及其衍生物(如酯类、内酯类、环状酰亚胺类)、腈类和硝基化合物。但是烯还原酶底物谱较窄,底物通常局限于小分子化合物。因此发展有效的方法解决上述问题具有重要意义。
技术实现思路
1、有鉴于此,本发明旨在提出一种烯还原酶,以使其可以催化外环α、β-不饱和羰基化合物(包括酮、内酯和内酰胺)底物的立体异构还原,不对称还原反应合成手性α-芳基甲基环羰基化合物。
2、为达到上述目的,本发明的技术方案是这样实现的:
3、本发明的第一方面,提供了一种烯还原酶,对如seq id no:2的烯还原酶进行突变而获得,所述突变包含seq id no:2第26、28、69、169位氨基酸中至少一个突变。
4、本发明的烯还原酶,可应用在催化外环α、β-不饱和羰基化合物(包括酮、内酯和内酰胺)发生不对称立体异构还原反应制备手性α-芳基甲基环羰基化合物。本发明所述的烯还原酶具有较高的还原活性和更广泛的底物特异性,满足高产率(高达98%)和α-碳优异对映选择性(92-99%ee)的要求,从而拓宽了er催化有机合成的范围。
5、优选的,所述的手性α-芳基甲基环羰基化合物包括但不限于:
6、r/s:2-苄基-1-环戊酮、2-(2-甲基苄基)-1-环戊酮、2-(3-甲基苄基)-1-环戊酮、2-(4-甲基苄基)-1-环戊酮、2-(4-氯苄基)-1-环戊酮、2-(2-溴苄基)-1-环戊酮、2-(4-溴苄基)-1-环戊酮、2-(2-甲氧基苄基)-1-环戊酮、2-(3-甲氧基苄基)-1-环戊酮、2-(4-甲氧基苄基)-1-环戊酮、2-(4-乙基苄基)-1-环戊酮、2-(2-硝基苄基)-1-环戊酮、3-苯基-1-环戊酮
7、r/s:2-苄基-1-环己酮、2-(4-甲基苄基)-1-环己酮、2-(4-硝基苄基)-1-环己酮、3-苯基-1-环己酮、3-苄基四氢-4h-吡喃-4-酮、2-(2-甲基苄基)-1-环庚酮、2-(3-甲基苄基)-1-环庚酮、2-(2-氟苄基)-1-环庚酮、2-(4-氯苄基)-1-环庚酮、2-(3-溴苄基)-1-环庚酮、2-(4-(三氟甲基)苄基)-1-环庚酮。
8、优选的,所述的潜手性外环α、β-不饱和羰基化合物包括但不限于:
9、2-(e)-亚苄基-1-环戊酮、2-(e)-(2-甲基亚苄基)-1-环戊酮、2-(e)-(3-甲基亚苄基)-1-环戊酮、2-(e)-(4-甲基亚苄基)-1-环戊酮、2-(e)-(4-氯亚苄基)-1-环戊酮、2-(e)-(2-溴亚苄基)-1-环戊酮、2-(e)-(4-溴亚苄基)-1-环戊酮、2-(e)-(2-甲氧基亚苄基)-1-环戊酮、2-(e)-(3-甲氧基亚苄基)-1-环戊酮、2-(e)-(4-甲氧基亚苄基)-1-环戊酮、2-(e)-(4-乙基亚苄基)-1-环戊酮、2-(e)-(2-硝基亚苄基)-1-环戊酮、3-苯基-1-环戊酮;
10、2-(e)-亚苄基-1-环己酮、2-(e)-(4-甲基亚苄基)-1-环己酮、2-(e)-(4-硝基亚苄基)-1-环己酮、3-苯基-1-环己酮、3-(e)-苄基四氢-4h-吡喃-4-酮、2-(e)-(2-甲基亚苄基)-1-环庚酮、2-(e)-(3-甲基亚苄基)-1-环庚酮、2-(e)-(2-氟亚苄基)-1-环庚酮、2-(e)-(4-氯亚苄基)-1-环庚酮、2-(e)-(3-溴亚苄基)-1-环庚酮、2-(e)-(4-(三氟甲基)亚苄基)-1-环庚酮。
11、进一步的,所述突变包含seq id no:2的下列突变中的至少一种:
12、a):第26位由c突变为g、a和f中的任一种;
13、b):第28位由y突变为a、i、v和f中的任一种;
14、c):第69位由i突变为20种氨基酸的任一种;
15、d):第169位由y突变为f。
16、具体来说,符合上规则所述的突变形式,均是可行的,本发明列举以下部分形式仅做示例性说明,包含由seq id no:2序列进行的下列突变(a1)-(a29)中的至少一种:
17、(a1)seq id no:2第69位氨基酸残基由i突变为w;
18、(a2)seq id no:2第69位氨基酸残基由i突变为c;
19、(a3)seq id no:2第69位氨基酸残基由i突变为m;
20、(a4)seq id no:2第69位氨基酸残基由i突变为d;
21、(a5)seq id no:2第69位氨基酸残基由i突变为r;
22、(a6)seq id no:2第69位氨基酸残基由i突变为n;
23、(a7)seq id no:2第69位氨基酸残基由i突变为h;
24、(a8)seq id no:2第69位氨基酸残基由i突变为e;
25、(a9)seq id no:2第69位氨基酸残基由i突变为k;
26、(a10)seq id no:2第69位氨基酸残基由i突变为p;
27、(a11)seq id no:2第69位氨基酸残基由i突变为q;
28、(a12)seq id no:2第69位氨基酸残基由i突变为s;
29、(a13)seq id no:2第69位氨基酸残基由i突变为t;
30、(a14)seq id no:2第69位氨基酸残基由i突变为l;
31、(a15)seq id no:2第69位氨基酸残基由i突变为f;
32、(a16)seq id no:2第69位氨基酸残基由i突变为a;
33、(a17)seq id no:2第69位氨基酸残基由i突变为v;
34、(a18)seq id no:2第69位氨基酸残基由i突变为g;
35、(a19)seq id no:2第69位氨基酸残基由i突变为y;
36、(a20)seq id no:2第26位氨基酸残基由c突变为f;
37、(a21)seq id no:2第28位氨基酸残基由y突变为a;
38、(a22)seq id no:2第169位氨基酸残基由y突变为f;
39、(a23)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为a;
40、(a24)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g;
41、(a25)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g,且第169位氨基酸残基由y突变为f;
42、(a26)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g,且第28位氨基酸残基由y突变为a;
43、(a27)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g,且第28位氨基酸残基由y突变为i;
44、(a28)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g,且第28位氨基酸残基由y突变为v;
45、(a29)seq id no:2第69位氨基酸残基由i突变为y,且第26位氨基酸残基由c突变为g,且第28位氨基酸残基由y突变为f。
46、本发明的第二方面,本发明提出了一种酶制剂,所述的酶制剂包括如上所述的烯还原酶。
47、本发明的第三方面,提供了一种编码如上所述的烯还原酶的核酸。
48、进一步的,所述的核酸为对seq id no:1的核苷酸序列进行下列至少一种突变而获得:
49、a):76-78位核苷酸由tgc突变为gca;
50、b):76、78位核苷酸由t、c突变为g、a;
51、c):77位核苷酸由g突变为t;
52、d):82-84位核苷酸由tat突变为gca或gta;
53、e):83-84位核苷酸由at突变为ca或tc;
54、f):206-207位核苷酸由ca突变为gg、gc、tc、ac;
55、g):205-207位核苷酸由tca突变为atg、gac、aac、cac、cag、agc、ctg;
56、h):205-206位核苷酸由tc突变为cg、ga、aa、gt、gg;
57、i):205位核苷酸由t突变为c、a、g;
58、j)506位核苷酸由a突变为t。
59、也就是说,所述的核酸为对seq id no:1的核苷酸序列进行a)-j)中任一种突变,或突变中任意多种突变的组合,如其可为任两种、三种、四种或多种突变的组合。
60、符合上规则所述的seq id no:1突变形式,均是可行的,本发明列举以下部分形式,仅做示例性说明,例如可为下述的突变:
61、(1)seq id no:1第77位核苷酸由g突变为t;
62、(2)seq id no:1第206-207位核苷酸由ca突变为gg;
63、(3)seq id no:1第206-207位核苷酸由ca突变为gc;
64、(4)seq id no:1第206-207位核苷酸由ca突变为tc;
65、(5)seq id no:1第206-207位核苷酸由ca突变为ac;
66、(6)seq id no:1第205-207位核苷酸由tca突变为atg;
67、(7)seq id no:1第205-207位核苷酸由tca突变为gac;
68、(8)seq id no:1第205-207位核苷酸由tca突变为aac;
69、(9)seq id no:1第205-207位核苷酸由tca突变为cac;
70、(10)seq id no:1第205-207位核苷酸由tca突变为cag;
71、(11)seq id no:1第205-207位核苷酸由tca突变为agc;
72、(12)seq id no:1第205-207位核苷酸由tca突变为ctg;
73、(13)seq id no:1第205-206位核苷酸由tc突变为cg;
74、(14)seq id no:1第205-206位核苷酸由tc突变为ga;
75、(15)seq id no:1第205-206位核苷酸由tc突变为aa;
76、(16)seq id no:1第205-206位核苷酸由tc突变为gt;
77、(17)seq id no:1第205-206位核苷酸由tc突变为gg;
78、(18)seq id no:1第205位核苷酸由t突变为c;
79、(19)seq id no:1第205位核苷酸由t突变为a;
80、(20)seq id no:1第205位核苷酸由t突变为g;
81、(21)seq id no:1第82-84位核苷酸由tat突变为gta;
82、(22)seq id no:1第506位核苷酸由a突变为t;
83、(23)seq id no:1第206-207位核苷酸由ca突变为ac,且第76-78位核苷酸由tgc突变为gca;
84、(24)seq id no:1第206-207位核苷酸由ca突变为ac,且第76、78位核苷酸由t、c突变为g、a;
85、(25)seq id no:1第206-207位核苷酸由ca突变为ac,第76、78位核苷酸由t、c突变为g、a,且第506位核苷酸由a突变为t;
86、(26)seq id no:1第206-207位核苷酸由ca突变为ac,第76、78位核苷酸由t、c突变为g、a,且第82-84位核苷酸由tat突变为gca;
87、(27)seq id no:1第206-207位核苷酸由ca突变为ac,第76、78位核苷酸由t、c突变为g、a,且第82-84位核苷酸由tat突变为gta;
88、(28)seq id no:1第206-207位核苷酸由ca突变为ac,第76、78位核苷酸由t、c突变为g、a,且第83-84位核苷酸由at突变为ca;
89、(29)seq id no:1第206-207位核苷酸由ca突变为ac,第76、78位核苷酸由t、c突变为g、a,且第83-84位核苷酸由at突变为tc;
90、本发明的第四方面,提供了一种包含如上所述的核酸的表达载体。
91、优选的,所述表达载体为pet-28b。
92、本发明的第五方面,提供了一种所述的烯还原酶的制备方法,所述的制备方法包括将编码所述的烯还原酶的核酸导入细胞中,培养该细胞,获得所述烯还原酶。
93、进一步的,该方法包括以下步骤:将编码烯还原酶的核酸导入宿主菌体细胞;单菌落培养,种子液培养,扩大培养;破碎所述菌体,得到菌体破碎液;将所述菌体破碎液离心取上清,得到烯还原酶。
94、优选的,所述宿主菌包括大肠杆菌,具体可为大肠杆菌bl21(de3)。优选的,所述的核酸可通过表达载体导入所述宿主菌。
95、本发明上述的制备方法具体可以包括如下步骤:
96、将编码烯还原酶的核酸导入宿主菌体细胞:取低温储存的感受态细胞,然后加入目的dna,混匀后冰浴30min,再42℃热激40s,再冰浴2min,最后向管中加入500微升无菌lb培养基,于37度培养1h使细菌复苏。
97、单菌落培养:取导入核酸的感受态细胞加到含卡那霉素的lb琼脂培养基上,均匀涂开,在平板中于37℃培养12h。
98、种子液培养:将单菌落接种于10ml lb液体培养基中,所述培养基中含有终浓度50μg/ml卡那霉素,37℃、180rpm振荡过夜培养12-16h。
99、扩大培养:将种子液接种到50ml的tb培养基中(接种量1%),所述培养基中含有终浓度50μg/ml卡那霉素,37℃、180rpm振荡培养至菌液od6000.6-0.8,加入终浓度0.1mm的iptg,继续20℃、180rpm振荡培养20h,5000rcf离心10min收集菌体。
100、破碎菌体的方法为:将所述重组菌菌体采用50mm ph=8.050m的pbs洗涤、重悬3次,重悬后利用匀浆机破碎,12000rpm离心15min,收集上清即为粗酶液。
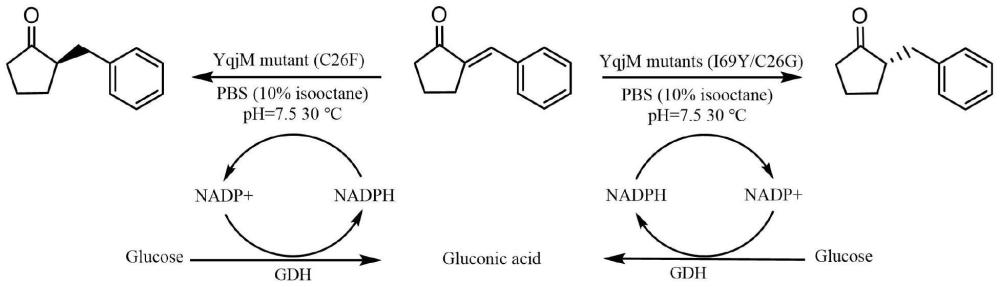
101、采用本发明的烯还原酶的制备方法所获得的烯还原酶,可以将活性较低的不对称催化c=c键还原烯醇(er)还原酶改造为高活性高底物范围,可以实现催化外环α、β-不饱和羰基化合物不对称合成r/s两种构型的烯还原酶(yqim)。利用烯还原酶(yqim)催化共轭c=c双键的立体选择性还原,将α、β-不饱和酮还原成α、β-手性酮,理论上没有副产物产生,具有绿色高效、成本低及产物光学纯度高的优点,提供一种理想的绿色合成途径。
102、本发明的第六方面,提供了所述烯还原酶的应用,其用于制备式ⅱ、ⅲ所示的化合物,所述化合物的制备方法包括以式i为底物在所述的烯还原酶催化下获得;
103、
104、
105、其中,
106、n=0、1、2;
107、x代表o、n、c中的任一种;
108、r1代表甲基、f基、br基、cl基、甲氧基、乙基、硝基、三氟甲基基团中的任意一种。
- 还没有人留言评论。精彩留言会获得点赞!