一种低氧培养用于血管修复的特络细胞及其制备方法与流程
本发明涉及一种用于血管修复的细胞及其培养方法,具体地,涉及一种低氧培养用于血管修复的特络细胞及其制备方法。
背景技术:
1、特络细胞telocyte(tcs)是一种新的间质细胞类型,表达cd34、c-kit、vimentin,对与免疫细胞间质类干细胞生长有支持与调节作用,对于成纤维细胞可以提供网状结构支撑,并且能够分泌多种生长因子,促进细胞生长,具有组织修复与免疫调节作用。肺tcs广泛于肺泡间质、小血管、小气道平滑肌层,表达血管内皮生长因子(vascular endothelialgrowth factor,vegf),参与血管和气血屏障形成。tcs能分泌更多的修复相关细胞因子如egf、vegf,gm-csf、hgf、fgf及炎症调节相关因子igf-1、tgf-β等,肺tcs表达血管内皮生长因子(vascular endothelial growth factor,vegf)并参与血管和气血屏障形成。在将人肺tcs条件培养基与lps损伤后的人肺微血管内皮细胞共同培养时,tcs所产生的vegf和表皮生长因子(epidermal growth factor,egf)等可显著促进人肺微血管再生。
2、hmgb-1是在组织损伤信号传导中重要的炎性介质,在衰老细胞中,hmgb-1从细胞核转移到细胞质和细胞外间隙,促进il-1β、il-6和mmp3等炎症因子的释放。前期研究发现缺氧培养条件下传代10代以上的tcs出核的hmgb-1明显低于正常培养的tcs。说明缺氧条件可以大大减缓tcs多次传代的衰老进程。
3、特络细胞几乎存在于人体各种组织器官当中,但由于其在各组织中的含量极低,细胞获取困难,且扩增起来难度较大。目前的技术大多在于分离小鼠器官组织中tc细胞作为研究,或者是将人肺组织中tcs分离出来后进行永生化处理,且需要运用胎牛血清培养才能大量扩增出用于研究的tcs细胞。而且,目前已经建立的tcs细胞系存在扩增速度慢,易老化,传几十代后表面标记物丢失的现象,同时旁分泌因子的浓度也十分有限不利于临床应用。
技术实现思路
1、本发明的目的是提供一种用于血管修复的特络细胞及其制备方法,能够解决现有技术中存在的问题,开发出最适合tcs生长的低氧培养体系,为tcs更安全更高效的应用于临床奠定坚实的基础。
2、为了达到上述目的,本发明提供了一种低氧培养用于血管修复的特络细胞的制备方法,其中,该方法包含:步骤1,提取原代特络细胞,建立种子库;步骤2,复苏特络细胞的种子细胞,通过实验确定缺氧的培养条件;步骤3,通过实验确定,特络细胞能够长时间在缺氧条件下培养;步骤4,通过所确定的条件对特络细胞进行低氧培养;步骤5,验证低氧培养的特络细胞的功能。
3、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤2中,包含:步骤2.1,复苏特络细胞的种子细胞,在正常氧含量,即o2浓度为21%、co2浓度为5%、温度为37℃的条件下培养细胞静置过夜;步骤2.2,将步骤2.1培养的细胞平均分为若干组,分别在正常氧含量和不同的低氧含量下培养,并每天进行细胞计数和形态观测;步骤2.3,在培养的第5天,通过elisa检测上清中的若干因子;步骤2.4,在培养10天后,通过流式破膜染色检测衰老相关蛋白hmgb-1出核情况;步骤2.5,确定缺氧的培养条件。
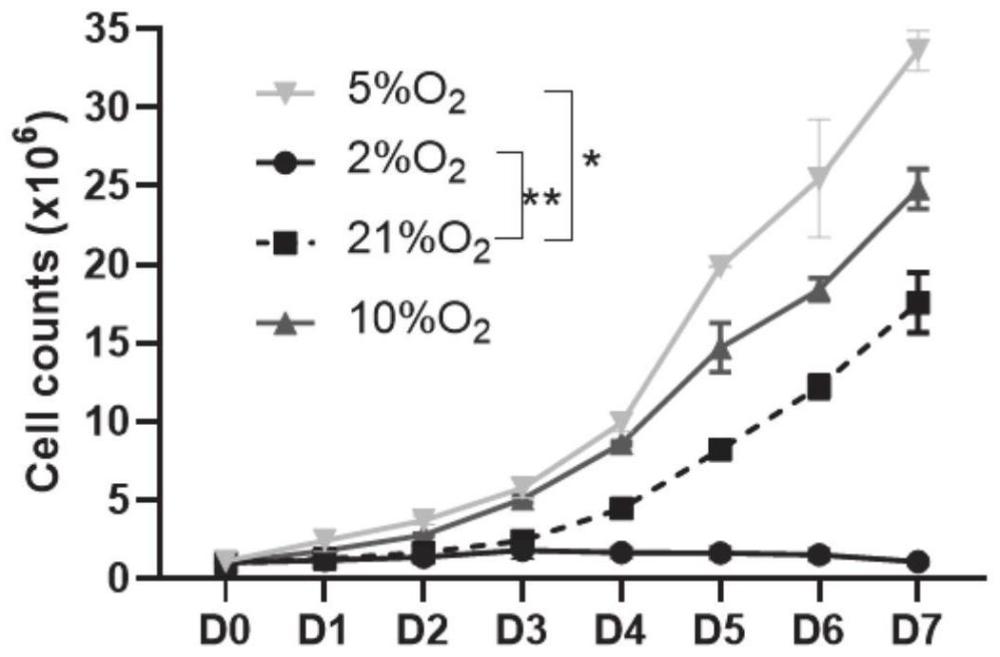
4、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤2.2中,将细胞分别在o2浓度为21%、10%、5%、2%的条件下培养;通过细胞状态观测,确定o2浓度为5%的细胞状态、折光度、饱满度均好于正常氧含量下培养的细胞;通过细胞计数,确定低氧条件下,除o2浓度为2%的一组外,细胞增殖能力均有提升,o2浓度为5%的细胞增殖最快。
5、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤2.3中,通过elisa检测,确定在o2浓度为5%的条件下培养的特络细胞上清中的各因子,特别是vegf的增长幅度显著大于其它低氧培养组。
6、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤2.4中,确定低氧条件下,除o2浓度为2%的一组外,其余组的hmgb-1出核情况均少于正常氧含量下培养的对照组,o2浓度为5%的细胞hmgb-1出核的占比最少。
7、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤2.5中,确定缺氧的培养条件是o2浓度为5%。
8、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤3中,包含:步骤3.1,复苏特络细胞的种子细胞,平均分为若干组,分别在正常氧含量,即o2浓度为21%,和低氧条件,包括o2浓度为5%下培养细胞;步骤3.2,分别记录每组在培养的3天、7天、2周、3周,以及1个月的细胞增殖总数;步骤3.3,通过流式检测每组细胞第1代和第10代的表面标记,o2浓度为21%的对照组在第10代时cd34与pdgfrα表达均减弱,o2浓度为5%的实验组表性表达均稳定;步骤3.4,通过elisa检测每组细胞第10代衰老相关炎症因子il-6、il-1β、mmp3及tnf-α的表达,o2浓度为5%的实验组培养到第10代时炎症因子的分泌均低于对照组,il-6与mmp3的表达差异特别显著,证明特络细胞能长期在5%的低氧含量的培养环境中培养,并保持其优势稳定优于正常培养环境中的对照组。
9、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤5中,包含:步骤5.1,复苏脐带血管内皮细胞,接种于经过组织培养表面处理的12孔板里;步骤5.2,配制基质胶;步骤5.3,在细胞融合度达到70%-80%时,将置于碎冰上并在4℃过夜融化后的基质胶通过涡旋振荡的方式,保证胶液处于均匀的状态,再将基质胶向孔板中添加;步骤5.4,使用胰酶消化细胞,同时在显微镜下观察,当细胞变圆时及时终止消化,基质胶上接种的细胞数量为3万个/孔;步骤5.5,收集培养5天后的细胞上清,分别加入正常氧含量下培养的特络细胞上清、5%的低氧含量下培养的特络细胞上清,以及空白培养基作为对照,每4个小时观察一次成管情况,72小时后记录成管情况。
10、上述的低氧培养用于血管修复的特络细胞的制备方法,其中,所述的步骤5.5中,成管最好的是o2浓度为5%的低氧培养组,成管分支点数量明显多于其它组,证明5%的低氧培养显著加强了特络细胞促进血管生成与修复的功能。
11、本发明还提供了上述的低氧培养用于血管修复的特络细胞的制备方法培养的特络细胞。
12、本发明提供的低氧培养用于血管修复的特络细胞及其制备方法具有以下优点:
13、本发明首次将固定低氧含量的培养体系应用于tcs细胞,并发现能快速提升tcs细胞扩增速度的同时大大增强其旁分泌与血管吸附功能,同时大大延缓了多次传代中的细胞衰老现象,通过非基因编辑改造手段实现tcs快速高效扩增且不衰老,保持表型稳定的同时大大提升其功能,为tcs更安全更高效的应用于临床奠定了坚实基础。
技术特征:
1.一种低氧培养用于血管修复的特络细胞的制备方法,其特征在于,该方法包含:
2.如权利要求1所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤2中,包含:
3.如权利要求2所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤2.2中,将细胞分别在o2浓度为21%、10%、5%、2%的条件下培养;通过细胞状态观测,确定o2浓度为5%的细胞状态、折光度、饱满度均好于正常氧含量下培养的细胞;通过细胞计数,确定低氧条件下,除o2浓度为2%的一组外,细胞增殖能力均有提升,o2浓度为5%的细胞增殖最快。
4.如权利要求2所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤2.3中,通过elisa检测,确定在o2浓度为5%的条件下培养的特络细胞上清中的各因子,特别是vegf的增长幅度显著大于其它低氧培养组。
5.如权利要求2所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤2.4中,确定低氧条件下,除o2浓度为2%的一组外,其余组的hmgb-1出核情况均少于正常氧含量下培养的对照组,o2浓度为5%的细胞hmgb-1出核的占比最少。
6.如权利要求2所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤2.5中,确定缺氧的培养条件是o2浓度为5%。
7.如权利要求1所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤3中,包含:
8.如权利要求1所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤5中,包含:
9.如权利要求8所述的低氧培养用于血管修复的特络细胞的制备方法,其特征在于,所述的步骤5.5中,成管最好的是o2浓度为5%的低氧培养组,成管分支点数量明显多于其它组,证明5%的低氧培养显著加强了特络细胞促进血管生成与修复的功能。
10.一种如权利要求1~9中任意一项所述的低氧培养用于血管修复的特络细胞的制备方法培养的特络细胞。
技术总结
本发明公开了一种低氧培养用于血管修复的特络细胞及其制备方法,该方法包含:步骤1,提取原代特络细胞,建立种子库;步骤2,复苏特络细胞的种子细胞,通过实验确定缺氧的培养条件;步骤3,通过实验确定,特络细胞能够长时间在缺氧条件下培养;步骤4,通过所确定的条件,即O<subgt;2</subgt;浓度为5%,对特络细胞进行低氧培养;步骤5,验证低氧培养的特络细胞的功能。本发明还提供了该方法制备的用于血管修复的特络细胞。本发明首次将固定低氧含量的培养体系应用于TCs细胞,以非基因编辑改造手段实现TCs快速高效扩增且不衰老,保持表型稳定的同时大大提升其功能,为TCs更安全更高效的应用于临床奠定了坚实基础。
技术研发人员:高戎戎,陈旭文,张煦,顾文文,王鑫,张幼麟
受保护的技术使用者:上海迈惠生物科技有限公司
技术研发日:
技术公布日:2024/3/27
- 还没有人留言评论。精彩留言会获得点赞!