一种抗VEGF和补体双功能融合蛋白及其应用的制作方法
本发明属于生物医药领域,涉及一种抗vegf和补体双功能融合蛋白及其应用。
背景技术:
1、年龄相关性黄斑变性(age-related macular degeneration,amd)是65岁以上患者视力损害的主要原因,全世界有1.96亿人患有amd,预计到2040年将增至2.88亿人。amd可分为两种类型:干性amd(非血管性, damd)和新生血管性amd(namd)。在干性amd的早期阶段,存在慢性低水平炎症、视网膜下间隙的玻璃体疣沉积、黄斑部视网膜色素上皮(rpe)和光感受器的不可逆性丧失,以及随后进行性的中央视力丧失。在干性amd的晚期,视网膜色素上皮变性变得融合,视力丧失恶化,称为地图样萎缩(geographic atrophy,ga)。在大约10%的患者中,amd可进展为更具攻击性的namd,该疾病与中心视力的快速丧失有关,其特征是异常的脉络膜血管生长进入黄斑,称为脉络膜新生血管(choroidal neovasculation,cnv)。这些血管“渗漏”,并且有过多的瘢痕组织。
2、amd的发病机制复杂,据文献报道,相关的信号通路主要包括血管新生相关通路(vegf、pdgf、fgf等)、补体相关通路(c3、c5等)、纤维化相关通路(fgf、tgfβ等)和免疫炎症因子通路(il-6、tnf-α等)。
3、血管内皮生长因子(vascular endothelial growth factor,vegf)能诱导已有血管的再生(血管再生)或新血管的生长(血管新生),是胚胎发育和血管修复的关键因子。vegf 家族包括 vegf-a、vegf-b、vegf-c、vegf-d、vegf-e 以及胎盘生长因子 1、2(pigf-1、pigf-2)。vegf-a 是迄今最有效且研究最多的血管生长诱导因子。vegf的家族成员由多个外显子编码,选择性剪接后可以产生不同的亚型,从而影响可溶性和受体结合情况。例如,vegf-a有7个亚型,而vegf-b 有2个亚型。vegf的家族成员通过与vegf受体(vegfr)结合,激活信号转导。vegfr为酪氨酸激酶受体,具有由7个免疫球蛋白样(immunoglobulin ,ig)结构域所组成的细胞外区域。vegfr-1(flt-1)结合vegf-a、vegf-b,以及pigf,并可作为vegf的诱饵受体或vegfr-2的调节剂。vegfr-2(kdr/flk-1)结合所有vegf同工型,且为vegf诱导的血管生成通路的主要媒介。vegfr-3(flt-4)结合vegf-c与vegf-d,但不结合vegf-a,是淋巴管生成的主要媒介。
4、补体系统为先天免疫系统的功能性效应子,由多种可溶性蛋白、膜结合蛋白和补体受体组成。补体活化导致一系列蛋白酶活化的级联反应,刺激细胞因子的释放与活化级联反应的放大。补体系统可通过三种不同的途径活化,即典型途径、旁路途径和凝集素途径。这3种途径都通过关键的c3转化酶与c5转化酶复合物,分别裂解补体分子c3与c5。补体活化的最终结果为细胞杀伤膜攻击复合物(membrane attack complex,mac)的活化、刺激免疫细胞释放炎症因子和趋化因子、由过敏毒素c3a与c5a引起的过敏反应,以及病原体的吞噬作用。
5、目前,抗vegf疗法(如贝伐单抗、雷尼单抗和阿柏西普)是唯一经批准上市的治疗namd的标准药物疗法,但是临床上仍有相当一部分患者对抗vegf药物的响应不完全,表现为持续性地渗漏、出血和视力恢复欠佳。此外长期注射抗vegf药物的namd患者中,有超过10%的比例转化为干性amd。在抗vegf药物长期使用的患者中,有超过40%的患者会伴随黄斑萎缩,与干性amd引起的地图样萎缩较为类似。而针对干性amd患者视力丧失的情况,apellis公司的补体因子3抑制剂pegcetacoplan(商品名syfovre)和astellas公司的补体因子5抑制剂avacincaptad pegol(商品名izervay)先后获fda批准上市,但在临床研究中均出现namd发生率增加的情况,在药品说明书中也特别指出了该种风险。本技术预期通过结合抑制vegf及抑制补体通路来进一步解决干性及湿性amd治疗过程中出现的问题。
技术实现思路
1、本发明的目的是提供一种表达量高、活性好、纯度高的抗vegf及补体靶点的双功能性融合蛋白,通过有效地抑制vegf及补体途径,能够治疗多种vegf及补体通路相关的疾病,例如湿性和干性amd,进而解决上述临床治疗过程中出现的问题。结果发现,本发明提供的抗vegf及补体双功能性融合蛋白既体现出更加高效的vegf拮抗活性,同时显著提高了抑制补体溶血活性,在干性和湿性amd动物模型中均体现出更优的药效,同时通过对分子中fc结构域的改造显著提高了分子的稳定性。
2、本发明的技术方案之一,是提供一种双功能性融合蛋白,该融合蛋白包含vegf结合域和补体结合域;
3、进一步地,所述双功能融合蛋白还包含人igg fc结构域;
4、优选地,所述的双功能性融合蛋白包含1-3个vegf结合域,较佳地,包括1个或2个vegf结合域;
5、进一步地,所述vegf结合域选自以下(1)-(4)中的任意一种:
6、(1)所述vegf结合域包含vegf受体1的胞外结构域2(vegfr1d2)和vegf受体2的胞外结构域3(vegfr2d3);
7、(2)所述vegf结合域包含vegf受体1的胞外结构域2(vegfr1d2);
8、(3)所述vegf结合域包含两个vegf受体1的胞外结构域2(vegfr1d2)的串联结构;
9、(4)所述vegf结合域包含衍生自雷尼单抗(ranibizumab)的重链区(heavy chain,hc)和轻链区(light chain,lc)的氨基酸序列;雷尼单抗的重链区(hc)和轻链区(lc)通过自剪切肽连接,包括p2a、t2a、e2a和f2a;或者所述vegf结合域包含衍生自雷尼单抗(ranibizumab)的重链可变区(vh)和轻链可变区(vl)的氨基酸序列;雷尼单抗的重链可变区(vh)和轻链可变区(vl)通过连接肽连接,如(ggggs)n、(gly)6-8和a(eaaak)na等。
10、优选地,所述的双功能性融合蛋白包含1个人igg fc结构域;
11、进一步地,所述人igg fc结构域选自以下(1)-(2)中的任意一种:
12、(1)所述人igg1 fc结构域,包含人igg1 hinge区10-15个氨基酸,ch2结构域和ch3结构域(含或不含末端k);
13、(2)所述人igg fc结构域是经过改造的突变型人iggfc结构域。
14、优选地,所述的双功能性融合蛋白包含1-2个补体结合域,较佳地,包括1个补体结合域;
15、进一步地,所述补体结合域选自以下(1)-(5)中的任意一种:
16、(1)所述补体结合域包含可溶性cd59(soluble cd59,scd59)结构域;
17、(2)所述补体结合域包含衍生自依库珠单抗(eculizumab)的重链可变区(vh)和轻链可变区(vl)的氨基酸序列,vh和vl序列通过(ggggs)3连接肽相连接;
18、(3)所述补体结合域包含衍生自培克珠单抗(pexelizumab)的氨基酸序列;
19、(4)所述补体结合域包含因子h样蛋白1(factor h-like protein1,fhl-1)结构域;
20、(5)所述补体结合域包含因子i蛋白(factor i,fi)结构域。
21、优选地,vegf结合域与人igg fc结构域,补体结合域与人igg fc结构域,vegf结合域与补体结合域之间直接串联或通过连接肽连接;
22、优选地,所述连接肽为(ggggs)n,优选地,n=3-6,更优选地n=3或4;
23、优选地,所述连接肽为kesgsvsseqlaqfrsld或(gly)6-8;
24、优选地,所述连接肽为a(eaaak)na,优选地,n=1-4,更优先地n= 4;优选地,所述连接肽为 (xp)n,x为a或者e或者k,n=5-10;
25、更优选地,所述双功能性融合蛋白包含vegf结合域、经过改造的人igg fc结构域和补体结合域。所述vegf结合域包含vegf受体1的胞外结构域2(vegfr1d2)和vegf受体2的胞外结构域3(vegfr2d3);所述经过改造的人igg fc结构域包含1-3个位点的氨基酸突变,更具体地,所采用的点突变为l234a/l235a/h435a(氨基酸编号由kabat中的eu索引指示);所述补体结合域包含可溶性cd59结构域结构(scd59)。所述vegf结合域与经过改造的人iggfc结构域(mhigg fc)直接连接,所述经过改造的人igg fc结构域和补体结合域(scd59)通过连接肽(ggggs)3连接。所述双功能性融合蛋白结构为:vegfr1d2-vegfr2d3-mhigg fc-(ggggs)3-scd59,氨基酸序列如seq id no.1所示:
26、sdtgrpfvemyseipeiihmtegrelvipcrvtspnitvtlkkfpldtlipdgkriiwdsrkgfiisnatykeiglltceatvnghlyktnylthrqtntiidvvlspshgielsvgeklvlnctartelnvgidfnweypsskhqhkklvnrdlktqsgsemkkflstltidgvtrsdqglytcaassglmtkknstfvrvhekdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnaytqkslslspgggggsggggsggggslqcyncpnptadcktavncssdfdaclitkaglqvynkcwkfehcnfndvttrlreneltyycckkdlcnfneqlen;
27、上述加粗氨基酸为人igg fc结构域突变位点;
28、进一步地,所述双功能性融合蛋白vegfr1d2-vegfr2d3-mhigg fc-(ggggs)3-scd59的编码基因如seq id no.7所示。
29、更优选地,所述双功能性融合蛋白包含vegf结合域、经过改造的人igg fc结构域和补体结合域;所述vegf结合域包含vegf受体1的胞外结构域2(vegfr1d2);所述经过改造的人igg fc结构域包含1-3个位点的氨基酸突变,更具体地,所采用的点突变为l234a/l235a/h435a(氨基酸编号由kabat中的eu索引指示);所述补体结合域包含可溶性cd59结构域结构scd59;所述vegf结合域与经过改造的人igg fc结构域(mhigg fc)直接连接,所述经过改造的人igg fc结构域和补体结合域(scd59)通过连接肽(ggggs)3连接。所述双功能性融合蛋白结构为:vegfr1d2-mhigg fc-(ggggs)3-scd59,氨基酸序列如seq id no.2所示:
30、sdtgrpfvemyseipeiihmtegrelvipcrvtspnitvtlkkfpldtlipdgkriiwdsrkgfiisnatykeiglltceatvnghlyktnylthrqtntiidkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnaytqkslslspgggggsggggsggggslqcyncpnptadcktavncssdfdaclitkaglqvynkcwkfehcnfndvttrlreneltyycckkdlcnfneqlen;
31、上述加粗氨基酸为人igg fc结构域突变位点;
32、进一步地,所述双功能性融合蛋白vegfr1d2-mhigg fc-(ggggs)3-scd59的编码基因如seq id no.8所示。
33、本发明的技术方案之二,是提供一种技术方案一所述双功能性融合蛋白的编码基因。
34、本发明的技术方案之三,是提供一种表达技术方案一所述双功能性融合蛋白的表达盒或重组载体,所述表达盒从5’-3’端包括如下式i所述结构:
35、e1-e2-e3-e4 (式i)
36、其中:
37、e1为启动子;
38、e2为信号肽;
39、e3为编码技术方案一所述双功能性融合蛋白的核苷酸序列;
40、e4为poly a序列。
41、优选地,所述启动子是可以启动目的基因转录的dna序列,该序列可以被rna聚合酶所识别,并开始转录合成rna。所述启动子包括但不限于天然、优化或组合启动子;
42、更进一步地,所述启动子优选cmv、cba、ef1a、sv40、pgk1、ubc、cag或minicag;
43、优选地,所述信号肽为human osm、gaussia luc、human il-2或者albumin (hsa);
44、优选地,所述poly a序列选自bgh polya、sv40 polya、hsv-tk polya或hghpolya;
45、进一步地,上述表达盒还包括调节元件,所述表达调控元件包括但不限于以下功能的调控元件:(1)增强子,增强子可以来自sv40病毒,cmv病毒或腺病毒等;(2)用于表达mirna和sirna序列的调控元件;(3)内含子;(4)调控元件还可以是部分的kozak序列,kozak序列为gncncn,例如gccacc等;(5)调控元件可以是wpre。
46、优选地,将所述双功能性融合蛋白表达盒,连接至瞬时转染载体;通过转染试剂将载体导入宿主细胞,表达所述双功能性融合蛋白。
47、进一步地,所述瞬时转染载体包括但不限于ptt5、pcdna3.1(-)、pcdna3.1(+)、ppiczαa、pgapzαa和pyes2.0等;优选地,瞬时转染载体为ptt5。
48、进一步地,所用的转染试剂包括lipo2000、lipo3000、pei、293fectin™、cellfectin、磷酸钙等;优选地,转染试剂为pei。
49、进一步地,本发明还提供一种表达技术方案一所述双功能融合蛋白的重组宿主细胞,所述重组宿主细胞包含技术方案二所述编码基因、或技术方案三所述表达盒或重组载体,所述重组宿主细胞所用的宿主细胞包括原核细胞或真核细胞;优选地,宿主细胞选自大肠杆菌、酵母细胞或哺乳动物细胞;更优选地,宿主细胞为expi293细胞。
50、本发明的技术方案之四,是一种包含技术方案二所述双功能融合蛋白编码基因或技术方案三所述表达盒的aav病毒,将所述编码基因或表达盒克隆至腺相关病毒aav骨架中两个末端重复序列itr之间,构建目的基因质粒goi,应用于aav包装载体系统,所述包装载体系统包括:目的基因质粒goi,携带aav rep、cap基因的载体以及辅助载体,上述载体通过三质粒瞬时转染生产细胞包装成为aav病毒。
51、本发明的技术方案之五,是提供一种药物组合物,所述药物组合物包含技术方案一所述的双功能性融合蛋白、或技术方案二所述编码基因、或技术方案三所述表达盒或重组载体或重组宿主细胞、或技术方案四所述aav病毒。
52、本发明的技术方案之六,是提供技术方案一所述双功能融合蛋白、或技术方案二所述编码基因、或技术方案三所述表达盒或重组载体或重组宿主细胞、或技术方案四所述aav病毒的应用;
53、进一步地,是在抑制vegf及补体途径中的应用;
54、进一步地,是在制备治疗血管内皮生长因子(vegf)及补体相关疾病的制剂或配方或药物组合物中的应用,相关疾病包括眼部疾病、炎性疾病、自身免疫性疾病或肿瘤等,特别是在制备治疗年龄相关性黄斑变性、糖尿病视网膜病变相关药物中的应用;
55、进一步地,所述制剂或配方或药物可以是任何剂型,包括但不限于注射剂型和软膏剂型;
56、进一步地,所述制剂或配方或药物中,包含上述双功能融合蛋白、表达盒或aav病毒为唯一活性成分。
57、进一步地,给药方式为aav病毒视网膜下腔注射方式;
58、更进一步地,终身单次给药,给药总剂量为1×108-1×1011个病毒基因组/眼。
59、有益效果:
60、本发明通过分子组合优化和分子改造提供了一种具有高表达、高活性和性质稳定的抗vegf和补体双功能融合蛋白,特别是vegfr1d2-vegfr2d3-mhigg fc-(ggggs)3-scd59和vegfr1d2-mhigg fc-(ggggs)3-scd59。
61、所述双功能融合蛋白采用经过人工改造的higg fc后,能够显著改善采用天然iggfc片段时制备双功能融合蛋白造成的蛋白聚集问题,一方面避免融合蛋白的活性降低,另一方面防止引起免疫原性问题,因此本发明中fc片段的改造有利于提高双功能性融合蛋白的稳定性避免聚集,并且更加安全有效。
62、所述双功能融合蛋白可以同时高效地结合vegf因子和补体分子,尤其是对于scd59的活性有显著提升,与scd59相比,所述双功能融合蛋白抑制补体溶血活性分别提高了4.6倍和10倍。
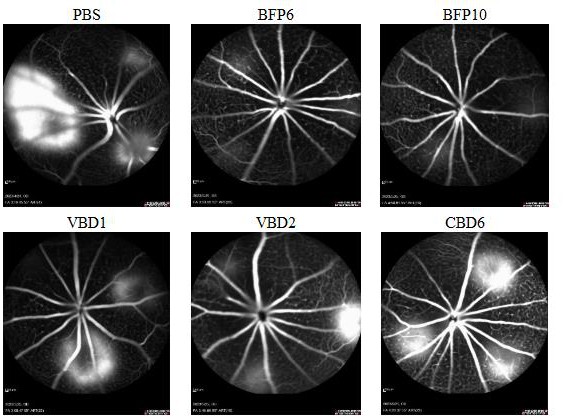
63、另外,所述双功能融合蛋白在干性和湿性amd模型中均有效。其中干性amd模型(实施例13中碘酸钠诱导的干性amd小鼠模型)中,显示出显著抑制erg波幅降低的效果。在湿性amd模型(实施例9中激光诱导小鼠cnv模型)中,从渗漏面积和渗漏评分来看,能有效抑制cnv,且双功能蛋白的抑制活性优于单体分子。
64、因此,本发明提供的双功能融合蛋白预期对治疗年龄相关性黄斑变性,尤其是并发有眼底血管新生的干性年龄相关性黄斑变性,或者伴随有黄斑萎缩的湿性年龄相关性黄斑变性,具有显著的治疗效果。
- 还没有人留言评论。精彩留言会获得点赞!