一种4,4`‑二(3‑氨基苯)‑2,2`‑双噻唑pH荧光探针及其制备和应用的制作方法
本发明属于化学分析检测技术领域,具体涉及一种4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针及其制备和应用。
背景技术:
pH作为一个重要参数,在食品生产、化学反应控制、环境分析、医学诊断以及生命科学等众多领域中都发挥着重要作用。对于有机生物体而言,维持体内pH平衡尤为重要,pH环境紊乱可能引起细胞的异常发育,甚至致癌。因此,生物体内pH的监测一直备受关注。已报道的pH检测方法有酸碱滴定法、电位滴定法和荧光分析法等。其中荧光分析法由于灵敏度高、选择性好、响应快、成本低且操作方便等优点而被广泛使用。而且,随着荧光探针与共聚焦激光扫描技术的结合,荧光成像技术为活细胞内pH的变化提供了高空间和时间的观察。目前,许多杰出的荧光探针都已被用于中性或弱酸性(pH 4-7)条件下生物体系中pH的监测,然而pH低于4或碱性条件下的探针却报道的很少。因此,设计研究这样的探针并应用于生物成像颇具挑战。
技术实现要素:
本发明为了解决现有pH荧光探针仅能用于中性或弱酸性(pH 4-7)条件下生物体系中pH的监测,而不能应用于pH低于4的条件下生物体系中pH监测的问题,提供了一种4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针及其制备和应用。
本发明由如下技术方案实现的:一种4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针,用二硫代乙二酰胺与2-溴-3'-硝基苯乙酮反应生成4,4'-二(3-硝基苯基)- 2,2'-双噻唑,然后将4,4'-二(3-硝基苯基)- 2,2'-双噻唑与水合肼反应生成4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针,所述4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针结构如式(1), 。
4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针的制备方法,包括如下步骤:
(1)4,4'-二(3-硝基苯基)- 2,2'-双噻唑的合成:将0.0082mol二硫代乙二酰胺和30ml无水乙醇加入到三口烧瓶中,启动磁力搅拌,加热使二硫代乙二酰胺溶于无水乙醇中,用恒压滴液漏斗将0.0042mol的2-溴-3'-硝基苯乙酮滴加到二硫代乙二酰胺的无水乙醇溶液中,加热回流反应2-3h,反应完成后,抽滤,滤饼用50~60℃的热乙醇清洗3-4次;粗产品用1,4-二氧六环重结晶得纯品4,4'-二(3-硝基苯基)- 2,2'-双噻唑,产率87.8%;
(2)4, 4'-二(3-氨基苯基)-2, 2'-双噻唑的合成:磁力搅拌并加热条件下,将步骤(1)所制备的4, 4'-二(3-硝基苯基)-2, 2'-双噻唑0.0024mol溶解于100ml的DMF中,溶解后再加入0.2g六水合三氯化铁和0.3g活性炭粒,控制温度为75-85℃,将50%水合肼50ml溶于50ml无水乙醇中并滴加入上述加有六水合三氯化铁和活性炭粒的4, 4'-二(3-硝基苯基)-2, 2'-双噻唑溶液中,溶液由棕黄色变为墨绿色,并析出灰黑色固体,继续在75-85℃反应11-13h,反应结束后,冷却抽滤,将滤液蒸发除去DMF后,加入100ml蒸馏水,析出浅绿色固体,抽滤,水洗,所得滤饼用无水乙醇重结晶,得纯品4, 4'-二(3-氨基苯基)-2, 2'-双噻唑,产率78.7%。
步骤(1)中所述反应采用TLC跟踪监测,TLC所用展开剂为:V乙酸乙酯:V石油醚=1:1;步骤(2)中所述反应采用TLC跟踪监测,TLC所用展开剂为:V乙酸乙酯:V石油醚=1:1。其具体合成路线如图1所示。
所述的4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针用于pH的荧光检测的步骤为:
(1)将4, 4'-二(3-氨基苯)-2, 2'-双噻唑用DMSO溶解,配制成浓度为1mmol/l的荧光探针储备液;
(2)将2ml的v/v为1/3的DMSO/水体系和20µl荧光探针储备液加入荧光比色皿中,在荧光分光光度仪上检测;
(3)用蒸馏水配制0.1M的H+溶液,将2ml的v/v为1/3的DMSO/水体系和20µl荧光探针储备液加入荧光比色皿中,进行pH滴定实验;以pH为横坐标,荧光强度F为纵坐标绘制图并进行Sigmoidal拟合,求得pKa=3.10;通过线性拟合得到该探针的最佳线性响应范围为pH 2.53-3.58, 回归方程为:F=4577.02-1194.34xpH,线性系数为R2 = 0.9990。
可逆性和稳定性实验证明该荧光探针对pH的测定具有良好的光稳定性和可逆性。
经实验验证,其它金属阳离子不干扰体系对H+的测定。
本发明的探针用于生物体内pH值的检测。
与现有技术相比,本发明作为选择性检测生物体内pH的荧光探针有如下优点:本发明所述荧光探针制备方法简单、快速;可用于极酸性条件下pH的检测;反应灵敏且选择性高;检测手段简单,只需要借助荧光光谱仪;该荧光探针还可用于生物成像。
附图说明
图1为本发明所述4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针的合成路线图;图2为实施例2中4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针的pH滴定荧光图;图3为4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针对pH响应的的工作曲线图;图4为实验例1中4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在中性和酸性条件下与各种金属阳离子的荧光柱状图;图5为实验例2中4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在不同pH条件下的可逆性检验图;图6为实验例2中4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在不同pH条件下的光稳定性检测图;图7为实验例3中4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在大肠杆菌内的荧光成像图,放大倍数为:63×10,图中白色圆圈内探针在共聚焦荧光成像仪下发显示的蓝色荧光。
具体实施方式
实施例1:一种4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针,结构如式1,。
4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针的制备方法,包括如下步骤:
(1)4,4'-二(3-硝基苯基)- 2,2'-双噻唑的合成:将0.0082mol即2g二硫代乙二酰胺和30ml无水乙醇加入到100ml三口烧瓶中,启动磁力搅拌,加热使二硫代乙二酰胺溶于无水乙醇中,趁热用恒压滴液漏斗将0.0042mol即0.5g的2-溴-3'-硝基苯乙酮溶于20ml无水乙醇并滴加到二硫代乙二酰胺的无水乙醇溶液中,加热回流反应2-3h,采用TLC跟踪监测,TLC所用展开剂为V乙酸乙酯:V石油醚=1:1,Rf=0.28。在254nm紫外灯下显示土黄色荧光。反应完成后,抽滤,滤饼用50~60℃的热乙醇清洗3-4次;粗产品用1,4-二氧六环重结晶得纯品4,4'-二(3-硝基苯基)- 2,2'-双噻唑1.47g,产率87.8%,熔点>300℃;
反应现象记录:滴入2-溴-3'-硝基苯乙酮后,反应约5分钟后出现橘黄色沉淀,继续反应,颜色逐渐变浅,最后变为土黄色。
1H NMR(DMSO: δ/ppm): 8.842 ppm (s, 1H, Th-H); 8.735 ppm (s, 1H, Ar-H); 8.502 ppm (d, 1H, Ar-H); 8.266 ppm (d, 1H, Ar-H); 7.831 ppm (m, 1H, Ar-H)。
(2)4, 4'-二(3-氨基苯基)-2, 2'-双噻唑的合成:磁力搅拌并加热条件下,将步骤(1)所制备的4, 4'-二(3-硝基苯基)-2, 2'-双噻唑0.0024mol即1g溶解于100ml的DMF中,溶解后再加入0.2g六水合三氯化铁和0.3g活性炭粒,控制温度为75-85℃,将50%水合肼50ml溶于50ml无水乙醇中并滴加入上述加有六水合三氯化铁和活性炭粒的4, 4'-二(3-硝基苯基)-2, 2'-双噻唑溶液中,溶液由棕黄色变为墨绿色,并析出灰黑色固体,继续在75-85℃反应11-13h,采用TLC跟踪监测,TLC所用展开剂为V乙酸乙酯:V石油醚=1:1,Rf=0.44。在254nm紫外灯下显示蓝色荧光。反应结束后,冷却抽滤,将滤液蒸发除去DMF后,加入100ml蒸馏水,析出浅绿色固体,抽滤,水洗,所得滤饼用无水乙醇重结晶,得纯品4, 4'-二(3-氨基苯基)-2, 2'-双噻唑0.67g,产率78.7%,熔点242℃-243℃。
反应现象记录:水合肼滴入溶液后,溶液逐渐由棕黄色变成墨绿色,并有灰黑色固体生成。
1H NMR(DMSO:δ/ppm): 8.114 ppm (s, 1H, Th-H),7.258 ppm (s,1H, Ar-H),7.131 ppm (d, 2H, Ar-H),6.593 ppm (m, 1H, Ar-H),5.240 ppm(s, 2H, N-H)。
其具体合成路线如图1所示。
实施例2:4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针用于pH的荧光检测的步骤为:
(1)将4, 4'-二(3-氨基苯)-2, 2'-双噻唑用DMSO溶解,配制成浓度为1mmol/l的荧光探针储备液;
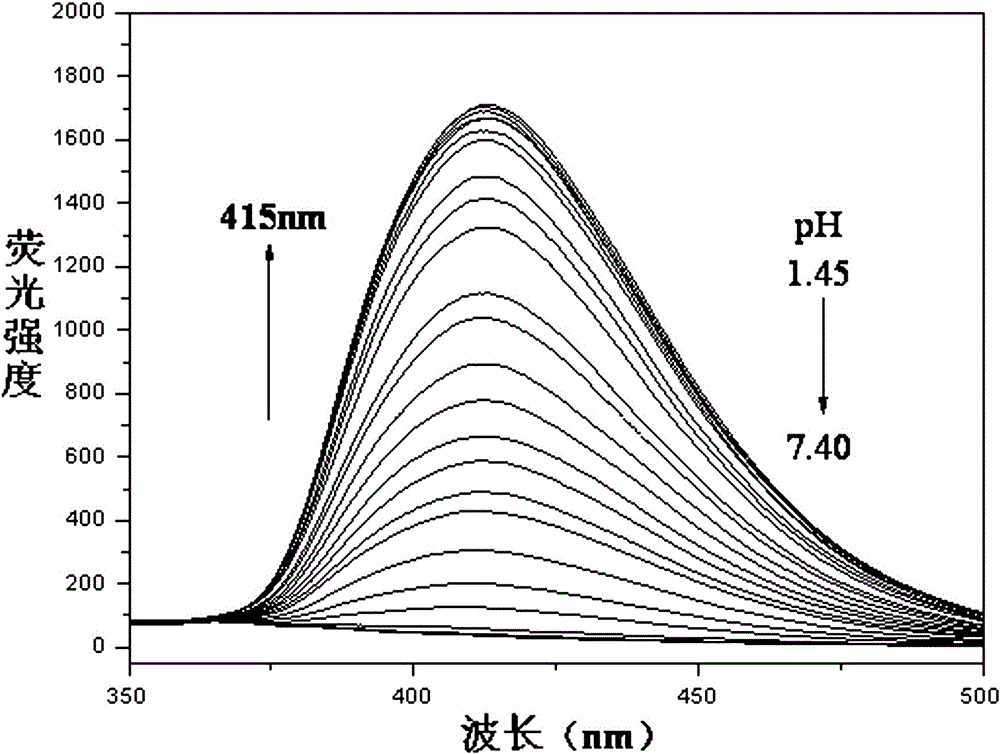
(2)将2ml的v/v为1/3的DMSO/水体系和20µl荧光探针储备液加入荧光比色皿中,在荧光分光光度仪上检测,进行pH应该滴定实验。实验结果见图2。结果显示,随着待测样的加入,415nm处的荧光强度逐渐增强。仪器参数:激发波长和发射波长的狭缝宽度分别为2.5 nm、5.0 nm,荧光探针溶液的最大激发波长为: λex为255 nm和最大荧光发射波长为: λem为415 nm。
实施例3:绘制4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针对pH响应的工作曲线:
用蒸馏水配制0.1M的H+溶液,将2ml的v/v为1/3的DMSO/水体系和20µl荧光探针储备液加入荧光比色皿中,进行pH滴定实验(pH变化范围为7.40-1.46);以pH为横坐标,荧光强度F为纵坐标绘制图,所得工作曲线图见图3,根据工作曲线图进行Sigmoidal拟合,求得pKa=3.10;通过线性拟合得到该探针的最佳线性响应范围为pH 2.53-3.58, 回归方程为:F=4577.02-1194.34xpH,线性系数为R2 = 0.9990。
实验例1:4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在添加入各种金属阳离子的中性和酸性条件下对pH的荧光检测:
在pH为7.40和pH 3.01的2mL DMSO/水 (1/3, v/v) 体系中均加入20µl荧光探针储备液,再分别加入其它的金属离子:0. Blank; 1.K+ (24mM); 2.Na+ (24mM); 3.Mg2+(0.5mM); 4.Ca2+ (2mM); 5.Al3+ (0.2mM); 6.Pb2+ (0.2mM); 7.Zn2+ (0.2mM); 8.Mn2+ (0.2mM); 9.Co2+ (0.2mM); 10.Cr3+ (0.2mM); 11.Ni2+ (0.2mM); 12.Hg2+ (0.2mM); 13.Cu2+ (0.05mM); 14.Bi+ (2mM); 15.Fe2+ (0.2mM); 16.Fe3+ (0.05mM),分别测其荧光光谱,绘制不同金属阳离子对415nm处荧光强度的柱状图,实验结果见图4。实验验证结果显示,其它金属阳离子不干扰体系对H+的测定。
实验例2:4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在不同pH条件下的可逆性和光稳定性的检测:
在2mL DMSO/水 (1/3, v/v) 体系中加入20µL荧光探针储备液,调节pH在7.40和2.01之间变化时,分别记录415 nm处荧光强度的变化。实验结果见图5,如图所示pH的降低会使荧光强度迅速升高,而快速升高pH至中性条件,则导致荧光强度瞬间淬灭,5次循环改变pH值后,酸性条件下的荧光强度仍然成功恢复。此外,探针对不同pH的响应和荧光恢复时间不超过1s。表明荧光探针对pH的响应具有很好的可逆性。
在pH 2.61, 3.31和7.40的DMSO/水 (1/3, v/v) 体系中,加入20 μL 荧光探针储备液,检测415 nm处的荧光强度随时间的变化。实验结果见图6,如图所示,2h内的荧光强度值基本保持不变,说明该荧光探针对外界空气、溶液体系等具有很好的光稳定性。
通过可逆性和稳定性实验证明本发明所述4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针对pH的测定具有良好的光稳定性和可逆性。
实验例3:4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针在大肠杆菌内的荧光成像检验:
将37℃含有大肠杆菌的LB培养基(胰蛋白胨19 g/L,酵母提取物5g/L,NaCl 10 g/L)放在180r/min的浓缩器上培养17 h,然后离心分离大肠杆菌。沉积物用无菌水洗涤然后使其悬浮在pH为5.02和1.21的缓冲溶液中培养,5min后加入DMSO溶解的荧光探针储备液使其最终浓度为20μM,最后放到摇床上振荡2h。共聚焦成像时将混合物涂到载玻片上,用波长为405 nm激光激发,收集发射波段为375-475 nm的蓝色荧光。实验结果如图7所示,探针在共聚焦荧光成像仪下发很弱的蓝色荧光,随着pH的减小,蓝色荧光逐渐增强。充分证明了本发明所述4, 4'-二(3-氨基苯)-2, 2'-双噻唑pH荧光探针能够用于生物体内pH值的检测,同时也能用作生物成像。
- 还没有人留言评论。精彩留言会获得点赞!
- 使用了2‑苯基‑4,4’‑二氨基二苯基醚类的清漆、成形性优异的酰亚胺树脂组合物及具有优异断裂伸长率的固化树脂成形体、以及使用了这些的预浸料、酰亚胺预浸料、及耐热性和机械强度优异的纤维强化材料的制造方法与工艺
- 一种制备5-乙酰乙酰氨基苯并咪唑酮过程中物料分离粉碎装置的制造方法
- 制备5,6-二氨基苯并咪唑酮的即热式蒸汽热水发生器的制造方法
- 一种2,4-二氨基苯磺酸钠尾气吸收装置的制造方法
- 一种用于进行吲哚试验的改良培养基的制作方法
- 二氨基苯功能化石墨烯掺杂的活性炭复合电极、制备及其在电吸附脱盐上的应用
- 聚合物泡沫的制作方法
- 一种3,5-二氨基苯甲酸的制备方法
- 一种制备5-乙酰乙酰氨基苯并咪唑酮工艺过程中大颗粒物分离装置的制造方法
- 一种用于回收5-乙酰乙酰氨基苯并咪唑酮粉末的装置的制造方法