一种含砷废水除砷的方法与流程
本发明涉及废水处理技术领域,尤其涉及一种含砷废水除砷的方法。
背景技术:
砷在自然界中广泛分布,具有类金属特性,其产品主要用于木材防腐剂、玻璃搪瓷工业、农药、合金材料、医药、饲料化工等领域,特别是在医药、合金材料方面具有特殊用途。因此,采矿、有色金属冶炼、硫酸制备、化工染料以及农药生产等工业领域排出的废水往往含有高浓度砷。
环境中砷多以五价砷和三价砷存在,尤其是三价砷具有高度稳定性和毒性,一旦进入水中,对人类健康造成极大的危害。国家污水综合排放标准规定砷为ⅰ类污染物,污水排放标准规定为0.5mg/l。随着人类环保意识的提高,国家环保法对工业废水的排放标准也愈加严格,因此研究水质除砷技术对环保环境、工业正常生产有着现实意义。
目前常用的除砷方法有沉淀法、吸附法、微生物法、膜处理法和电化学法等。其中,共沉淀法已经被美国环保局指定为最佳的除砷技术,而as3+在共沉淀时比as5+难处理,因此,通常情况下需将as3+先氧化成as5+再沉淀。臭葱石(feaso4·2h2o)是较好的载砷矿物,但是以臭葱石形式沉淀的方法处理步骤复杂,成本高,载砷容量低,很难大规模实际应用。此外,一些高级氧化技术,如uv/h2o2、芬顿试剂、uv/亚硝酸盐、过硫酸盐以及uv/过硫酸盐等,也可先将三价砷氧化,然后再用吸附剂吸附,但是该方法氧化和沉淀去除砷不能一次性完成。中国专利201610876924.7公开了铁元素去除水中砷的方法,其主要采用过硫酸盐/铁粉/亚铁盐(nh4)2fe(so4)2.6h2o复合体系去除砷,该体系中加入过硫酸盐的目的主要是与铁元素(铁粉/亚铁盐)反应产生三价铁离子,而三价铁离子只有在ph大于或等于7的碱性条件下转变为絮凝剂,进而沉淀五价砷。因此,该发明工艺仅可沉淀废水中的五价砷,无法对三价砷进行絮凝沉淀,此外,含五价砷的絮凝物在水中分离困难,极易引起二次污染。
因此,基于含三价砷废水(或三价砷和五价砷共存)的实际处理工艺要求,开发一种高效便捷、可同时去除废水中三价砷和五价砷的方法具有重要意义。
技术实现要素:
本发明所要解决的技术问题是提供一种含砷废水除砷的方法,解决现有处理技术复杂,且无法同时去除废水中三价砷和五价砷的问题。
本发明解决上述技术问题的技术方案如下:一种含砷废水除砷的方法,包括以下步骤:将处理剂加入到含砷废水中,并向含砷废水中加入氢氧化钠,得到混合溶液,进行水热反应,生成图水羟砷铁矾或无定型含砷铁共沉淀物;
所述含砷废水中含有as3+和as5+中的任意一种或两种;
所述混合溶液中含有fe3+、so42-和oh-;
其中,所述混合溶液中fe3+的质量浓度为as3+和as5+浓度和的(0.8-15)倍。
使用该方法处理含砷废水时,当废水中含有fe3+、so42-、以及as3+和as5+中的任意一种或两种时,仅需向废水中再加入氢氧化钠,体系中的fe3+、so42-、oh-以及as3+和as5+中的任意一种或两种发生水热反应,生成图水羟砷铁矾(fe6(aso3)4so4(oh)4·4h2o)或无定型含砷铁共沉淀物,进而捕获了大量的as3+和as5+,可有效去除废水中的砷离子;当废水中含有fe3+、以及as3+和as5+中的任意一种或两种时,需向废水中加入硫酸钠或其他形式的硫酸盐,以提供so42-,然后再加入氢氧化钠,此时,体系中的fe3+、so42-、oh-以及as3+和as5+中的任意一种或两种发生水热反应,生成含砷铁共沉淀物;当废水中仅含有as3+和as5+中的任意一种或两种时,需要向废水中加入fe3+和so42-,然后再加入氢氧化钠,进行水热反应,生成含砷铁共沉淀物。该方法不需要单独添加氧化剂或吸附剂,直接可以形成固态矿物或无定型物,形成的固态矿物或无定型物可以捕获大量的砷离子,达到去除废水中砷离子的目的。
而加入处理剂后fe3+的质量浓度为as3+和as5+浓度和的(0.8-15)倍时处理效率最高,废水中的砷浓度也可得到大幅度降低。
进一步,具体包括以下步骤:
s1、将硫酸铁加入到废水中,并加入稀硫酸调至酸性,得到酸性溶液;
s2、将所述酸性溶液进行预热,并向废水中滴加氢氧化钠溶液,进行水热反应;
s3、将反应后的物料进行固液分离。
该方法主要包括以下步骤:首先将硫酸铁加入到废水中,为反应体系提供fe3+和so42-,然后加入稀硫酸,为反应体系提供酸性环境;将酸性溶液进行预热,为水热反应提供适宜的反应温度,此时再向废水中加入氢氧化钠,为反应体系提供oh-,此时,在酸性环境下,oh-、fe3+、so42-以及as3+和as5+中的任意一种或两种发生水热反应,生成图水羟砷铁矾或无定型含砷铁共沉淀物,当无法继续降低废水中的砷离子浓度时,可向体系中补加oh-、fe3+或so42-,并调节反应体系ph值。该处理方法高效便捷、可同时去除废水中三价砷和五价砷的方法。
进一步,步骤s1中,加入稀硫酸调节溶液ph至2-7。
研究表明,在水热反应之前,向废水中加入稀硫酸调节溶液ph至2-7,可以使得沉淀物的晶型更加完整,而完整的晶型结构可提高对砷离子的捕获能力,进而提供废水处理效率。
进一步,步骤s2中,所述预热时,于80-105℃下搅拌0.2-0.8h。
将酸性溶液于80-105℃下搅拌0.2-0.8h进行预热,可以提高oh-、fe3+、so42-以及as3+和as5+的反应活性,进而促进图水羟砷铁矾或无定型含砷铁共沉淀物的生成。
进一步,步骤s2中,所述水热反应包括依次进行的反应阶段和熟化阶段;
所述反应阶段包括:在搅拌条件下向酸性溶液中滴加氢氧化钠溶液;
所述熟化阶段包括:于80-105℃下恒温熟化1-3h;
其中,所述滴加速率为3-7ml/min,所述滴加时间为1-5h。
水热反应主要包括反应阶段和熟化阶段,其中,反应阶段主要指在搅拌条件下向酸性溶液中滴加氢氧化钠溶液,熟化阶段主要是为晶体的生长提供适宜的环境,以防止自发成核,形成细小的晶核,阻碍晶体的长大。
反应阶段需在搅拌条件下向酸性溶液中滴加氢氧化钠,因结晶过程为缓慢过程,所以氢氧化钠必须以滴加的形式加入到体系中,以防止影响晶体的成核与生长。
进一步,所述氢氧化钠溶液的浓度为0.5-2mol/l。
氢氧化钠的浓度过小时,不能为晶核生成提供所需的oh-,而当氢氧化钠浓度过高时,会影响晶体的成核与生长,进而影响废水中除砷的效果。
进一步,所述搅拌的速率为30-80rpm。
体系的预热及水热反应的反应阶段均需缓慢搅拌整个反应体系,以防止局部反应物浓度过大,当将搅拌速率控制为30-80rpm时,可为晶核的形成及晶体的长大提供适宜的环境。
进一步,所述稀硫酸的浓度为1-5mol/l。
本发明与现有技术相比,本发明的有益效果在于:
本发明在含有一定浓度的三价砷和/或五价砷的废水中,利用废水中的fe3+、so42-,或补加fe3+、so42-,然后加入氢氧化钠,在特定条件下进行水热反应,此时,废水中的as3+和as5+可形成砷铁共沉淀物图水羟砷铁钒(fe6(aso3)4so4(oh)4·4h2o)或无定型含砷铁共沉淀物,进而实现去除水中的砷离子。本发明无需额外光照,无需添加辅助试剂、氧化剂、吸附剂,体系自身在水热条件下即可形成砷铁共沉淀物。该方法适用于含有任意比例as3+和as5+的废水,即as3+和as5+比例为0:10、1:9、2:8、3:7、4:6、5:5、6:4、7:3、8:2、9:1、10:0的废水,均可通过形成共沉淀产物进行固化去除,高浓度砷的去除率可达70%以上,废水中砷的浓度得到大幅度降低。
附图说明
图1为图水羟砷铁矾的xrd谱图与标准卡对比图;
图2为图水羟砷铁矾的红外光谱;
图3为水中三价砷、三价铁的浓度及ph变化;
图4为11组固化产物的颜色变化;
图5为5组固化产物的xrd谱图对比图;
图6为6组固化产物的xrd谱图对比图;
图7为11组无定型物的红外光谱对比图;
图8为四组代表性的扫描电镜照片。
具体实施方式
应该指出,以下详细说明都是例示性的,旨在对本申请提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本申请所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本申请的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也包括复数形式,此外,还应当理解的是,当在本说明中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
下面将对本发明技术方案的实施例进行详细的描述。以下实施例仅用于更加清楚地说明本发明的技术方案,因此只作为示例,而不能以此来限制本发明的保护范围。
实施例1
将0.1335mol的硫酸铁加入到2l含有0.1335molas3+的含砷废水中,用稀硫酸调节溶液至ph=2,将混合溶液倒入水热反应器中,于105℃下以30rpm的搅拌速率搅拌0.2h进行预热,然后以3ml/min流速加入浓度为2mol/l氢氧化钠溶液,持续搅拌5h,逐渐形成沉淀,于105℃下恒温熟化1h,固液分离。反应形成了大量图水羟砷铁矾(fe6(aso3)4so4(oh)4·4h2o)捕获了大量的亚砷酸根。高浓度砷的去除率在65%以上,砷离子浓度大幅度降低。
实施例2
将0.1335mol的硫酸铁加入到2l含有0.1335molas3+的含砷废水中,用稀硫酸调节溶液至ph=2,将混合溶液倒入水热反应器中,于80℃下以80rpm的搅拌速率搅拌0.8h进行预热,然后以7ml/min流速加入浓度为0.5mol/l氢氧化钠溶液,持续搅拌1h,逐渐形成沉淀,于80℃下恒温熟化3h,固液分离。反应形成了大量图水羟砷铁矾(fe6(aso3)4so4(oh)4·4h2o)捕获了大量的亚砷酸根。高浓度砷的去除率在70%以上,砷离子浓度大幅度降低。
实施例3
将0.1335mol的硫酸铁加入到2l含有0.1335molas3+的含砷废水中,用稀硫酸及氢氧化钠调节溶液至ph=2-11,将混合溶液倒入水热反应器中,于95℃下以50rpm的搅拌速率搅拌0.5h进行预热,然后按5ml/min流速加入浓度为1mol/l氢氧化钠溶液,持续搅拌2h,逐渐形成沉淀,恒温熟化2h,固液分离。
实施例4
将0.1335mol的硫酸铁加入到2l含有0.1335mol砷(不同比例的as3+/as5+=10:0,9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9,0:1)的废水中,将混合溶液倒入水热反应器中,于95℃下以50rpm的搅拌速率搅拌0.5h进行预热,然后按5ml/min流速加入浓度为1mol/l氢氧化钠溶液,持续搅拌2h,逐渐形成沉淀,恒温熟化2h,固液分离。反应形成了大量图水羟砷铁矾(fe6(aso3)4so4(oh)4·4h2o)或无定型含砷铁共沉淀物,捕获了大量的亚砷酸根及砷酸根。
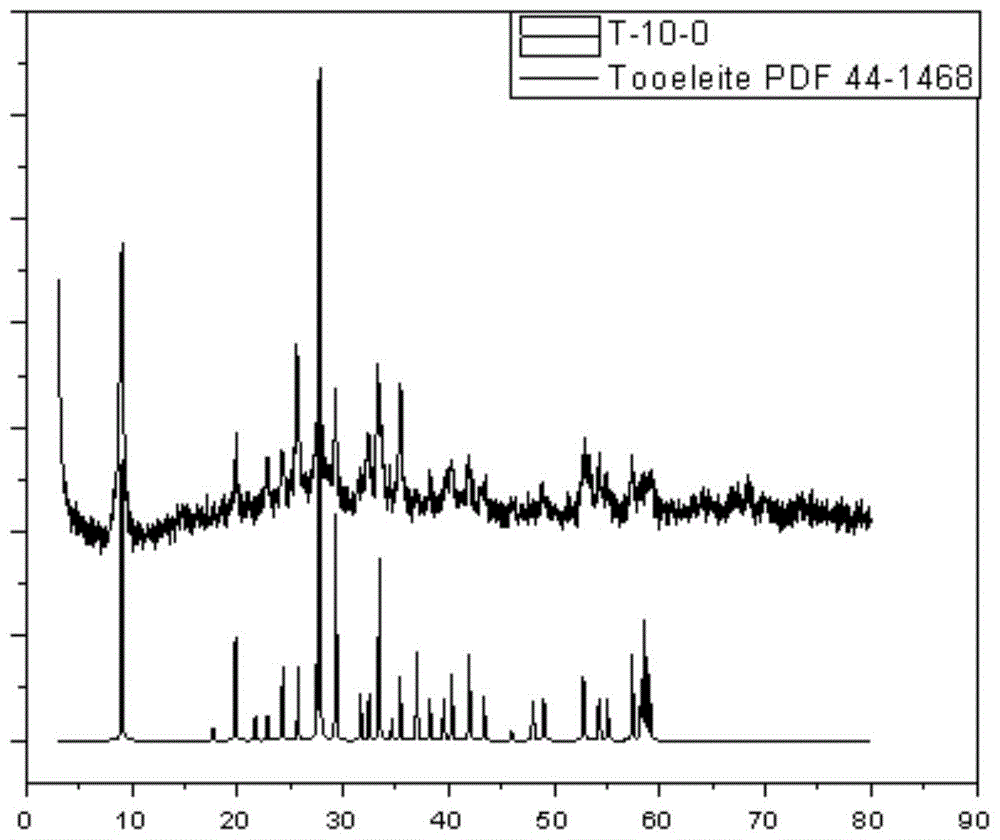
对实施例1所得金黄色固体粉末进行物性分析。图1为图水羟砷铁矾的xrd谱图与标准卡对比图。通过x射线衍射实验证明,合成矿物的xrd与国家衍射数据所中心公布的图水羟砷铁矾粉末衍射标准卡的文件中pdf44-1468的数据完全相符,即合成实验所得矿物为较纯净的图水羟砷铁矾矿物晶体。
图2为图水羟砷铁矾的红外光谱,由图可知,在400-4000cm-1范围内,以0.6239cm/s的速度扫描分辨率为4cm-1,在1109,981和618cm-1处的吸收峰分别来自结构中so42-的不对称伸缩振动(ν3)、对称伸缩振动(ν1)和对称弯曲振动(ν4),而as-o伸缩振动出现在618.89cm-1,通过对原样红外光谱3800-2800cm-1处的重合峰进行分峰拟合处理,发现在3410和3206cm-1出现两个吸收峰,已有对水铁矿(ferrihydrite)的文献报道表明它们分别来自结构h2o中ν(o-h)振动和吸附h2o振动,而硫酸根的吸收峰位于1109cm-1处。因此,红外谱图进一步表明该沉淀物为图水羟砷铁矾矿物晶体。
对实施例3不同ph下水中三价砷、三价铁的浓度进行分析。图3为水中三价砷、三价铁的浓度及ph变化,由图可知,反应在不同酸碱度下都形成了大量图水羟砷铁矾(fe6(aso3)4so4(oh)4·4h2o)捕获了大量的亚砷酸根。可见,图水羟砷铁矾在ph2-9下均可形成,但ph越低,晶形越好,而较好的晶型结构也会进一步提高对砷离子的捕获能力。
对实施例4不同as3+/as5+比例废水产生的固化物进行分析。图4为11组固化产物的颜色变化,从左至右依次为as3+/as5+比例由10:0到0:10的11组不定型物,t-10-0中的砷来源全部为as3+,t-0-10的砷来源全部为as5+。而t-10-0即是图水羟砷铁矾矿物。由所得不定型物粉末颜色可以看出,含as3+的比例越高,不定型物粉末的颜色越黄,含as5+的比例越高,粉末的颜色越白,按照as3+/as5的比例,粉末呈明显的梯度变化。t-10-0的颜色为黄褐色,这与在美国犹他州金山尾矿堆发现的自然界存在的图水羟砷铁矾矿物颜色相同。沉淀的颜色随着五价砷的加入比例的增加,由黄褐色逐渐变成淡黄色,直至呈淡白色。最终t-0-10号含砷铁不定型沉淀的颜色类似于
图5和图6为11组固化产物的xrd谱图对比图,由系列不定型物xrd结果可以看出,as3+所占总砷的比例越高,矿物结晶度越明显,as3+/as5+在10:0时形成图水羟砷铁矾矿物。当as3+/as5+的比例在8:2以下时,所得含砷废渣的xrd峰极其不明显,其中t-7-3、t-6-4、t-5-5、t-4-6、t-7-3、t-8-2、t-1-9、t-0-10号8组不定型物没有明显的衍射峰,由此说明,以上各组合成所得均不是矿物,属于含砷铁的不定型混合物质。同时由t-9-1、t-8-2、t-7-3三组有特征的变化可以看出,衍射峰形由尖锐逐渐变得平缓直至消失,说明水热合成在as3+比例较高情况下,更利于以矿物形式将溶液中的砷铁固定下来,as5+比例较高时,更容易以不定型物的形式将砷从溶液中固定。
此外,图5和图6还可以用来精确的讨论加入五价砷后对图水羟砷铁矾结晶度的影响。由图5和图6可以看出,从t-10-0开始到t-9-1、t-8-2,x射线衍射峰的强度逐渐降低,直至t-7-3时衍射峰消失。当as5+占总砷摩尔的量达到30%时,xrd显示没有明显的结晶图水羟砷铁矾矿物出现。于2θ=30°处,在t-7-3和t-6-4中一个宽的谱带可以被观测到,该波段的振动同时也出现在了t-5-5,最终消失在t-4-6,说明此时沉淀是低结晶的铁类物质。根据fe3+/as3+和fe3+/as5+相的矿物学研究,反映了低结晶的砷铁不定型物之间由as3+/as5+比例不同而产生变化。
图7为11组无定型物的红外光谱对比图。由图可知,,as3+所占总砷的比例越高,系列矿物特征峰越明显,as3+/as5+在10:0时形成图水羟砷铁矾矿物,as3+/as5+在8:2以下时,所得含砷废渣的红外光谱峰极其不明显,说明没有形成特征矿物。该结果与xrd的结果一致,说明在t-7-3之后的样品中没有出现图水羟砷铁矾矿物,而是形成比图水羟砷铁矾更复杂的as3+/as5+/fe3+共存体系。
图8为四组代表性的扫描电镜照片。由图可知,t-10-0的粒径大小在10μm左右,t-8-2的形貌特征明显,粒径在1μm左右,呈片状或针状结构。而t-0-10和t-2-8两组照片,粒径在0.2μm左右,没有形成明显的矿物特征。对四组照片的形态学观察,从端点代表(t-10-0)可以看出,纯净的图水羟砷铁矾矿物呈片状结构(1μm),聚集在一起。随着as5+的加入,由t-8-2可以看出,片状颗粒仍然可以观察到,但是粒径变小,逐渐由片状变成球型结构,而t-2-8和t-0-10只有较小的纳米级粒子,由此说明,五价砷的出现抑制了图水羟砷铁矾晶体生长。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!