一种高亲水性核酸适配体功能萃取材料及其应用的制作方法
本发明属于分析化学技术领域,具体涉及一种高亲水性核酸适配体功能萃取材料的制备方法。
背景技术:
多环芳烃、邻苯二甲酸酯类物质和芳香族化合物等疏水性化合物在环境中普遍存在,这些化合物普遍具有较大的辛醇/水分配系数(kow),这种难溶于水的理化性质使得它们易存在于生物体的体脂中,对生命机体产生一定的致癌和治病作用,严重危害人体生命健康。因此,需要建立一种快速、高效的检测方法来检测环境中的痕量疏水性化合物。hplc由于成本低、稳定性好、使用寿命长等优点成为目前应用最广泛的检测方法。然而,实际样品中痕量疏水性化合物在色谱分析检测前通常要进行样品的预处理或预浓缩,常见的预处理有浊液萃取、液液萃取和固相萃取等,固相萃取技术因其有机溶剂消耗少、成本低、高效等优点成为最常见的预处理技术,其可以使用单体、交联剂等聚合物形成整体材料来富集疏水性化合物。然而,由于疏水性化合物与整体材料之间产生疏水相互作用而带来的非特异性吸附给固相萃取过程带来了不小的困难。
为了降低对疏水性化合物的非特异性吸附,常用的方法是提高材料单体或者交联剂的极性来提高整体材料的亲水性。近年来许多人通过引入亲水性单体来提高整体材料的亲水性,以降低对疏水性目标物的非特异性吸附,例如2-丙烯酰胺-2-甲基丙烷磺酸(amps)、硫代甜菜碱和磷酸胆碱(pc)等。然而,亲水性官能团单体的变化并不能显著提高整体固定相的亲水性。而交联剂的极性、大小以及它们各自在聚合溶液中的浓度,也会影响在聚合反应早期阶段发生的相分离和第一个交联聚合物核的形成。因此,交联剂的类型和极性可能会影响整体聚合物的色谱性能,例如聚合物骨架的亲水性及其选择性。n'n-亚甲基双丙烯酰胺(mba)是一种高亲水性交联剂,有助于聚合物凝胶化。mba可通过共价键、物理作用、氢键和范德华力连接反应混合物(聚合物和单体)。蒋正巾等(analyticalchemistry.2007,79,1243-1250)使用1,4-双(丙烯酰基)哌嗪(pda)、edma和mba分别作为交联剂制备了三个磺基烷基甜菜碱官能化的整体固定相,机理研究表明,交联剂的极性可以显着影响所得整体材料的亲水性。
核酸适配体(apt)是一段通过selex方法筛选出的短链dna或rna序列,对目标物具有高度的亲和性和高度的特异性。阿纳尔萨(foodchemistry.2011,127,1378–1384)等人通过凝胶与赭曲霉毒素a(ota)适配体偶联用于固相萃取柱的制备,然后对小麦进行液相色谱(hplc)和荧光检测(fld)分析。本杰明(analbioanalchem.2011,400,1199–1207)等人通过共价结合(溴化氰活化琼脂糖凝胶)或非共价结合(链霉亲和素激活琼脂糖)将ota的核酸适配体固定在固相萃取小柱中,并用来检测红酒中的ota。但是到目前为止,还没有利用核酸适配体固定到固相萃取柱中用于检测邻苯二甲酸酯(paes)的报道。
技术实现要素:
本发明的目的在于提供一种高亲水性核酸适配体功能萃取材料及其应用。该萃取材料骨架结构均匀,核酸适配体反应效率高,特异性识别能力强,负载量大,机械性能稳定,制备方法简便快捷,并能实现对目标物的高效识别。
为实现上述目的,本发明采用如下技术方案:
一种高亲水性核酸适配体功能萃取材料,其是以高亲水交联剂、高亲水有机聚合单体、三元致孔剂和引发剂混合制成预聚液,并加入paes核酸适配体溶液混匀,然后通过一步热聚合法制备得到用于吸附paes的高亲水性核酸适配体功能萃取材料。
各原料用量按重量百分数计为,高亲水交联剂10wt%-16wt%、高亲水有机聚合单体5wt%、三元致孔剂78.74wt%-84.74%、引发剂0.02wt%、paes核酸适配体0.24wt%,其重量百分数之和为100%。
其中,所述高亲水交联剂为n,n-亚甲基双丙烯酰胺。所述高亲水有机聚合单体为2-丙烯酰胺-2-甲基丙磺酸。所述三元致孔剂是由n,n-二甲基甲酰胺、peg10000和水按质量百分数之比为20:(71-75):(5-9)构成。所述引发剂为偶氮二异丁腈(aibn)。
所述paes核酸适配体的序列为5’-sh-c6-ctttctgtccttccgtcacatcccacgcattctccacat-3’。
所述热聚合法是于55℃水浴反应12h。
本发明通过“一步聚合”的方式,采用“巯基-烯”点击化学反应,在预聚合体系中引入核酸适配体,并利用自由基聚合反应制备了高亲水性的核酸适配体功能萃取材料,所得高亲水性核酸适配体功能萃取材料可用于饮用水中邻苯二甲酸酯类物质的分离和富集。
本发明的显著优点在于:
(1)本发明制备的高亲水性核酸适配体功能萃取材料可通过适配体对paes的酯基和苯甲酰基产生特殊的基团选择性,而与paes发生π-π堆积和氢键的特异性相互作用,从而达到特异性识别环境中邻苯二甲酸酯类物质的目的。经测算,本发明高亲水性核酸适配体功能萃取材料对paes的最大富集倍数达80;
(2)本发明高亲水性核酸适配体功能萃取材料中由于引入高亲水交联剂,获得了良好的亲水性,可降低与paes之间因为疏水相互作用而带来的非特异性吸附。
附图说明
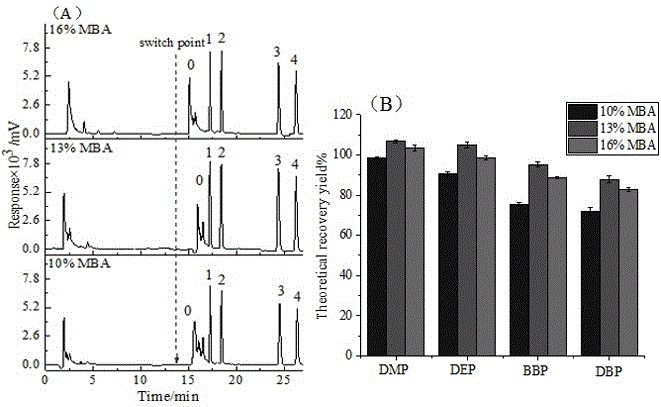
图1为不同交联剂含量对高亲水性核酸适配体功能萃取材料特异性识别(a)和非特异性吸附(b)的影响(其中,1为dmp、2为dep、3为bbp、4为dbp)。
图2为不同交联剂含量制备的萃取材料的接触角(a为10%mba、b为13%mba、c为16%mba);
图3为实施例9中不含核酸适配体的萃取材料(a)和高亲水性核酸适配体功能萃取材料(b)对paes的特异性识别对比情况图(其中,1为dmp、2为dep、3为bbp、4为dbp)。
图4为疏水性交联剂制备的核酸适配体功能萃取材料(a1)和高亲水性核酸适配体功能萃取材料(a2)对paes的非特异性吸附对比情况图(其中,1为dmp、2为dep、3为bbp、4为dbp)。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1
一种高亲水性核酸适配体功能萃取材料,其具体制备步骤为:
(1)移取146μl20mmol/l配制好的bb缓冲液(其组成为10mmol/ltris-hcl、120mmol/lnacl、5mmol/lkcl和20mmol/lcacl2,ph=7.90)于含10od的5,-sh修饰的paes核酸适配体(购自上海生工生物有限公司)中,8000rmp的转速下离心10min,待两者混匀后置于90℃恒温水浴锅中加热3min进行退火处理,然后在室温中自然冷却(约30min),得200μmol/l的核酸适配体溶液,备用;
(2)准确称取高亲水交联剂mba、有机聚合功能单体amps、三元致孔剂(三元致孔剂中n,n-二甲基甲酰胺、peg10000和水的含量分别为20wt%、73wt%、7wt%)、引发剂aibn以及稀释后浓度为120μmol/l的核酸适配体溶液于2ml的离心管中,涡旋振荡至完全溶解,得到均一的预聚合溶液,然后低温(≤20℃)超声脱气20min,再置于55℃的水浴锅中反应12h;其中,高亲水交联剂的用量为13wt%、有机聚合功能单体的用量为5wt%、三元致孔剂的用量为81.74wt%、引发剂aibn的用量为0.02wt%、核酸适配体的用量为0.24wt%;
(3)聚合成功后使用甲醇和水冲洗聚合物,再用缓冲盐溶液清洗聚合物两遍,然后置于烘箱中干燥,最后研磨成粉末,得到高亲水性核酸适配体功能萃取材料;
(4)称取15mg所得高亲水性核酸适配体功能萃取材料,用筛板固定,加入到购买的1ml固相萃取小柱中,并加入1ml的bb缓冲溶液,密封好上下两个端口,储存在4℃以便后续实验使用,得到固相萃取小柱c2。
实施例2
将实施例1步骤2)所用三元致孔剂中水的含量调节为5wt%,其他步骤如实施例1,得到固相萃取小柱c1。
实施例3
将实施例1步骤2)所用三元致孔剂中水的含量调节为9wt%,其他步骤如实施例1,得到固相萃取小柱c3。
实施例4
将实施例1步骤2)所用高亲水交联剂的用量调整为10wt%,三元致孔剂的用量调整为84.74%,其他步骤如实施例1,得到固相萃取小柱c4。
实施例5
将实施例1步骤2)所用高亲水交联剂的用量调整为16wt%,三元致孔剂的用量调整为78.74%,其他步骤如实施例1,得到固相萃取小柱c5。
实施例6
将实施例1步骤2)中核酸适配体溶液的浓度调整为80μmol/l,其他步骤如实施例1,得到固相萃取小柱材料c6。
实施例7
将实施例1步骤2)中核酸适配体溶液的浓度调整为100μmol/l,其他步骤如实施例1,得到固相萃取小柱c7。
实施例8
将实施例1步骤2)中核酸适配体溶液的浓度调整为140μmol/l,其他步骤如实施例1,得到固相萃取小柱c8。
利用实施例1-8所得固相萃取小柱对paes进行富集,表1为具体条件优化情况。
表1高亲水性核酸适配体功能萃取材料制备条件优化表
结果显示,实施例1制备的固相萃取小柱c2对paes的回收率最高,为87.90%-106.74%。
实施例9高亲水性核酸适配体功能萃取材料的特异性测试
检测实施例1所得固相萃取小柱c2对4种邻苯二甲酸酯类物质(dmp、dep、bbp、dbp)的特异性识别能力,并以不含核酸适配体的萃取材料制备的固相萃取小柱作为对照组。其具体实施步骤如下:
(1)平衡:先用1ml结合缓冲液平衡,所述结合缓冲液的组成为10mmol/ltris-hcl、120mmol/lnacl、5mmol/lkcl和20mmol/lcacl2,ph=7.90;
(2)富集:将1ml浓度为500μg/l的邻苯二甲酸酯混合溶液注入固相萃取小柱中,使其通过重力作用流过萃取材料并进行富集,然后用2ml洗净的离心管收集尾液;
(3)清洗:将结合缓冲液注入固相萃取小柱进行清洗,使清洗液通过重力作用流过萃取材料,用2ml洗净的离心管收集清洗尾液;
(4)洗脱:用1ml甲醇作为洗脱液注入固相萃取小柱中,将邻苯二甲酸酯类物质从萃取材料中洗脱下来,然后用2ml洗净的离心管收集洗脱尾液。采用hplc-紫外检测器检测收集的尾液。检测时所用色谱分离柱为alltimatmhpc18柱(alltech,usa,5μm,4.6mmi.d.×250mm),激发波长和发射波长分别为190nm和800nm,采用水溶液/乙腈=25/75(v/v)流动相在等梯度模式下进行色谱分离,流速为1.0ml/min,进样体积20μl。
由图3可见,不含核酸适配体的萃取材料对邻苯二甲酸酯类物质的特异性识别较差(a),而核酸适配体功能萃取材料能够将各种邻苯二甲酸酯类物质有效识别、富集和洗脱下来,且特异性高(b)。
实施例10用于吸附邻苯二甲酸酯的核酸适配体功能萃取材料的最大富集倍数测定
考察在不同试样体积条件下,萃取材料对paes的富集性能。其具体实施操作为:分别将含有10μgpaes的体积为10、20、40、60、80、100、120和140ml的样本溶液经实施例1所得固相萃取小柱c2萃取富集,然后通过对paes回收率的测定来研究其最大富集倍数,结果见表2。
表2富集性能表
由表2可见,当试样体积大于80ml时,dmp的回收率降至89.10%以下,dep的回收率降至83.15%以下,bbp的回收率降至83.61%以下,dbp的回收率降至81.96%以下。这说明萃取材料对paes具有良好的萃取富集能力,由于1ml甲醇溶液就能实现定量回收paes,故其最大富集倍数为80。
实施例11
采用实施例1所得固相萃取小柱测试其对饮用水中邻苯二甲酸酯类物质的富集效率。结果显示,将可饮用的矿泉水直接通过hplc,并不能检测出邻苯二甲酸酯类物质;而通过实施例1所得固相萃取小柱富集之后,矿泉水样品中的邻苯二甲酸酯类物质可以被有效识别富集并洗脱下来,测定其中paes的含量为0.16μg/l-1.28μg/l。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
sequencelisting
<110>福州大学
<120>一种高亲水性核酸适配体功能萃取材料及其应用
<160>1
<170>patentinversion3.3
<210>1
<211>39
<212>dna
<213>artificial
<400>1
ctttctgtccttccgtcacatcccacgcattctccacat39
- 还没有人留言评论。精彩留言会获得点赞!