一种用于高效去除废水中六价铬离子的壳聚糖/EDTA/聚吡咯吸附材料及其制备方法与流程
一种用于高效去除废水中六价铬离子的壳聚糖/edta/聚吡咯吸附材料及其制备方法
技术领域
1.本发明属于废水净化技术领域,具体涉及一种用于高效去除废水中六价铬离子的壳聚糖/edta/聚吡咯吸附材料及其制备方法。
背景技术:
2.水是生命的源泉,是人类赖以生存和发展的不可缺少的最重要的物质资源之一。然而随着工农业的快速发展,各种重金属(如pb(ii)、hg(ii)、cu(ii)、zn(ii)、cr(vi)和cd(ii))被排放进入环境,直接威胁全球水资源安全。铬(cr)是最常见且毒性最高的重金属污染物之一。cr在自然环境中主要以三价铬(cr(iii))和六价铬(cr(vi))形态存在。cr(iii)是微毒甚至无毒的,而cr(vi)因其致癌性、高毒性、致畸性及生物富集性被广泛关注,是美国epa指定的首要有毒污染物之一。2019年7月23日,“六价铬及其化合物”也被我国列入第一批有毒有害水污染物名录。世界卫生组织(who)将地表水和饮用水中cr(vi)的最大允许浓度分别设定为0.1mg/l和0.05mg/l。钢铁制造、纺织、电镀、镀铬等污染性行业每年都会产生高浓度cr(vi)废水。因此,这些含铬废水需要进行处理,达到排放标准的要求。
3.迄今为止,已开发出一系列去除废水中cr(vi)的技术,如化学氧化、溶剂萃取、离子交换、共沉淀、电凝聚、生物处理、膜分离等,这些方法能耗高、需要大型仪器、成本高等,极大的降低了实际应用。吸附法具有环境友好、成本低、操作简单、效率高等优点,被认为是最有发展前景的方法,并具有成为近年来的研究和应用热点。吸附效率主要与吸附剂的种类有关。目前,生物炭、蒙脱土、纤维素、零价铁等多种吸附剂被广泛用于去除水中的cr(vi)。然而由于吸附容量低、成本高、再生困难等缺点,限制了它们的进一步应用,如naghipour d等人(naghipour d,et,al.water and environment journal,2020,34(1):45-56.)用海绿石低成本去除水中的cr(vi),但是该吸附材料对cr(vi)的吸附容量只有12.21mg/g。xiangl等人(xiang l,et,al.chemical engineering journal,2021,408:127281.)用聚吡咯包裹二硫化钼作为吸附剂去除水中的cr(vi),吸附容量为257.73mg/g,同样存在着吸附容量低等问题,同时,同时利用这几种材料制备出去除废水中六价铬离子的吸附材料的文章还未见报道。
技术实现要素:
4.针对上述现有技术的不足,本发明的目的是制备环境友好型、多吸附位点、高吸附容量的吸附材料,可通过吸附和还原作用去除废水中的六价铬离子,即本发明用于高效去除废水中六价铬离子的壳聚糖/edta/聚吡咯吸附材料的制备方法,通过壳聚糖作为该吸附材料的骨架,表面的羟基可与吡咯通过氢键作用结合,表面的氨基可与乙二胺四乙酸二酐交联生成聚合物。吡咯分子上带正电的氮原子,可通过静电引力和还原作用去除六价铬离子,乙二胺四乙酸可通过羧基和氨基的螯合作用去除六价铬离子或还原后的三价铬离子,三种材料均参与六价铬离子的去除,其具体步骤如下:
5.s1:以壳聚糖与乙二胺四乙酸二酐通过酰胺反应生成壳聚糖/edta聚合物;
6.s2:将吡咯单体通过氢键作用力附着于壳聚糖/edta的表面,随后通过原位聚合形成聚吡咯包覆在壳聚糖/edta的表面,获得壳聚糖/edta/聚吡咯复合吸附材料。
7.优选的,s1中壳聚糖/edta聚合物的制备步骤如下:
8.s11:将壳聚糖溶解在醋酸溶液中,然后加入甲醇搅拌均匀,将乙二胺四乙酸二酐加入壳聚糖溶液中,在室温下搅拌直至出现凝胶;
9.s12:反应结束后,过滤沉淀物并用naoh溶液洗涤,以除去未反应的乙二胺四乙酸二酐;
10.s13:用稀盐酸、去离子水和乙醇洗涤并干燥产物,获得壳聚糖/edta聚合物。
11.优选的,s2中包括如下步骤:
12.s21:将干燥的壳聚糖/edta研磨粉碎,加入到装有去离子水的烧杯中搅拌均匀,加入盐酸调节ph;
13.s22:在上述s21的溶液中加入吡咯溶液并搅拌,接着向上述溶液中加入fecl3溶液,继续搅拌,溶液逐渐变为深绿色;
14.s23:在4℃下密封一定时间,然后将所得产物过滤并用蒸馏水和乙醇洗涤至滤液呈中性,干燥保存得到壳聚糖/edta/聚吡咯吸附材料。
15.优选的,s11中壳聚糖与醋酸溶液的固液比1:8~1:20(g:ml),醋酸溶液的体积浓度为8%-20%。
16.优选的,s11中醋酸溶液与甲醇的体积比为1:3~1:6。
17.优选的,s11中壳聚糖与乙二胺四乙酸二酐的质量比为1:0.05~1:2,搅拌时间为8~36小时。
18.优选的,s22中壳聚糖/edta聚合物与吡咯加入量的固液比为1:0.05~1:1.2(g:ml),吡咯与fecl3的摩尔比为1:4~3:1。
19.优选的,s22中fecl3溶液的浓度为0.4~2mol/l。
20.优选的,s23中密封时间为8~36小时。
21.一种用于高效去除废水中六价铬离子的壳聚糖/edta/聚吡咯吸附材料,采用上述制备方法进行制备。
22.与已有技术相比,本发明的有益效果体现在:
23.1.本发明使用的原材料包括,壳聚糖、edta、聚吡咯,全部是环境友好型材料,不会对环境产生二次污染。
24.2.该材料制备方法简单,价格低廉,在用于去除废水中六价铬离子时有很大的经济效益优势。
25.3.该吸附材料三种原材料均参与去除六价铬离子,去除方式包括静电引力、还原、螯合、离子交换等,使得该材料对六价铬离子有较大的吸附容量。
26.4.干扰离子so
42-、no
3-、cu(ii)、zn(ii)等对六价铬离子的去除几乎没有影响,因此该材料适合在复杂废水环境中去除六价铬离子。
27.5.该材料具有良好的可再生性能,吸附解析循环五次后,对六价铬离子的去除率仍能保持80%以上。
附图说明
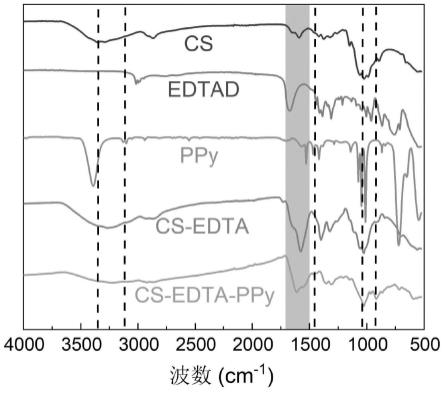
28.图1为壳聚糖/edta/聚吡咯吸附材料与原材料单体的红外光谱图;
29.图2-4为聚吡咯、壳聚糖/edta、壳聚糖/edta/聚吡咯吸附材料的扫描电镜图;
30.图5为不同吸附时间对六价铬离子吸附量的影响图示;
31.图6为不同温度下,溶液中六价铬离子浓度对吸附量的影响图示;
32.图7为不同ph对六价铬离子去除率的影响图示;
33.图8为共存离子对六价铬离子吸附量的影响图示;
34.图9为五次吸附-解吸循环对六价铬离子去除率的影响图示。
具体实施方式
35.下面详细描述本发明的实施例。下面描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。
36.实例一
37.s1:壳聚糖/edta聚合物的制备:
38.s11:将1g壳聚糖溶于20ml浓度为10%的醋酸溶液中,然后加入80ml甲醇并搅拌30分钟。将乙二胺四乙酸二酐(1g溶于10ml甲醇中)加入溶液中,在室温下搅拌24小时,直至出现凝胶;
39.s12:反应结束后,过滤沉淀物并用ph为11的naoh溶液洗涤以除去未反应的乙二胺四乙酸二酐。
40.s13:用0.1mol/l的盐酸、去离子水和乙醇洗涤沉淀物。最终产品在烘箱中在40℃下干燥48小时并储存在干燥器中。
41.s2:壳聚糖/edta/聚吡咯吸附材料的制备:
42.s21:将0.25g干燥的壳聚糖/edta聚合物研磨粉碎,加入装有100ml去离子水的烧杯中搅拌5分钟,接着加入1ml浓盐酸,继续搅拌30分钟;
43.s22:在上述s21的溶液中加入150μl吡咯,连续搅拌3小时,之后加入6.5ml浓度为0.1mol/l的fecl3溶液,继续搅拌10分钟;
44.s23:在4℃下密封24小时。将所得产物过滤并用蒸馏水和乙醇洗涤至滤液呈中性,将产物在烘箱中40℃干燥48小时,储存在干燥器中。
45.吸附性能:在24小时时吸附达到平衡。在45℃、ph为2时,对水溶液中六价铬离子的最大吸附容量为401.25mg/g。循环吸附解析5次后,吸附容量保持81.26%。
46.实例二
47.s1:壳聚糖/edta聚合物的制备:
48.s11:将1g壳聚糖溶于20ml浓度为10%的醋酸溶液中,然后加入80ml甲醇并搅拌30分钟。将乙二胺四乙酸二酐(1.5g溶于10ml甲醇中)加入溶液中,在室温下搅拌24小时,直至出现凝胶;
49.s12:反应结束后,过滤沉淀物并用ph为11的naoh溶液洗涤以除去未反应的乙二胺四乙酸二酐;
50.s13:最后用0.1mol/l的盐酸、去离子水和乙醇洗涤沉淀物,最终产品在烘箱中在
40℃下干燥48小时并储存在干燥器中。
51.s2:壳聚糖/edta/聚吡咯吸附材料的制备:
52.s21:将0.25g干燥的壳聚糖/edta聚合物研磨粉碎,加入装有100ml去离子水的烧杯中搅拌5分钟,接着加入1ml浓盐酸,继续搅拌30分钟;
53.s22:在上述s21的溶液中加入150μl吡咯,连续搅拌3小时,之后加入6.5ml浓度为0.1mol/l的fecl3溶液,继续搅拌10分钟。
54.s23:在4℃下密封24小时,将所得产物过滤并用蒸馏水和乙醇洗涤至滤液呈中性,将产物在烘箱中40℃干燥48小时,储存在干燥器中。
55.吸附性能:在16小时时吸附达到平衡。在45℃、ph为2时,对水溶液中六价铬离子的最大吸附容量为375.49mg/g。循环吸附解析5次后,吸附容量保持85.43%。
56.实例三
57.s1:壳聚糖/edta聚合物的制备:
58.s11:将1g壳聚糖溶于20ml浓度为10%的醋酸溶液中,然后加入80ml甲醇并搅拌30分钟。将乙二胺四乙酸二酐(1.5g溶于10ml甲醇中)加入溶液中,在室温下搅拌24小时,直至出现凝胶;
59.s12:反应结束后,过滤沉淀物并用ph为11的naoh溶液洗涤以除去未反应的乙二胺四乙酸二酐;
60.s13:用0.1mol/l的盐酸、去离子水和乙醇洗涤沉淀物。最终产品在烘箱中在40℃下干燥48小时并储存在干燥器中。
61.s2:壳聚糖/edta/聚吡咯吸附材料的制备:
62.s21:将0.25g干燥的壳聚糖/edta聚合物研磨粉碎,加入装有100ml去离子水的烧杯中搅拌5分钟,接着加入1ml浓盐酸,继续搅拌30分钟;
63.s22:在上述s21的溶液中加入100μl吡咯,连续搅拌3小时,之后加入4ml浓度为0.1mol/l的fecl3溶液,继续搅拌10分钟;
64.s23:在4℃下密封24小时。将所得产物过滤并用蒸馏水和乙醇洗涤至滤液呈中性,将产物在烘箱中40℃干燥48小时,储存在干燥器中。
65.吸附性能:在28小时时吸附达到平衡。在45℃、ph为2时,对水溶液中六价铬离子的最大吸附容量为349.59mg/g。循环吸附解析5次后,吸附容量保持84.39%。
66.在上述实施例的基础上,再通过红外光谱、扫描电镜对本发明制备的壳聚糖/edta/聚吡咯吸附材料的结构和形貌进行进一步分析说明。
67.1.红外(ft-ir)分析
68.采用赛默飞nicolet6700型红外光谱仪(ft-ir)表征吸附材料的结构,波数400~4000cm-1
。图1为原料和吸附剂的红外光谱。壳聚糖中的主要信号是糖环信号(1034cm-1
、1165cm-1
)、酰胺i(1653cm-1
)和酰胺ii(1594cm-1
)的振动。壳聚糖/edta光谱中1623cm-1
和1725cm-1
处的两个新的振动峰可分别归因于酰胺的羰基和羧基的羰基。此外,与壳聚糖/edta相比,壳聚糖/edta/聚吡咯在1540cm-1
、1455cm-1
、1033cm-1
和897cm-1
处有新的峰,这归因于吡咯环对称振动、c-n分别为拉伸、c-h拉伸和c-h弯曲振动。
69.2.扫描电镜(sem)分析
70.采用日本hitach公司的su8010型扫描电镜观察吸附材料的形貌。图2-4为放大
10000倍下的扫描电镜图。从图2可以发现聚吡咯是球形颗粒团聚形成的团聚体,图3中壳聚糖/edta的表面相对光滑,图4中壳聚糖/edta/聚吡咯的表面由于聚吡咯的覆盖而明显变得粗糙。
71.3.壳聚糖/edta/聚吡咯吸附材料对水中六价铬离子的吸附性能
72.3.1.吸附动力学
73.称取6mg壳聚糖/edta/聚吡咯吸附材料,加入到装有18ml的100mg/l的六价铬溶液的闪烁瓶中,每隔一段时间取出0.2ml溶液并用0.45μm聚丙烯膜过滤,然后加入1,5-二苯碳酰二肼溶液染色,最后使用紫外可见分光光度计在波长为540nm处测定溶液中六价铬的浓度。吸附材料对六价铬离子的吸附量可按照以下公式进行计算:
[0074][0075]
式中c0、c
t
分别为溶液中六价铬离子的初始浓度、t时刻的浓度,mg/l;v为溶液体积,ml;m为吸附剂的质量,mg;q
t
为t时刻吸附材料对六价铬离子的吸附量,mg/g。
[0076]
图5为吸附材料对六价铬离子的吸附量随时间变化关系,壳聚糖/edta/聚吡咯能够在8小时内去除溶液中85%的六价铬离子,平衡吸附容量为279.63mg/g。作为对比,壳聚糖/edta在8小时内只能去除溶液中24%的六价铬离子,平衡吸附量为98.66mg/g,说明了壳聚糖/edta/聚吡咯吸附材料对六价铬离子具有较高吸附容量。
[0077]
3.2.吸附等温线
[0078]
图6为壳聚糖/edta/聚吡咯吸附材料在不同温度下对六价铬离子的吸附等温线,可以看出,随着温度的升高,壳聚糖/edta/聚吡咯吸附材料对六价铬离子的最大吸附量从330.75mg/g(25℃)增加到401.25mg/g(45℃),这表明该材料对六价铬离子的吸附是一个吸热过程,另外吸附过程符合langmuir吸附等温模型,说明该材料对六价铬离子的吸附过程主要是单层吸附。
[0079]
3.3.ph对吸附性能的影响
[0080]
图7为壳聚糖/edta/聚吡咯吸附材料在不同ph下对六价铬离子的去除率。可以发现,在ph为2时,对cr(vi)的去除率最高为93.1%。随着ph值的升高,六价铬离子的去除率逐渐下降,在ph为6时去除率为71.9%。之后随着ph值的升高,六价铬离子的去除率迅速下降,在ph为8时,六价铬离子的去除率仅为35.3%。这是因为在较低的ph下,壳聚糖/edta/聚吡咯吸附材料中氮原子质子化程度高,壳聚糖/edta/聚吡咯吸附材料表面电位升高,因此可通过静电引力作用去除更多的六价铬离子。
[0081]
3.4.干扰离子对吸附性能的影响
[0082]
在25℃下研究了共存离子对六价铬离子去除的影响,共存离子(cu(ii)、zn(ii)、so
42-、no
3-和so
42-/no
3-)和六价铬离子的浓度均为100mg/l。由图8可以发现,当溶液中含有cu(ii)或zn(ii)时,共存离子对去除溶液中六价铬离子的影响较小,这是因为在酸性环境中,带正电的壳聚糖/edta/聚吡咯吸附材料与金属的静电排斥作用所致。阴离so
42-或no
3-是低亲和力配体,与壳聚糖/edta/聚吡咯吸附材料的相互作用较弱。
[0083]
3.5.吸附材料的再生性能
[0084]
通过五个连续的吸附-解吸循环实验研究壳聚糖/edta/聚吡咯吸附材料的再生性能。首先,将30mg壳聚糖/edta/聚吡咯吸附材料添加到90ml浓度为100mg/l的六价铬溶液中
吸附24h。然后将吸附后的材料在0.5mol/l的naoh溶液中搅拌2小时以完成解吸。接着将吸附材料添加到1mol/l的盐酸溶液中并搅拌2小时以再生吸附活性位点。最后用去离子水将吸附材料洗涤至中性,重新用于下一次吸附试验。
[0085]
图9为吸附-解析五个循环图示。可以发现前三个循环对六价铬离子的去除率分别为91.3%、88.1%和85.6%,去除率没有明显下降,表明吸附剂具有良好的重复使用性。在第四和第五次循环中,去除率分别下降到82.81%和81.26%,这是由于六价铬离子的重复氧化作用使聚吡咯链断裂所致。此外,经过五次循环后,壳聚糖/edta/聚吡咯吸附材料可以直接从水溶液中分离出来,吸附材料重量没有明显损失,进一步说明壳聚糖/edta/聚吡咯吸附材料的实际应用价值。
[0086]
综上所述,由于壳聚糖/edta/聚吡咯吸附材料具有较多的吸附位点,如吡咯上带正电的氮原子可以通过静电引力和还原作用去除六价铬离子,壳聚糖和edta表面的羧基、羟基、氨基基团可以螯合六价铬和三价铬离子。三种材料均参与去除溶液中的六价铬离子,使得壳聚糖/edta/聚吡咯吸附材料对六价铬离子有较大的吸附容量。另外该材料经过多次吸附-解吸循环之后,仍具有良好的再生和重复利用性。因此,壳聚糖/edta/聚吡咯是一种优良的从废水中去除六价铬离子的吸附材料。
[0087]
所以,本发明制备的对cr(vi)具有吸附和还原性能的吸附材料,采用环保材料壳聚糖、乙二胺四乙酸二酐、吡咯为原材料。壳聚糖(cs)是一种由虾等甲壳类动物壳碱水解产生的线性氨基葡萄糖多糖,由于胺基的反应性和稳定的螯合作用,被广泛用作重金属去除的低成本吸附剂。乙二胺四乙酸(edta)是一种优良的金属离子螯合剂,具有四个羧基和两个氨基,被广泛用作交联剂或改性剂,以提高吸附剂去除水中重金属离子的性能。吡咯具有带正电的氮原子,可以通过静电引力与cr(vi)结合,同时能有效地将cr(vi)还原为cr(iii)。壳聚糖与乙二胺四乙酸二酐通过酰胺反应生成壳聚糖/edta聚合物,吡咯中的-nh-基团与壳聚糖中丰富的羟基形成氢键。在fecl3的催化下,吡咯原位聚合生成聚吡咯包裹在壳聚糖/edta聚合物的表面,形成壳聚糖/edta/聚吡咯吸附材料。同时壳聚糖/edta的存在可以解决聚吡咯的团聚问题。实验发现,该吸附材料对cr(vi)的最大吸附容量为401.25mg/g,循环吸附解析5次后,吸附容量仍能保持80%以上。
[0088]
尽管前面结合附图对本发明进行了详细说明,但本发明并不仅仅局限于前述的具体实施方式,以上的具体实施方式仅是示意性的,并不作限制。本领域的研究人员在本发明的启示下,在不脱离本发明前提下,还可以做出很多不同比例吡啶复合壳聚糖/edta种类的变形,这些均属于本发明的保护之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1