一种含双键的液态聚硅烷的电化学合成方法与流程
本发明涉及一种含双键的液态聚硅烷的电化学合成方法,具体涉及一种以电解质和含双键卤代硅烷电化学合成含双键的液态聚硅烷的方法。
背景技术:
碳化硅(SiC)陶瓷是以SiC为主要成分的新型陶瓷材料。SiC陶瓷具有优异的高温性能、高硬度、高模量、低化学活性和低比重等优点,在空间反射镜、核燃料包壳、摩擦材料,高温半导体,高温薄膜和催化剂载体等领域得到了广泛的关注。纳米结构SiC还具有独特的电学,光学和超疏水性能,在吸波材料、光电纳米器件等领域极具应用前景。单体SiC对缺陷的敏感性强,为克服其固有的脆性,人们通过颗粒、晶须和纤维等增强体对SiC陶瓷进行增强增韧。其中,连续碳化硅纤维增强碳化硅基复合材料(SiCf/SiC)具有伪塑性的断裂行为和可调控的结构、性能,为其在航空航天高温结构部件以及核反应堆结构、功能材料等领域的应用提供了可能性,成为了国内外材料研究关注的热点。
SiCf/SiC复合材料凭借其高强度、高模量、优异的高温稳定性、耐冲击、抗氧化、抗蠕变等诸多优异性能在新能源、国防军工、航空航天等领域具有广阔的应用前景,如火箭发动机喷管、高推质比姿控和轨控发动机推力室、高效燃气轮机内衬、涡轮发动机叶片、航天飞行器防热瓦、SiC基反射镜的基底及空间支架、超高温耐烧蚀端头部件、先进武器隐身材料等。纤维增强SiC基复合材料长期以来一直是国内外材料研究领域关注的热点,也是目前世界各强国竞相研究开发的课题。同时由于性能与结构上的稳定性,陶瓷基复合材料可望进行循环或长时间服役,因此其经济效益和社会效益都相当可观。由于其技术难度大且耗资巨大,目前只有法国、美国、日本等少数国家掌握了连续纤维增强SiC陶瓷基复合材料的产业化技术。美国在SiCf/SiC应用于航空发动机方面做了大量的研究。已经制备和通过试验的SiCf/SiC发动机构件主要有:燃烧室内衬套(combustor liner)、燃烧室筒(combustor call)、翼或螺旋桨前缘(1eading edge)、喷口导流叶片(guide vane)、涡轮叶片(turbine vane)和涡轮壳环(turbine shroud ring)等。
SiCf/SiC复合材料制备工艺的发展和完善是复合材料性能提高的根本,核领域应用对SiCf/SiC复合材料提出的新要求包括高致密度、高热导率,好的化学相容性、辐照稳定性以及低成本等,目前针对核领域要求的制备工艺研究主要集中在纳米浸渍与瞬时共晶相(NITE,Nano Infiltration and Transient Eutectic)工艺、化学气相渗透(CVI,Chemical Vapor Infiltration)工艺和先驱体浸渍裂解(PIP,Polymer Infiltration and Pyrolysis)工艺上。PIP工艺由于适于制备大型异形构件以及低成本而受到重视,其工艺流程为:以纤维预制件为骨架,真空排除预制件中的空气,采用溶液或熔融的聚合物先驱体浸渍,经交联固化后在惰性气体保护下高温裂解,最后重复浸渍裂解过程使材料致密化。传统PIP工艺采用聚碳硅烷(PCS)作为先驱体,制备的非化学计量比、无定形的SiC基体是该工艺的局限所在,对此,采用新型先驱体是改善基体结构的有效途径。含有可交联基团的聚硅烷也可用于SiC陶瓷基体的先驱体制备。
聚硅烷的合成的方法有Wurtz偶合法、均相脱氢偶合法、开环聚合法、阴离子聚合法和电化学还原法等。Wurtz偶合法合成均聚物和共聚物,分子量高,但反应条件激烈,速率难以控制,取代基类型受到限制,分子量分布不均匀,分子量分布呈多分散性;均相脱氢偶合法产率高,SiRH2封端,几乎无环状物生成,分子量分布窄,可引入新的官能侧基,选择性好,但原料成本高,分子量低,呈多峰分布,空间位阻影响大;开环聚合法反应条件温和,聚合物的微观结构可控,但可引入的活性功能基团十分有限,同时体积较大的取代基的阻聚作用很明显;阴离子聚合法分子量高,分子量分布窄,产率高,可精细控制聚硅烷结构,但可直接引入的取代基十分有限,取代基的位阻效应明显。
电化学还原法是近年来兴起的一种聚硅烷合成方法,该法是通过电解池中阴极还原硅烷单体来制取聚硅烷。电化学反应条件温和,能够合成结构规则有序且分子量分布较窄的聚硅烷,产率高。特别是可引入羟基、氨基等活性基团,从而使聚硅烷的官能化得到拓宽,因此电化学还原法具有良好的发展前景,有望替代Wurtz法合成聚二甲基硅烷。
1999年,日本大阪瓦斯公司开发了一条电化学路线,在一个电解池内含有一个镁阳极,一个铁阴电极,氯化锂和氯化亚铁电解质,四氢呋喃溶剂,在室温和常压下,二氯烷基硅烷还原聚合,生成的聚硅烷平均分子量约为1万,但所需电压较高。Kunai等以水银为阳极,铂为阴极,乙二醇二甲醚为溶剂合成了各种二硅烷,产率为45~94%。Shono以镁为电极在同一电解槽中以THF和LiClO4为电解液,电解甲基苯基二氯硅烷合成网状聚硅烷(PMPS),产率为22%,分子量为3200,分子量分布指数为3.8,在500~1500nm波长有强吸收。
综上,目前存在的方法,有的反应条件剧烈,有一定的危险性且反应不易控制;有的原料成本较高;有的不能在硅主链上引入活性基团;有的在通电过程中由于电解质较差的导电性,所需电压较高、通电时间较长或产率较低,导致聚硅烷产率或分子量较低。
技术实现要素:
本发明要解决的技术问题是,克服现有技术的缺陷,提供一种在常温常压、较小的电压下,一种含双键的液态聚硅烷的电化学合成方法以及SiC陶瓷先驱体。
本发明解决其技术问题采用的技术方案如下:一种含双键的液态聚硅烷的电化学合成方法,包括以下步骤:
(1)将含双键的卤代硅烷单体置于反应器中,加入有机溶剂溶解,搅拌并加入电解质,反应系统内抽真空,再用惰性气体置换反应系统内气体至常压,重复≥3次,反应得活性组分a;
(2)在惰性气氛中,对活性组分a通电,搅拌发生聚合反应得到组分b,滴加反应终止剂至反应终止,过滤并浓缩滤液,加入正己烷中离心,收集上层液体;继续浓缩,离心,收集上层液体,反复两次后即得含双键的液态聚硅烷。
进一步,步骤(1)中,所述卤代硅烷单体的分子式为R4-mSiXm,其中,R为不含氧的有机基团,优选为C原子数≤10的饱和烃基、不饱和烃基、卤代烃基、芳香基中的一种或几种,且至少有一个R基含不饱和双键,X为无机基团Cl、Br、I、F中的一种或几种,m为与Si相连的无机基团个数。
进一步,步骤(1)中,所述电解槽为配备Mg-Mg、Fe-Fe、Al-Al等电极的电解槽。
进一步,步骤(1)中,所述电解质为LiAlH4、NaAlH4、KAlH4中的一种或几种。
进一步,步骤(1)和(2)中,所述有机溶剂为四氢呋喃、苯、甲苯、二甲苯、一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳、乙二醇二甲醚、丙酮、N,N-二甲基亚砜中的一种或几种。所述有机溶剂只是作为溶剂,不参与合成反应。
进一步,步骤(2)中,所述反应终止剂为甲基溴化镁、溴乙烷、一氯丁烷、氯苯、烯丙基氯的一种或几种。
进一步,步骤(1)和(2)中,所述反应时间按照通电电流的大小来决定。
进一步,步骤(1)和(2)中,所述惰性气体为氮气或氩气。
一种SiC陶瓷先驱体,所述SiC陶瓷先驱体包括根据上述的含双键的液态聚硅烷的电化学合成方法所制备的液态聚硅烷。
相对于现有技术,采用氢化铝盐作为电解质,通过电化学反应制备聚硅烷的优点是:电化学还原法制备聚硅烷可在常温常压下发生聚合,反应条件温和,危险性低,无需高温高压等苛刻条件;氢化铝盐作为电解质,其导电性高于普通锂盐,如LiCl、LiClO4、LiBH4以及其它常用于电解质的盐类如NaCl、AlCl3、Et4NBF4等;电解还原反应可以在较小的电压下发生,并保持一定大小的电流强度;另外,可以利用氢化铝盐与水反应的活泼性来达到溶剂进一步除水的目的。本发明方法具有如下优点:
(1)通过电化学方法制备聚硅烷,无需高温、高压等条件,常温常压下即可对含卤素硅烷进行聚合,条件易于控制且节约能源;
(2)电解质与含卤硅烷单体均不含氧,聚合不会引入额外的氧,因此能降低产物聚硅烷的氧含量;
(3)电解质的导电性优良,可以在较小的电压下实现较大强度的电解电流;
(4)由单体的水平开始,逐步聚合,产物链长可控且均匀性好,可制备纯度高、均匀性好的聚硅烷。
附图说明
以下,结合附图来详细说明本发明的实施方案,其中:
图1为本发明实施例1中单体聚合的反应式;
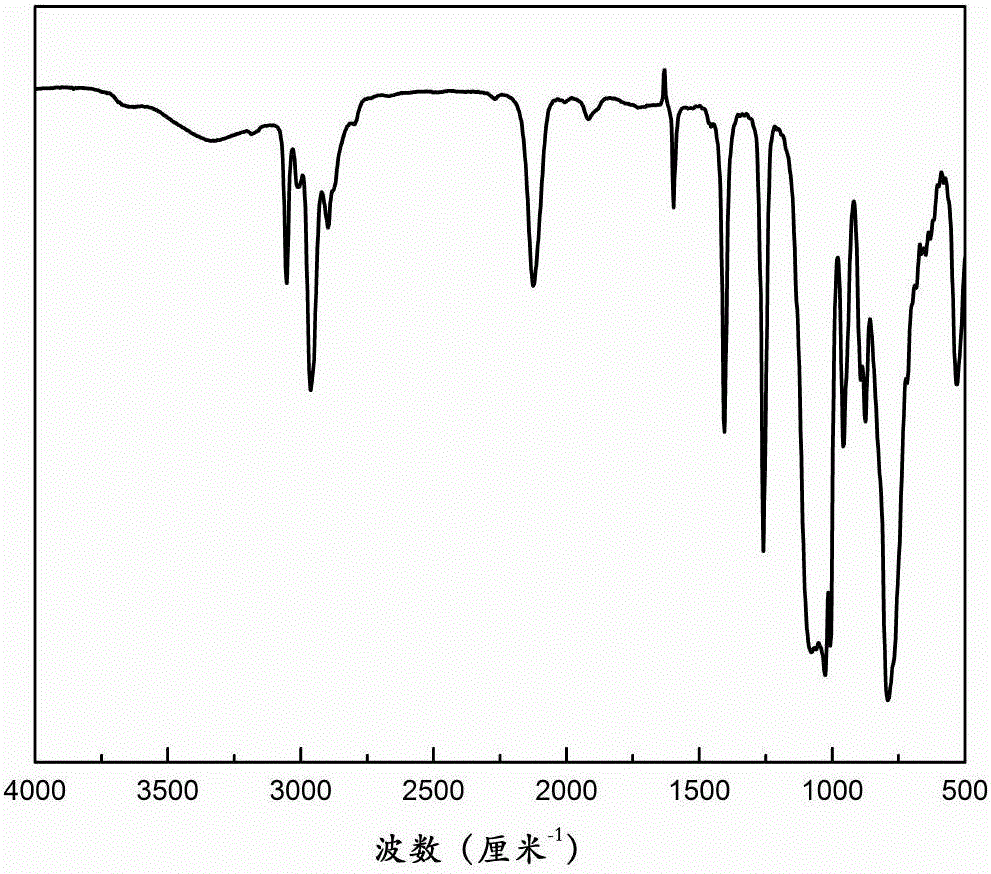
图2为本发明实施例1的液态聚硅烷的红外谱图(FTIR);
图3为本发明实施例1的液态聚硅烷在氘氯中的核磁共振氢谱图(1H-NMR)
图4为本发明实施例1的液态聚硅烷的凝胶渗透色谱(GPC);
图5为本发明实施例1的交联聚硅烷的红外谱图(FTIR);
图6为本发明实施例1的交联聚硅烷的热重曲线(TG);
图7为本发明实施例1的交联聚硅烷热解后的X-射线衍射曲线(XRD);
具体实施方式
下面结合实施例和附图对本发明作进一步说明。
实施例1
本实施例包括以下步骤:
(1)将14.1g(CH3)(CH2CH)SiCl2(0.1mol)置于烧瓶中,加入1g LiAlH4,再加入100mL无水四氢呋喃溶解,反应系统内抽真空,再用氮气置换反应系统内气体至常压,重复3次,搅拌(组分a);
(2)在氮气气氛保护下,对步骤(1)中反应体系进行通电,通电电流设置为200mA,26.8小时发生图1所示反应,加入1mlCH3MgBr终止反应,过滤并浓缩滤液,再加入50ml正己烷,离心取上层液体,继续浓缩,离心,收集上层液体,反复两次后即得含双键的液态聚硅烷。该液态聚硅烷可作为SiC陶瓷的先驱体。
图2为本发明实施例1的含双键的液态聚硅烷的红外谱图,由图可知,波长1000~1050cm-1处的峰为Si-O-Si键的面外振动峰,2130cm-1处为Si-H键的伸缩振动峰,950-800cm-1处的峰是Si-H键的变形振动峰。而3000cm-1处的峰为甲基上饱和C-H键的伸缩振动峰,1270cm-1处的峰为Si-CH3中CH3键的变形振动峰,770cm-1处的峰为Si-C键的伸缩振动峰,1600cm-1处的峰是C=C双键的伸缩振动峰。
图3为本发明实施例1的含双键的液态聚硅烷在氘氯中的核磁氢谱图,可以得知,化学位移δ=7.26ppm处的尖峰为氘氯本征氢核磁峰,化学位移δ=0.24ppm处尖峰为氘氯内标TMS峰,δ=5.7~6.2ppm处的宽峰属于乙烯基上的氢,化学位移δ=0.35ppm处的尖峰对应于Si-CH3上的氢,δ=3.8~4.0ppm处宽峰属于Si-H上的氢。该图结果表明含有乙烯基的单体发生了聚合反应并与LiAlH4反应生成了Si-H键。
图4为本实施例1制备的液态聚硅烷的GPC谱图,其结果表明,液态聚硅烷的数均分子量Mn为448,重均分子量Mw为593.6,分子量分布系数PDi(Mw/Mn)为1.32,说明液态聚硅烷分子量得到了很好的控制,分子量分布较窄。
图5为本发明实施例1的液态聚硅烷交联产物的红外谱图,由图可知,波长1000~1050cm-1处的峰为Si-O-Si键的面外振动峰,2130cm-1处为Si-H键的伸缩振动峰,950-800cm-1处的峰是Si-H键的变形振动峰。而3000cm-1处的峰为甲基上饱和C-H键的伸缩振动峰,1270cm-1处的峰为Si-CH3中CH3键的变形振动峰,770cm-1处的峰为Si-C键的伸缩振动峰,1600cm-1处的峰是C=C双键的伸缩振动峰。与液态聚硅烷的红外光谱图对比可知,C=C双键和Si-H键峰的强度均减弱,说明交联过程中C=C双键和Si-H键发生了反应。
图6为本实施例1制备的交联聚硅烷的TG曲线,从图中可知,聚硅烷在氮气气氛中1000℃时陶瓷产率为57.9%。
图7为本实施例1制备的交联聚硅烷在1000℃、1200℃、1400℃高温下氩气中陶瓷化产物的X射线衍射图,由图可知,在氮气气氛中1400℃的高温下,陶瓷化产物在衍射角38.5°、60.5°、72.5°位置的衍射峰为SiC的(1 1 1)晶面衍射峰(JCPDS PDF#65-0360),说明在此超高温下产物为SiC晶体,证明本实施案例的聚硅烷可以制备SiC陶瓷。
由实施例1可知,电解法还原氯硅烷单体制备含嵌段结构的聚硅烷,常温常压下无需施加高电压,即可引发并与含卤素硅烷进行聚合,可实现逐步聚合,产物链长可控且均匀性好,可进一步制备纯度高、均匀性好的陶瓷,条件易于控制且节约能源。工艺简便,且可连续进行,适于大规模生产。
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
- 还没有人留言评论。精彩留言会获得点赞!