一种血浆中利培酮及9‑羟基利培酮的检测方法与流程
本发明涉及一种利培酮及9-羟基利培酮的检测方法,尤其是一种血浆中利培酮及9-羟基利培酮的检测方法。
背景技术:
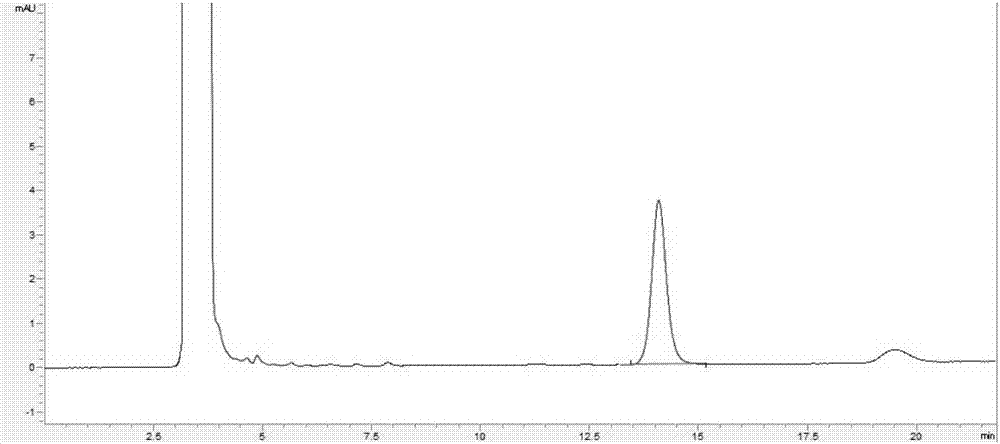
:利培酮,化学名称为3-[2-[4-(6-氟-1,2-苯并异恶唑-3-基)-1-哌啶基]乙基]-6,7,8,9-四氢-2-甲基-4h-吡啶并[1,2-α]嘧啶-4-酮,是苯并异恶唑衍生物,是新一代的抗精神病药。在体内部分代谢为9-羟基利培酮,具有同样的药理活性。利培酮是一种具有独特性质的选择性单胺能拮抗剂,它与5—羟色胺能的5-ht2受体和多巴胺的d2受体有很高的亲和力。利培酮也能与肾上腺素能受体结合,并且以较低的亲和力与h1—组胺能受体和α2-肾上腺素受体结合。利培酮不与胆碱能受体结合。利培酮是强有力的d2拮抗剂,可以改善精神分裂症的阳性症状,但它引起的运动功能抑制,以及强直性昏厥都要比经典的抗精神病药少,对中枢系统的5—羟色胺和多巴胺拮抗作用的平衡可以减少发生锥体外系副作用的可能,并将其治疗作用扩展到精神分裂症的阴性症状和情感症状。目前从血浆中提取利培酮和9-羟基利培酮主要有两种方法,固相萃取法(spe)和液液萃取法。spe方法使用进口固相萃取小柱成本较高,液液萃取方法使用乙醚萃取时发现乙醚会使ep管材料中的一些组分溶出,与利培酮保留时间一致,干扰利培酮的测定;使用二氯甲烷萃取血浆中的活性成分时,因二氯甲烷密度较大,二氯甲烷在溶液底部,分离时较困难;将有机相中的利培酮和9-羟基利培酮反向萃取到酸性水相溶液中,水相溶液使用ph2.2磷酸盐缓冲液时,发现9-羟基利培酮的萃取率较低,还需要降低溶液的ph值;使用c18反相色谱柱进行血浆样品检测时,血浆中的内源物质有较多干扰。技术实现要素:基于此,本发明的目的在于克服上述现有技术的不足之处而提供一种血浆中利培酮及9-羟基利培酮的检测方法。本方法成本低,可方便检测人或动物血浆中的利培酮和9-羟基利培酮,方法重复性好,准确度高,可操作性强。为实现上述目的,本发明所采取的技术方案为:一种血浆中利培酮及9-羟基利培酮的检测方法,包括如下步骤:(1)将血浆样品进行前处理,得到血浆样品上样液;(2)用高效液相色谱法对步骤(1)得到的血浆样品上样液进行测定,并分析血浆样品上样液的测定结果;其中,高效液相色谱条件为:a)色谱柱:c4柱,4.6mm×250mm,粒径5μm;b)流动相为磷酸二氢钾溶液与乙腈的混合物,其中,所述磷酸二氢钾溶液与所述乙腈的体积比为65:35~85:15;流速为0.5~1.5ml/min;检测波长为278nm。磷酸二氢钾与乙腈比例太高,利培酮、9-羟基利培酮及内标保留时间延长,增加分析时间,磷酸二氢钾与乙腈比例太少,9-羟基利培酮出峰较快,与血浆中组分不能有效分离,本申请发明人经过大量尝试,发现上述体积比的磷酸二氢钾溶液和乙腈混合,既能有效分离血浆中的组分,又能适当控制分析时间。更优选地,所述磷酸二氢钾溶液与所述乙腈的体积比为77:23。此体积比的磷酸二氢钾溶液和乙腈混合作为流动相,能保证在控制分析时间的同时,使血浆中组分的分离效果更好。优选地,高效液相色谱的进样量为100μl;柱温为35℃。本发明采用c4色谱柱进行检测,与c18色谱柱相比,减少了血浆中内源性物质干扰。与使用spe固相萃取柱相比,大大节省了成本,同时采用常规hplc检测,避免了仪器的限制。优选地,所述步骤(1)中,所述血浆样品的前处理过程为:在血浆样品中加入强碱溶液调节酸度至溶液的ph值为12以上,然后加入乙酸乙酯进行萃取、抽提,得到乙酸乙酯层;用盐酸溶液对乙酸乙酯层进行萃取、抽提,得到下层水相,将下层水相吹干;用盐酸溶液复溶,得到血浆样品上样液。由于采用spe方法处理血浆样品成本高,本发明采用液液萃取方法提取血浆中的利培酮和9-羟基利培酮,优化了提取条件及样品检测的色谱条件,利培酮和9-羟基利培酮的萃取率提高,同时消除了血浆中内源物质干扰,可方便、快速检测血浆中的利培酮和9-羟基利培酮,方法的专属性、准确度、精确度良好。优选地,所述步骤(1)中,所述血浆样品在进行前处理前,还加入内标物。更优选地,所述内标物为氯氮平,所述氯氮平与所述血浆样品的重量体积比为0.1μg/ml,即每毫升血浆样品中加入0.1μg氯氮平。优选地,所述乙酸乙酯与所述血浆样品的体积比为4:1。用乙酸乙酯旋涡振荡萃取抽提其中的利培酮和9-羟基利培酮,与使用乙醚相比,避免了ep、pp管(离心管)材质中可溶出组分对利培酮测定的干扰,利培酮和9-羟基利培酮的萃取率均在80%以上,上述体积比的乙酸乙酯,对利培酮和9-羟基利培酮的萃取效果更好。优选地,所述对乙酸乙酯层进行萃取、抽提的盐酸溶液中,盐酸的浓度为0.5mol/l~5mol/l,所述盐酸溶液与所述乙酸乙酯的体积比为1:100~1:20。更优选地,所述对乙酸乙酯层进行萃取、抽提的盐酸溶液中,盐酸的浓度为2mol/l,所述盐酸溶液与所述乙酸乙酯的体积比为3:80。发明人意外发现,上述浓度及体积的盐酸,可以将乙酸乙酯中利培酮和9-羟基利培酮提取到hcl溶液中,有效去除其中脂溶性物质,减少干扰,提高提取效果。优选地,所述对下层水相进行复溶的盐酸溶液中,盐酸的浓度为0.1mol/l。更优选地,所述盐酸溶液与所述血浆样品的体积比为3:20。优选地,所述强碱溶液为氢氧化钠溶液,所述氢氧化钠溶液中氢氧化钠的浓度为2mol/l。更优选地,所述氢氧化钠溶液与所述血浆样品的体积比为1:1。优选地,所述磷酸二氢钾溶液的ph值为2.0~6.0。本申请发明人经过大量尝试发现,磷酸二氢钾溶液的ph在上述范围之外时,利培酮和9-羟基利培酮和内标溶液保留时间均明显延后,样品分析时间变长,其中利培酮和内标峰变宽,拖尾,造成积分困难。更优选地,所述磷酸二氢钾溶液的ph值为4.0。本申请发明人意外发现,当磷酸二氢钾溶液的ph值为4.0时,峰型较好,与血浆中组分无干扰,各组分能有效分离,色谱条件最优。优选地,所述磷酸二氢钾溶液的浓度为0.05mol/l。当磷酸二氢钾溶液的浓度低于0.05mol/l时,9-羟基利培酮和血浆中组分分离度达不到要求(小于1.5),当磷酸二氢钾溶液的浓度大于0.05mol/l时,与0.05mol/l的浓度相比分离度没有明显改善,故磷酸二氢钾溶液的浓度选择为0.05mol/l。优选地,所述血浆样品中,利培酮和9-羟基利培酮的浓度分别为5~100ng/ml。相对于现有技术,本发明的有益效果为:本发明采用液液萃取方法提取血浆中的利培酮和9-羟基利培酮,采用c4色谱柱进行检测,优化了提取条件及样品检测的色谱条件,利培酮和9-羟基利培酮的萃取率提高,同时消除了血浆中内源物质干扰,可方便、快速检测血浆中的利培酮和9-羟基利培酮,方法的专属性、准确度、精确度良好。附图说明图1为本发明所述血浆样品的液相色谱图;图2为本发明所述空白血浆的液相色谱图;图3为利用无水乙醚提取血浆样品后的液相色谱图;图4为利用c18色谱柱对血浆样品进行测试的液相色谱图;图5为9-羟基利培酮与氯氮平的峰面积比与含药浓度的关系曲线图;图6为利培酮与氯氮平的峰面积比与含药浓度的关系曲线图。具体实施方式为更好的说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。其中,实施例中的仪器为:安捷伦1260高效液相色谱仪vwd检测器,色谱柱为资生堂proteonavi4.6mm×250mm,c4蛋白分析用色谱柱(孔径);实施例中的试剂为:磷酸二氢钾分析纯天津大茂化学试剂厂;乙腈色谱纯美国天地;利培酮、氯氮平对照品均购自中国食品与药品检定研究院;9-羟基利培酮对照品购自usp药典。实施例1本发明所述血浆中利培酮及9-羟基利培酮的检测方法的一种实施例,本实施例所述方法包括如下步骤:(1)将血浆样品进行前处理:在血浆样品中,按照氢氧化钠溶液与血浆样品的体积比为1:1,加入氢氧化钠浓度为2mol/l的氢氧化钠溶液,调节酸度至溶液的ph值为12以上,然后按照乙酸乙酯与血浆样品的体积比为4:1,加入乙酸乙酯,漩涡振荡5min,10000rpm离心10min,进行萃取、抽提,得到乙酸乙酯层;按照盐酸溶液与乙酸乙酯的体积比为1:100,用盐酸的浓度为0.5mol/l的盐酸溶液对乙酸乙酯层进行萃取、抽提,漩涡振荡5min,静置,得到下层水相,将下层水相吹干;按照盐酸溶液与血浆样品的体积比为3:20,用盐酸的浓度为0.1mol/l的盐酸溶液复溶,得到血浆样品上样液。(2)用高效液相色谱法对步骤(1)得到的血浆样品上样液进行测定,并分析血浆样品上样液的测定结果;其中,高效液相色谱条件为:色谱柱为资生堂proteonavi4.6mm×250mm,c4蛋白分析用色谱柱(孔径粒径5μm);流动相为0.05mol/l的磷酸二氢钾溶液(磷酸二氢钾溶液的ph值为2.0)和乙腈按照体积比为65:35进行混合的混合溶液,流速为0.5ml/min;检测波长为278nm;进样量为100μl;柱温为35℃。实施例2本发明所述血浆中利培酮及9-羟基利培酮的检测方法的一种实施例,本实施例所述方法包括如下步骤:(1)将血浆样品进行前处理:在血浆样品中,按照每毫升血浆样品中加入0.1μg氯氮平的比例,加入氯氮平混合均匀;按照氢氧化钠溶液与血浆样品的体积比为1:1,加入氢氧化钠浓度为2mol/l的氢氧化钠溶液,调节酸度至溶液的ph值为12以上,然后按照乙酸乙酯与血浆样品的体积比为4:1,加入乙酸乙酯,漩涡振荡5min,10000rpm离心10min,进行萃取、抽提,得到乙酸乙酯层;按照盐酸溶液与乙酸乙酯的体积比为3:80,用盐酸的浓度为2mol/l的盐酸溶液对乙酸乙酯层进行萃取、抽提,漩涡振荡5min,静置,得到下层水相,将下层水相吹干;按照盐酸溶液与血浆样品的体积比为3:20,用盐酸的浓度为0.1mol/l的盐酸溶液复溶,得到血浆样品上样液。(2)用高效液相色谱法对步骤(1)得到的血浆样品上样液进行测定,并分析血浆样品上样液的测定结果;其中,高效液相色谱条件为:色谱柱为资生堂proteonavi4.6mm×250mm,c4蛋白分析用色谱柱(孔径粒径5μm);流动相为0.05mol/l的磷酸二氢钾溶液(磷酸二氢钾溶液的ph值为4.0)和乙腈按照体积比为77:23进行混合的混合溶液,流速为1.5ml/min;检测波长为278nm;进样量为100μl;柱温为35℃。实施例3本发明所述血浆中利培酮及9-羟基利培酮的检测方法的一种实施例,本实施例所述方法包括如下步骤:(1)将血浆样品进行前处理:在血浆样品中,按照氢氧化钠溶液与血浆样品的体积比为1:1,加入氢氧化钠浓度为2mol/l的氢氧化钠溶液,调节酸度至溶液的ph值为12以上,然后按照乙酸乙酯与血浆样品的体积比为4:1,加入乙酸乙酯,漩涡振荡5min,10000rpm离心10min,进行萃取、抽提,得到乙酸乙酯层;按照盐酸溶液与乙酸乙酯的体积比为1:20,用盐酸的浓度为5mol/l的盐酸溶液对乙酸乙酯层进行萃取、抽提,漩涡振荡5min,静置,得到下层水相,将下层水相吹干;按照盐酸溶液与血浆样品的体积比为3:20,用盐酸的浓度为0.1mol/l的盐酸溶液复溶,得到血浆样品上样液。(2)用高效液相色谱法对步骤(1)得到的血浆样品上样液进行测定,并分析血浆样品上样液的测定结果;其中,高效液相色谱条件为:色谱柱为资生堂proteonavi4.6mm×250mm,c4蛋白分析用色谱柱(孔径粒径5μm);流动相为0.05mol/l的磷酸二氢钾溶液(磷酸二氢钾溶液的ph值为6.0)和乙腈按照体积比为85:15进行混合的混合溶液,流速为0.5ml/min;检测波长为278nm;进样量为100μl;柱温为35℃。实施例4本实施例对本发明所述血浆中利培酮及9-羟基利培酮的检测方法的检测效果进行了验证。空白血浆前处理:取空白血浆1ml至10mlep管中,加100μl1μg/ml的氯氮平溶液,混匀,加入1ml2mol/l的氢氧化钠溶液,混匀,加入4ml乙酸乙酯,漩涡振荡5min,10000rpm离心10min,取上层乙酸乙酯至5mlep管中(ep管中预先加入150μl2mol/l的hcl溶液),漩涡振荡5min,静置,弃去上层乙酸乙酯,下层水相用氮吹仪吹干,用150μl0.1mol/l的hcl复溶,进液相检测。血浆样品前处理:取利培酮、9-羟基利培酮浓度各为50ng/ml的血浆样品,前处理操作同空白血浆前处理的步骤。色谱柱为资生堂proteonavi4.6mm×250mm,c4蛋白分析用色谱柱(孔径);流动相为0.05mol/l的磷酸二氢钾溶液和乙腈按照体积比为77:23进行混合的混合溶液,流速为1ml/min;检测波长为278nm;进样量为100μl;柱温为35℃。检测结果:如图1和图2所示的液相色谱图中,横坐标为保留时间,纵坐标为信号强度,其中,血浆样品的液相色谱图1中,9-羟基利培酮的保留时间为6.716min,利培酮的保留时间为8.466min,氯氮平的保留时间为14.113min,由和图2空白血浆液相色谱图的对照中,可以看出,血浆样品在利培酮、9-羟基利培酮、氯氮平出峰处无干扰,利培酮和9-羟基利培酮分离良好。实施例5本实施例除了将实施例4中的乙酸乙酯换为无水乙醚外,其他方法步骤均同实施例4进行空白血浆、血浆样品中利培酮和9-羟基利培酮、氯氮平的检测。检测结果:血浆样品在9-羟基利培酮处有杂质峰,干扰样品测定,如附图3所示;通过和实施例4中的检测效果进行对比,进一步说明本发明有机溶剂选择乙酸乙酯的进步性。实施例6本实施例除了将实施例4中的色谱柱由c4更换为菲罗门gemini、安捷伦zorbaxsb-c18、luna色谱柱外,其他方法步骤均同实施例4进行对空白血浆、血浆样品中利培酮和9-羟基利培酮的检测。检测结果:血浆样品在9-羟基利培酮处,血浆中其他物质未完全分离,与9-羟基利培酮有重叠,干扰样品的测定,如附图4所示。这也进一步说明了本发明测定方法中选择c4色谱柱的进步性。实施例7本实施例通过实验探究对有机溶剂层进行萃取、抽提的盐酸溶液的浓度对利培酮、9-羟基利培酮、氯氮平的萃取效果。空白血浆和血浆样品制备同实施例4,分别制备利培酮、9-羟基利培酮浓度各为5ng/ml、20ng/ml、50ng/ml的血浆样品。在将乙酸乙酯中利培酮和9-羟基利培酮转移至水相时,水相溶液分别使用相同含量的2mol/lhcl溶液、0.1mol/lhcl溶液、ph2.2的磷酸盐缓冲液,比较利培酮、9-羟基利培酮、氯氮平的萃取率,实验结果如表1所示:表1不同浓度的盐酸溶液对利培酮、9-羟基利培酮、氯氮平的萃取效果从表1中可以看出,使用2mol/l的hcl溶液,利培酮、9-羟基利培酮、氯氮平均具有更高的萃取率。实施例8本实施例对流动相中磷酸二氢钾溶液的ph对利培酮、9-羟基利培酮、氯氮平的萃取效果的影响进行了相关探究。研究方法:按照实施例4方法制备空白血浆和血浆样品,分别使用ph3.0、ph4.0、ph5.0的磷酸二氢钾溶液和乙腈配制流动相,利用与实施例4中相同的方法检测利培酮、9-羟基利培酮、氯氮平。检测结果:使用ph3.0磷酸二氢钾溶液配制流动相时,三种物质的保留时间均提前,造成9-羟基利培酮与血浆中组分未完全分离,干扰9-羟基利培酮的检测;使用ph5.0磷酸二氢钾溶液配制流动相时,三种物质的保留时间明显延后,且色谱峰明显变宽,拖尾,造成积分困难;使用ph4.0磷酸二氢钾溶液配制流动相时,峰型良好,与血浆中组分无干扰,各组分能有效分离,色谱条件最优。实施例9本实施例按照生物样品分析方法指导原则,对本发明所述检测方法进行了专属性、标准曲线(线性、范围)、准确度、精密度、检测限、定量限等进行了验证。专属性分析:分别测定了6个不同个体的空白血浆,实验结果表明6个不同个体的空白血浆对活性成分及内标(氯氮平)的测定均无干扰。标准曲线:按照本发明所述检测方法制备了利培酮、9-羟基利培酮的浓度分别为5ng/ml~100ng/ml的血浆样品并进行了液相色谱检测,研究了利培酮、9-羟基利培酮与氯氮平的峰面积比与含药浓度之间的关系,具体数据结果如表2、表3、图5、图6所示。表29-羟基利培酮与氯氮平的峰面积数据含药浓度ng/ml9-羟利培酮峰面积内标峰面积9-羟利培酮/内标4.995957713913540.049.9910820513751500.0819.9823324512615850.1829.9736751213748000.2739.9652970514093480.3849.9561585613853970.4474.9297796714654150.6799.90131627613874270.95表3利培酮与氯氮平的峰面积数据浓度ng/ml利培酮峰面积内标峰面积利培酮/内标5.027858213913540.0610.0313065713751500.1020.0725634312615850.2030.1041611413748000.3040.1456331714093480.4050.1766136213853970.4875.26104356314654150.71100.35134061913874270.97从表2、表3中的数据可以看出,在利培酮、9-羟基利培酮的浓度分别为5ng/ml~100ng/ml的血浆样品浓度范围内,利培酮、9-羟基利培酮与氯氮平的峰面积相关系数的平方r2均大于0.99;从图5、图6可以看出,在上述含药浓度范围内,利培酮、9-羟基利培酮与氯氮平的峰面积比与含药浓度呈良好的线性关系。准确度、重复性探究:分别配制利培酮、9-羟基利培酮的浓度各为10ng/ml、20ng/ml、50ng/ml作为低、中、高含药浓度血浆样品,每个浓度平行5个样品,计算每个浓度样品的回收率及rsd,具体数据如表4所示。表4样品的回收率及rsd数据从表4中的数据可以看出,高、中、低三个浓度的样品回收率均在85%~115%的可接受范围内,rsd均小于15%,说明本发明所述检测方法的准确度和重复性良好。检测限、定量限:配制不同浓度的血浆样品,记录信噪比10为定量限浓度,信噪比3为检测限浓度,实验得到:利培酮和9-羟基利培酮的检测限为1ng/ml,定量限为5ng/ml。最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1