一种布洛芬、其钠盐及其制剂有关物质的检测方法与流程
本发明属于药品质量检测领域,特别是涉及一种布洛芬、其钠盐及其制剂有关物质的检测方法。
背景技术:
布洛芬(ibuprofen)是世界卫生组织、美国联邦药品管理局(fda)唯一共同推荐的儿童退烧药,是公认的儿童首选抗炎药。布洛芬具有抗炎、镇痛、解热作用。治疗风湿和类风湿关节炎的疗效稍逊于乙酰水杨酸和保泰松。适用于治疗风湿性关节炎、类风湿性关节炎、骨关节炎、强直性脊椎炎和神经炎等。而布洛芬钠由于溶解性好,更容易达到高的血药浓度。
目前,欧洲药典8.0版分别采用了反相色谱和气相色谱两套系统对布洛芬有关物质进行了检查,其中反相色谱控制了杂质a、b、d和杂质e,选择了柱长为15cm的十八烷基硅烷键合硅胶色谱柱及磷酸溶液-乙腈与乙腈的流动相体系梯度洗脱,一次洗脱时间为70min,洗脱时间较长。但经本发明人重复该检测方法,发现杂质a与主峰分离度低于1.5,无法实现有效分离,后将方法略作调整仍无法实现杂质a与主峰的完全分离。欧洲药典8.0版还利用衍生化气相色谱的方法试图对布洛芬中存在的毒性杂质g进行控制,但衍生化气相色谱法操作繁琐,且采用不常用的氦气作载气,因此该检测方法便利性较低,技术要求较高。
美国药典36版利用反相色谱只介绍了对布洛芬杂质f作为已知杂质进行控制,其监测的已知杂质较少。中国药典2015版与日本药典16版均采用薄层色谱法来检查布洛芬中的有关物质,但该方法无法实现杂质的准确定性与定量,只是粗略检查布洛芬中杂质情况。
此外,针对布洛芬钠盐的检测方法,尚未在各国药典或文献见到收载或报道。
技术实现要素:
面对上述技术问题,本发明提出一种布洛芬、其钠盐及其制剂有关物质的检测方法,本方法采用反相色谱系统对布洛芬及其钠盐中6中已知杂质(杂质a、b、c、d、e和杂质f)进行检测,以实现各色谱峰之间的有效分离(分离度大于1.5),准确定性及定量布洛芬及其钠盐中杂质情况。此外,本发明还提出一种采用正相色谱检测杂质g的方法,使得杂质g的检查更为方便。并且,利用上述方法可以对布洛芬及其钠盐制成的制剂的有关物质的检测。
为实现上述目的,本发明所述的一种布洛芬或其钠盐有关物质检测的方法,其中,所述有关物质包括杂质a、b、c、d、e和f,其包括:
供试品溶液的制备:取布洛芬或布洛芬钠原料适量,置一定体积量瓶中,加色谱条件下的流动相溶解后稀释至刻度,摇匀、滤过,得到一定浓度的供试品溶液;
样品检测:上述述供试品溶液注入色谱仪得到色谱图,其中色谱条件如下,
色谱柱:十八烷基硅烷键合硅胶为填充剂(250×4.6mm,5μm);
柱温:20~40℃;
流动相:有机相乙腈占水相磷酸水溶液的体积比为32%~48%,磷酸水溶液中磷酸加入量为0.01~0.1%(质量分数);
流速:1.0~2.3ml/min;
检测波长:205-225nm;
进样量:20μl。
进一步地,所述供试品溶液的浓度为2mg/ml;所述柱温为30℃。
具体地,所述磷酸水溶液中磷酸加入量为0.05%;所述乙腈占所述磷酸水溶液的体积比为40:60。
优选地,所述流速为2.0ml/min;所述检测波长为214nm。
本发明所述的一种检测有关物质杂质g的方法,包括:
供试品溶液的制备:取布洛芬或布洛芬钠原料适量,置一定体积量瓶中,加色谱条件下的流动相溶解后稀释至刻度,摇匀、滤过,得到一定浓度的供试品溶液;
样品检测:将上述供试品溶液注入色谱仪得到色谱图,其中色谱条件如下,
色谱柱:硅胶柱(4.6×250mm,5μm);
柱温:20~40℃;
流动相:正己烷、乙酸乙酯以及三氟乙酸混合物,其中,乙酸乙酯占总体积的2%~8%,三氟乙酸加入量为总体积的0.2%~1%;
流速:0.5~1.5ml/min;
检测波长:260~280nm;
进样量:20μl。
具体地,所述供试品溶液的浓度为5mg/ml;所述柱温为35℃。
进一步地,所述流动相正己烷:乙酸乙酯:三氟乙酸的体积比为97:3:0.95。
优选地,所述流速为1.0ml/min;所述检测波长为264nm。
本发明还提出了一种布洛芬钠片剂的有关物质进行检测的方法,其特征在于,所述方法包括:
供试品溶液的制备:取布洛芬钠片剂,除去包衣后,研细,取细粉适量,置一定体积量瓶中,加流动相适量,超声使布洛芬钠溶解,用流动相稀释至刻度,摇匀、滤过,制成布洛芬钠浓度约为2mg/ml和5mg/ml供试品溶液,分别注入色谱仪;其中,
2mg/ml的供试品溶液用于杂质a、b、c、d、e、f的检测,其色谱条件如下:
色谱柱:十八烷基硅烷键合硅胶为填充剂,250×4.6mm,5μm;
柱温:20~40℃;
流动相:有机相乙腈占水相磷酸水溶液的体积比例为32%~48%,磷酸水溶液中磷酸加入量为0.01~0.1%;
流速:1.0~2.3ml/min;
检测波长:205-225nm;
5mg/ml的供试品溶液用于杂质g的检测,其色谱条件如下:
色谱柱:硅胶柱,4.6×250mm,5μm;
柱温:20~40℃;
流动相:正己烷、乙酸乙酯以及三氟乙酸混合物,乙酸乙酯占总体积的2%~8%,三氟乙酸加入量为总体积的0.2%~1%;
流速:0.5~1.5ml/min;
检测波长:260~280nm。
此外,本发明提出了上述任一检测有关物质的方法在布洛芬或布洛芬钠制剂有关物质检测中的应用。
本发明所述方法能实现多种杂质的有效分离及定量检测,即实现各色谱峰之间的有效分离(分离度大于1.5),准确定性及定量布洛芬及其钠盐中杂质情况;采用本发明提出的杂质g的检测方法能更为便利地实现杂质g的控制;此外,利用本发明检测有关物质杂质a、b、c、d、e、f、g的方法可以实现对布洛芬或者布洛芬钠制剂有关物质的检测,并且该方法简便易行,能够准确地对杂质进行定性和定量。与现有技术相比,能够用更为简便的方法实现对布洛芬、布洛芬钠以及其制剂更多杂质的定性和定量,从而能提高药品的安全性。
附图说明
图1为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中采用ep8.0布洛芬有关物质检测方法检测含有6种杂质的布洛芬钠溶液的典型色谱图。
图2为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中采用经修改的ep8.0布洛芬有关物质检测方法检测混有6种杂质的布洛芬钠溶液的典型色谱图。
图3为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中柱温在20℃时含有6种杂质的布洛芬钠溶液的色谱图。
图4为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中柱温在40℃时含有6种杂质的布洛芬钠溶液的色谱图。
图5为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流动相中有机相比例为32%时含有6种杂质的布洛芬钠溶液的色谱图。
图6为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流动相中有机相比例为48%时含有6种杂质的布洛芬钠溶液的色谱图。
图7为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流速为1.0ml/min时含有6种杂质的布洛芬钠溶液的色谱图。
图8为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流速为2.3ml/min时含有6种杂质的布洛芬钠溶液的色谱图。
图9为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流动相中不加磷酸时含有6种杂质的布洛芬钠溶液的色谱图。
图10为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流动相磷酸加入量为0.025%时含有6种杂质的布洛芬钠溶液的色谱图。
图11为本发明关于杂质a、b、c、d、e和f的检测方法筛选过程中流动相磷酸加入量为0.1%时含有6种杂质的布洛芬钠溶液的色谱图。
图12为本发明关于杂质g的检测方法筛选过程中柱温在20℃时含有杂质g的布洛芬钠溶液的色谱图。
图13为本发明关于杂质g的检测方法筛选过程中柱温在40℃时含有杂质g的布洛芬钠溶液的色谱图。
图14为本发明关于杂质g的检测方法筛选过程中流动相中乙酸乙酯比例为2%时含有杂质g的布洛芬钠溶液色谱图。
图15为本发明关于杂质g的检测方法筛选过程中流动相中乙酸乙酯比例为8%时含有杂质g的布洛芬钠溶液色谱图。
图16为本发明关于杂质g的检测方法筛选过程中流速0.5ml/min时含有杂质g的布洛芬钠溶液色谱图。
图17为本发明关于杂质g的检测方法筛选过程中流速1.5ml/min时含有杂质g的布洛芬钠溶液色谱图。
图18为本发明关于杂质g的检测方法筛选过程中三氟乙酸加入量为0.2%时含有杂质g的布洛芬钠溶液色谱图。
图19为本发明关于杂质g的检测方法筛选过程中三氟乙酸加入量为0.8%时含有杂质g的布洛芬钠溶液色谱图。
图20为本发明关于杂质g的检测方法筛选过程中三氟乙酸加入量为1%时含有杂质g的布洛芬钠溶液色谱图。
图21为本发明关于布洛芬钠反向检测条件下的典型色谱图。
图22为本发明关于布洛芬钠正向检测条件下的典型色谱图。
图23为本发明关于布洛芬钠片剂反向检测条件下的典型色谱图。
图24为本发明关于布洛芬钠片剂正向检测条件下的典型色谱图。
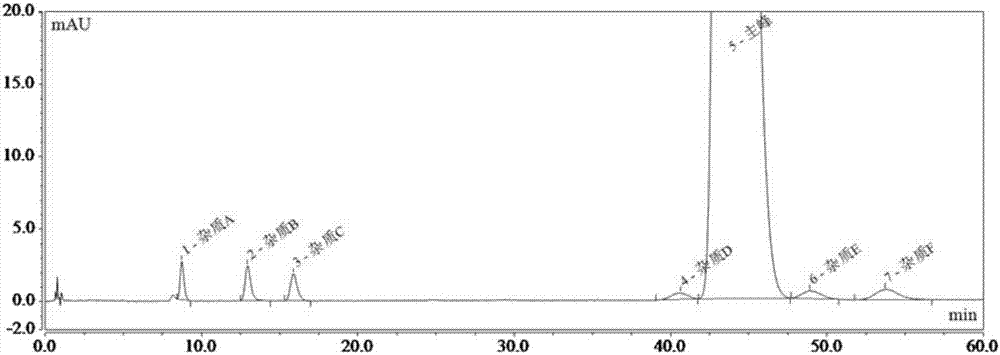
图25为本发明关于反向色谱系统的方法学研究的系统适应性色谱图;其中,(i)空白溶剂,(ii)供试品溶液,(iii)含有6种杂质的供试品溶液;其中,峰1-杂质a,峰2-杂质b,峰3-杂质c,峰4-杂质d,峰5-主峰,峰6杂质e,峰7-杂质f。
图26为本发明关于反向色谱系统的方法学研究的布洛芬钠破坏性试验色谱图;其中,
(a).未破坏;(b).酸破坏;(c).碱破坏;(d).氧化破坏;(e).光照破坏;(f).高温破坏。
图27为本发明关于正向色谱系统的方法学研究的含有杂质g的供试品溶液的典型色谱图;其中,峰1-未知杂质,峰2-溶剂峰,峰3-主峰和峰4-杂质g。
具体实施方式
如前所述,本发明旨在提出一种布洛芬、其钠盐及其制剂有关物质a、b、c、d、e、f和g的检测方法,以实现各杂质色谱峰之间的有效分离(分离度大于1.5),并准确定性及定量布洛芬、其钠盐及其制剂中的杂质情况。
达到本发明本发明目的主要使用的仪器与试药如下:
dv215cd电子天平(美国ohaus公司);dionexultimate3000高效液相色谱仪(美国dionex公司);shimadzulc-15c岛津高效液相色谱仪(岛津仪器(苏州)有限公司)。
磷酸(分析纯,上海凌峰化学试剂有限公司);乙腈(色谱纯,美国tedia公司);正己烷(色谱纯,天津康科德科技有限公司);三氟乙酸(分析纯,南京化学试剂有限公司);乙酸乙酯(分析纯,无锡市亚盛化工有限公司);水为市售纯净水(杭州娃哈哈集团)。
杂质a对照品,含量:99.5%(tlcpharmachem.,inc.);杂质b对照品,含量:97.4%(tlcpharmachem.,inc.);杂质c对照品,含量:99.8%(tlcpharmachem.,inc.);杂质d,含量:98.1%(tlcpharmachem.,inc.);杂质e对照品,含量:99.2%(tlcpharmachem.,inc.);杂质f对照品,含量:99.8%(tlcpharmachem.,inc.);杂质g(councilofeurope,europeandirectorateforthequalitycontrolofmedicines)。
布洛芬原料药:南京九寿堂医药科技有限公司;布洛芬钠原料药,批号:150630、150703、150710,南京九寿堂医药科技有限公司;布洛芬钠片剂,规格256mg,pfizerinc.。
需要注意的是,如未注明具体条件者,均按照常规条件或制造商建议的条件进行,如所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
本发明所检测的杂质化学结构式如下表:
下面,关于本发明布洛芬、其钠盐及其制剂杂质a、b、c、d、e、f和g的检测方法,将分以下几个方面逐一介绍。
一、关于杂质a、b、c、d、e和f的检测方法
本发明提供了一种布洛芬或其钠盐有关物质检测的方法,其有关物质包括杂质a、b、c、d、e和f,所述方法包括,供试品溶液的配制和样品检测两个步骤。
供试品溶液配制
分别取布洛芬钠样品和各杂质对照品适量,置于一定体积量瓶中,加流动相溶解稀释至刻度,摇匀、滤过。
样品检测
为了实现杂质a、b、c、d、e和f的有效分离(分离度大于1.5),我们参考了欧洲药典8.0版关于布洛芬的检测方法,拟定采用反相色谱系统围绕色谱柱、检测波长、柱温、流动相中有机相比例、流速、ph的考察(磷酸加入量)对色谱的条件进行筛选。具体筛选过程如下:
色谱柱的选择
在前期实验中,我们参考欧洲药典8.0中布洛芬有关物质条件,使用十八烷基硅烷键合硅胶作为填充剂(柱长:15cm)的色谱柱,发现杂质d与主峰分离度无法满足要求,典型色谱图见图1,即使适当改变欧洲药典8.0方法,分离效果有所改善,仍无法实现杂质d与主峰的分离度大于1.5,且保留时间较长,典型色谱图见图2。经过尝试增加色谱柱柱长以改善分离效果,即选择柱长为25cm的十八烷基硅烷键合硅胶为填充剂的色谱柱进行尝试,经初步试验,发现该类型色谱柱可实现各色谱峰之间的有效分离,分离度和峰形良好,满足检测的要求,因此,采用该类型色谱柱作进一步色谱条件优化。
检测波长的选择
利用紫外-可见分光光度计对各杂质及布洛芬钠进行全波长扫描,发现各杂质与布洛芬钠在低波长段200-225nm有较大吸收,同时我们参考了欧洲药典8.0布洛芬有关物质检查的检测波长选择波长,考虑205-225nm范围作为检测波长。
并且试验中发现,全波长扫描时发现在214nm波长时,色谱峰多,可代表的信息较全面,色谱峰基线平稳且各色谱峰分离较好,因此优选214nm作为检测波长。
柱温的考察
实验考察了不同柱温下样品与杂质的分离情况,发现柱温对保留时间有一定的影响。如果柱温增加,则保留时间降低,但不同温度如20℃、40℃下,各色谱峰均能各杂质与主峰及各杂质之间的分离度均符合要求,详见图3-4,因此考虑选择的温度范围为20~40℃。后期试验中,暂以30℃作为柱温做进一步色谱条件优化。
流动相中有机相比例考察
虽然随着流动相中有机相比例的增加,各色谱峰出峰时间缩短,但最难分离对杂质d与主峰的分离度却减小,详见图5-6。实验发现,流动相中有机相乙腈比例范围32%~48%时,分离度均能达到要求。后期试验中,暂以有机相乙腈比例为40%做进一步色谱条件优化。
流速的考察
在一定范围内,流速降低能够提高色谱峰的分离度,但同时保留时间也增加,典型色谱图见图7-8。实验发现,流速范围在1.0~2.3ml/min,分离度均能达到要求。后期试验中,暂选择流速2.0ml/min做进一步色谱条件优化。
ph的考察(磷酸加入量)
磷酸的加入降低了流动相ph,抑制酸性化合物的解离,因而能够改善峰形,但加入量过多,ph过低会对色谱柱有损伤,不同磷酸加入量的典型色谱图见图9-11。由图中可以看出,不加磷酸时峰形很差,磷酸加入量达到磷酸水溶液中的0.01%和0.1%时峰形均较好,优选磷酸加入量为0.05%。
通过以上筛选,我们得到的布洛芬钠有关物质杂质a、b、c、d、e和f的检测方法包括:
供试品溶液的制备:取布洛芬钠原料适量,置一定体积量瓶中,加色谱条件下的流动相溶解后稀释至刻度,摇匀、滤过,得到一定浓度的供试品溶液;
样品检测:上述述供试品溶液注入色谱仪得到色谱图,其中色谱条件如下,
色谱柱:十八烷基硅烷键合硅胶为填充剂(250×4.6mm,5μm);
柱温:20~40℃;
流动相:有机相乙腈占水相磷酸水溶液的体积比为32%~48%,磷酸水溶液中磷酸加入量为0.01~0.1%(质量分数);
流速:1.0~2.3ml/min;
检测波长:205-225nm;
进样量:20μl。
进一步地,所述供试品溶液的浓度为2mg/ml;所述柱温为30℃。
具体地,所述磷酸水溶液中磷酸加入量为0.05%;所述乙腈占所述磷酸水溶液的体积比为40:60。
优选地,所述流速为2.0ml/min;所述检测波长为214nm。
二、杂质g的检测方法
本发明还提供了一种布洛芬或其钠盐有关物质检测的方法,其有关物质包括杂质g,所述方法包括,供试品溶液的配制和样品检测两个步骤。
供试品溶液配制
分别取布洛芬钠样品和杂质g对照品适量,置于一定体积量瓶中,加流动相溶解稀释至刻度,摇匀、滤过。
样品检测
欧洲药典8.0版关于布洛芬杂质g的检测采用了衍生化气相色谱的方法,但此法操作繁琐,本发明为了更为方便实现杂质g的检测,拟定采用正相色谱围绕色谱柱、检测波长、柱温、流动相中乙酸乙酯比例、流速、流动相中三氟乙酸加入量对色谱的条件进行筛选。具体筛选过程如下:
色谱柱的选择
选择正相色谱常用的硅胶柱。
检测波长的选择
利用紫外-可见分光光度计对布洛芬钠和杂质g进行全波长扫描,发现两者在低波长段260~280nm有较大吸收,并且试验中发现,发现两者均在272nm和264nm处有最大吸收波长,色谱峰基线平稳且各色谱峰分离较好。后期试验中,暂选择264nm作为检测波长。
柱温的考察
实验考察了各柱温下杂质g与主峰分离效果,发现在较宽的温度范围内杂质g与主峰均能有效分离,如图12-13,因此考虑选择的温度范围为20~40℃。后期试验中,暂以35℃作为柱温做进一步色谱条件优化。
流动相中乙酸乙酯比例的选择
随着乙酸乙酯比例的降低,杂质g与主峰分离度提高,且在一定范围内,主峰峰形有所改善,典型色谱图见14-15。实验发现流动相中乙酸乙酯占总体积比例范围为2%~8%时,分离度均能达到要求。后期试验中,暂以乙酸乙酯比例为3%做进一步色谱条件优化。
流速的选择
色谱图见图16-17。当流速范围在0.5~1.5ml/min时,分离度均能达到要求。后期试验中,暂以流速1.0ml/min做进一步色谱条件优化。
流动相中三氟乙酸加入量考察
三氟乙酸加入量的增加可明显改善色谱峰拖尾的情况,但加入量过高,色谱峰会出现前延现象。实验发现三氟乙酸加入量体积分数为0.2%~1%时,峰形良好,典型色谱图见图18-20,优选三氟乙酸加入量的体积分数为0.95%。
通过以上筛选,我们得到的布洛芬钠有关物质杂质g的方法,包括:
供试品溶液的制备:取布洛芬或布洛芬钠原料适量,置一定体积量瓶中,加色谱条件下的流动相溶解后稀释至刻度,摇匀、滤过,得到一定浓度的供试品溶液;
样品检测:将上述供试品溶液注入色谱仪得到色谱图,其中色谱条件如下,
色谱柱:硅胶柱(4.6×250mm,5μm);
柱温:20~40℃;
流动相:正己烷、乙酸乙酯以及三氟乙酸混合物,其中,乙酸乙酯占总体积的2%~8%,三氟乙酸加入量为总体积的0.2%~1%;
流速:0.5~1.5ml/min;
检测波长:260~280nm;
进样量:20μl。
具体地,所述供试品溶液的浓度为5mg/ml;所述柱温为35℃。
进一步地,所述流动相正己烷:乙酸乙酯:三氟乙酸的体积比为97:3:0.95。
优选地,所述流速为1.0ml/min;所述检测波长为264nm。
此外,由于布洛芬钠盐由布洛芬和氢氧化钠反应成盐而来,且通过实验检测已表明两者均含有杂质a、b、c、d、e、f和g,并均可以用同样的方法检测。
综上所述,我们确定了最优选的布洛芬或其钠盐有关物质的检测方法,其测定色谱条件为:
(1)反相色谱条件,即杂质a、b、c、d、e和f的检测条件:
色谱柱:十八烷基硅烷键合硅胶为填充剂(250×4.6mm,5μm)
柱温:30℃
流动相:乙腈:0.05%磷酸水(40:60,v/v)
流速:2.0ml/min
检测波长:214nm
进样量:20μl
(2)正相色谱条件,即杂质g的检测条件
色谱柱:硅胶柱(4.6×250mm,5μm)
柱温:35℃
流动相:正己烷:乙酸乙酯:三氟乙酸(97:3:0.95,v/v/v)
流速:1.0ml/min
检测波长:264nm
进样量:20μl
反相及正相检测条件下布洛芬钠典型图谱分别见图21和图22,根据图谱我们发现,在上述反相色谱条件下,布洛芬钠的杂质a、b、c、d、e、f能被同时有效分离,主峰与杂质之间分离度均符合规定,因而该法能够用于杂质的定性和定量;利用上述正相色谱条件,布洛芬钠的杂质g能够被检测,将该发用于杂质g的定性和定量大大提高了其检测的简便程度。
三、布洛芬钠片剂有关物质的检测
本发明拟将上述杂质a、b、c、d、e、f、g的检测方法用于布洛芬钠片剂有关物质检测中,检测方法包括:
供试品溶液的制备:取布洛芬钠片剂,除去包衣后,研细,取细粉适量,置一定体积量瓶中,加流动相适量,超声使布洛芬钠溶解,用流动相稀释至刻度,摇匀、滤过,制成布洛芬钠浓度约为2mg/ml和5mg/ml的供试品溶液,分别注入色谱仪;其中,
2mg/ml的供试品溶液用于杂质a、b、c、d、e、f的检测,其色谱条件如下:
色谱柱:十八烷基硅烷键合硅胶为填充剂,250×4.6mm,5μm;
柱温:20~40℃;
流动相:有机相乙腈占水相磷酸水溶液的体积比例为32%~48%,磷酸水溶液中磷酸加入量为0.01~0.1%;
流速:1.0~2.3ml/min;
检测波长:205-225nm。
优选地,所述供试品溶液的浓度为2mg/ml;所述柱温为30℃;所述磷酸水溶液中磷酸加入量为0.05%;所述乙腈占所述磷酸水溶液的体积比为40:60;所述流速为2.0ml/min;所述检测波长为214nm。
5mg/ml的供试品溶液用于杂质g的检测,其色谱条件如下:
色谱柱:硅胶柱,4.6×250mm,5μm;
柱温:20~40℃;
流动相:正己烷、乙酸乙酯以及三氟乙酸混合物,乙酸乙酯占总体积的2%~8%,三氟乙酸加入量为总体积的0.2%~1%;
流速:0.5~1.5ml/min;
检测波长:260~280nm。
优选地,所述供试品溶液的浓度为5mg/ml;所述柱温为35℃;所述流动相正己烷:乙酸乙酯:三氟乙酸的体积比为97:3:0.95;所述流速为1.0ml/min;所述检测波长为264nm。
最终发现,按上述条件对有关物质进行检测得到的色谱峰基线平稳,各色谱峰分离以及峰形较好,因此,该法能够被用于布洛芬钠片剂的有关物质检测,按优选条件下测得的反向和正相典型色谱图分别见图23和图24。并且,本领域技术人员可以预料的是,上述任一检测有关物质杂质a、b、c、d、e、f、g的方法均可以用于布洛芬或布洛芬钠制剂有关物质的检测。
四、反向色谱系统的方法学研究
反相色谱系统溶液制备:供试品溶液:精密称取布洛芬钠样品适量,用流动相制成每1ml中含布洛芬钠2mg,作为供试品溶液;空白溶液:即流动相;对照品溶液:取各杂质对照品适量,置于同一量瓶中,用流动相稀释至刻度,摇匀、滤过,取续滤液作为对照品溶液;系统适用性溶液:分别取布洛芬钠样品与各杂质对照品适量,置于同一量瓶中,加流动相溶解稀释至刻度,摇匀、滤过,取续滤液作为系统适用性溶液。
系统适用性:各杂质与主峰及各杂质之间分离度均大于1.5,各色谱峰拖尾因子小于2.0,理论塔板数大于5000,因此,该方法系统适用性良好。代表性谱图见图25。
专属性:空白溶剂对各色谱峰无干扰,各色谱峰之间分离度良好。此外,样品经破坏,在高温及氧化破坏条件下有降解产物,降解产物与主峰均能有效分离,峰纯度符合要求。因此,该方法专属性较好,详见图26。
溶液稳定性:供试品溶液与对照品溶液于室温下放置24h后,色谱图均无明显变化,因此,溶液稳定性较好。
检测限定量限:精密称取各杂质对照品适量,以流动相溶解并依次稀释,分别取20μl注入高效液相色谱仪,记录色谱图。结果表明各杂质检测限定量限均低于报告限0.05%。
线性:取杂质a对照品约10mg,精密称定,置于一定体积量瓶中,用流动相溶解并稀释至刻度,摇匀,作为杂质a对照品母液;同法配制杂质b、杂质c、杂质d、杂质e和杂质f对照品母液。分别精密量取各杂质对照品母液适量,稀释得到一系列浓度对照品溶液,再分别取20μl注入高效液相色谱仪,记录色谱图。结果表明各杂质在一定范围内线性关系良好,相关系数均大于0.999。
精密度:包括重复性和中间精密度,按拟定的方法配制6份供试品溶液,分别进样,结果表明,各杂质与主峰的峰面积rsd值均低于2.0%,方法精密度良好。
准确度:精密称取布洛芬钠样品一定量,置于一定体积量瓶中,向其中分别加入50%水平、100%水平、150%水平的各杂质对照品溶液,再用流动相稀释至刻度作为样品溶液。每个浓度水平配制3份平行样。方法准确度采用加样回收率计算,经试验,各杂质回收率均在95%~105%范围内,各杂质回收率rsd值均低于2.0%,表明各杂质回收率良好。
耐用性:通过改变柱温、流速、流动相中有机相比例以及选择不同品牌批号色谱柱,各色谱峰均能有效分离,表明该方法耐用性良好。
5正相色谱系统的方法学研究
正相色谱系统溶液制备:供试品溶液:精密称取布洛芬钠样品适量,用流动相制成每1ml中含布洛芬钠5mg,作为供试品溶液;空白溶液:即流动相;对照品溶液:取杂质g对照品适量,置于一定体积量瓶中,用流动相稀释至刻度,摇匀、滤过,作为对照品溶液;系统适用性溶液:分别取布洛芬钠样品与杂质g对照品适量,置于同一量瓶中,加流动相溶解稀释至刻度,摇匀、滤过,取续滤液作为系统适用性溶液。
系统适用性:杂质g与主峰间分离度均大于1.5,各色谱峰拖尾因子小于2.0,理论塔板数大于5000,因此,该方法系统适用性良好。代表性谱图见图27。
专属性:空白溶剂对各色谱峰无干扰,杂质与主峰分离度良好。此外,样品经破坏,在高温及氧化破坏条件下有降解产物,降解产物与主峰均能有效分离。因此,该方法专属性较好。
溶液稳定性:供试品溶液与对照品溶液于室温下放置24h后,色谱图均无明显变化,因此,溶液稳定性较好。
检测限定量限:精密称取杂质g对照品适量,以流动相溶解并依次稀释,分别取20μl注入高效液相色谱仪,记录色谱图。结果表明,杂质g检测限定量限均低于报告限0.05%。
线性:取杂质g对照品约10mg,精密称定,置于一定体积量瓶中,用流动相溶解并稀释至刻度,摇匀,作为杂质g对照品母液;精密量取杂质g对照品母液适量,稀释得到一系列浓度对照品溶液,再分别取20μl注入高效液相色谱仪,记录色谱图。结果表明,杂质g在一定范围内线性关系良好,相关系数大于0.999。
精密度:包括重复性和中间精密度,按拟定的方法配制6份供试品溶液,分别进样,结果表明,杂质g与主峰峰面积rsd值均低于3.0%,方法精密度良好。
准确度:精密称取布洛芬钠样品一定量,置于一定体积量瓶中,向其中分别加入50%水平、100%水平、150%水平的杂质g对照品溶液,再用流动相稀释至刻度作为样品溶液。每个浓度水平配制3份平行样。方法准确度采用加样回收率计算,经试验,杂质g回收率在95%~105%范围内,回收率rsd值低于3.0%,表明该方法回收率良好。
耐用性:通过改变柱温、流速以及流动相中有机相比例,各色谱峰均能有效分离,表明该方法耐用性良好。
以上实施方式不用于限制本发明,本发明的保护范围由权利要求书限定。本领域技术人员可以在本发明的实质和保护范围内,对本发明做出各种修改或等同替换,这种修改或等同替换也应视为落在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!