一种可变电容式微纳米生物检测芯片及其加工方法与流程
本发明属于医疗器械技术领域,具体涉及一种可变电容式微纳米生物检测芯片及其加工方法该芯片可用于临床生物样本快速检测与诊断。
背景技术:
目前临床诊断中对抗原、抗体、小分子物质的检测主要以胶乳增强免疫比浊法、化学发光法、免疫荧光法、胶体金法等方法为主,均以光学原理为基础,光学仪器的分析精密度为≤5%,检测范围从0.001-3.500abs,存在精密度一般,检验范围较窄的情况。而细菌检测临床以培养为主,存在操作麻烦、检测周期长、漏检率高等问题。病毒检验一般是以pcr扩增的方式进行检测,检测过程麻烦,需要专门的pcr实验室,检验周期长。dna或片段目前的检测方式主要为基因测序,代价高,成本昂贵。
技术实现要素:
本发明的目的是提供一种可变电容式微纳米生物检测芯片及其加工方法,该芯片可用于蛋白质、细菌、病毒、dna或片段、其它小分子有特异性结合物质的快速检测。
本发明解决技术问题采用如下技术方案:
一种可变电容式微纳米生物检测芯片,其特点在于,包括
一极板一,所述极板一上设有若干个检测孔,所述检测孔底部通过一层弹性绝缘薄膜封底,被封底的检测孔内自底部覆有一层导体或半导体镀膜;位于所述检测孔底部的导体或半导体镀膜上表面固化有可发生特异性结合的物质;
一极板二,所述极板二的上表面覆有一层与极板一检测孔面积相匹配的导体或半导体镀膜。
进一步,所述极板一的上表面和极板二上的上表面均设有与对应导体或半导体镀膜连接的测量触点。
进一步,所述的检测孔底部弹性绝缘薄膜厚度为10nm-100μm。
进一步,所述的检测孔底部的导体或半导体镀膜厚度为10nm-5000nm。
进一步,所述检测孔的个数为1个或2个或2个以上;所述检测孔的直径为50μm-2cm。
进一步,所述检测孔底部及内壁均覆有导体或半导体镀膜,所述检测孔底部的导体或半导体镀膜与弹性绝缘薄膜结合为一体式柔性可变形薄膜。
一种可变电容式微纳米生物检测芯片检测器,其特点在于,包括如上所述的极板一和极板二,所述检测器还包括一用于可拆卸固定极板一和极板二的支架或固定座,以及一连接极板一和极板二测量触电的检测仪,所述检测仪用于检测极板一和极板二间的电容值。
进一步,所述极板一和极板二间的介电介质为气体,所述极板一和极板二的导体或半导体镀膜间距为10nm-5mm。
一种生物样本定性或定量检测方法,其特点在于,将可发生特异性结合的物质通过化学或物理手段固化在权利要求1所述的极板一上,当被检测样品通过检测孔时,若被检测样品中含有与极板一上固化的物质发生特异性结合的成分时,则两种物质发生特异性结合,产生收缩力,极板一薄膜收缩,通过极板一、极板二间的电容值来判定待测样品中是否还有特定成分及特定成分的含量多少。
一种可变电容式微纳米生物检测芯片的加工方法,其特点在于,包括如下步骤:
一、极板一加工
a1:以绝缘或半导体基材为极板一,通过化学气相沉积法,在基材的上下表面同时生长弹性绝缘薄膜;
a2:首先在弹性绝缘薄膜上蚀刻出若干检测孔,裸漏出基材,然后再蚀刻掉检测孔下的基材至基材下表面的弹性绝缘薄膜;
a3:在检测孔内镀上相应的导体或半导体材料;并保证极板一测量触点可以从该导体或半导体镀膜中连续延伸出来;
a4:在位于检测孔底部的导体或半导体镀膜上表面进行生物活性化处理,固化可与后续检测物质发生特异性结合的物质;极板一加工完成;
二、极板二加工
b1:以绝缘基材为极板二,在极板二基材的上表面镀上一层与极板一检测孔面积相匹配的导体或半导体镀膜区域;极板二加工完成。
与已有技术相比,本发明有益效果体现在:
本发明是以被检测物的特异性结合为基础,以力学形变带动微电容的变化为原理,通过测定检测器电容的变化,定量或定性测定样本中的被测物,理论测量范围从0.0001pf—9.9999f,测量精度为0.1%,具有很高的测试线性范围和测量精度。
附图说明
图1为本发明芯片极板一结构示意图。
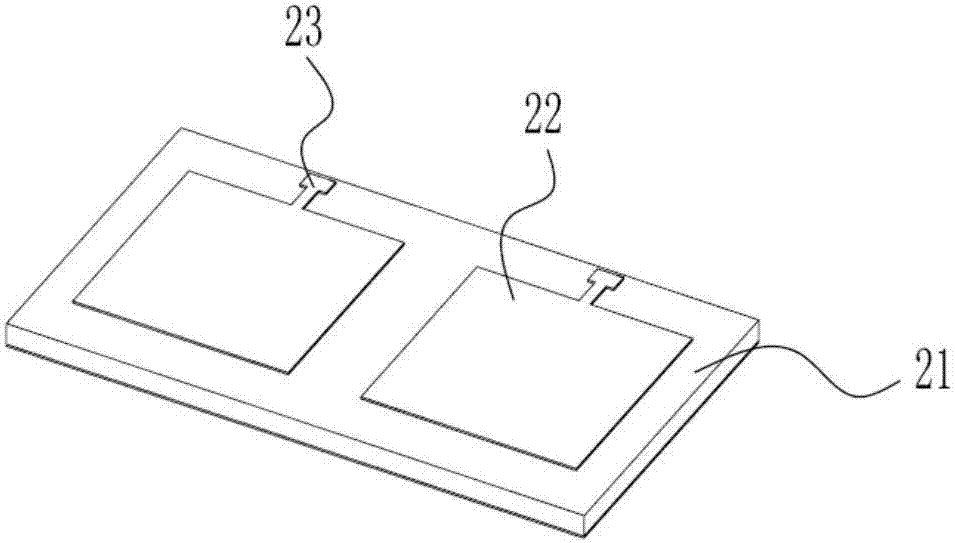
图2是本发明芯片极板二结构示意图。
图3为极板一的分解示意图。
图4为极板二加工示意图。
图5为本发明极板一加工流程图。
图6是本发明实施例5试验结果。
图中附图标记:
11、极板一;
12、导体或半导体镀膜;
13、检测孔;
14、极板一测量触点;
15、弹性薄膜;
16、特异性结合物质
21、极板二;
22、导体或半导体镀膜;
23、极板二测量触点;
3、模具。
具体实施方式
下面结合实施例,对本发明作进一步地描述。
以下实施例中,导体或半导体镀膜包括但不限于au、pt、cu、al及其它导体或半导体材料;极板一基材包括但不限于晶圆、有机玻璃,极板二基材为任意绝缘材料。
实施例1
一种可变电容式微纳米生物检测芯片,包括极板一和极板二。
如图1、3所示,极板一11包括绝缘基材本体,基材本体上设有1个或多个检测孔13,检测孔底部通过一层弹性绝缘薄膜15封底,被封底的检测孔13内自底部覆有一层导体或半导体镀膜12;位于所述检测孔底部的导体或半导体镀膜上表面固化有可发生特异性结合的物质16;
具体实施时,检测孔底部及内壁均覆有导体或半导体镀膜,检测孔底部的导体或半导体镀膜与弹性绝缘薄膜结合为一体式柔性可变形薄膜。
如图2所示,极板二21包括绝缘基材本体,极板二的上表面覆有一层与极板一检测孔面积相匹配的导体或半导体镀膜22。
在具体实施应用时,为了便于对极板一/极板二间的电容值检测,在极板一和极板二上的上均设有与相应导体或半导体镀膜连接的极板一测量触点14和极板二测量触点23。
其中,具体应用中导体或半导体镀膜厚度为10-5000nm;弹性绝缘薄膜厚度为10nm-100μm;检测孔的直径为50μm-2cm。
实施例2
该实施例为一种可变电容式微纳米生物检测芯片检测器,包括实施例1中的极板一和极板二,该检测器还包括一用于可拆卸固定极板一和极板二的支架或固定座(如现有结构形式中的夹具夹持固定或卡槽式固定座卡合固定)以及一连接极板一和极板二测量触点的检测仪,检测仪用于检测极板一和极板二间的电容值。该检测器中极板一和极板二间的介电介质为气体为宜,其中极板一和极板二的导体或半导体镀膜间距约为50μm。
实施例3
一种生物样本定性或定量检测方法,具体是将可发生特异性结合的物质通过化学或物理手段固化在实施例1的极板一上,当被检测样品通过检测孔时,若被检测样品中含有与极板一上固化的物质发生特异性结合的成分时,则两种物质发生特异性结合,产生收缩力,极板一薄膜收缩,通过极板一、极板二间的电容值来判定待测样品中是否还有特定成分及特定成分的含量多少。
例如,将抗原通过化学或物理手段固化在极板一检测孔中的导体或半导体镀膜上表面,当被检测样品通过或停留在检测孔中时,若被检测样品中含有对应于抗原的抗体,则抗体与极板表面的抗原特异性结合,产生收缩力,正、极板二间的电容值发生变化,从而可以对样品进行定性检测;同时也可以通过正、极板二间的电容值的变化量来检测样本中与抗原相对的抗体含量。
实施例4
以下进一步提供一种实施例1芯片的加工方法。
一、极板一制作
参见图5,制作方法如下:
步骤(1):使用低压化学气相沉积(lpcvd)方法,在450μm厚、直径100mm的双面抛光的硅晶圆两侧面上同时生长500nm厚的氮化硅(sin)薄膜,形成上氮化硅薄膜和下氮化硅薄膜;
步骤(2):使用标准紫外光刻技术(uvphotolithography)和反应式离子刻蚀技术(reactiveionetching,rie),在上氮化硅薄膜12上蚀刻出若干个直径为6mm的检测孔,使硅晶圆暴露出来;
步骤(3):使用深反应式离子刻蚀技术(deepreactiveionetching,drie)将暴露出的硅晶圆材料完全刻蚀,不贯通下氮化硅薄膜,形成极板一检测孔;
步骤(4):通过金属镀膜技术(如:电子束蒸发镀膜),在极板一检测孔底部及内壁上沉积厚度为50nm的金膜,同时在极板一上表面形成测量触点,镀膜由于金膜冷却收缩,从而使导体或半导体镀膜与弹性绝缘薄膜结合为一体的柔性可变形薄膜形成一个弧度膜。
步骤(5):在检测孔底部固化dna,巯基化的单链dna直接通过自身巯基的硫原子共价结合到金膜的表面;完成极板一的加工。
二、极板二加工
步骤(1):选择亚克力板为极板二基材,如图4所示,制作指定形状的模具3,将模具3贴合在极板二上,通过电子蒸发镀膜技术,在极板二未被模具3遮盖的表面镀上一层100nm厚的金膜区域,该区域与极板一的检测孔面积相当或稍大,且从该区域引出极板二测量触点,极板二完成。
实施例5
将实施例4加工所得的极板一/极板二通过固定夹具进行上下正对固定,在夹具中,极板一/极板二间金膜的间距约为50μm,然后将极板一、极板二的检测触点通过信号接口连接组件(安捷伦keysight16048a)连接至电容检测仪(安捷伦keysighte4980al)。检测时,向检测孔中按顺序分别加入以下待测液体:1.缓冲液(1mpbs),2.非互补不相匹配的dna单链(1μm的dna单链在pbs缓冲液中),3.互补相匹配的dna单链(1μm的dna单链在pbs缓冲液中),每次加入的液滴容量为300μl,所得结果如图6所示。
以上所述仅为本发明的实施例,并非因此限制本发明型的专利范围,凡是利用发明说明书及附图内容所作的等效结构或等效流程变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!