用于确定先兆子痫的风险的测定方法与流程
本发明涉及来自妊娠女性的样品中fk506结合蛋白样(fkbpl)的检测,以及fkbpl作为发展先兆子痫(pre-eclampsia)的预测性生物标志物的用途。本发明还涉及用于检测fkbpl的试剂盒和预防先兆子痫的方法。
背景
先兆子痫(pe)是一种影响一些妊娠女性的状况,症状通常在妊娠34周后出现。先兆子痫在5%-8%的妊娠中发生,引起显著的母亲和胎儿的发病率和死亡率。
目前,pe是基于临床症状,例如伴随或不伴随蛋白尿的血压升高进行诊断的。在不存在蛋白尿时,以下任何症状,诸如血小板减少症(血小板<100,000/μl)、肝功能受损、进行性肾功能不全、肺水肿或脑或视觉障碍,也将指示pe的诊断。然而,单独的临床标准可能不足以预测不良结果。
因此,需要生化测定来在妊娠早期预测pe发展的风险。这将允许更密切地监测处于发展pe的高风险的女性,以预防与潜在的pe相关的并发症,并将允许在妊娠早期开始潜在的新治疗。这样的测试还可以减少妊娠晚期被诊断患有pe的女性或未被准确诊断的女性和早产所需的昂贵的急救护理。
发明概述
本发明人已经确定,fkbpl蛋白和/或基因表达水平可以提供妊娠女性是否处于pe的增加的风险的早期指示。这是基于他们确定在妊娠期间发展pe的女性中fkbpl蛋白表达水平降低。
因此,本发明提供了一种确定妊娠女性中先兆子痫的风险的方法,该方法包括:
a)量化在第一时间点从妊娠女性采集的生物样品中fkbpl的表达水平;
b)量化在第二时间点从妊娠女性采集的生物样品中fkbpl的表达水平,其中第二时间点在妊娠中晚于第一时间点;
c)将在第一时间点和第二时间点的所述表达水平进行比较;
其中如果存在从第一时间点至第二时间点的所述表达水平的降低,则所述女性处于发展先兆子痫的增加的风险。
本发明还提供了一种确定妊娠女性中先兆子痫的风险的方法,该方法包括:
a)在第一时间点从妊娠女性采集第一生物样品;
b)量化第一生物样品中fkbpl的表达水平;
c)在第二时间点从妊娠女性采集第二生物样品,其中第二时间点在妊娠中晚于第一时间点;
d)量化第二生物样品中fkbpl的表达水平;和
e)将在第一时间点和第二时间点的所述表达水平进行比较,
其中如果存在从第一时间点至第二时间点的所述表达水平的降低,则所述女性处于发展先兆子痫的增加的风险。任选地,该方法还包括如果检测到从第一时间点至第二时间点的所述表达水平的降低,则选择所述女性进行额外的产前监测。
在本发明的另一方面,提供了一种检测妊娠女性中fkbpl的方法,该方法包括:
a)在第一时间点从妊娠女性采集第一生物样品;和
b)通过将样品与抗fkbpl抗体接触并检测fkbpl和抗体之间的结合来量化第一生物样品中的fkbpl。优选地,该方法还可以包括在第二时间点从妊娠女性采集第二生物样品,并通过将样品与抗fkbpl抗体接触并检测fkbpl和抗体之间的结合来量化第二生物样品中的fkbpl蛋白水平,其中第二时间点在妊娠中晚于第一时间点。任选地,该方法包括首先选择妊娠女性进行测试和/或将在第一时间点和第二时间点的fkbpl水平进行比较。
在本发明的另一方面,提供了一种检测妊娠女性中fkbpl的方法,该方法包括通过将在第一时间点从妊娠女性采集的第一生物样品与抗fkbpl抗体接触并检测fkbpl和抗体之间的结合来量化第一生物样品中的fkbpl蛋白水平。优选地,该方法还可以包括通过将在第二时间点从妊娠女性采集的第二生物样品与抗fkbpl抗体接触并检测fkbpl和抗体之间的结合来量化第二生物样品中的fkbpl蛋白水平,其中第二时间点在妊娠中晚于第一时间点。任选地,该方法包括首先选择妊娠女性进行测试和/或将在第一时间点和第二时间点的fkbpl水平进行比较。
在本发明的另一方面,提供了一种确定先兆子痫风险的方法,其中仅采集一个生物样品。例如:
-量化在妊娠的第5周-第30周之间从妊娠女性采集的生物样品中fkbpl的表达水平;
-将fkbpl的表达水平与对照标准或对照样品中fkbpl的表达进行比较;
其中如果与所述对照标准或所述对照样品中fkbpl的表达相比,所述生物样品中fkbpl表达存在降低,则所述女性处于发展pe的增加的风险。
在本发明的另一方面,提供了一种预防妊娠女性中先兆子痫的方法,该方法包括:
a)在第一时间点从妊娠女性采集第一生物样品;
b)量化第一生物样品中fkbpl的表达水平;
c)在第二时间点从妊娠女性采集第二生物样品,其中第二时间点在妊娠中晚于第一时间点;
d)量化第二生物样品中fkbpl的表达水平;和
e)将在第一时间点和第二时间点的所述表达水平进行比较,和
f)如果存在从第一时间点至第二时间点的所述表达水平的降低,则施用治疗有效量的fkbpl激动剂。
在本发明的另一方面,提供了fkbpl激动剂,所述fkbpl激动剂用于在预防妊娠女性中先兆子痫的方法中使用。任选地,该方法还包括:
a)量化在第一时间点从妊娠女性采集的生物样品中fkbpl的表达水平;
b)量化在第二时间点从妊娠女性采集的生物样品中fkbpl的表达水平,其中第二时间点在妊娠中晚于第一时间点;
c)将在第一时间点和第二时间点的表达水平进行比较;和
d)如果存在从第一时间点至第二时间点的所述表达水平的降低,则施用治疗有效量的fkbpl激动剂。
fkbpl激动剂可以是他汀类(statin),任选地普伐他汀(pravastatin);贝特类(fibrate),任选地非诺贝特(fenofibrate);芪类(stilbenoid),任选地白藜芦醇(resveratrol);或者二甲双胍。
关于从妊娠女性采集生物样品的时间点,第一时间点可以是在妊娠的第3周-第14周之间,优选地在妊娠的第10周-第14周之间;并且第二时间点可以是在妊娠的第15周-第30周之间,优选地在妊娠的第15周-第23周之间。当只采集一个样品时,这可以从妊娠的第10周-第20周采集。
生物样品可以是血液、血浆、血清或胎盘。
fkbpl表达水平优选地使用特异性结合fkbpl蛋白的蛋白例如抗体来确定。
在本发明的另一方面,提供了fkbpl作为妊娠女性中先兆子痫的生物标志物的用途。
在本发明的另一方面,提供了一种试剂盒,所述试剂盒包含选自以下的试剂:具有针对fkbpl的结合特异性的抗体、抗体衍生物或抗体片段,所述试剂盒用于在诊断妊娠女性是否处于先兆子痫的增加的风险的方法中使用。
确定或测试fkbpl表达水平可以包括量化fkbpl蛋白表达或分泌;和/或量化fkbpl基因表达。
待测试的妊娠女性可以患有妊娠前糖尿病。
本发明的这些方面和另外的方面仅通过示例的方式在下文更详细地并参考所附的实施例来描述。
附图描述
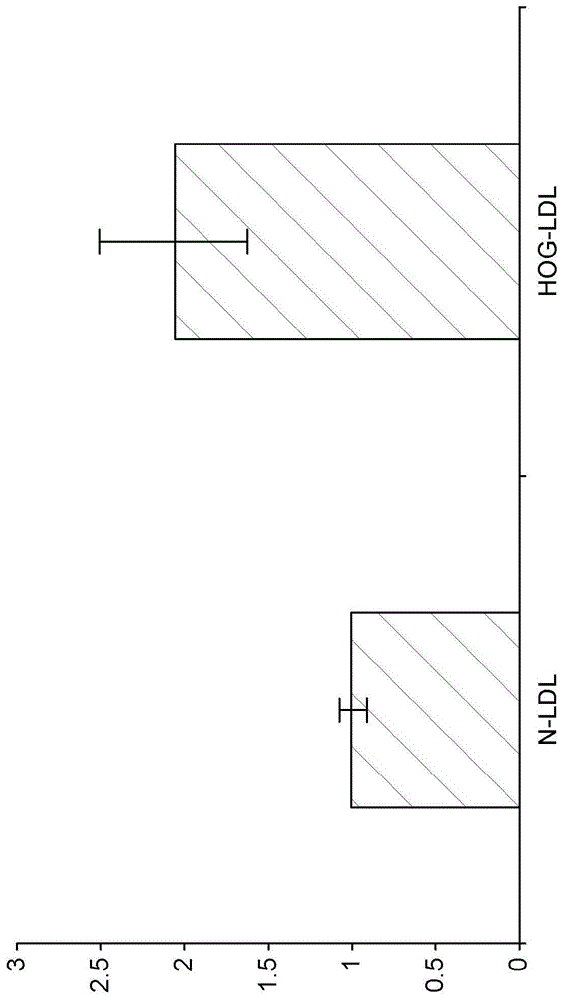
图1示出了在用高度氧化和糖化的脂蛋白(hog-ldl;代表氧化应激)处理后的htr8.sv.neo细胞中fkbpl蛋白水平的上调。在不含血清的培养基中,使用25μg/ml的hog-ldl或天然(n)-ldl持续24小时进行处理。误差棒:sem;n≥3(非配对t检验)。
图2示出了用高葡萄糖(10mm-40mm)处理48h后bewo细胞中fkbplmrna水平的上调(n=3,t=48h)。变化被测量为fkbplmrna与对照葡萄糖浓度(5.5mm)相比的倍数变化。误差棒:sem;n≥3。
图3示出了暴露于低氧24h后htr8.sv.neo滋养层细胞中fkbpl蛋白表达的下调。误差棒:sem;n≥3。
图4示出了暴露于低氧24h后huvec(人脐静脉内皮细胞)中fkbpl蛋白表达的下调。误差棒:sem;n≥3。
图5示出了用dmog(hif-1α活化剂;10μm)处理24h后htr8.sv.neo细胞中fkbplmrna水平的下调。在含血清的培养基中用4-hne(脂质过氧化产物;10μm)处理后未观察到变化。误差棒:sem,n≥3。
图6示出了在含血清培养基中用4-hne(10μm)或dmog(10μm)处理后bewo滋养层细胞系中fkbpl蛋白表达的下调。误差棒:sem,n≥3。
图7示出了在合体滋养细胞(syncytiotrophoblast)和内皮细胞中强烈地检测出绒毛膜绒毛内的fkbpl蛋白表达(a)。还呈现了绒毛膜绒毛中内皮/血管的cd31染色(b)。
图8示出了仅在发展pe的患有1型糖尿病的女性中,在妊娠第1期(firsttrimester)和妊娠第2期(secondtrimester)之间的fkbpl血浆水平的下调。血浆fkbpl水平使用elisa测量,并在妊娠第1期和妊娠第2期之间进行wilcoxon符号秩检验。dm-:非糖尿病(v1,n=16;v2,n=12;v3,n=12);dm+pe-:1型糖尿病、未患先兆子痫(v1,n=19;v2,n=16;v3,n=13);dm+pe+:1型糖尿病、患有先兆子痫(v1,n=17;v2,n=14;v3,n=16)。误差棒:标准差。
图9示出了与健康对照(对照,n=53)相比,在妊娠15周发展先兆子痫的未患糖尿病的初产(nulliparous)女性(pe,n=52)的更低的血浆fkbpl水平。进行了学生t检验,以确定发展了先兆子痫的女性和健康对照的组之间的任何显著差异。误差棒:标准差。
图10示出了在5周时非诺贝特增加了非糖尿病大鼠中fkbpl蛋白水平。使用链脲佐菌素(stz)注射使大鼠患糖尿病,并将非诺贝特治疗作为食物(chowfood)的一部分给予,持续4周。误差棒:sem;每组中n=6。
图11示出了非诺贝特酸(ffa;10μm)增加了htr8.sv.neo滋养层细胞中的fkbpl蛋白水平。非诺贝特酸(ffa)是非诺贝特在细胞培养物中的活性形式。确定了针对媒介物对照归一化的相对蛋白水平。误差棒:sem;n=3。
图12a和12b示出了在暴露于低氧(1%)后二甲双胍(10μm)上调huvec中的fkbpl(a)。(b)示出了fkbpl、sirtuin-1(sirt1)水平(对照)和α微管蛋白(一种管家蛋白)的蛋白印迹。fkbpl表达针对媒介物对照处理进行归一化。vc-媒介物对照。误差棒:sem,n≥3。
图13示出了(a)二甲双胍处理(10μm)不影响常氧(normoxia)条件下huvec中的fkbpl的水平。(b)示出了fkbpl、sirtuin-1(sirt-1)水平(对照)和α微管蛋白(一种管家蛋白)的蛋白印迹。fkbpl表达针对媒介物对照处理进行归一化。误差棒:sem,n≥3。
详细描述
先兆子痫(pe)是一种仅在妊娠期间发生的紊乱(disorder),并且影响母亲和未出生的婴儿两者。影响所有妊娠的至少5%-8%,pe是一种快速进行性状况(condition),以高血压和尿液中出现蛋白为特征。脚踝肿胀、体重突然增加、头痛和视力改变是另外的重要症状。然而,一些具有快速进展性疾病的女性被报道几乎没有症状。
通常,pe发生于妊娠晚期:在妊娠第3期(inthe3rdtrimester)。适当的产前护理对诊断和管理pe至关重要。在全球,pe和其他妊娠高血压紊乱是母婴疾病和死亡的一个主要原因。据保守估计,这些紊乱是每年76,000名母亲和500,000名婴儿死亡的原因。pe的确切原因尚不清楚。然而,专家认为可能是因为由于氧和营养物的血液供应受限导致的胎盘发育不良。
fkbpl作为生物标志物
本发明人已经发现fkbpl可以用作发展pe的生物标志物。即,来自妊娠女性的样品中fkbpl的水平可以提供关于发展pe的风险或可能性的指示。
fkbpl
fkbpl属于fk506结合蛋白的家族。它是血管发生(angiogenesis)的重要调控物,并靶向cd44途径。
“fkbpl”意指包括全长fkbpl以及fkbpl变体、fkbpl片段和fkbpl变体片段。为了简洁,fkbpl用于表示fkbpl蛋白和fkbpl基因两者。
fkbpl可以由核苷酸序列编码:
(登录号nm_022110)
并且可以具有氨基酸序列:
或其变体或片段。
fkbpl蛋白变体可以具有插入到fkbpl(seqidno2)中、从fkbpl(seqidno2)中缺失或在fkbpl(seqidno2)中被取代的25个或更少、更优选地15个或更少、甚至更优选地10个或更少、2个或更少的氨基酸;同时提供具有fkbpl活性的蛋白。
可选地,变体可以与fkbpl(seqidno2)具有至少30%、40%、50%、60%、70%、80%、90%、95%或99%的同一性,同时保持fkbpl活性。
多种功能测定可用于测试fkbpl活性。例如,fkbpl是一种抗血管发生蛋白。fkbpl的抗血管发生活性可以如valentine等人(2011):clinicalcancerresearch,mar1;17(5):1044-56和yakkundi等人(2013):plosone;8(2):e55075中描述的来测试。简言之,fkbpl的活性可以在一系列功能细胞测定中来评价。fkbpl抑制迁移和基质胶依赖性小管形成的能力可以被确定。另外的测试可以在新生血管形成(neovascularization)的离体大鼠模型和血管发生的体内小鼠模型,即海绵植入和活体显微术模型中进行。抗肿瘤效力可以在人肿瘤异种移植物模型中确定。
可选地,fkbpl变体可以由核酸序列编码,所述核酸序列包含:
并且具有氨基酸序列:
fkbpl/fkbpl变体的片段可以包含至少5个至7个连续氨基酸、通常至少7个至9个连续氨基酸、典型地9个至13个连续氨基酸、更优选地至少20个至30个或更多个连续氨基酸、最优选地至少30个至40个或更多个连续氨基酸的氨基酸残基的链段(stretch)。片段可以保留fkbpl活性,fkbpl活性的测试在上文描述。
为了简洁,在随后对本发明的说明中仅提及fkbpl。然而,随后对本发明的方法和试剂盒的说明同样适用于fkbpl变体、fkbpl片段和fkbpl变体片段。
检测fkbpl
检测是指确定两种剂例如两种蛋白或两种核酸之间存在或不存在相互作用。例如,fkbpl与fkbpl特异性抗体的相互作用;或fkbplmrna与fkbpl基因特异性核酸探针的相互作用。
检测可以包括量化。检测可以包括使用能够使用例如分光光度法、流式细胞术或显微术来检测的剂(标记物)。示例性标记物包括放射性同位素(诸如3h、14c、15n、35s、90v、99tc、111ln、125i或131i)、荧光团(诸如荧光素、异硫氰酸荧光素、罗丹明等)、发色团、配体、化学发光剂、生物发光剂(诸如萤光素酶、绿色荧光蛋白(gfp)或黄色荧光蛋白)、可以产生可检测的反应产物的酶(诸如辣根过氧化物酶、萤光素酶、碱性磷酸酶、β半乳糖苷酶)及其组合。
检测的具体实例在下文提供。
量化fkbpl的表达水平
量化fkbpl的表达水平包括测试从妊娠女性采集的生物样品,以确定所述样品中fkbpl的量。
这可以包括测试fkbpl蛋白向生物样品中的分泌。例如,fkbpl从a)内皮细胞和/或b)胎盘向血液中的分泌。
可选地或另外地,可以测试胎盘组织中fkbpl基因的表达。
蛋白表达和分泌的量化
免疫组织化学(ihc)可用于检测蛋白表达。蛋白印迹和elisa是可用于检测蛋白表达和分泌的方法。特异性结合fkbpl的抗体可以在这些方法中使用。ihc样品可以使用自动化图像分析系统来分析,以便提供盲法分析。为此,可以首先使用scanscopextslidescanner(aperiotechnologies)以20x捕获全载玻片数字图像。其次,正像素计数算法(aperiotechnologies)可以用于开发用于fkbpl表达的量化评分模型。组织微阵列衍生的数据的统计分析可以使用v2趋势检验、fisher精确检验和mann-whitney检验来进行,并且kaplan-meier绘图可以用于生存分析,并使用对数秩检验来对曲线进行比较。cox比例风险回归可用于估计比例风险比率,并如前所述的进行多变量分析。所有计算都可以用spssv11.0(spss,il)来进行。此外,为了便于生成离散的多标志物测试,加荧光标签的抗fkbpl、以及抗另外的相关胎盘生物标志物的抗体(携带非重叠的荧光团)可以被同时使用。有利的是,可以使用来自aperio的最近开发的荧光扫描系统,例如scanscopefl系统。该测定方法通过提供比传统明场成像所提供的更多的量化分析,将提供更进一层的复杂性。
可以使用elisa夹心酶免疫测定,例如来自cloud-clonecorp的用于fk506结合蛋白样蛋白的elisa试剂盒(目录号sel523hu)。该试剂盒提供了用fkbpl特异性抗体预包被的微量滴定板。然后将标准品或样品添加至平板孔,随后添加生物素缀合的fkbpl特异性抗体。接下来,将与辣根过氧化物酶(hrp)缀合的亲和素添加至每个微孔板孔并孵育。在加入tmb底物溶液(3,3',5,5'-四甲基联苯胺:作为用于通过hrp将过氧化氢还原为水的氢供体的发色底物)后,只有包含fkbpl、生物素缀合的抗体和酶缀合的亲和素的那些孔将显示颜色的变化。酶-底物反应通过添加硫酸溶液来终止,并且颜色变化在450nm±10nm的波长处用分光光度法测量。然后样品中fkbpl的浓度通过将样品的o.d.与标准曲线进行比较来确定。
蛋白印迹包括:1)通过凝胶电泳按大小分离蛋白;2)将蛋白从凝胶转移到膜固体支持物,例如pvdf膜;和3)使用一抗和任选地二抗使靶蛋白可视化。结合的一抗或二抗是可检测的,例如,作为与hrp缀合的结果。添加发色底物后产生的信号允许例如使用imagej软件(nih,usa)并在针对方案中使用的标准品进行调整后量化凝胶中原始蛋白条带。最佳地,抗fkbpl抗体是来自proteintechil,usa的fkbpl兔多克隆一抗(目录号10060-1-ap)。为了检测该一抗,可以使用抗兔igg辣根过氧化物酶二抗(gehealthcare,目录号na934v)。
特异性结合fkbpl的蛋白
fkbpl蛋白可以使用对fkbpl具有结合特异性的一抗来检测。一抗可以用可检测的部分标记,或者可以与半抗原(诸如生物素等)缀合,其中半抗原通过可检测地标记的关联(cognate)半抗原结合分子例如链霉亲和素辣根过氧化物酶是可检测的。可选地,可以使用特异性结合第一一抗的二抗,并且替代地,该二抗如上文针对一抗描述的可以是可检测的。
fkbpl抗体(对fkbpl具有结合特异性的抗体)的结合特异性可使用蛋白印迹联合福尔马林固定的、石蜡包埋的模拟胎盘样品的细胞系的免疫组织化学分析来建立。简言之,可将胎盘细胞系+/-fkbpl靶向的sirna,连同fkbpl过表达的稳定克隆用于优化抗fkbpl抗体。可以将细胞系在pfa中固定30min,并在70%乙醇中重新悬浮过夜,然后包埋在石蜡中并使用组织阵列仪(tissuearrayer)排列。然后可以将免疫细胞化学染色的细胞团(pellet)阵列与蛋白印迹数据进行比较,以检查抗体的特异性和适用性,以及使用spearman秩检验确定相关性的显著性。在两种测定之间显示出最相当的表达水平的抗体可用于筛选。
术语抗体是指与特定抗原特异性结合或免疫反应的免疫球蛋白分子或其组合,并且包括多克隆的、单克隆的、遗传工程化的和以其他方式修饰的形式的抗体,不限于嵌合抗体、人源化抗体、异源缀合抗体(例如双特异性抗体、双抗体(diabodies)、三抗体(triabodies)和四抗体(tetrabodies))、单链fv抗体(scfv)或包含足以赋予与多肽特异性抗原结合的免疫球蛋白的至少一部分的多肽。抗体片段包括蛋白水解抗体片段诸如f(ab’)2片段、fab’片段、fab’-sh片段、fab片段、fv、rigg,重组抗体片段诸如sfv片段、dsfv片段、双特异性sfv片段、双特异性dsfv片段、互补决定区(cdr)片段,骆驼抗体以及软骨鱼和硬骨鱼产生的抗体及其分离的结合结构域。fab片段是由vl、vh、cl和ch1结构域组成的单价片段;f(ab’)2片段是包含通过铰链区的二硫桥连接的两个fab片段的二价片段;fd片段由vh和ch1结构域组成;fv片段由抗体的单臂的vl和vh结构域组成;以及dab片段由vh结构域组成。单链抗体(scfv)是一种抗体,其中vl区和vh区经由使它们能够成为单一蛋白链的合成接头配对来形成单价分子。双抗体是二价的双特异性抗体,其中vh和vl结构域在单一多肽链上表达,但是使用过短以至于不允许同一链上的两个结构域之间的配对的接头,从而迫使结构域与另一条链的互补结构域配对,并产生两个抗原结合位点。嵌合抗体是包含来自一种抗体的一个或更多个区域和来自一种或更多种其他抗体的一个或更多个区域的抗体。抗体可以具有一个或更多个结合位点。如果存在多于一个结合位点,则结合位点可以彼此相同或可以不同。例如,天然存在的免疫球蛋白具有两个相同的结合位点,单链抗体或fab片段具有一个结合位点,而双特异性抗体或双功能抗体具有两个不同的结合位点。
特异性结合fkbpl的抗体的一个实例是fkbpl兔多克隆一抗(proteintechil,usa,目录号10060-1-ap)。为了检测该一抗,可以使用抗兔igg辣根过氧化物酶二抗(gehealthcare,目录号na934v)。
可选地,能够选择性结合的其他蛋白也可以用于检测。
例如,fkbpl可以使用以下来检测:适体(例如呈现特定的序列依赖性形状并以高亲和力和高特异性结合fkbpl蛋白的单链核酸分子(诸如dna或rna));镜像适体(spiegelmertm);工程化的非免疫球蛋白结合蛋白,例如基于支架的非免疫球蛋白结合蛋白,包括纤连蛋白(adnectinstm)、ctla-1(evibodiestm)、脂质运载蛋白(anticalinstm)、蛋白a结构域(affibodiestm)等。
基因表达的量化
fkbpl基因的表达水平也可以被检测。例如,胎盘组织中fkbpl基因的表达水平。
基因表达水平可以使用本领域已知的任何技术来确定,例如基于多核苷酸(mrna转录物)的杂交的方法、基于对多核苷酸进行测序或对多核苷酸进行扩增的方法。
样品中mrna基因转录物的量化可以使用但不限于以下来进行:rna印迹、原位杂交、rna酶蛋白酶测定、基于pcr的方法诸如逆转录聚合酶链式反应(rt-pcr)和实时定量pcr(qrt-pcr)。可选地,可以使用对核酸双链体具有结合特异性的抗体来确定mrna水平。可以使用利用针对感兴趣的rna的特异性结合成员的微阵列技术,例如对感兴趣的rna特异性的cdna或寡核苷酸探针或感兴趣的rna特异性的抗体,其中特异性结合成员被铺在或排列在基底上,例如玻璃载玻片或微芯片基底上。特异性结合成员可以在基底上的可寻址的位置处提供,并且可寻址的位置的数量可以从例如至少三个、至少10个、至少50个、至少100个、至少1000个或至少10,000个或更多个变化。在实施方案中,可寻址的位置的数量可以从小于1000、小于100、小于50、小于10、或小于5变化。在这样的实例中,将样品与阵列接触,并且排列的特异性结合成员可以与样品中的靶形成可检测的相互作用。相互作用可以使用合适的标记物来检测。当使用寡核苷酸探针时,在适当的条件下,寡核苷酸探针可以与靶核酸序列“杂交”,以与具有互补碱基序列的核酸分子形成碱基配对的双链体。导致特定的严格性程度的杂交条件将取决于杂交方法的性质以及杂交的核酸序列的组成和长度而变化。
当核酸以最小的背景结合靶核酸时,发生严格的杂交。通常,为了实现严格的杂交,使用低于tm(一半分子从其配偶体解离的解链温度)约1℃至约20℃、更优选地约5℃至约20℃的温度。然而,它还由溶液的离子强度和ph来定义。合适的杂交条件是本领域技术人员已知的,示例性杂交条件为:
非常高的严格性(检测共有至少90%同一性的序列)-5xssc在65℃持续约16小时的杂交,
高严格性(检测共有至少80%同一性的序列)-5x-6xssc在65℃持续16小时的杂交,和
低严格性(检测共有至少50%同一性的序列)-6xssc在室温至55℃持续20至30分钟的杂交。
高度严格的洗涤条件的实例为0.15mnacl在72℃持续约15分钟。严格的洗涤条件的实例为0.2x氯化钠和柠檬酸钠(ssc)在65℃洗涤15分钟(参见下文的sambrook和russell对ssc缓冲液的描述,例如通过将175.3g的nacl和88.9g的柠檬酸钠溶解在800ml蒸馏水中制成的20xssc。用hcl(1m)调节ph至ph7.0,并用蒸馏水调节体积至1l)。通常,在高严格性洗涤之前进行低严格性洗涤以去除背景探针信号。对于例如多于100个核苷酸的双链体的中等严格性洗涤的实例为1xssc在45℃持续15分钟。对于例如多于100个核苷酸的双链体的低严格性洗涤的实例为4x-6xssc在40℃持续15分钟。对于短探针(例如约10至50个核苷酸),严格的条件通常包括在ph7.0至ph8.3的小于约1.5m、更优选地约0.01至1.0m的钠离子浓度(或其他盐)的盐浓度,并且温度通常为至少30℃,和对于长探针(例如>50个核苷酸),温度通常为至少约60℃。
在pcr方法中使用的方法,例如rt-pcr,将是本领域技术人员熟知的。
一些方法可能需要从样品中分离rna。这样的分离技术是本领域已知的,并且可以使用来自生产商诸如qiagen的商购可得的rna分离试剂盒。
特异性结合
特异性结合是指一个结合配偶体和另一个结合配偶体,例如引物和靶序列或蛋白特异性抗体和蛋白之间的优先的相互作用。一个结合配偶体和另一个结合配偶体之间的相互作用可以通过一个或更多个非共价键,通常多于一个非共价键来介导。表征特异性结合的示例性方法是通过特异性结合曲线。
接触样品
接触是指使一种剂与另一种剂紧密接近,以便两种剂可以彼此相互作用。例如,可以使抗体或其他结合成员与样品中的蛋白紧密接近,并且当抗体对蛋白具有结合特异性时,抗体将结合蛋白。
可选地,可以使第一核酸与第二互补核酸(引物与靶序列)紧密接近,并且可以进行孵育,以便可以检测到结合或者可以发生靶序列的扩增。
生物样品
生物样品可以是血液样品,或来源于血液样品的血浆或血清样品,或使用标准程序从受试者分离的细胞或组织。
例如,胎盘样品可以从妊娠女性采集。这可以通过绒毛膜绒毛取样(cvs)来进行。该程序包括从胎盘中取出小的细胞样品。该程序可以通过经腹途径来进行,其中将针头通过女性的腹部插入。可选地,可以使用经子宫颈途径,其中将管或小镊子通过子宫颈插入。
胎盘样品可以在福尔马林中固定,并在石蜡(ffpe)中包埋,或者使用液氮速冻。
表达水平的降低
将来自第一时间点的fkbpl表达水平和来自第二时间点的fkbpl表达水平进行比较。在具有增加的pe的风险的女性中,本发明人发现,与处于妊娠中较早的第一时间点相比,处于妊娠中较晚的第二时间点的fkbpl表达的统计上显著降低。即fkbpl表达水平随妊娠进展而降低。
更详细地,并参考实施例,当将组内发展pe的所有女性合并在一起时,当将所有血液样品使用wilcoxon符号秩检验分析时,在时间点1和时间点2之间存在fkbpl的总体显著降低(p=0.013)。在任何其他测试的组中,在这些时间点采集的样品之间不存在差异。
表达水平的降低可以为至少约1%、至少约2%、至少约5%、至少约10%、至少约20%、至少约25%、至少约30%、至少约50%、至少约75%、至少约100%或更多。
可选地,表达水平可以降低至少约2倍、至少约3倍、至少约5倍、至少约8倍、至少约10倍、至少约20倍、至少约100倍。
例如,血浆中的fkbpl表达水平可从在时间点1的3ng/ml降至在时间点2的1.5ng/ml。
与健康女性,即不继续发展pe的女性相比,也可以观察到降低。例如,在非糖尿病的女性群组中,下文实验部分中详细描述的期中分析(interimanalysis)显示,发展了pe的女性中在妊娠15周时血浆中的fkbpl浓度(0.8819ng/ml±0.03893sem)显著地(p<0.01)低于健康对照中在妊娠15周时血浆中的fkbpl浓度(1.036ng/ml±0.04312sem)。针对年龄和bmi匹配了样品。
当蛋白表达通过免疫组织化学来确定时,表达水平可以半定量地测量,例如用0、-1、-2和-3来标注蛋白表达水平,其中0为来自对照的表达没有可检测的降低,并且-3为蛋白表达水平的最大的检测到的降低。
可以使用统计计算机程序包例如ibmspss软件来分析数据。样品的合并分析将具有约90%的检验力(power)来在5%显著性水平上将0.5的中等cohen效应量(即平均值的差异,其大小为标准偏差的一半)检测为显著的。独立样品t检验可用于提供测试的组之间的比较,并且这些比较将通过协方差的分析来支持,以调整可能的干扰因子(confounder)。分布将使用三分位数来划分,以允许使用逻辑回归来检查生物标志物水平和pe风险之间的关系的阈值效应或非线性。
增加的风险
“增加的风险”,在本发明的上下文中,这将反映更高的相对风险程度。本发明人已经发现fkbpl表达或分泌的降低是发展pe的风险的一个强烈且早期的指标。在具有发展pe的增加的风险的女性中,与处于妊娠中较早的第一时间点相比,处于妊娠中较晚的第二时间点存在fkbpl表达的统计上显著的降低。增加的风险是指与在第二时间点未显示fkbpl表达的降低的妊娠女性相比,更有可能发展pe的妊娠女性。
妊娠中的时间点
时间点根据妊娠的周数来确定。这基于末次月经期来计算。末次月经期的第一天计为妊娠的第1天。妊娠的第1周自末次月经期的第一天开始的一周。妊娠的第2周自末次月经期的第一天开始的2周。
本发明人已经发现,fkbpl水平从妊娠早期至妊娠晚期的降低指示发展pe的更高的风险。
第一样品可以在妊娠早期的第一时间点采集。例如,第3周-第19周;或从第3周、第4周、第5周、第6周、第7周、第8周、第9周、第10周、第11周、第12周、第13周、第14周、第15周、第16周、第17周或第18周开始,并在第4周、第5周、第6周、第7周、第8周、第9周、第10周、第11周、第12周、第13周、第14周、第15周、第16周、第17周、第18周或第19周结束的任何周的范围。例如,第一时间点可以在第3周-第14周之间。
第二样品在第二时间点采集,所述第二时间点在妊娠中晚于第一时间点。在妊娠中更晚是指更接近分娩。例如第10周-第30周;或从第11周、第12周、第13周、第14周、第15周、第16周、第17周、第18周、第19周、第20周、第21周、第22周、第23周、第24周、第25周、第26周、第27周、第28周或第29周开始,并在第12周、第13周、第14周、第15周、第16周、第17周、第18周、第19周、第20周、第21周、第22周、第23周、第24周、第25周、第26周、第27周、第28周、第29周或第30周结束的任何周的范围。
例如,第一样品在妊娠早期的第一时间点,例如在12周采集。第二样品在妊娠中随后,例如在15周-20周采集。然后测量这些样品中fkbpl蛋白或fkbpl基因的表达水平,并将第一样品和第二样品中的fkbpl量进行比较。
还提供了一种确定pe的风险的方法,其中仅采集一个样品。例如,生物样品可以在从第5周、第6周、第7周、第8周、第9周、第10周、第11周、第12周、第13周、第14周、第15周、第16周、第17周或第18周、第19周、第20周、第21周、第22周、第23周、第24周、第25周、第26周、第27周、第28周、第29周开始,并在第6周、第7周、第8周、第9周、第10周、第11周、第12周、第13周、第14周、第15周、第16周、第17周、第18周、第19周、第20周、第21周、第22周、第23周、第24周、第25周、第26周、第27周、第28周、第29周或第30周结束的任何周的范围内采集。例如,生物样品可以在第10周-第20周之间采集。将该样品与对照进行比较,而不是与来自另一个时间点的样品进行比较。
妊娠也可以按妊娠期(trimester)来量度。妊娠分为以下妊娠期:妊娠第1期是从第1周至第12周结束;妊娠第2期是从第13周至第26周结束;且妊娠第3期是从第27周至妊娠结束。第一样品可以在妊娠第1期采集。第二样品可以在妊娠第2期采集。当仅采集一个样品时,这可以在妊娠第2期进行。
样品也可以从第30周起在妊娠中较晚地采集。例如,从第30周、第31周、第32周、第33周、第34周、第35周、第36周、第37周、第38周和第39周开始,并在第31周、第32周、第33周、第34周、第35周、第36周、第37周、第38周、第39周或第40周结束的任何周的范围。这可以是采集的唯一样品,或者这可以是当第二样品被采集的时间点。
对照标准或对照样品
对照标准可以是从研究来自不继续发展pe的女性的平均值而确定的数值。例如,如实验部分中示出的,本发明人示出了,在非糖尿病女性群组中,期中分析显示,发展了pe的女性中在妊娠15周时血浆中的fkbpl浓度(0.8819ng/ml±0.03893sem)显著地(p<0.01)低于健康对照中在妊娠15周时血浆中的fkbpl浓度(1.036ng/ml±0.04312sem)。
对照标准将取决于fkbpl表达分析的方法而变化。当实验室使用标准化试剂和设备处理许多受试样品时,这样的标准可以被确定。
可以将对照样品与生物样品在确定fkbpl表达的任何方法中并行地运行,来替代数值对照标准。对照样品可以来自未发展pe的女性。或者对照样品可以是具有预先确定的fkbpl浓度的样品,该预先确定的fkbpl浓度代表未患pe的妊娠女性的fkbpl浓度。内部对照将通常与受试样品同时被分析。
对照标准和样品可以针对年龄和bmi被匹配。
pe的临床特征
与pe相关的临床特征可与fkbpl水平监测结合使用,以增强fkbpl测试的预测价值。所监测的临床特征可以是以下中的任何一项或更多项:血压、bmi、平均子宫动脉阻力指数、蛋白尿、脂质谱(lipidprofile)或营养。
妊娠前糖尿病
妊娠前糖尿病是指患有在怀孕前即存在的i型糖尿病或ii型糖尿病的女性。
额外的产前监测
如果存在发展pe的高风险,则女性和婴儿可以进行额外的产前监测。例如,可以更经常地检查女性的血压。将定期采集尿样来测量蛋白水平。可以进行血液测试来检查女性的肾脏功能和肝脏功能。可以进行额外的超声扫描来检查通过胎盘的血流、测量婴儿的生长、并观察婴儿的呼吸和运动。也可以检查其他相关的生物标志物。
预防pe的方法
如果确定妊娠女性处于发展pe的高风险,则可以开具靶向fkbpl途径并引起fkbpl表达的增加的治疗(fkbpl激动剂)的处方。例如,他汀类,任选地普伐他汀;贝特类,任选地非诺贝特;芪类,任选地白藜芦醇;或者二甲双胍。
治疗pe的方法
pe的治疗可以包括降低血压的药物(也称为抗高血压剂)。该类型的药物的实例包括拉贝洛尔(labetalol)、硝苯地平(nifedipine)或甲基多巴(methyldopa)。
如果你患有严重的pe,则可以开具皮质类固醇的处方,这些可以暂时改善肝脏功能和血小板功能,以帮助延长妊娠。皮质类固醇也可以帮助婴儿的肺部发育,为早产做准备。
严重的pe也可以用抗痉挛药物诸如硫酸镁来治疗,以预防突然发作(seizure)。
以上部分中提到的所有药物都旨在包括所有药学上可接受的盐、溶剂化物、水合物、多晶型物(polymorphs)、前药、代谢物、立体异构体和互变异构的异构体。
治疗有效量
治疗有效量是指在妊娠女性中引起生物学反应或医学反应的治疗的量。
试剂盒
试剂盒是包含至少一种试剂,例如抗体、引物或另一种探针,特别地用于检测fkbpl的抗体、引物或另一种探针的任何制品(例如包装或容器)。
试剂盒可以包含对照样品,诸如已知不表达fkbpl的组织样品。试剂盒可以包括公开如何使用试剂盒来检测fkbpl的指导材料。
贯穿本说明书,除非上下文另有要求,否则术语“包含/包括(comprise)”或“包括(include)”或变体诸如“包含/包括(comprises)”或“包含/包括(comprising)”、“包括(includes)”或“包括(including)”将被理解为意指方法或试剂盒包括所提到的整数或整数的组,但不排除任何其他整数或整数的组。
本文中引用的每一个文件、参考文献、专利申请或专利通过引用以其整体明确地并入本文,这意味着其应该被读者阅读并且认作本文的一部分。仅仅是出于简洁的原因,本文中引用的文件、参考文献、专利申请或专利在本文中没有被重述。参考本文中引用的材料或包含的信息不应被理解为承认该材料或信息是公知常识的一部分或在任何国家是已知的。
实施例
本发明的方面和实施方案现将参考以下实验通过示例性的方式来说明。
实施例1:确定滋养层细胞和内皮细胞中fkbpl的表达水平
方法:患有妊娠前糖尿病的女性比一般群体具有更高的pe发病率(四倍的增加)。因此,选择了糖尿病细胞模型(见下文(i))以及pe细胞模型(见下文(ii),胎盘的低氧为先兆子痫的一个关键特征)用于评价。
将滋养层细胞(htr8.sv.neo,bewo)和内皮细胞(huvec)暴露于:
i.呈高度氧化和糖化的低密度脂蛋白(hog-ldl,25μg/ml)/4hne(10μm)或高葡萄糖(10mm、20mm、30mm、40mm)形式的糖尿病性刺激;或
ii.低氧(1%)或dmog(10μm);
然后测量fkbpl/sirt1蛋白和rna水平。
结果:显示了在用hog-ldl处理后,htr8.sv.neo细胞中fkbpl蛋白水平的统计上显著的增加(p<0.05,图1)。在暴露于高葡萄糖环境48h后,bewo细胞中fkbplmrna也被上调(10mm,p<0.01;20mm,p<0.05;40mm,p<0.01,图2)。相反地,将htr8.sv.neo滋养层细胞或huvec/内皮细胞暴露于低氧1%持续24h,则导致fkbpl蛋白表达下调(htr8.sv.neo,p<0.01,图3;huvec,p<0.01,图4)。相似地,用dmog、hif-1α活化剂处理导致htr8.sv.neo细胞中fkbplmrna水平的降低(p<0.05,图5)和bewo细胞中fkbpl蛋白水平的降低(p<0.05,图6)。在含血清培养基中,当脂质过氧化产物4hne被用作htr8.sv.neo细胞的处理时,未观察到fkbplmrna水平的变化(图5),而在bewofkbpl蛋白水平中观察到fkbpl蛋白水平的降低(图6)。然而,这是在血清存在的情况下,而用hog-ldl处理是在无血清培养基中进行的。本发明人推测含血清培养基可能具有抗氧化作用,这隐藏了fkbpl水平的最初的增加。
实施例2:fkbpl是妊娠女性中的pe的预测性生物标志物
确定了胎盘内fkbpl的表达。然后使用来自在t1dm和健康妊娠女性中的两项前瞻性纵向研究中的患者血浆样品来研究fkbpl的pe生物标志物潜力。
方法:使用fkbpl抗体进行免疫荧光,以确定从健康妊娠女性分娩时收集的胎盘组织的绒毛膜绒毛中fkbpl的表达。还进行了cd31蛋白染色,以便确定绒毛膜绒毛内的血管/内皮细胞的位置。
血液样品采集自发展或不发展先兆子痫的1型糖尿病妊娠女性和健康妊娠女性。对于患有1型糖尿病的女性,在妊娠第1期(妊娠12.2±1.9周,[平均值±sd])、妊娠第2期(21.6±1.5周)和妊娠第3期(31.5±1.7周)采集血液样品,所有采集都在pe发生前进行。对于未患糖尿病的女性,在妊娠15周采集血液样品。将全血收集到经抗凝血剂处理的管中,例如经edta处理的管(淡紫色顶端)或经柠檬酸盐处理的管(浅蓝色顶端)或肝素化的管(绿色顶端)。通过使用冷冻离心机在1,000xg-2,000xg离心10分钟,从血浆中去除细胞。在2,000xg离心15分钟除尽血浆样品中的血小板。所得上清液被称为血浆。在操作时将样品维持在2℃-8℃。
使用商业的elisa试剂盒(cloud-clone)来测定所得血浆样品。将100μl标准品和血浆样品添加至每个孔,并将每个样品一式两份地测试。
测试的样品如下:
dm-pe-组(未患糖尿病、未发展pe的女性)
·妊娠第1期-16个样品
·妊娠第2期-12个样品
·妊娠第3期-12个样品
dm+pe-组(患有t1dm、但未发展pe的女性)
·妊娠第1期-19个样品
·妊娠第2期-16个样品
·妊娠第3期-13个样品
dm+pe+组(患有t1dm、发展了pe的女性)
·妊娠第1期-17个样品
·妊娠第2期-14个样品
·妊娠第3期-16个样品
在非糖尿病群组中,未发展先兆子痫的健康女性的血浆样品(n=53)和发展了先兆子痫的女性的血浆样品(n=52)在第15周收集。
(上文样品数量由于不可能获得用于测试的所有样品而不同)
结果:在来自健康妊娠的胎盘组织内证实了fkbpl的强烈表达(图7、图8)。使用fkbpl抗体对胎盘组织进行免疫荧光染色示出fkbpl在合体滋养细胞和血管/内皮细胞中的强烈表达(图8)。当在患者血浆样品中测量分泌的fkbpl水平时,在妊娠34周后发展了pe的个体t1dm女性中,在时间点1(约第12周)和时间点2(约第22周)之间存在fkbpl水平的统计上显著的降低(p=0.013)(dm+pe+)。fkbpl的确切浓度在女性之间变化。然而,这里的结果显示fkbpl浓度范围在时间点1为0.5-2ng/ml,并且在时间点2为0.25-1.5ng/ml。在未患pe的t1dm女性(dm+pe-)或未患pe的非糖尿病女性(dm-)中不存在fkbpl水平的纵向改变。参见图9。在非糖尿病的女性群组中,我们的期中分析显示,在妊娠15周时,发展了pe的女性的血浆中的fkbpl浓度(0.8819ng/ml±0.03893sem)显著地(p<0.01)低于健康对照的血浆中的fkbpl浓度(1.036ng/ml±0.04312sem)。针对年龄和bmi匹配了样品。
结论:与后来继续发展pe的1型糖尿病妊娠女性中的访视1相比,在未患糖尿病的女性中,在妊娠第2期早期(第15周)并且朝向妊娠第2期的结束(第20周)检测到血浆中fkbpl蛋白的降低。
目前诊断pe的测定测试(sflt-1/plgf)使用仅在妊娠第3期、症状发作前约4周可检测的生物标志物。相比之下,本测试允许在妊娠第2期(远早于在任何症状出现之前)关于女性发展pe的可能性的早期指示。
本发明人推测fkbpl可能在胎盘发育中起作用。在小鼠中的fkbpl的敲低实验导致了未存活的胚胎。在小鼠中部分fkbpl敲低产生了可存活的小鼠胚胎,然而胎盘中的血管变化是可见的。
实施例3
研究了在患有糖尿病的患者中容易使用且在妊娠中安全的治疗剂,以确定它们对fkbpl蛋白表达的激动作用。选择这些剂是因为它们靶向与fkbpl相关的途径的确定的能力。
方法
将8周-12周的spraguedawley大鼠随机分为非糖尿病组(对照/柠檬酸钠注射)或糖尿病组(链脲佐菌素(stz)诱导的组)。在施用注射物后一周,将糖尿病大鼠和对照大鼠分为两组,一组喂饲具有非诺贝特(0.18%)的食物持续5周,并且第二组喂饲正常食物持续5周。在用非诺贝特或对照治疗5周后,切除心脏,提取蛋白,并使用蛋白印迹测量fkbpl的蛋白表达。
将htr8.sv.neo细胞用非诺贝特或非诺贝特酸(10μm)或媒介物对照处理24h,然后制备蛋白裂解物并使用蛋白印迹确定fkbpl表达。
将huvec接种,并且然后在二甲双胍或媒介物对照(vc)的存在下,暴露于低氧(1%)或常氧(21%)持续24h。制备蛋白裂解物,并使用蛋白印迹测量fkbpl蛋白水平。
结果
非诺贝特增加了未患糖尿病的正常大鼠中的fkbpl蛋白表达。在5周的早期糖尿病时间点也增加了fkbpl的水平(图10)。
与对照或非诺贝特相比,非诺贝特的活性代谢物非诺贝特酸(ffa)在滋养层细胞中显示出趋向更高水平的fkbpl的强烈趋势(图11)。
在下调fkbpl的低氧中,二甲双胍治疗能够通过增加fkbpl的蛋白表达来补救这种下调(图12)。在用二甲双胍治疗后,在常氧中未观察到fkbpl水平的变化(图13)。
结论
非诺贝特或其活性代谢物和二甲双胍能够作为fkbpl激动剂起作用,并因此可以作为先兆子痫的治疗选择与作为生物标志物的fkbpl结合来探索。
序列表
<110>英国贝尔法斯特女王大学
<120>测定方法
<130>p181006.wo.01
<150>gb1615753.9
<151>2016-09-15
<160>4
<170>patentin3.5版
<210>1
<211>1087
<212>dna
<213>智人(homosapiens)
<400>1
atggagacgccaccagtcaatacaattggagaaaaggacacctctcagccgcaacaagag60
tgggaaaagaaccttcgggagaaccttgattcagttattcagattaggcagcagccccga120
gaccctcctaccgaaacgcttgagctggaagtaagcccagatccagccagccaaattcta180
gagcatactcaaggagctgaaaaactggttgctgaacttgaaggagactctcataagtct240
catggatcaaccagtcagatgccagaggcccttcaagcttctgatctctggtactgcccc300
gatgggagctttgtcaagaagatcgtaatccgtggccatggcttggacaaacccaaacta360
ggctcctgctgccgggtactggctttggggtttcctttcggatcagggccgccagagggc420
tggacagagctaactatgggcgtagggccatggagggaggaaacttggggggagctcata480
gagaaatgcttggagtccatgtgtcaaggtgaggaagcagagcttcagctgcctgggcac540
tctggacctcctgtcaggctcacactggcatccttcactcaaggccgagactcctgggag600
ctggagactagcgagaaggaagccctggccagggaagaacgtgcaaggggcacagaacta660
tttcgagctgggaaccctgaaggagctgcccgatgctatggacgggctcttcggctgctc720
ctgactttacccccacctggccctccagaacgaactgtccttcatgccaatctggctgcc780
tgtcagttgttgctagggcagcctcagttggcagcccagagctgtgaccgggtgttggag840
cgggagcctggccatttaaaggccttataccgaaggggggttgcccaggctgcccttggg900
aacctggaaaaagcaactgctgacctcaagaaggtgctggcgatagatcccaaaaaccgg960
gcagcccaggaggaactggggaaggtggtcattcaggggaagaaccaggatgcagggctg1020
gctcagggtctgcgcaagatgtttggctgattaaaagttaaaccttaaaagagaaaaaaa1080
aaaaaaa1087
<210>2
<211>349
<212>prt
<213>智人(homosapiens)
<400>2
metgluthrproprovalasnthrileglyglulysaspthrsergln
151015
proglnglnglutrpglulysasnleuarggluasnleuaspserval
202530
ileglnileargglnglnproargaspproprothrgluthrleuglu
354045
leugluvalserproaspproalaserglnileleugluhisthrgln
505560
glyalaglulysleuvalalagluleugluglyaspserhislysser
65707580
hisglyserthrserglnmetproglualaleuglnalaseraspleu
859095
trptyrcysproaspglyserphevallyslysilevalilearggly
100105110
hisglyleuasplysprolysleuglysercyscysargvalleuala
115120125
leuglyphepropheglyserglyproprogluglytrpthrgluleu
130135140
thrmetglyvalglyprotrpargglugluthrtrpglygluleuile
145150155160
glulyscysleuglusermetcysglnglygluglualagluleugln
165170175
leuproglyhisserglyproprovalargleuthrleualaserphe
180185190
thrglnglyargaspsertrpgluleugluthrserglulysgluala
195200205
leualaargglugluargalaargglythrgluleupheargalagly
210215220
asnprogluglyalaalaargcystyrglyargalaleuargleuleu
225230235240
leuthrleuproproproglyproprogluargthrvalleuhisala
245250255
asnleualaalacysglnleuleuleuglyglnproglnleualaala
260265270
glnsercysaspargvalleugluarggluproglyhisleulysala
275280285
leutyrargargglyvalalaglnalaalaleuglyasnleuglulys
290295300
alathralaaspleulyslysvalleualaileaspprolysasnarg
305310315320
alaalaglnglugluleuglylysvalvalileglnglylysasngln
325330335
aspalaglyleualaglnglyleuarglysmetphegly
340345
<210>3
<211>1087
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>智人(homosapiens)fkbpl变体的核苷酸序列
<400>3
atggagacgccaccagtcaatacaattggagaaaaggacacctctcagccgcaacaagag60
tgggaaaagaaccttcgggagaaccttgattcagttattcagattaggcagcagccccga120
gaccctcctaccgaaacgcttgagctggaagtaagcccagatccagccagccaaattcta180
gagcatactcaaggagctgaaaaactggttgctgaacttgaaggagactctcataagtct240
catggatcaaccagtcagatgccagaggcccttcaagcttctgatctctggtactgcccc300
gatgggagctttgtcaagaagatcgtaatccgtggccatggcttggacaaacccaaacta360
ggctcctgctgccgggtactggctttggggtttcctttcggatcagggccgccagagggc420
tggacagagctaactatgggcgtagggccatggagggaggaaacttggggggagctcata480
gagaaatgcttggagtccatgtgtcaaggtgaggaagcagagcttcagctgcctgggcac540
actggacctcctgtcgggctcacactggcatccttcactcaaggccgagactcctgggag600
ctggagactagcgagaaggaagccctggccagggaagaacgtgcaaggggcacagaacta660
tttcgagctgggaaccctgaaggagctgcccgatgctatggacgggctcttcggctgctc720
ctgactttacccccacctggccctccagaacgaactgtccttcatgccaatctggctgcc780
tgtcagttgttgctagggcagcctcagttggcagcccagagctgtgaccgggtgttggag840
cgggagcctggccatttaaaggccttataccgaaggggggttgcccaggctgcccttggg900
aacctggaaaaagcaactgctgacctcaagaaggtgctggcgatagatcccaaaaaccgg960
gcagcccaggaggaactggggaaggtggtcattcaggggaagaaccaggatgcagggctg1020
gctcagggtctgcgcaagatgtttggctgattaaaagttaaaccttaaaagagaaaaaaa1080
aaaaaaa1087
<210>4
<211>349
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>智人(homosapiens)fkbpl变体的氨基酸序列
<400>4
metgluthrproprovalasnthrileglyglulysaspthrsergln
151015
proglnglnglutrpglulysasnleuarggluasnleuaspserval
202530
ileglnileargglnglnproargaspproprothrgluthrleuglu
354045
leugluvalserproaspproalaserglnileleugluhisthrgln
505560
glyalaglulysleuvalalagluleugluglyaspserhislysser
65707580
hisglyserthrserglnmetproglualaleuglnalaseraspleu
859095
trptyrcysproaspglyserphevallyslysilevalilearggly
100105110
hisglyleuasplysprolysleuglysercyscysargvalleuala
115120125
leuglyphepropheglyserglyproprogluglytrpthrgluleu
130135140
thrmetglyvalglyprotrpargglugluthrtrpglygluleuile
145150155160
glulyscysleuglusermetcysglnglygluglualagluleugln
165170175
leuproglyhisthrglyproprovalglyleuthrleualaserphe
180185190
thrglnglyargaspsertrpgluleugluthrserglulysgluala
195200205
leualaargglugluargalaargglythrgluleupheargalagly
210215220
asnprogluglyalaalaargcystyrglyargalaleuargleuleu
225230235240
leuthrleuproproproglyproprogluargthrvalleuhisala
245250255
asnleualaalacysglnleuleuleuglyglnproglnleualaala
260265270
glnsercysaspargvalleugluarggluproglyhisleulysala
275280285
leutyrargargglyvalalaglnalaalaleuglyasnleuglulys
290295300
alathralaaspleulyslysvalleualaileaspprolysasnarg
305310315320
alaalaglnglugluleuglylysvalvalileglnglylysasngln
325330335
aspalaglyleualaglnglyleuarglysmetphegly
340345
- 还没有人留言评论。精彩留言会获得点赞!