生物体液中植物生长调节剂乙烯利的检测方法与流程
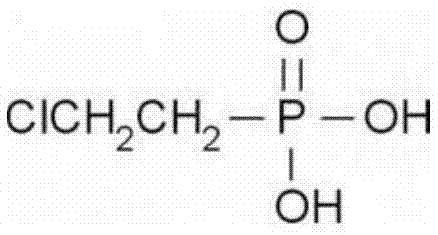
本发明涉及法医药品分析领域。更具体地,涉及一种生物体液中植物生长调节剂乙烯利的检测方法。
背景技术
植物生长调节剂是用于调节植物生长发育的一类农药,可在植物体内传导至作用部位,以促进或抑制其生命过程中的某些环节,使之向符合人类的需要发展。随着农业现代化进程的加速推进,运用植物生长调节剂调控植物的生长发育和产量形成(即作物化学控制技术),已经逐渐成为农业生产中不可缺少的重要措施。与传统农药相比,植物生长调节剂具有许多优越性,它能够调控基因的表达,实现作物生长的“人为”调控。国内外已经把植物生长调节剂的应用作为21世纪农业实现超产的主要措施之一。
乙烯利是近年来案件中常出现较多的植物生长调节剂。乙烯利的物化性质及药物性质总结如下:
乙烯利又名乙烯磷,一试灵,英文名称ethephon,其化学名为2-氯乙基膦酸,分子式为c2h6clo3p,分子量144.5,熔点74-75℃,易溶于水、甲醇。
乙烯利纯品为无色针状晶体,是一种优质高效植物生长调节剂。其进入植物体内后的主要作用方式是作为外源乙烯的载体,释放出乙烯,对植物细胞分裂扩大、营养生长、休眠、萌发、开花、性别分化、果实成熟以及器官衰老脱落等方面都起着重要的调节作用,在水稻、玉米、甘蔗、茶叶、番茄、香蕉、菠萝、黄瓜等作物上被广泛应用。乙烯利属低毒类农药,ld50(口服):大鼠3030mg/kg,ld50(经皮):兔1560mg/kg。
这种植物生长调节剂的特点:为化学合成类农药,在生产上被作为生长促进剂广泛应用,但目前乙烯利植物生长调节剂缺乏相应的系统性的检验方法,因此建立生物体液(血、尿)中植物生长调节剂乙烯利的快速灵敏的检验方法,并利用简单的动物模型,反应其在血液中的代谢情况以解决案件中的检验难题,是法庭科学的实际工作中的现实需要。
技术实现要素:
本发明的一个目的在于提供一种简便快速、灵敏度高、重现性好、结果准确可靠的生物体液中植物生长调节剂乙烯利的检测方法。
为达到上述目的,本发明采用下述技术方案:生物体液中植物生长调节剂乙烯利的检测方法,包括如下步骤:
(1)生物体液预处理;
(2)植物生长调节剂乙烯利的检测。
上述生物体液中植物生长调节剂乙烯利的检测方法,步骤(1)中,生物体液为血液或尿液。
上述生物体液中植物生长调节剂乙烯利的检测方法,步骤(1)中,含乙烯利生物体液的预处理采用顶空反应法。
上述生物体液中植物生长调节剂乙烯利的检测方法,步骤(1)中,所述顶空反应法包括如下步骤:取含乙烯利生物体液样品于顶空瓶中,加入饱和koh溶液,加盖密封混合均匀后,放入自动顶空进样器,留待检测;每1ml含乙烯利生物体液、饱和koh溶液加入量为0.5ml-2ml;顶空平衡温度为60℃-80℃;顶空平衡时间为10min-30min。
上述生物体液中植物生长调节剂乙烯利的检测方法,步骤(2)中,将自动顶空进样器与顶空气相色谱连接,检测含乙烯利生物体液中乙烯利的含量:
顶空气相色谱的色谱条件为:色谱柱:j&w123-9134毛细管柱,规格:30m×0.32mm×0.18mm;程序升温:40℃起始,保持4min,以20℃/min升至150℃,保持2min;进样口温度200℃;载气:高纯氮气;流速:1.5ml/min;分流比:20:1;压力:4.90psi;补偿气:氮气,流速25ml/min,空气,流速400ml/min,氢气,流速60ml/min;
顶空气相色谱质谱的质谱条件为:传输线温度200℃;离子源温度230℃;离子源:ei,电子轰击能量70ev;扫描方式:scan;扫描范围:40amu~450amu;溶剂延迟时间:3min;
自动顶空进样器的自动顶空条件:载气压力:4psi;顶空瓶加压时间:0.2min;顶空瓶加热平衡时间:15min;定量圈平衡时间:0.05min;定量圈充样气时间:0.2min;进样时间:1min;循环时间:15min;顶空瓶加热温度:70℃;定量圈温度:95℃;传输线温度:110℃。
上述生物体液中植物生长调节剂乙烯利的检测方法,含乙烯利体液在-20℃条件下保存,保存时间小于或等于1月个月;经冷冻保存之后的含乙烯利体液,冻融后在72h内进行检测。
本发明的有益效果如下:
(1)生物体液中,乙烯利在1μg/ml的添加水平,方法的回收率可达70%,精密度小于8%。
(2)生物体液中乙烯利的gc-fid方法的检出限为0.1μg/ml,仪器检出限为0.3μg/ml。
(3)建立染毒动物模型,通过测定植物生长调节剂乙烯利在染毒大鼠血液中浓度,验证方法的可靠性,为植物生长调节剂相关中毒案件的检验提供科学依据。
附图说明
下面结合附图对本发明的具体实施方式作进一步详细的说明。
图1乙烯利的化学结构
图2乙烯利标准工作曲线;
图3空白血样乙烯利的色谱图;
图4添加血样中乙烯利的色谱图;
图5空白尿样乙烯利的色谱图;
图6添加尿样中乙烯利的色谱图;
图7乙烯利峰面积随平衡温度和时间变化趋势的柱状图。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例和附图对本发明做进一步的说明。附图中相似的部件以相同的附图标记进行表示。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
第一部分乙烯利检测方法
一、实验部分
1实验材料
1.1药品与试剂
乙烯利购自dr.ehrenstorfer公司(德国),纯度98.0%;
koh、hcl等酸碱试剂(分析纯,北京化学试剂公司);
去离子水经milliporesimplicity纯水系统制备。
1.2生物样品
空白人全血购自北京市红十字血液中心;
空白尿采自一周内未服用任何药物的健康志愿者。
1.3标准溶液的配制
1.3.1储备液的配制:
乙烯利储备液的配制:精确称取乙烯利标准品10mg于10ml容量瓶中,加少量0.1mhcl溶解并定容至刻度,配制成含1mg/ml乙烯利储备液,4℃冰箱中保存,备用。
1.3.2工作液的配制:
乙烯利标准工作液的配置:移取各标准储备液一定量,稀释为100μg/ml、50μg/ml、10μg/ml、5μg/ml、1μg/ml、0.5μg/ml浓度乙烯利的标准工作溶液,4℃冰箱中避光保存。
1.4仪器及参考条件
气相色谱仪:美国安捷伦公司,型号agilent7890a
配氢火焰离子化检测器(fid)
色谱柱:peelite-wax(30m×0.32mm×0.25mm)
j&w123-9134(30m×0.32mm×0.18mm)
milliporesimlicity纯水净化系统(法国)
scientificindustries漩涡振荡器(usa)
sorvall高速冷冻离心机(德国)
eyela高速振荡器(日本)
eyelacutemixercm100振荡器(日本京东);
10~100μl,10~1000μl自动移液枪(德国eppendorf)
2样品的制备方法
取标准工作样品或生物体液样品(血、尿)1ml于10ml顶空瓶中,加入饱和koh溶液1ml,加盖密封混合均匀后放入自动顶空进样器进行测定。
3仪器参考条件
3.1气相色谱条件(gc):
a)色谱柱:j&w123-9134毛细管柱(30m×0.32mm×0.18mm)
peelite-wax毛细管柱(30m×0.32mm×0.25mm);
b)进样口温度:200℃;
c)程序升温:40℃起始,保持4min,以20℃/min升至150℃,保持2min;d)检测器:氢火焰检测器(fid)温度280℃;
e)载气:高纯氮气;
f)流速:1.5ml/min;
g)分流比:20:1;
h)压力:4.90psi;
i)补偿气:氮气,流速25ml/min;
空气,流速400ml/min;
氢气,流速60ml/min。
质谱条件:
a)传输线温度200℃;
b)离子源温度230℃;
c)离子源:ei,电子轰击能量70ev;
d)扫描方式:scan;
e)扫描范围:40amu~450amu;
f)溶剂延迟时间:3min。
3.2自动顶空条件:
a)载气压力:4psi;
b)顶空瓶加压时间:0.2min;
c)顶空瓶加热平衡时间:15min;
d)定量圈平衡时间:0.05min;
e)定量圈充样气时间:0.2min;
f)进样时间:1min;
g)循环时间:15min;
h)顶空瓶加热温度:70℃;
i)定量圈温度:95℃;
j)传输线温度:110℃。
4方法确证实验
4.1顶空气相色谱检验方法
按照“2样品的制备方法”对样品进行处理,按照“3.1和3.2气相色谱条件和自动顶空条件”进行仪器检测,对方法进行方法论证。包括方法的专属性、灵敏度、回收率、精密度等指标。
4.1.1标准工作曲线
用移液器精确吸取标准工作液适量,用0.1mhcl稀释定容成最终浓度为0.5,1,5,10,50,100μg/ml的标准工作液,各取1ml三份分别处理后进行色谱分析,即每个样品平行分析三次,用峰面积(y)对标准工作液乙烯利浓度(x)进行线性回归,求得乙烯利的回归方程为y=1.526x-1.052r2=0.999,工作曲线见图2。结果表明乙烯利在0.5~100μg/ml浓度范围内有着良好的线性关系。
4.1.2方法专属性
取空白血或尿,加入一定量的乙烯利标准溶液,按照“2样品的制备方法方法”进行样品制备,“3.1和3.2气相色谱条件和自动顶空条件”进行分析检测,同时做空白血的对照试验,将二者的图谱进行比较(见图3至图6)。结果在乙烯利保留时间段内,空白血及尿均未出现明显的色谱峰,表明生物体液中内源性杂质不会对乙烯利的的测定造成干扰,说明本发明建立的方法具有较高的专属性。
4.1.3方法的回收率
用标准加入法进行回收率实验,取空白的血样、尿样,分别加入一系列浓度的乙烯利标准工作液使其在每一种样品中的添加浓度分别为1、10、50μg/ml,每一样品每一浓度平行3份,按照“2样品的制备方法方法”进行样品制备,“3.1和3.2气相色谱条件和自动顶空条件”进行分析检测,以测得的添加各样品中乙烯利的保留时间的峰面积与对照品相同浓度峰面积的比值来计算回收率,结果见表1。
表1血液样品中添加乙烯利的平均回收率(%)n=3
4.1.4方法线性考察
取空白的血样、尿样,分别加入适量的乙烯利标准液使其在每一种样品中的添加浓度分别为0.5、1、5、10、50、100μg/ml,每一样品每一浓度平行3份,按照“2样品的制备方法方法”进行样品制备,“3.1和3.2气相色谱条件和自动顶空条件”进行分析检测,用峰面积为纵坐标(y),以添加乙烯利的浓度为横坐标(x)进行线性回归,求得线性回归方程,结果如下:
血液中乙烯利:y=1.738x+0.099r2=0.997
尿液中乙烯利:y=1.936x–0.944r2=0.999
以上结果表明,该方法对血液、尿液样本中的乙烯利在0.5μg~100μg/ml范围内有着良好的线性关系。
4.1.5方法的精密度
用标准溶液加入法对方法的精密度进行考察。取空白的血样、尿样,加入适量的乙烯利标准液使其在每一种样品中的添加浓度分别为1,10,50μg/ml,每一样品每一浓度平行3份,按照“2样品的制备方法”进行样品制备,“3.1和3.2气相色谱条件和自动顶空条件”进行分析检测,每份样品平行进样3次,连续测定三天,计算各组分峰面积的标准偏差,得到日内精密度与日间精密度(见表2、3)。结果表明乙烯利日内精密度介于2.95~5.99%之间,日间精密度介于4.33~7.95%之间,说明该方法的重现性良好。
表2尿液样品中添加乙烯利的精密度实验n=3
表3血液样品中添加乙烯利的精密度实验n=3
4.1.6方法的灵敏度
按照“2样品的制备方法方法”进行样品制备,“3.1和3.2气相色谱条件和自动顶空条件”进行分析检测,以信噪比3/1计,该方法的最小检出限为0.1μg/ml,以信噪比10/1计,该方法的最小定量限为0.3μg/ml。
二、结果与讨论
2.1样品制备方法
2.1.1碱液的添加量
顶空瓶中加入的待测样品和碱液总体积过大,会使顶空瓶上部空间过小,导致反应后顶空气体浓度和压力过大,且顶空进样针会插入碱性液体中造成进样针及定量管等的污染和腐蚀;如果装样量过小,顶空瓶上部空间过大,相当于稀释了乙烯气体,会造成灵敏度降低。乙烯利在碱性条件下加热可分解释放出乙稀,碱液用量对乙烯利分解的影响很大,若碱液用量过少,乙烯利分解将不完全。基于中毒案件的生物检材量相对较少,故固定样品量(1ml),每份样品中都加入10μl、50μg/ml的乙烯利标准工作液,分别加入0.5、1、2mlkoh饱和溶液,研究回收率的变化。
结果表明,随着碱液体积的增加,乙烯利分解的完全程度和速度逐渐增加,对于血液来说,当饱和氢氧化钾溶液加入量为1ml时,能够使样品中的乙烯利回收率最高,再增加碱液用量时,乙烯利的回收率有降低的趋势;对于尿液来说,当饱和氢氧化钾溶液加入量为1ml时,能够使样品中的乙烯利回收率达到比较理想的水平,再增加碱液用量时,乙烯利的回收率增大并不明显;因此本实验中碱液用量设为1ml。不同装液量回收率结果见表4。
表4碱液装液量的选择
2.1.2顶空条件的选择
平衡温度和平衡时间在样品瓶容量和样品量一定的情况下,被测组分在气液两相分配比受环境因素影响较大,即随着温度升高,顶空气体中待测组分的浓度升高,色谱峰面积增大,检测灵敏度提高,同时平衡时间缩短。但温度过高会引起顶空瓶的耐压和气密性问题,还可能导致气体浓度太大造成色谱柱过载;此外,温度过高会产生较多水汽并随样品进入色谱柱,极性很强的水分子对大多数毛细管柱固定相有较强的破坏性,造成柱流失,导致柱效降低。在60、70、80℃条件下分别加热10、15、30min,以选择合适的顶空平衡温度和平衡时间,峰面积随提取温度时间变化趋势见图7。综合考虑灵敏度和平衡时间等因素,最终选择平衡温度70℃,平衡时间15min。
2.1.3色谱条件的选择
2.1.3.1柱温的选择
一般色谱柱的初始温度接近或略低于待测组分沸点温度,以改善峰形。但乙烯沸点很低,为-103.9℃。本实验选择的程序升温条件为:40℃保持4min,以20℃/min速度升温至150℃,保持2min,可缩短分析时间,提高分析效率。
2.1.3.2分流比的选择
降低分流比,会提高检测灵敏度,但易造成色谱柱过载,使色谱柱使用寿命缩短;分流比过大,则会降低灵敏度。固定色谱柱及程序升温条件,选择合适的分流比。在分流比为100∶1、50∶1、20∶1、5∶1时,乙烯的色谱峰面积不断增加,相应地检测限也不断降低,但当分流比降到5∶1时,色谱峰出现裂分,采用20∶1的分流比可得到良好的峰形,且灵敏度符合检测要求,因此本实验确定分流比为20∶1。
三、结论
本发明建立了生物体液中乙烯利的顶空气相色谱检测方法。所建立的方法回收率高、重现性好。添加的平均回收率在70%以上,方法简便快速、灵敏度高、重现性好、结果准确可靠,为进一步研究乙烯利在动物体内的含量测定及稳定性研究提供了技术手段。本发明方法可满足涉及乙烯利中毒案件的检测。
第二部分稳定性考察
植物生长调节剂乙烯利在不同的介质及不同的储存条件下放置过久其含量可能发生变化,为保证定量的准确,必须对植物生长调节剂乙烯利的稳定性进行考察。在毒物分析中从现场检材的提取到送实验室检验,需要经历一定的时间段,由于植物生长调节剂乙烯利本身的理化性质及生物样品中一些内源性物质的作用,可能导致植物生长调节剂乙烯利在生物检材中发生分解。所以检材存放的条件和时间对植物生长调节剂乙烯利的浓度有很大的影响,本发明对植物生长调节剂乙烯利在不同溶剂和血液样本中的稳定性进行了考察。
一、试剂、材料与仪器(同前)
二、实验部分
2.1溶液中稳定性考察
分别配制含10、50、100μg/ml乙烯利的0.1mhcl溶液,每一浓度各3份,密封,置于4℃冰箱中保存,放置0、1、2、3、4周后,按“第一部分3分析方法”对样品进行分析,每次结果与浓标新稀释后的相同浓度的作比较,此两种植物生长调节剂在1、2、3、4周的测定结果相互间差异无统计学意义(p>0.05),说明乙烯利的0.1mhcl溶液在4℃冰箱中1月内具有稳定性。
2.2提取样品反复冻融的稳定性的考察
用空白血或空白尿的提取液,配置20μg/ml的药物溶液3份,-20℃保存,放置24、48、72h后,按“第一部分3分析方法”对样品反复进行分析,(分析完样品密封保存,待下一时间点分析),每次分析结果与标准品进行比较,结果乙烯利在72小时的测定结果相互间差异无统计学意义(p>0.05),说明植物生长调节剂乙烯利在提取样品溶液中72h内具有稳定性。
2.3乙烯利植物生长调节剂在血液、尿液中稳定性的考察
准备1ml血液及尿若干份于塑料试管中,向每份中添加1μg的乙烯利标准物质,将其分成2份,每份中有5组、每组3样本,分别于常温及-20℃冰箱中保存,在放置的第0、7、14、21、30天,用顶空气相色谱法对乙烯利进行检验,每次检测需有新配制新鲜血液样本平行操作,并以新配制血液样本计算被测样本中的含量。设定第0天的样品的检测量为100%,每次的检测量按照起初值的百分比来计。结果在-20℃冰箱中保存的样本中植物生长调节剂乙烯利的含量无明显变化。
三、结论
1、乙烯利溶液在4℃冰箱中1月内具有良好的稳定性。
2、含乙烯利生物体液冷冻后,在72h内反复冻融不影响含量。
3、含乙烯利体液在-20℃条件下保存1月,其含量不会发生明显变化。
第三部分动物实验
一、材料
1.1仪器
同第一部分。
1.2试剂
除生理盐水外,其余均同第一部分。
1.3动物
实验用wistar雄性大鼠,体重500g±20g,购于华富康生物科技股份有限公司。适应性喂养2天。饲养环境:温度17℃,湿度45%~65%,通风换气良好,光照合理,笼具和垫料卫生、无毒,喂营养颗粒饲料和高压消毒灭菌水。
1.4药物配制
精确称取乙烯利一定量,充分溶解于生理盐水中,混匀,配制成浓度为10mg/ml的乙烯利溶液,置4℃冰箱保存。
2.动物实验方法
2.1乙烯利灌胃给药模型及检材的采集
健康wistar雄性大鼠6只,实验前禁食12h,自由饮水。其中1只做空白对照,其余5只以30mg/kg剂量灌胃给予乙烯利溶液,于3h将大鼠处死,取血、尿,采用顶空气相色谱分析。
2.2乙烯利样品的测定
取灌服乙烯利大鼠血或尿液1ml于10ml顶空瓶中,加入饱和koh溶液1ml,涡旋30s,加盖密封混合均匀后放入自动顶空进样器进行测定。
气相色谱条件:色谱柱:j&w123-9134毛细管柱(30m×0.32mm×0.18mm);程序升温:40℃起始,保持4min,以20℃/min升至150℃,保持2min;进样口温度200℃;载气:高纯氮气;流速:1.5ml/min;分流比:20:1
自动顶空条件:载气压力:4psi;顶空瓶加压时间:0.2min;顶空瓶加热平衡时间:15min;定量圈平衡时间:0.05min;定量圈充样气时间:0.2min;进样时间:1min;循环时间:15min;顶空瓶加热温度:70℃;定量圈温度:95℃;传输线温度:110℃。
3.结果
3.1工作曲线
分别在空白大鼠血、尿中加乙烯利标准品,使其浓度为0.5、1、5、10、20、50μg/ml,按照2.1.2方式进行检测,以目标物的浓度为横坐标(x),以其峰面积为纵坐标(y)进行线性回归,求得回归方程:
血中乙烯利回归方程:y=1.435x-0.740r2=0.998
尿中乙烯利回归方程:y=3.557x-1.140r2=0.999
3.2专属性实验
取空白大鼠的血液各1ml,加入一定量的乙烯利标准溶液,按照2.3方法进行样品制备及检测,同时做空白对照,将二者的图谱进行比较,结果表明均无内源性杂质对乙烯利植物生长调节剂的测定造成干扰。
3.3乙烯利植物生长调节剂给药后大鼠血、尿中含量
取动物实验所得血液、尿液样本,按照2.3方法进行样品制备及检测,以保留时间(乙烯利)进行定性,以标准曲线法进行定量。大鼠血液、尿液样本中植物生长调节剂浓度见表9。
表9植物生长调节剂乙烯利在大鼠血、尿中的浓度(n=5)
4结论
本发明研究主要是通过进行动物实验,验证检验方法的可行性。给药后,在血液、尿液等检材中均检出了乙烯利植物生长调节剂。此外,本实验给药量为30mg/kg,远低于植物生长调节剂的ld50,证明在因投毒、误服植物生长调节剂导致死亡的实际案件中对血液、尿液等检材进行检验是可行的。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定,对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无法对所有的实施方式予以穷举,凡是属于本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之列。
- 还没有人留言评论。精彩留言会获得点赞!