一种探针试剂的应用的制作方法
本发明涉及一种探针试剂的应用,特别是一种三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针的应用。
背景技术
荧光探针技术作为一种化学传感器能够对环境、生物等特殊环境中的离子实现快速、实时、在线检测,具备检测灵敏度高、选择性好、速度快、样品处理方便及成本低廉等有点,有别于其他如色谱、光谱等离子检测的方法。探针能够以高灵敏、高选择的方式,直观、快速地检测环境和生物样品中微量离子的浓度及其变化。同时,探针还能够以其特征的吸收或发射波长的不同,在适当的条件下实现同一探针对多种离子的选择性检测,更是其有别于其他检测技术的优势所在。探针检测以颜色和光谱视觉变化的形式反馈离子的信息,既可作为比色染色剂方便和灵巧的检测,能够可视化地描绘出离子的分布,提供定位动态信息及分子水平的定性、定量检测。目前大多数的单探针只能用于1~2种离子的同时检测,能同时检测金属离子、酸根阴离子等3种及其以上多种离子的单探针技术,不仅能有效提高检测效率、降低成本、且有利于对复杂微观系统的分析。但对于能同时检测金属离子、酸根阴离子等3种及其以上多种离子的单探针技术,目前尚未有相关文献进行报道。
技术实现要素:
本发明的目的在于,提供一种三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用,本发明将三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂用于检测ph、f-、aco-、h2po4-和/或hg2+;实现了单一探针对金属离子、酸根阴离子等多种离子的检测,能有效提高检测效率、降低成本、且有利于对复杂微观系统的分析。
本发明的技术方案:三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用,将探针用于检测ph、f-、aco-、h2po4-和/或hg2+;所述探针的结构式为
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的将探针用于检测ph、f-、aco-、h2po4-和/或hg2+是:
(1)以探针为试剂,用紫外-可见吸收光谱法对ph、f-、aco-和/或h2po4-的检测;
(2)以探针为试剂,用紫外-可见吸收光谱法对hg2+的检测;
(3)以探针为试剂,用荧光光谱法对hg2+的检测;
(4)以探针为试剂,用目视比色法对ph、f-、aco-、h2po4-和/或hg2+离子的检测;
(5)以探针为试剂,用探针测试滤纸法对ph的检测。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的以探针为试剂,用紫外-可见吸收光谱法对ph、f-、aco-和/或h2po4-的检测是;
用紫外-可见吸收光谱法对ph的检测是:在体积比为95/5的二甲基亚砜/三羟甲基氨基甲烷(tris)-hcl缓冲溶液中,在ph2~10的范围,探针在500nm~550nm范围的最大吸收波长处的吸光度与ph值呈线性关系,pka为6.685,用校正曲线法检测ph;在体积比为95/5的二甲基亚砜/n-2-羟乙基哌嗪-n'-乙磺酸(hepes)-naoh缓冲溶液中,在ph10~13的范围,探针在550nm~595nm范围的最大吸收波长处的吸光度与ph值呈线性关系,pka为11.50,用校正曲线法检测ph,检测的最低ph值为2,最高ph值为13;
用紫外-可见吸收光谱法对f-的检测是:在乙腈溶液中,探针在575nm处的吸光度与f-浓度呈线性关系,用校正曲线法检测f-,检测的浓度线性范围为1.0~20μm,检出限为0.47μm,其他共存阴离子包括aco-、hso4-、h2po4-、pf6-、cl-、br-、i-、no3-之一,在浓度与f-浓度相同时,对f-的测定无干扰;
用紫外-可见吸收光谱法对aco-的检测是:在乙腈溶液中,探针在530nm处的吸光度与aco-浓度呈线性关系,用校正曲线法检测aco-,检测的浓度线性范围为1.0~20μm,检出限为0.98μm,其他共存阴离子包括f-、hso4-、h2po4-、pf6-、cl-、br-、i-、no3-之一,在浓度与aco-浓度相同时,其他共存阴离子对aco-的测定无干扰;
用紫外-可见吸收光谱法对h2po4-的检测是;在乙腈溶液中,探针在505nm处的吸光度与h2po4-浓度呈线性关系,用校正曲线法检测h2po4-,检测的浓度线性范围为1.0~20μm,检出限为0.83μm,其他共存阴离子包括:f-、aco-、hso4-、pf6-、cl-、br-、i-、no3-之一,在浓度与h2po4-浓度相同时,对h2po4-的测定无干扰。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的以探针为试剂,用紫外-可见吸收光谱法对hg2+的检测是;在体积比为95/5的乙腈/h2o溶液中,探针在560nm处的吸光度与hg2+浓度呈线性关系,用校正曲线法检测hg2+,检测的浓度线性范围为10~20μm,检出限为5.5μm,其他共存金属离子包括:li+、na+、k+、mg2+、ca2+、ba2+、sr2+、fe3+、sr2+、zn2+、co2+、ni2+、cd2+、pb2+、cr3+、al3+、ag+、cu2+或mn2+,在浓度与hg2+浓度相同时,对hg2+的测定无干扰。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的以探针为试剂,用荧光光谱法对hg2+的检测是;在体积比为95/5的乙腈/h2o溶液中,以500nm为激发波长,探针在583nm处的荧光强度与hg2+浓度呈线性关系,用校正曲线法检测hg2+,检测的浓度线性范围为5.0~10μm,检出限为0.017μm,其他共存金属离子包括:li+、na+、k+、mg2+、ca2+、ba2+、sr2+、fe3+、sr2+、zn2+、co2+、ni2+、cd2+、pb2+、cr3+、al3+、ag+、cu2+或mn2+,在浓度与hg2+浓度相同时,对hg2+的测定无干扰。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的以探针为试剂,用目视比色法对ph、f-、aco-、h2po4-和/或hg2+离子的检测是;
用目视比色法对ph是;日光下,在体积比为95/5的二甲基亚砜/三羟甲基氨基甲烷(tris)-hcl缓冲溶液中,在ph2~10范围,探针溶液颜色随ph值增大由淡黄色、粉色、粉红色、紫红色、紫色到蓝色的变化过程;在体积比为95/5的二甲基亚砜/n-2-羟乙基哌嗪-n'-乙磺酸(hepes)-naoh缓冲溶液中,在ph10~13范围,探针溶液颜色随ph值增大由紫色、蓝紫色到蓝色的变化过程;
用目视比色法对f-的检测是;是日光下,在乙腈溶液中,f-的加入使探针溶液颜色明显变化,f-浓度在0~200μm范围,探针从橙黄色逐渐变化粉红色最后变化到紫蓝色,可目视检测浓度在0~200μm的f-;
用目视比色法对aco-的检测是;日光下,在乙腈溶液中,aco-的加入使探针溶液颜色明显变化,aco-浓度在0~200μm范围,探针从橙黄色逐渐变化到暗红色,可目视检测浓度在0~200μm的aco-;
用目视比色法对h2po4-的检测是;日光下,在乙腈溶液中,h2po4-的加入使探针溶液颜色明显变化,h2po4-浓度在0~200μm范围,探针从橙黄色逐渐变化到暗红色,可目视检测浓度在0~200μm的h2po4-;
用目视比色法对hg2+离子的检测是;日光下,在体积比为95/5的乙腈/h2o溶液中,hg2+的加入使探针溶液颜色明显变化,hg2+浓度在0~200μm范围,探针从橙黄色逐渐变化到玫红色,可目视检测浓度在0~200μm的hg2+。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的以探针为试剂,用探针测试滤纸法对ph的检测是;日光下,负载有探针的二甲基亚砜溶液的测试滤纸条,对ph2~12范围的缓冲溶液,测试滤纸条颜色从淡黄色、橙色、粉红色、桃红色至紫色的变化过程,可目视检测范围在2~12的ph。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的探针试剂是以三(2-氨乙基)胺、罗丹明b和偶氮醛为主要原料,以乙醇为溶剂,首先合成中间体,再由中间体和偶氮醛在二氯甲烷和甲醇溶剂中反应得到。
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的的探针试剂的合成路线为:
前述的三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的应用中,所述的探针试剂是这样制备的:100ml的三口瓶中,加入三(2-氨乙基)胺27.36mmol、罗丹明b3.42mmol和60ml的无水乙醇,氮气保护下回流36小时,减压蒸去乙醇,用二氯甲烷萃取,有机相用无水硫酸镁干燥过夜,蒸去溶剂,得红色粘稠状物,经硅胶柱层析分离,得到中间体;反应时间:36h,反应溶剂:无水乙醇,洗脱剂:体积比为甲醇/三氯甲烷/三乙胺=9/1/1的混合液;
10ml的三口烧瓶中加入中间体1mmol、偶氮醛2mmol和50ml二氯甲烷,氮气保护下常温反应12h,加入10ml的甲醇,分批加入硼氢化钠8.6mol,继续反应5h,减压蒸去溶剂,用三氯甲烷萃取,有机相用无水硫酸镁干燥过夜,蒸去溶剂得深红色的油状液体,硅胶柱层析分离和洗脱,得探针化合物,反应时间:17h,反应溶剂:二氯甲烷和甲醇,洗脱剂:体积比为二氯甲烷/甲醇/三乙胺=100/2/1的混合液。
与现有技术相比,本发明具有以下有益效果:
1、本发明所采用的探针检测性能优越。在不同溶剂中,利用波长分辨、吸收增强、荧光增强方法,选择性检测很宽范围的ph以及f-、aco-,h2po4-,hg2+多种质子、阴及重金属离子。不仅能用紫外-可见吸收和荧光光谱两种方式高选择性、高灵敏度检测,而且还能用目视比色法,简便、快速、定性、定量检测多种目标离子。检测时波长均在可见光范围,可视性强,便于快速检测。
2、在体积比为95/5的二甲基亚砜/缓冲溶液中,在ph2~10,探针在500nm~550nm的最大波长处的吸光度与ph值呈线性关系;在ph10~13,探针在550nm~595nm的最大波长处的吸光度与ph值呈线性关系;计算得pka分别为6.685和11.50,利用紫外-可见吸收光谱,探针可在极酸、中性及极碱的宽范围内检测溶液的ph。这种探针检测ph的技术有别于电极检测技术,不受检测对象的体积或状态等环境因素的影响。
3、在乙腈溶液中,用紫外-可见吸收光谱法,探针在不同波长下对不同阴离子的选择性吸收,用吸收增强方式,分别测量575nm处的吸光度检测溶液中微量f-、测量530nm处的吸光度检测溶液中微量aco-、测量505nm处的吸光度检测溶液中微量h2po4-。
4、在体积比为95/5的乙腈/h2o溶液中,用紫外-可见吸收光谱法,探针对hg2+有选择性吸收,测量560nm处的吸光度检测溶液中微量hg2+;
5、在体积比为95/5的乙腈/h2o溶液中,用荧光光谱法,探针对hg2+有选择性荧光发射,测量583nm处的荧光强度检测溶液中微量hg2+;
6、在二甲基亚砜/缓冲溶液中,探针作为试剂在可见光下可目视比色检测ph2~10及ph10~13范围的缓冲溶液,颜色变化敏锐;
7、在乙腈溶液中,探针作为试剂在可见光下可目视比色检测0~200μm的f-、aco-、h2po4-,颜色变化敏锐;
8、在体积比为95/5的乙腈/h2o溶液中,探针作为试剂在可见光下可目视比色检测0~200μm的hg2+,颜色变化敏锐;
9、用负载有探针的二甲基亚砜溶液的滤纸条,作为测试纸在可见光下可目视检测ph2~12范围的溶液ph值,测试滤纸颜色变化敏锐。
单探针多目标识别技术主要体现在所选用的探针结构独特、制备成本低廉、识别方式多样、检测性能优越、操作条件易于控制,应用前景好等方面。
综上所述,本发明将三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂用于检测ph、f-、aco-、h2po4-和/或hg2+;实现了单一探针对金属离子、酸根阴离子等多种离子的检测,能有效提高检测效率、降低成本、且有利于对复杂微观系统的分析。
附图说明:
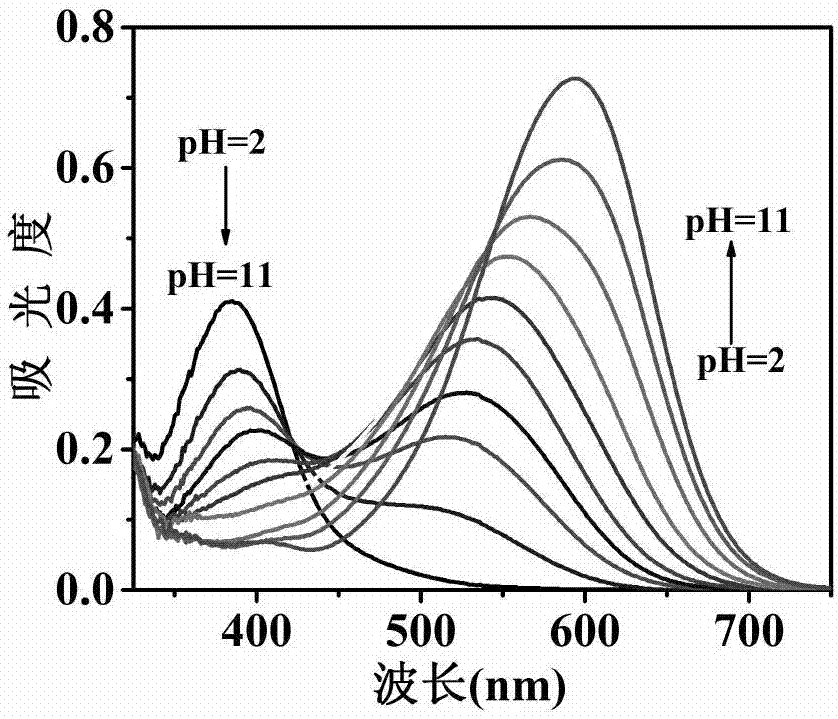
图1是探针检测ph(ph在2~10范围)的紫外-可见吸收光谱图;
图2是探针检测ph(ph在2~10范围)在550nm~595nm范围的最大波长处的吸光度与ph的关系曲线;
图3是探针检测ph(ph在10~13范围)的紫外-可见吸收光谱图;
图4是探针检测ph(ph在10~13范围)在550nm~595nm范围的最大波长处的吸光度与ph的关系曲线;
图5是探针检测f-,aco-,h2po4-的紫外-可见吸收光谱;
图6是探针检测不同浓度的f-的紫外-可见吸收光谱滴定图;
图7是探针检测f-的校正曲线;
图8是共存阴离子对探针检测f-的吸光度影响;
图9是探针检测不同浓度的aco-的紫外-可见吸收光谱滴定图;
图10是探针检测aco-的校正曲线;
图11是共存阴离子对探针检测aco-的吸光度影响;
图12是探针检测不同浓度的h2po4-的紫外-可见吸收光谱滴定图;
图13是探针检测h2po4-的校正曲线;
图14是共存阴离子对探针检测h2po4-的吸光度影响;
图15是探针检测hg2+的紫外-可见吸收光谱;
图16是探针检测不同浓度的hg2+的紫外-可见吸收光谱滴定图;
图17是探针检测hg2+的吸光度校正曲线;
图18是共存金属离子对探针检测hg2+的吸光度影响;
图19是探针检测hg2+的荧光光谱;
图20是不同浓度的hg2+与探针的荧光光谱滴定图;
图21是探针检测hg2+的荧光校正曲线;
图22是共存金属离子对探针检测hg2+的荧光强度影响;
图23是日光下探针在不同ph缓冲溶液中颜色变化图;
图24是日光下探针在不同浓度的f-溶液中的颜色变化图;
图25是日光下探针在不同浓度的aco-溶液中的颜色变化图;
图26是日光下探针在不同浓度的h2po4-溶液中的颜色变化图;
图27是日光下不同浓度的hg2+在探针溶液中的颜色变化图;
图28是日光下负载探针的测试滤纸对不同ph缓冲溶液的颜色变化图。
具体实施方式
实施例1:
1、三[2,2’-二[3-(4-硝基苯偶氮)-6-羟基]苯甲氨基乙基-2”-罗丹明甲酰氨基乙基]胺探针试剂的化学结构式为:
其合成路线如下:
其具体制备方法为:
(1)中间体的制备:
100ml的三口瓶中,加入三(2-氨乙基)胺(4.0g,27.36mmol)、罗丹明b(1.638g,3.42mmol)和60ml的无水乙醇,氮气保护下回流36小时,减压蒸去乙醇,用二氯甲烷(3×100ml)萃取,有机相用无水硫酸镁干燥过夜,蒸去溶剂,得红色粘稠状物,经硅胶柱层析分离,得到中间体1.71g,产率87.3%。;反应时间:36h,反应溶剂:无水乙醇,洗脱剂:体积比为甲醇/三氯甲烷/三乙胺=9/1/1的混合液。中间体结构表征数据:1hnmr(500mhz,cdcl3,ppm)δ:7.877(s,1h,arh),7.437(s,2h,arh),7.087(bs,1h,arh),6.406(d,j=10hz,4h,arh),6.272(d,j=9.0hz,2h,arh),3.355~3.313(m,8h,-ch2ch3),3.144(t,j=8.0hz,2h,ocnch2-),2.547(t,j=6.0hz,4h,-ch2nh2),2.347(t,j=5.5hz,4h,nch2ch2),2.272(t,j=7.5hz,2h,nch2ch2),1.837(bs,4h,ch2nh2),1.159(t,j=7.0hz,12h,-ch2ch3)。
(2)探针的制备:
10ml的三口烧瓶中加入中间体(570mg,1mmol),偶氮醛(540mg,2mmol),50ml二氯甲烷,氮气保护下常温反应12h,加入10ml的甲醇,分批加入硼氢化钠(320mg,8.6mol),继续反应5h,减压蒸去溶剂,用chcl3(3×60ml)萃取,有机相用无水硫酸镁干燥过夜,蒸去溶剂得深红色的油状液体,硅胶柱层析分离和洗脱,得深红色固体探针化合物470mg,产率43.4%,反应时间:17h,反应溶剂:二氯甲烷和甲醇,洗脱剂:体积比为二氯甲烷/甲醇/三乙胺=100/2/1的混合液。探针结构表征数据:m.p.147.3-148.5℃,ir(kbr,νcm-1):3440(o-h,n-h),1611(c=c),1543(-no2),1470(c=c),1379(-no2),854(ar-h),756(ar-h)。1hnmr(500mhz,cdcl3,ppm)δ:8.353(d,j=9.0,4h,arh),7.950(d,j=9.0,4h,arh),7.840~7.811(m,3h,arh),7.697(s,2h,arh),7.511~7.438(m,2h,arh),7.148(d,j=7.5,1h,arh),6.867(d,j=8.5,2h,arh),6.405(t,j=9.0hz,4h,arh),6.306(s,2h,arh),4.078(s,4h,arch2nh×2),3.342~3.314(m,8h,ch2ch3×4),3.151(t,j=6.5,2h,nch2ch2),2.613(s,4h,nch2ch2-),2.516(t,j=4.5,4h,nch2ch2×2),2.225(t,j=6.5,2h,nch2ch2),1.138(t,j=7.0,12h,-ch2ch3×4)。ms(maldi-tof)calcdfor[c60h62n12o8]:m/z1081.50,found:m/z1081.663[m+h]+。
实施例2.试剂配制
(1)探针溶液的配制:称取10.80mg探针(按实施例1进行制备),用二甲基亚砜(dmso)溶解,并配制成浓度为1mm的探针储备液10ml;或用乙腈(ch3cn)溶解,并配制成浓度为1mm的探针储备液10ml;
(2)hg2+储备液配制::称取453.54mg高氯酸汞,用超纯水溶解,配制成浓度为20mm的溶液50ml;
(3)其他金属离子(li+,na+,k+,mg2+,ca2+,ba2+,sr2+,fe3+,sr2+,zn2+,co2+,ni2+,cd2+,pb2+,cr3+,al3+,ag+,cu2+,mn2+)储备液的配制:分别取相应金属离子的高氯酸盐,其他金属离子均用超纯水配成20mm的各金属离子储备液;
(4)f-储备液配制:称取0.1847g四丁基氟化胺,用乙腈溶解,配制成浓度为20mm的f-离子溶液;
(5)aco-储备液配制:称取0.1507g四丁基醋酸铵,用乙腈溶解,配制成浓度为20mm的aco-离子溶液;
(6)h2po4-储备液配制:称取四丁基醋酸铵0.1697g,用乙腈溶解,配制成浓度为20mm的h2po4-离子溶液;
(7)其他阴离子(hso4-,pf6-,clo4-,cl-,br-,i-,no3-)储备液的配制:分别取相应的阴离子四丁基铵盐,用乙腈溶解,配制成20mm的阴离子乙腈储备液;
(8)tris-hcl缓冲液:用浓度为0.2m的三羟甲基氨基甲烷(tris)和0.2mhcl配制,调节ph2~10,用ph计测试,调节至所需;
(9)hepes-naoh缓冲液:用浓度为0.2m的n-2-羟乙基哌嗪-n'-乙磺酸(hepes)和0.2mnaoh配制,调节ph10~13,用ph测试,计调节至所需。
所用试剂为分析纯试剂,试验用水为超纯水。
所用紫外-可见分光光度计型号为uv-1800,日本岛津公司生产;荧光分光光度计型号为caryeclipse荧光分光光度计,美国varian公司生产;酸度计型号为奥立龙818,美国奥立龙(orion)公司生产;手提式紫外灯wfh-204b上海光学仪器厂。
实施例3.荧光光谱法对ph的检测
在10ml容量瓶中加入探针的二甲基亚砜储备液(1mm,0.1ml)后,用二甲基亚砜/缓冲液稀释至刻度,使探针测试溶液中二甲基亚砜/缓冲液体积比为95/5,摇匀,取约3ml移入1cm的石英比色皿进行紫外-可见吸收光谱测定。
在1cm的比色皿中,加入浓度为10μm的探针溶液,再分别加入ph为2、3、4、5、6、7、8、9、10的三羟甲基氨基甲烷(tris)-hcl缓冲溶液或ph为11、12、13的n-2-羟乙基哌嗪-n'-乙磺酸(hepes)-naoh缓冲液,使测试溶液的溶剂比为(二甲基亚砜/tris-hcl或二甲基亚砜/hepes-naoh,v/v,3/2)。将溶液进行紫外-可见吸收光谱测定,当ph值不断增大时,385nm处的吸收峰不断下降,500nm处出现一个新的紫外-可见吸收峰也随着ph值不断增大,吸收峰不断增强并且红移,如图1所示。由滴定在500nm~550nm处的最大吸收波长处的吸光度,通过henderson-hasselbach质量作用方程log[(amax-a)(a-amin)]=ph-pka,式中amax为最大吸光度,a为任意ph条件下的吸光度,amin为最小吸光度,计算出pka为6.685。如图2所示。
在ph为10~13探针溶液中,ph为11~12探针变化迅速,ph大于12以后紫外吸收几乎没有改变,探针的吸收峰从550nm变化到595nm如图3,由滴定在550nm~595nm处的最大吸收波长处的吸光度,按上述同样的方法,计算出pka为11.50,如图4所示。
实施例4.探针对f-、aco-、h2po4-光谱测定
1、紫外-可见吸收光谱法对f-的检测
在10ml容量瓶中加入探针乙腈储备液(1mm,0.1ml),用乙腈稀释至刻度,制成探针测试溶液,取溶液约3ml于1cm的比色皿中进行紫外-可见光谱测定。
探针的乙腈溶液中分别加入相当于探针20倍的aco-、f-、hso4-、h2po4-、pf6-、cl-、br-、i-、no3-等阴离子稀释至刻度摇匀,取溶液约3ml于1cm的比色皿中进行紫外-可见吸收光谱测定。
浓度为10μm的探针的乙腈溶液在400nm处有吸收峰;分别加入(20mm,0.1ml)的f-,aco-,hso4-,h2po4-,pf6-,clo4-,cl-,br-,i-,no3-,随着f-的加入,探针溶液在575nm处出现一个新的强的吸收峰如图5,表明在此条件下探针溶液对f-有识别检测作用。
在浓度为10μm的探针的乙腈溶液中,加入不同浓度的f-,测定紫外-可见吸收光谱滴定曲线(具体见图6)。测定f-浓度变化时探针溶液在575nm处的吸光度,获得紫外-可见吸收校正曲线(见图7)。由校正曲线的斜率和测定10次空白值的标准偏差,测定并计算得到探针检测f-的浓度线性范围和检出限列于表1。
探针溶液检测f-时,在aco-,hso4-,h2po4-,pf6-,clo4-,cl-,br-,i-,no3-分别作为共存阴离子存在于探针-f-混合溶液中,当加入的共存阴离子浓度与f-浓度相同时,上述其他阴离子对探针检测f-的吸光度影响的相对偏差在5%以内,不干扰测定(见图8)。
2、紫外-可见吸收光谱法对aco-的检测
在10ml容量瓶中加入探针乙腈储备液(1mm,0.1ml),用乙腈稀释至刻度,制成探针测试溶液,取溶液约3ml于1cm的比色皿中进行紫外-可见光谱测定。
探针的乙腈溶液中分别加入相当于探针20倍的aco-、f-、hso4-、h2po4-、pf6-、cl-、br-、i-、no3-等阴离子稀释至刻度摇匀,取溶液约3ml于1cm的比色皿中进行紫外-可见吸收光谱测定。
浓度为10μm的探针乙腈溶液在400nm处有吸收峰;分别加入(20mm,0.1ml)的f-,aco-,hso4-,h2po4-,pf6-,clo4-,cl-,br-,i-,no3-,随着aco-的加入,探针溶液在540nm处出现一个新的强的吸收峰如图5,表明在此条件下探针溶液对aco-有识别检测作用。
在浓度为10μm的探针的乙腈溶液中,加入不同浓度的aco-,测定紫外-可见吸收光谱滴定曲线(具体见图9)。测定aco-浓度变化时探针溶液在530nm处的吸光度,获得紫外-可见吸收校正曲线(见图10)。由校正曲线的斜率和测定10次空白值的标准偏差,测定并计算得到探针检测aco-的浓度线性范围和检出限列于表1。
探针溶液检测aco-时,在f-,hso4-,h2po4-,pf6-,clo4-,cl-,br-,i-,no3-分别作为共存阴离子存在于探针-aco-混合溶液中,当加入的共存阴离子浓度与aco-浓度相同时,除f-略有影响外,上述其他阴离子对探针检测aco-的吸光度影响的相对偏差在5%以内,不干扰测定(见图11)。
3、紫外-可见吸收光谱法对h2po4-的检测。
在10ml容量瓶中加入探针乙腈储备液(1mm,0.1ml),用乙腈稀释至刻度,制成探针测试溶液,取溶液约3ml于1cm的比色皿中进行紫外-可见光谱测定。
探针的乙腈溶液中分别加入相当于探针20倍的aco-、f-、hso4-、h2po4-、pf6-、cl-、br-、i-、no3-等阴离子稀释至刻度摇匀,取溶液约3ml于1cm的比色皿中进行紫外-可见吸收光谱测定。
浓度为10μm的探针乙腈溶液在400nm处有吸收峰;分别加入(20mm,0.1ml)的f-,aco-,hso4-,h2po4-,pf6-,clo4-,cl-,br-,i-,no3-后,随着h2po4-的加入,探针溶液在510nm处出现一个新的强的吸收峰如图5,表明在此条件下探针溶液对h2po4-有识别检测作用。
在浓度为10μm的探针的乙腈溶液中,加入不同浓度的h2po4-,测定紫外-可见吸收光谱滴定曲线(见图12)。测定h2po4-浓度变化时探针溶液在505nm处的吸光度,获得紫外-可见吸收校正曲线(见图13)。由校正曲线的斜率和测定10次空白值的标准偏差,测定并计算得到探针检测h2po4-的浓度线性范围和检出限列于表1。
探针溶液检测h2po4-时,在f-,hso4-,aco-,pf6-,clo4-,cl-,br-,i-,no3-分别作为共存阴离子存在于探针-h2po4-混合溶液中,当加入的共存阴离子浓度与h2po4-浓度同相当时,上述其他阴离子对探针检测h2po4-的吸光度影响的相对偏差在5%以内,不干扰测定(见图14)。
表1探针检测f-、aco-、h2po4-的分析参数
实施例5对hg2+光谱测定
1、探针对hg2+紫外-可见吸收光谱的测定。
在浓度为5μm的探针在体积比为95/5的乙腈/水溶液中,分别加入20倍量金属离子li+,na+,k+,mg2+,ca2+,ba2+,sr2+,fe3+,sr2+,zn2+,co2+,ni2+,cd2+,pb2+,cr3+,al3+,ag+,cu2+,mn2+时,探针在390nm处产生吸收峰,hg2+(200μm)加入后,探针在560nm处出现一个新的吸收峰,而其他上述实验金属离子对光谱的影响很小(见图15)。
在浓度为5μm的探针在体积比为95/5的乙腈/水溶液中,加入不同浓度的hg2+,测定紫外-可见吸收光谱滴定曲线(具体见图16)。测定探针在560nm处荧光光谱随hg2+浓度变化,获得紫外-可见吸收校正曲线(见图17)。由校正曲线的斜率和测定10次空白值的标准偏差,测定并计算得到探针检测hg2+的浓度线性范围和检出限列于表2。
探针溶液检测hg2+时,在li+,na+,k+,mg2+,ca2+,ba2+,sr2+,fe3+,sr2+,zn2+,co2+,ni2+,cd2+,pb2+,cr3+,al3+,ag+,cu2+,mn2+,分别作为共存金属离子存在于探针-hg2+混合溶液中,当加入的共存离子浓度与hg2+浓度相当时,上述其他金属离子对探针检测hg2+的吸光度影响的相对偏差在5%以内,不干扰测定(见图18)。
2、探针对hg2+-荧光光谱的测定。
在浓度为5μm的探针在体积比为95/5的乙腈/水溶液中,以500nm为激发波长,分别加入20倍量的金属离子hg2+,li+,na+,k+,mg2+,ca2+,ba2+,sr2+,fe3+,sr2+,zn2+,co2+,ni2+,cd2+,pb2+,cr3+,al3+,ag+,cu2+,mn2+离子,只有hg2+的加入使探针溶液在583nm处出现了一个强的荧光发射峰(见图19)。
在浓度为5μm的探针在体积比为95/5的乙腈/水溶液中,加入不同浓度的hg2+,测定荧光光谱滴定曲线(具体见图20)。测定探针在583nm处荧光光谱随hg2+浓度变化,获得荧光光谱校正曲线(见图21)。由校正曲线的斜率和测定10次空白值的标准偏差,测定并计算得到探针检测hg2+的浓度线性范围和检出限列于表2。
探针溶液检测hg2+时,在li+,na+,k+,mg2+,ca2+,ba2+,sr2+,fe3+,sr2+,zn2+,co2+,ni2+,cd2+,pb2+,cr3+,al3+,ag+,cu2+,mn2+分别作为共存金属离子存在于探针—hg2+混合溶液中,当加入的共存金属离子浓度与hg2+浓度相同时,上述其他金属离子对探针检测hg2+的荧光强度影响的相对偏差在5%以内,不干扰测定(见图22)。
表2探针检测hg2+的分析参数
实施例6:探针目视比色法检测ph,f-,aco-,h2po4-,hg2+。
1、检测ph
日光下,在体积比为95/5的二甲基亚砜/缓冲液中,浓度为10μm探针在ph2~10(tris-hcl)缓冲液中,探针溶液颜色随ph值增大由淡黄色、粉色、粉红色、紫红色、紫色到蓝色的变化过程;在ph11~13(hepes-naoh)缓冲液中,探针溶液颜色随ph值增大由紫色、蓝紫色到蓝色的变化过程;探针可以通过目视检测溶液ph为2~13范围的极酸、中性至极碱性溶液的ph(见图23)。
在日光下,将剪裁好的测试滤纸条浸入探针浓度为1mm的二甲基亚砜溶液中,5秒后取出测试滤纸条;再将测试的滤纸条分别浸入浓度为0.2m的ph为2、4、6、8、10、11.5、12的缓冲液中,发现测试滤纸条立即变色,2秒后取出测试滤纸条颜色从淡黄色、橙色、粉红色、桃红色至紫色的变化过程。(见图28)
2、检测f-
日光下,在体积比为95/5的乙腈/h2o溶液中,在浓度为10μm的探针中分别加入浓度为0,10,20,40,60,100,200μm的f-。日光下,随着f-的浓度增加,探针从橙黄色逐渐变化粉红色最后变化到紫蓝色。通过目视比色,最低能检测10μm的f-,最高能检测200μm的f-。(见图24)。
3、检测aco-
日光下,在体积比为95/5的乙腈/h2o溶液中,在浓度为10μm的探针中分别加入浓度为0,10,20,200μm的aco-。日光下,随aco-浓度的增大,探针从橙黄色逐渐变化到暗红色后颜色。通过目视比色,最低能检测10μm的aco-,最高能检测200μm的aco-。(见图25)。
4、检测h2po4-
日光下,在体积比为95/5的乙腈/h2o溶液中,在浓度为10μm的探针中分别加入浓度为0,10,20,100,200μm的h2po4-。日光下,随h2po4-浓度的增大,探针从橙黄色逐渐变化到暗红色。通过目视比色,最低能检测10μm的h2po4-,最高能检测200μm的h2po4-。(见图26)。
5、检测hg2+
在体积比为95/5的乙腈/h2o溶液中,在浓度为10μm的探针中分别加入浓度为0,10,20,60,100,200μm的。日光下,随hg2+浓度的增大,探针从橙黄色逐渐变化到玫红色。通过目视比色,最低能检测10μm的hg2+,最高能检测200μm的h2po4-。(见图27)。
- 还没有人留言评论。精彩留言会获得点赞!