一种基于CsPbBr3钙钛矿量子点-分子印迹荧光传感器的辛硫磷的检测方法与流程
本发明属于分析化学
技术领域:
,具体涉及一种基于cspbbr3钙钛矿量子点-分子印迹荧光传感器的辛硫磷的检测方法。
背景技术:
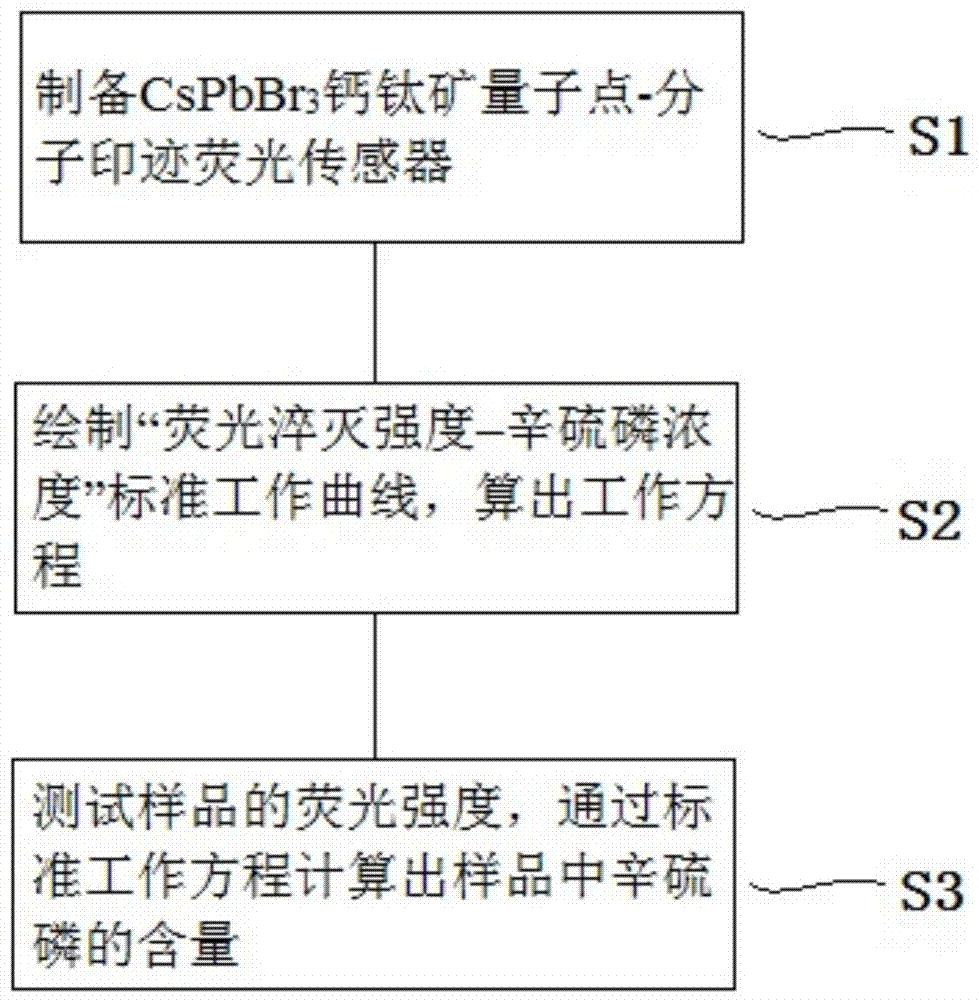
:新型的钙钛矿量子点光致发光量子产率(plqy)高,荧光发射谱窄且可调。优秀的发光性能吸引了众多研究者的关注和研究。有机-无机杂化铅卤量子点(mapbx3)是钙钛矿量子的一个大类。有机-无机量子点尽管具有优秀的性能,但是,对氧气和水汽的极度敏感极大地限制的它在实际应用中的发展。值得关注的是近几年出现的全无机钙钛矿量子点(cspbx3)的稳定更佳,对氧气和水汽的耐受程度更大,因而这种全无机的钙钛矿量子点成为又一个研究方向。除了稳定性之外,阴离子交换反应也是导致cspbx3量子点不稳定的重要因素。从维持材料稳定性的角度出发,对量子点进行包裹可以对量子点进行保护。根据关于二氧化硅包裹的钙钛矿量子点的研究,具有一定机械强度的硅基材料可以提高量子点的稳定性。目前,关于钙钛矿量子点的研究主要集中在其在发光二级管(led)中应用潜力。优秀的荧光发光性能也是使得该量子点也能够用作荧光传感器,构建基于快速,高效荧光传感的分析方法。但是,将钙钛矿量子点用于荧光分析的报道并不多。其中,针对三硝基苯酚和hcl气体的检测是基于检测对象与量子点之间的相互作用,在方法选择性和目标物分子的识别还有所欠缺。分子印迹聚合物(moleculeimprintingpolymer,mip),也被称为人工抗体,是一种带有与给定的模板(目标物)互补的特异性空穴的人造聚合物。选定的功能单体和交联剂在模板分子存在的情况下进行聚合。在去除模板之后,这种人工合成的聚合物材料能够特异性地识别目标物。因此,它们吸引了不同领域的研究者的关注,在样品前处理(色谱分离)和传感器领域得到应用。将发光性能优越的钙钛矿量子点和mip相结合,有望获得性能优秀的mip/qds荧光传感器。有机磷杀虫剂(opps)广泛用于农业生产和植物保护等行业,这也带来了环境和食品污染的风险。opps的毒性体现在它们对乙酰胆碱酯酶的抑制作用,从而对人类及其他动物的健康带来威胁。色谱分析法是环境和农产品中检测opps的有效方法。结合质谱分析高灵敏度的特性和物质定性的能力,液相色谱-质谱联用技术也用于痕量opps的检测。尽管上述分析方法经过多年的发展和应用,检测的准确性和灵敏度都达到了较高的水平,可以满足日常检测的需要,但是,因为有些实际样品中待分析物含量低,基质干扰严重,所以样品前处理是一个必不可少的步骤。目前,采用的前处理方法主要有固相萃取、液-液萃取、基质分散固相萃取、固相微萃取、超临界流体萃取和柱层析等。由于基质固相分散萃取具有样品用量少、消耗有机溶剂少等优点,基质固相分散萃取已被广泛应用于环境、生物和食品中药物、有机污染物和天然产物的分析。但基于商品化的基质固相分散萃取吸附剂往往选择性较差,目标物与吸附剂之间的作用力是非特异性的,提取净化的效率不高,很难彻底清除基质的干扰,且成本也较高。随着高毒性杀虫剂的禁用,广谱,高效,低毒的辛硫磷仍在被大批量地生产和大范围地使用,给环境和各种生物带来潜在的风险。因此,利用量子点-分子印迹荧光传感器来建立一种对辛硫磷具有高选择性、高灵敏度的检测方法成为发展的趋势。技术实现要素:为了克服上述技术缺陷,本发明提供了一种基于cspbbr3钙钛矿量子点-分子印迹荧光传感器的辛硫磷的检测方法,其步骤简单,能快速、灵敏和专一性地检测样品中的辛硫磷的含量。为了解决上述问题,本发明按以下技术方案予以实现的:一种基于cspbbr3钙钛矿量子点-分子印迹荧光传感器的辛硫磷的检测方法,包括以下步骤:s1:cspbbr3钙钛矿量子点-分子印迹荧光传感器的制备首先,由油酸铯溶液加入十八烯(ode)、油酸(oa)、油胺(oam)和溴化铅(pbbr2)形成cspbbr3钙钛矿量子点;然后,由模板分子辛硫磷、十八烯、所述cspbbr3钙钛矿量子点和n-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)形成cspbbr3钙钛矿量子点-分子印迹聚合物;最后,将所述cspbbr3钙钛矿量子点-分子印迹聚合物中的所述模版分子辛硫磷洗脱,得到cspbbr3钙钛矿量子点-分子印迹荧光传感器;s2:绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程将步骤s1所制得的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在溶剂中,再分别与一系列浓度梯度的辛硫磷溶液混合,在温度为15-30℃条件下,反应时间为5-40分钟,测试其在520nm处的荧光强度;根据辛硫磷浓度和520nm处的荧光强度,绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程;s3:测定样品中的辛硫磷的含量将步骤s1所制得的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在溶剂中,再与样品溶液混合,在温度为15-30℃条件下,反应时间为5-40分钟,测试其在520nm处的荧光强度;将所得荧光强度数值带入所述工作方程得到样品中的辛硫磷的含量。进一步的,所述步骤s1包括以下步骤:(1)制备cspbbr3钙钛矿量子点将油酸铯溶液加入十八烯、油酸、油胺和溴化铅的混合物中,搅拌均匀,进行冷却、结晶、纯化,再溶解于正己烷中,得到均匀的黄色的cspbbr3qds溶液;(2)制备cspbbr3钙钛矿量子点-分子印迹聚合物将模板分子辛硫磷、n-苯基-n’-(3-(三乙氧硅基)丙基)脲和十八烯搅拌均匀,再加入步骤(1)所制得的cspbbr3qds溶液、以及交联剂,搅拌12小时,制得cspbbr3钙钛矿量子点-分子印迹聚合物;(3)洗脱模板分子辛硫磷将步骤(2)所制得的cspbbr3钙钛矿量子点-分子印迹聚合物离心,去掉上清液,用二氯甲烷(dcm)除去所述模板分子辛硫磷,得到cspbbr3钙钛矿量子点-分子印迹荧光传感器。进一步的,所述步骤(1)包括以下步骤:1)将碳酸铯、油酸、十八烯混合均匀,真空脱气10分钟,在真空条件下加热至120℃恒温1小时,再在通入氮气的条件下,加热至150℃,恒温2小时至溶液澄清,制得所述油酸铯溶液;2)将所述十八烯、所述油胺、所述油酸、所述溴化铅混合,搅拌均匀,真空脱气10分钟,并升温至100℃,保温30分钟,再在通入氮气的条件下,升温至170℃,保温10分钟;3)将步骤1)所制得的油酸铯溶液预热100℃,向步骤2)的溶液中快速注入预热后的所述油酸铯溶液,搅拌均匀,5秒后采用冰水浴快速冷却,形成cspbbr3纳米晶体;4)将步骤3)所制得的cspbbr3纳米晶体加入乙酸乙酯,重复混合,在转速为12000rpm的条件下离心5分钟,弃去上清液,所得的cspbbr3qds固体溶解于正己烷中,获得均匀的所述黄色cspbbr3qds溶液。进一步的,在步骤1)中,所述碳酸铯与所述油酸、所述十八烯的摩尔体积比为1mmol:(1.0-1.1)ml:(12.0-12.3)ml;在步骤2)中,所述溴化铅与所述十八烯、所述油酸、所述油胺的摩尔体积比为1mmol:(20-30)ml:(2.5-3.0)ml:(5.4-5.7)ml;在步骤3)中,所述油酸铯溶液与所述溴化铅的摩尔体积比为(2-3)ml:1mmol。进一步的,在步骤(2)中,所述交联剂为正硅酸乙酯(teos),所述模板分子辛硫磷与所述n-苯基-n’-(3-(三乙氧硅基)丙基)脲、所述cspbbr3钙钛矿量子点、所述正硅酸乙酯的摩尔体积比为1mmol:(3-5)mmol:(5.27×10-3-7.27×10-3)mmol:(0.6-0.7)ml。进一步的,在步骤(2)中,所述n-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)的制备方法为:将异氰酸丙基三乙氧基硅烷(teospi)溶解在二氯甲烷中,室温下搅拌15分钟,再注入苯胺,搅拌15分钟,减压蒸馏,去除溶剂后获得所述n-苯基-n’-(3-(三乙氧硅基)丙基)脲;其中,所述异氰酸丙基三乙氧基硅烷与所述苯胺、所述二氯甲烷的摩尔体积比为:1mmol:(1.0-1.1)mmol:(4.0-4.5)ml。进一步的,在步骤s2和s3中,所述溶剂为二氯甲烷(dcm),所述反应时间为25分钟。进一步的,在步骤s2中,将步骤s1制备的所述cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,所述一系列浓度梯度的辛硫磷溶液是质量浓度分别为0ng/ml、10ng/ml、20ng/ml、30ng/ml、40ng/ml、50ng/ml、60ng/ml、70ng/ml、80ng/ml、90ng/ml、100ng/ml、120ng/ml、140ng/ml的辛硫磷溶液。进一步的,在步骤s2和s3中,测定荧光强度的条件均为采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。进一步的,所述检测方法对辛硫磷的线性检测范围为5-100ng/ml,线性相关系数为0.9980,检测限为1.45ng/ml。与现有技术相比,本发明的有益效果是:1、本发明的检测方法利用了一种以cspbbr3量子点为信号元件,再包裹上以n-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)作为多功能单体的分子印迹聚合物层的具有对辛硫磷灵敏识别功能的cspbbr3钙钛矿量子点-分子印迹荧光传感器,实现了对辛硫磷高选择性、高灵敏性的检测。2、本发明的检测方法对辛硫磷的线性检测范围为5-100ng/ml,线性相关系数为0.9980,检测限为1.45ng/ml,检测精密度为4.0%(rsd)。3、本发明的检测方法应用于实际样品中辛硫磷的加标检测及农产品中超痕量辛硫磷残留物的直接检测,在加标检测中回收率在89.90-98.25%,且相对标准偏差均小于2.2%;试验结果均表明本发明的检测方法对辛硫磷具有实际检测价值和意义。4、本发明进行了选择性试验,证明了本发明的检测方法对辛硫磷具有很好的选择性。附图说明下面结合附图对本发明的具体实施方式作进一步详细的说明,其中:图1为本发明所述的检测方法的工艺流程图;图2是时间对本发明的检测方法测定辛硫磷的影响试验结果图;图3是本发明所述cspbbr3qds在不同极性有机溶液中的荧光光谱图;图4是本发明所述mip/cspbbr3qds在不同极性有机溶液中的荧光光谱图;图5是本发明所述mip/cspbbr3qds对不同浓度的辛硫磷的荧光响应试验结果图;图6是本发明所述nip/cspbbr3qds对不同浓度的辛硫磷的荧光响应试验结果图;图7是实施例1的检测方法所得到的“荧光淬灭强度–辛硫磷浓度”标准工作曲线;图8是对比例1的检测方法所得到的“荧光淬灭强度–辛硫磷浓度”标准工作曲线;图9是实施例1和对比例1的检测方法对辛硫磷及其结构类似物的选择性试验结果图。具体实施方式各种试验仪器与试剂均为市售商品,均为可通过商业途径购买获得;其中,碳酸铯(csco3),油酸(oa),油胺(oam),溴化铅(pbbr2),十八烯(ode),正硅酸乙酯(teos),苯甲胺,异氰酸丙基三乙氧基硅烷(teospi)购买于上海麦克林生化科技有限公司。二氯甲烷(dcm),正己烷,正庚烷,乙酸乙酯,无水乙醇购买于广东广州光华科技有限公司。辛硫磷,氧化乐果,乐果,敌敌畏,水胺硫磷购买于上海阿拉丁生化科技有限公司。下面通过具体实施例结合检测条件试验例和效果试验例对本发明的技术方案做进一步说明,但本发明并不仅限于以下的实施例。实施例1如图1所示,一种基于cspbbr3钙钛矿量子点-分子印迹荧光传感器的辛硫磷的检测方法,包括以下步骤:s1:cspbbr3钙钛矿量子点-分子印迹荧光传感器的制备(1)制备cspbbr3钙钛矿量子点1)将0.8g碳酸铯、2.5ml油酸(oa)、30ml十八烯(ode)加入到50ml三颈圆底烧瓶中充分混合均匀,采用真气泵脱气处理10分钟,混合物在高真空度的条件下,密闭加热至120℃恒温1小时,再在通入氮气的条件下,加热至150℃,恒温2小时至溶液澄清,制得油酸铯溶液;2)将10ml十八烯(ode),2.07ml油胺(oam),1.03ml油酸(oa)注入100ml的三颈圆底烧瓶中,磁力搅拌均匀,然后加入0.138g溴化铅(pbbr2),搅拌均匀,将烧瓶与真空泵相连,真空脱气10分钟,将烧瓶密闭,升温至100℃,保温30分钟,随后向烧瓶中通入氮气,并升温至170℃,保温10分钟;3)将步骤1)所制得的油酸铯溶液预热100℃,向步骤2)的溶液中快速注入1ml预热后的油酸铯溶液,搅拌均匀,5秒后采用冰水浴快速冷却,形成cspbbr3纳米晶体;4)将步骤3)所制得的cspbbr3纳米晶体加入乙酸乙酯,重复混合,在转速为12000rpm的条件下离心5分钟,弃去上清液,所得的cspbbr3qds固体溶解于40ml正己烷中,获得均匀的黄色cspbbr3qds溶液,其摩尔浓度为9.4mol/l。(2)制备cspbbr3钙钛矿量子点-分子印迹聚合物1)将2.5mmol异氰酸丙基三乙氧基硅烷(teospi)溶解在10ml的二氯甲烷(dcm)中,室温下搅拌15分钟,然后向溶液中缓慢注入2.5mmol苯胺,反应在室温下进行,磁力搅拌15分钟后,减压蒸馏,去除溶剂获得透明的油状液体n-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos);2)将0.6mmoln-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)和0.15mmol辛硫磷溶解在1ml二氯甲烷(dcm)中,二者充分混合,在室温下预作用4小时,再将100μl步骤(1)所制得的cspbbr3qds溶液溶解于10ml十八烯(ode)中,置于50ml烧瓶中,搅拌均匀,然后将预作用溶液和100μl正硅酸乙酯(teos)依次加入到烧瓶中,持续搅拌12h,制得cspbbr3钙钛矿量子点-分子印迹聚合物。(3)洗脱模版分子辛硫磷将步骤(2)所制得的cspbbr3钙钛矿量子点-分子印迹聚合物在转速为1200rpm的条件下离心,去掉上清液,用二氯甲烷(dcm)洗涤10次,除去未反应的小分子物质以及模板分子辛硫磷,得到cspbbr3钙钛矿量子点-分子印迹荧光传感器(mip/cspbbr3qds)。s2:绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程将步骤s1所制得的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,再分别与质量浓度为0ng/ml、10ng/ml、20ng/ml、30ng/ml、40ng/ml、50ng/ml、60ng/ml、70ng/ml、80ng/ml、90ng/ml、100ng/ml、120ng/ml、140ng/ml的辛硫磷溶液混合,在温度为25℃条件下,反应时间为25分钟,测试其在520nm处的荧光强度;根据辛硫磷浓度和520nm处的荧光强度,绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程;其中,标准工作曲线如图7所示,工作方程如效果试验例1所示。s3:测定样品中的辛硫磷的含量将步骤s1制备的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,再与样品溶液混合,在温度为25℃条件下,反应时间为25分钟,测试其在520nm处的荧光强度;将所得荧光强度数值带入工作方程得到样品中的辛硫磷的含量。其中,在步骤s2和s3中,测定荧光强度的条件均为采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。检测结果如效果试验例1、效果试验例2所示。实施例2-8实施例2-8与实施例1的区别在于:实施例2在在步骤s2和s3中,反应时间均为5分钟;实施例3在在步骤s2和s3中,反应时间均为10分钟;实施例4在在步骤s2和s3中,反应时间均为15分钟;实施例5在在步骤s2和s3中,反应时间均为20分钟;实施例6在在步骤s2和s3中,反应时间均为30分钟;实施例7在在步骤s2和s3中,反应时间均为35分钟;实施例8在在步骤s2和s3中,反应时间均为40分钟;其余步骤均与实施例1相同。实施例9-12实施例9-12与实施例1的区别在于:实施例9在步骤s2和s3中,均将步骤s1制备的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在正己烷中配置成质量浓度为5×10-6g/ml的溶液;实施例10在步骤s2和s3中,均将步骤s1制备的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在正庚烷中配置成质量浓度为5×10-6g/ml的溶液;实施例11在步骤s2和s3中,均将步骤s1制备的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在甲苯中配置成质量浓度为5×10-6g/ml的溶液;实施例12在步骤s2和s3中,均将步骤s1制备的cspbbr3钙钛矿量子点-分子印迹荧光传感器分散在乙酸乙酯中配置成质量浓度为5×10-6g/ml的溶液;其余步骤均与实施例1相同。对比例1一种基于cspbbr3钙钛矿量子点-分子非印迹荧光传感器的辛硫磷的检测方法,包括以下步骤:s1:cspbbr3钙钛矿量子点-分子非印迹荧光传感器的制备(1)制备cspbbr3钙钛矿量子点本对比例中的cspbbr3钙钛矿量子点的制备方法同实施例1。(2)制备cspbbr3钙钛矿量子点-分子非印迹聚合物1)本对比例中的n-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)的制备方法同实施例1;2)将0.6mmoln-苯基-n’-(3-(三乙氧硅基)丙基)脲(bupteos)溶解在1ml二氯甲烷(dcm)中,在室温下预作用4小时,再将100μl步骤(1)所制得的cspbbr3qds溶液溶解于10ml十八烯(ode)中,置于50ml烧瓶中,搅拌均匀,然后将预作用溶液和100μl正硅酸乙酯(teos)依次加入到烧瓶中,持续搅拌12h,制得cspbbr3钙钛矿量子点-分子非印迹聚合物。(3)洗脱将步骤(2)所制得的cspbbr3钙钛矿量子点-分子非印迹聚合物在转速为1200rpm的条件下离心,去掉上清液,用二氯甲烷(dcm)洗涤10次,得到cspbbr3钙钛矿量子点-分子非印迹荧光传感器(nip/cspbbr3qds)。s2:绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程将步骤s1所制得的cspbbr3钙钛矿量子点-分子非印迹荧光传感器分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,再分别与质量浓度为0ng/ml、10ng/ml、20ng/ml、30ng/ml、40ng/ml、50ng/ml、60ng/ml、70ng/ml、80ng/ml、90ng/ml、100ng/ml、120ng/ml、140ng/ml的辛硫磷溶液混合,在温度为25℃条件下,反应时间为25分钟,测试其在520nm处的荧光强度;根据辛硫磷浓度和520nm处的荧光强度,绘制“荧光淬灭强度–辛硫磷浓度”标准工作曲线,算出工作方程;其中,标准工作曲线如图8所示,工作方程如效果试验例1所示。s3:测定样品中的辛硫磷的含量将步骤s1制备的cspbbr3钙钛矿量子点-分子非印迹荧光传感器分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,再与样品溶液混合,在温度为25℃条件下,反应时间为25分钟,测试其在520nm处的荧光强度;将所得荧光强度数值带入工作方程得到样品中的辛硫磷的含量。其中,在步骤s2和s3中,测定荧光强度的条件均为采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。对比例2-8对比例2-8与对比例1的区别在于:对比例2在在步骤s2和s3中,反应时间均为5分钟;对比例3在在步骤s2和s3中,反应时间均为10分钟;对比例4在在步骤s2和s3中,反应时间均为15分钟;对比例5在在步骤s2和s3中,反应时间均为20分钟;对比例6在在步骤s2和s3中,反应时间均为30分钟;对比例7在在步骤s2和s3中,反应时间均为35分钟;对比例8在在步骤s2和s3中,反应时间均为40分钟;其余步骤均与对比例1相同。检测条件试验例1:反应时间试验方法:将实施例1-8步骤s1制备的mip/cspbbr3qds和对比例1-8步骤s1制备的nip/cspbbr3qds分别分散在二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,再分别与90ng/ml的辛硫磷混合,在25℃的条件下水浴,测试不同反应时间下(5、10、15、20、25、30、35、40min),mip/cspbbr3qds和nip/cspbbr3qds在520nm处的荧光强度。每个时间点设置3个平行样品。探索两种复合物的吸附动力学,试验结果如图2所示。荧光测试条件:采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。由图2可以看出,在吸附刚刚开始时,mip/cspbbr3qds荧光强度下降比较明显,随后荧光猝灭逐步减慢,在吸附25分钟后,荧光信号趋于稳定,说明在此时,吸附和脱附到达了平衡。与mip/cspbbr3qds相比,nip/cspbbr3qds荧光强度下降的速率和程度更慢和更小。在吸附20分钟后,nip/cspbbr3qds的荧光强度趋于稳定。恒定的强度值表示当吸附和解吸速率相等时的平衡状态。因此,优选的孵育时间为25分钟。这一结果说明,mip/cspbbr3qds的印迹聚合物具有对辛硫磷的特异性识别的印迹空穴,而nip/cspbbr3qds中的功能单体是无序分布的,因此辛硫磷需要更长的时间进入mip的印迹空穴。检测条件试验例2:反应的溶剂条件试验方法:取实施例1、9、10、11、12步骤s1制备的cspbbr3qds和mip/cspbbr3qds分别分散到2ml二氯甲烷(dcm)、正己烷、正庚烷、甲苯、乙酸乙酯中,配置成质量浓度5×10-6g/ml的溶液。测试cspbbr3qds和mip/cspbbr3qds在520nm处的荧光强度。试验结果如图3-4所示,其中,图3是cspbbr3qds在不同极性有机溶液中的荧光光谱图;图4是mip/cspbbr3qds在不同极性有机溶液中的荧光光谱图。荧光测试条件:与检测条件试验例1的荧光测试条件相同。由图3-4可以看出,cspbbr3qds溶解在正己烷和正庚烷中时,量子点荧光处于高亮度状态,说明在非极性的溶剂中cspbbr3qds的稳定性和发光能力良好。同样量的cspbbr3qds分散在相同体积的甲苯(弱极性)中时,量子的荧光强度发生下降,且发射峰位置发生偏移。当量子点分散在中等极性的乙酸乙酯和二氯甲烷中时,荧光强度下降明显,发射峰位置明显偏移。结合前人关于cspbbr3qds表面化学状态的研究工作,实验结果与他们的研究的结论基本相符,cspbbr3qds的表面形成了油胺溴、油胺和油酸-油胺三者的快速动态稳定体系,从而使量子点内部的晶体结构稳定存在。在弱极性条件下,这个平衡体系相对稳定,溶剂极性提高后,可能对表面的平衡体系造成影响,破坏了量子晶体的结构。将量子点包裹进硅基的mip内部后,二氧化硅基体外层可能使量子点表面与溶剂相对隔绝,从而表现出了对cspbbr3qds的保护作用。mip/cspbbr3qds对中等极性的溶剂(二氯甲烷、甲苯)的耐受程度明显高于裸量子点。考虑到辛硫磷在二氯甲烷(dcm)中溶解度高,且溶剂毒性较小,因此,本工作采用dcm作为后续实验的溶剂。效果试验例1:分别根据实施例1步骤s1、s2和对比例1步骤s1、s2,得到不同辛硫磷浓度下mip/cspbbr3qds和nip/cspbbr3qds的荧光光谱图(如图5-6),并绘制出“荧光淬灭强度–辛硫磷浓度”标准工作曲线(如图7-8)。由图5-6可以看出,mip/cspbbr3qds和nip/cspbbr3qds都对模板分子表现出光谱响应。然而,在相同的浓度条件下,mip/cspbbr3qds的荧光强度下降的程度更大,这是由于mip/cspbbr3qds的印迹层有对辛硫磷特异性结合的印迹空穴,对辛硫磷的结合能力更强。这一荧光猝灭的体系,在一定的浓度范围内符合stern-volmer方程,即(f0-f)/f=ksvcq,cq是猝灭剂的浓度,ksv是stern-volmer方程的常数。由图7-8可以看出,(f0-f)/f与mip/cspbbr3qds和nip/cspbbr3qds的猝灭剂的浓度(cq)的校准曲线都具有良好的线性关系。计算得出,mip/cspbbr3qds的猝灭方程为线性方程:(f0-f)/f=0.03700c-0.08054(r2=0.9980),在辛硫磷浓度在5到100ng/ml的范围内;nip/cspbbr3qds的猝灭方程为线性方程:(f0-f)/f=0.01228c-0.005983(r2=0.9952)。试验还根据3σiupac准则(3σ/s)计算检测极限,其中σ是空白信号的标准偏差(通过测试10次空白信号计算得到标准偏差σ),s是线性校准的斜率,计算出mip/cspbbr3qds的辛硫磷检出限为1.45ng/ml。平行测定含有10ng/ml的辛硫磷的mip/cspbbr3qds荧光信号,相对标准偏差为4.0%(rsd)。另外,斜率ksv是衡量检测方法灵敏度的重要指标,mip/cspbbr3qds和nip/cspbbr3qds对应的斜率分别为0.0370和0.0123,二者的比值if为3.01,这一结果说明mip/cspbbr3qds对辛硫磷具有特异性识别能力,使得检测灵敏度得到提升。效果试验例2:实际样品检测考察为了考察本发明的mip/cspbbr3qds能否在实际样品中使用,检测了从市场购买的土豆中辛硫磷的残留量。样品提取程序后,样品中没有发现目标分析物。因此,使用加标样品的回收率测试进行评估。另外,mip/cspbbr3qds的实用性很大程度上取决于农产品中超痕量辛硫磷残留物的直接检测。试验方法:提取液中加入20,50,80ng/ml的辛硫磷得到低、中和高添加浓度的样品;再取实施例1制备的mip/cspbbr3qds分散在10ml二氯甲烷中配置成质量浓度为5×10-6g/ml的溶液,与样品溶液混合,充分相互作用25分钟,测试其在520nm处的荧光强度。对应于低、中和高添加浓度的回收分别进行三次。试验结果见表1。荧光测试条件:采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。表1对土豆样品检测的回收率(n=3)由表1可以看出,加标土豆样品的回收率为89.90-98.25%,相对标准偏差小于2.2%(rsd)。结果表明,mip/cspbbr3qds对加标样品中农药的分析具有可靠性和实用性,具有较高的准确度和重复性,可以满足在实际样品中对辛硫磷的检测。效果试验例3:选择性考察选用了水胺硫磷(isocarbophos),乐果(dimethoate),氧化乐果(omethoate),和敌敌畏(dichlorve)作为辛硫磷的结构类似物,用来考察mip/cspbbr3qds的选择性。试验方法:取实施例1制备的mip/cspbbr3qds和对比例1制备的nip/cspbbr3qds分散在二氯甲烷中,分别与相同浓度(0.13μmol/l)的水胺硫磷、乐果、氧化乐果、敌敌畏进行混合,充分反应25分钟,测试其在520nm处的荧光强度。采用选择性因子(α)来评价mip/cspbbr3qds和nip/cspbbr3qds的选择性,由下式计算:(α)来评价mip/cspbbr3qds和nip/cspbbr3qds的选择性,α=(f0-f)/f(模板)/(f0-f)/f(类似物),当α值越接近1.00,材料对模板的选择性越高。试验结果见图9和表2。荧光测试条件:采用300nm作为激发波长,激发光和发射光的狭缝宽度均为10nm,光电倍增管电压为400v。表2mip/cspbbr3qds和nip/cspbbr3qds的选择性因子αmip/cspbbr3qdsαnip/cspbbr3qds辛硫磷1.001.00氧化乐果3.531.78乐果4.912.33水胺硫磷5.181.96敌敌畏5.682.03由图9和表2可以看出,在所有选择的有机磷农药中,mip/cspbbr3qds对辛硫磷的反应最强。这一结果表明mip/cspbbr3qds对辛硫磷具有较高的特异性,因为在尺寸,形状和化学组方面,定制的印迹腔与辛硫磷互补。与辛硫磷相比,其他农药具有不同的结构,不能进入mip/cspbbr3qds的识别空腔。因此,相对较弱的反应是由于非特异性吸附造成的。此外,nip/cspbbr3qds对模板和所有类似物的选择性因子接近于1.00,表明nip/cspbbr3qds对类似物和模板没有选择性。结果表明,mip/cspbbr3qds对辛硫磷具有特异性。效果试验例4:与现有技术比较检出限与现有技术的荧光分析法检测有机磷杀虫剂的对比,结果如表3所示。表3检出限比较由表3可以看出,本发明的cspbbr3钙钛矿量子点-分子印迹荧光传感器的检出限较低,且灵敏度高,选择性好。以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,故凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何修改、等同变化与修饰,均仍属于本发明技术方案的范围内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1