一种利用硫量子点检测钴离子及接力识别诺氟沙星的方法与流程
本发明涉及化学技术领域,特别涉及一种利用硫量子点检测钴离子及接力识别诺氟沙星的方法。
背景技术:
钴是人体生长发育所必需的微量元素之一,其与人体健康有着密切联系,长期缺乏钴会引起恶性贫血症,但摄入过量也会对人体造成危害。水环境中的钴超标,会产生许多对人体不利的影响,例如导致间质纤维化或心肌衰弱等。因此,在环境检测中,钴被列为重要的检测项目之一。
目前,钴离子的检测方法主要为化学发光法、分光光度法和原子吸收光谱法等。采用这些方法对钴离子进行检测时,均需对待检测样品进行前处理,例如,需要对待检测样品中的干扰离子进行掩蔽或分离,这导致钴离子的检测耗时较长。
技术实现要素:
本发明实施例提供了一种利用硫量子点检测钴离子及接力识别诺氟沙星的方法,能缩短检测时长。
第一方面,本发明实施例提供了一种利用硫量子点检测钴离子的方法,包括:
分别将第一质量份的所述硫量子点溶解于蒸馏水,形成空白溶液;
将第二质量份的所述硫量子点溶解于待测溶液中,形成样品溶液;
还包括:
通过荧光分光光度计扫描所述空白溶液在360nm激发波长下,在380nm~450nm范围内的空白荧光发射光谱;
通过荧光分光光度计扫描所述样品溶液在360nm激发波长下,在380nm~450nm范围内的样品荧光发射光谱;
当所述样品荧光发射光谱在395nm~415nm范围内未出现波峰时,确定所述待测溶液中含有钴离子;其中,所述波峰出现在所述空白荧光发射光谱的395nm~415nm范围内。
经过检测结果表明,空白溶液的空白荧光发射光谱在395nm~415nm范围内出现最大吸收波长,即出现波峰,而含有钴离子的样品溶液的样品荧光发射光谱在395nm~415nm范围内的荧光强度远小于空白荧光发射光谱在该范围内的荧光强度,空白荧光发射光谱原有的波峰消失,说明硫量子点的荧光强度会受钴离子影响,钴离子对硫量子点有猝灭效应。另外,经过进一步检测试验发现,na+、fe3+、cu2+、mg2+、zn2+、pb2+、cd2+、nh4+、ag+、ni2+和bi3+的水溶液的荧光发射光谱在395nm~415nm范围内也出现波峰,说明这些阳离子不会对硫量子点的荧光强度产生较大影响,从而说明了硫量子点对钴离子具有特征传感性,能用于钴离子的检测。
优选地,
在所述将第二质量份的所述硫量子点溶解于待测溶液中之前,进一步包括:调节所述待测溶液的ph为7~8。
优选地,
在所述确定所述待测溶液中含有钴离子之后,进一步包括:
分别检测所述样品溶液和空白溶液在360nm激发波长下的荧光强度;
根据以下公式,计算所述待测溶液中钴离子的浓度;
f0/f1=5.73194+9325c1
其中,f1表征所述样品溶液在360nm处的荧光强度,f0表征所述空白溶液在360nm处的荧光强度,c1表征所述待测溶液中钴离子的浓度。
优选地,
在所述将第二质量份的所述硫量子点溶解于待测溶液中,形成样品溶液之前,进一步包括:
检测所述待测溶液中是否存在钙离子,如果是,对所述待测溶液中的钙离子进行分离。
优选地,
当所述蒸馏水的体积与所述待测溶液的体积相等时,所述第一质量份与所述第二质量份相等。
第二方面,本发明实施例提供了一种利用硫量子点接力识别诺氟沙星的方法,包括:
当利用本发明上述任一实施例提供的方法确定样品荧光发射光谱在395nm~415nm范围内未出现波峰时,还包括:
向样品溶液中加入目标溶液;
通过荧光分光光度计扫描加入所述目标溶液后的所述样品溶液在360nm激发波长下,在380nm~450nm范围内的目标荧光发射光谱;
当所述目标荧光发射光谱中的荧光强度大于所述样品荧光发射光谱中对应波长下的荧光强度时,确定所述目标溶液中含有诺氟沙星,并恢复所述样品溶液中的硫量子点对钴离子的检测活性。
优选地,
在所述确定所述目标溶液中含有诺氟沙星之后,进一步包括:
检测加入所述目标溶液后的样品溶液在360nm激发波长下的荧光强度;
根据以下计算公式,计算所述诺氟沙星溶液的浓度;
f2=359.79632+2.85108×10-6c2
其中,f2表征加入所述目标溶液后的样品溶液在360nm激发波长下的荧光强度,c2表征所述诺氟沙星溶液的浓度。
优选地,
在所述确定样品荧光发射光谱在395nm~415nm范围内未出现波峰之后,在所述向所述样品溶液中加入目标溶液之前,进一步包括:
按照预设时间周期,检测所述样品溶液在360nm激发波长下的荧光强度;
确定各个所述时间周期对应的所述荧光强度之间的强度差值;
当所述强度差值小于预设阈值时,执行所述向所述样品溶液中加入目标溶液。
本发明实施例提供了一种利用硫量子点检测钴离子及接力识别诺氟沙星的方法,空白溶液的空白荧光发射光谱在395nm~415nm范围内出现最大吸收波长,即出现波峰,而含有钴离子的样品溶液的样品荧光发射光谱在395nm~415nm范围内的荧光强度远小于空白荧光发射光谱在该范围内的荧光强度,空白荧光发射光谱原有的波峰消失,说明硫量子点的荧光强度会受钴离子影响,钴离子对硫量子点有猝灭效应。另外,经过进一步检测试验发现,na+、fe3+、cu2+、mg2+、zn2+、pb2+、cd2+、nh4+、ag+、ni2+和bi3+的水溶液的荧光发射光谱在395nm~415nm范围内也出现波峰,说明这些阳离子不会对硫量子点的荧光强度产生较大影响,从而说明了硫量子点对钴离子具有特征传感性,能用于钴离子的检测。由此,可直接利用硫量子点对待测溶液中的钴离子进行检测,而无需对待测溶液中的其他阳离子进行掩蔽或分离,从而缩短了钴离子的检测时长。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
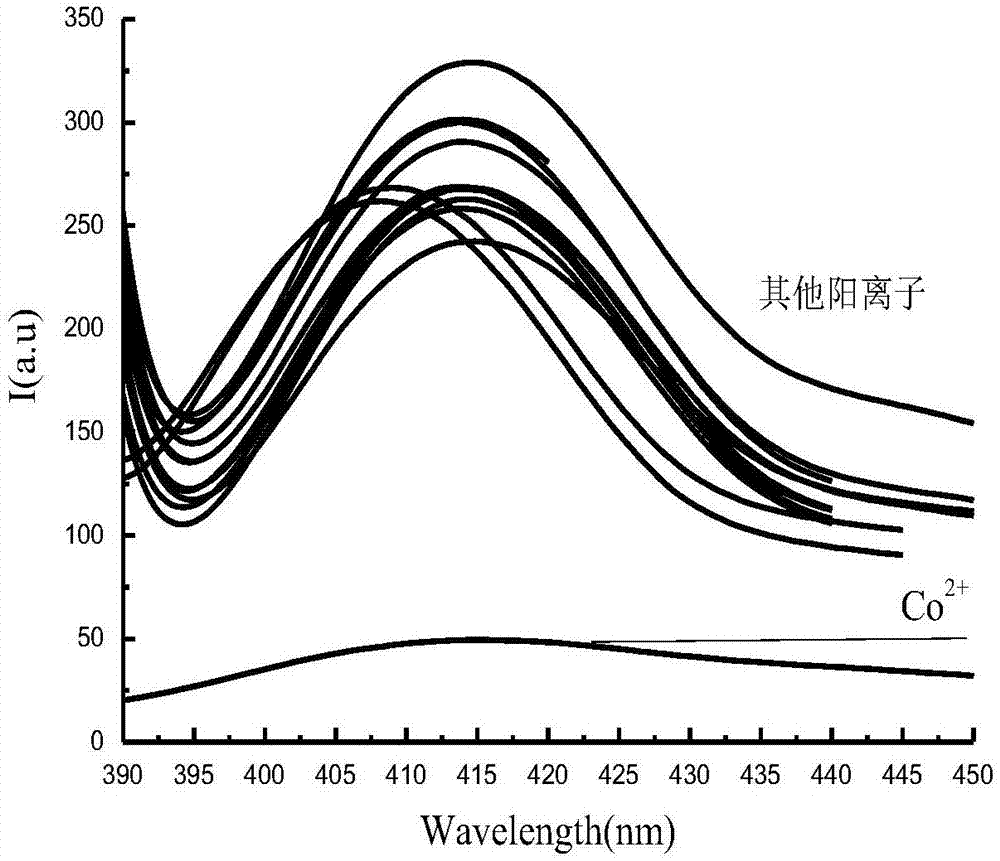
图1是本发明一个实施例提供的含有硫量子点的不同阳离子溶液对应的荧光发射光谱图;
图2是本发明一个实施例提供的含有硫量子点的不同钴离子浓度的荧光光谱图;
图3是本发明一个实施例提供的钴离子浓度-荧光强度直线关系图;
图4是本发明一个实施例提供的紫外吸收光谱图;
图5是本发明一个实施例提供的不同ph值条件下的硫量子点的荧光光谱图;
图6是本发明一个实施例提供的含有硫量子点和钴离子的不同阳离子溶液的荧光强度图;
图7是本发明一个实施例提供的含有硫量子点和钴离子的不同阳离子溶液的荧光光谱图;
图8是本发明一个实施例提供的可逆性检测结果示意图;
图9是本发明一个实施例提供的含有硫量子点和钴离子的不同浓度的诺氟沙星的荧光光谱图;
图10是本发明一个实施例提供的诺氟沙星浓度-荧光强度直线关系图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例,基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中,所使用的各类设备、试剂和材料若无特别说明,均为常规市售可得。
实施例1:测定硫量子点的特征传感物质
通过对溶解有硫量子点的不同样品溶液的荧光发射光谱进行扫描,确定硫量子点的特征传感离子,测定时的具体步骤如下:
步骤a1:分别配置浓度为0.001mol/l的硝酸铜、硝酸镁、硫酸锌、硝酸铅、硝酸钠、氯化铵、硝酸钴、硝酸银、硝酸镉、硝酸镍、硫酸铁、硝酸铋溶液各100ml作为待测溶液。
针对配置出的每一种待测溶液,执行步骤b1和步骤c1;每检测完一种待测溶液,用蒸馏水清洗比色皿5次;
步骤b1:取一比色皿加入2ml蒸馏水和50μl的硫量子点,制得空白溶液。待体系平衡时扫描其对应的空白荧光发射光谱,扫描时的激发波长设置为360nm,发射波长的起始值为380nm,终止值为450nm。
步骤c1:用微量进样器向步骤b1的空白溶液中加入50μl待测溶液,形成样品溶液。待体系平衡时扫描该样品溶液对应的样品荧光发射光谱,扫描时的激发波长设置为360nm,发射波长的起始值为380nm,终止值为450nm。
实施例1的扫描结果如图1所示,从图1中可以看出,在同等条件下扫描各个样品溶液的发射光谱,除硝酸钴溶液制得的样品溶液外,其他阳离子(na+、fe3+、cu2+、mg2+、zn2+、pb2+、cd2+、nh4+、ag+、ni2+和bi3+)样品溶液在波长395nm~415nm范围内出现最大吸收波长,各种离子溶液中只有钴离子溶液对应的样品荧光发射光谱相较于空白荧光发射光谱的变化最明显,它在395nm~415nm范围内的荧光强度远离其他离子,且远小于空白荧光发射光谱在该范围内的荧光强度,因此说明钴离子对硫量子点有猝灭效应。这可能是因为钴离子与硫量子点的表面基团发生了作用,使得硫量子点表面的电荷发生了转移,钴离子与硫量子点之间发生了聚集诱导效应,而硫量子点表面电荷的转移使得硫量子点的荧光强度下降,从而出现了猝灭效应。
实施例2
通过测定不同浓度的钴离子溶液对硫量子点荧光强度的影响,进一步确定硫量子点对钴离子的传感。
实施例2可以包括以下步骤:
步骤a2:取一比色皿加入2ml蒸馏水和50μl的硫量子点,制得空白溶液。待体系平衡时扫描其对应的空白荧光发射光谱,扫描时的激发波长设置为360nm,发射波长的起始值为380nm,终止值为450nm。
以下步骤中,激发波长均设置为360nm,发射波长的起始值均设置为380nm,发射波长的终止值均设置为450nm。
步骤b2:用微量进样器向步骤a2制得的空白溶液中加入20μl浓度为0.001mol/l的硝酸钴溶液,于同等条件下测定该样品溶液的荧光发射光谱。然后逐次增加20μl硝酸钴溶液,测定其荧光发射光谱,直至荧光发射光谱不再随样品溶液中钴离子浓度的增大而有所变化。
实施例2的测定结果如图2所示,其中,图2标示出1到11对应的钴离子浓度(mol/l)依次为:0,10-5,2×10-5,3×10-5,4×10-5,5×10-5,6×10-5,7×10-5,8×10-5,9×10-5,即1对应的钴离子浓度为0,即为步骤a2得到的空白荧光发射光谱。从图2可以看出,随着钴离子浓度增加,硫量子点的荧光强度逐渐降低,这也说明硫量子点对钴离子的传感性。
通过进一步对不同浓度的硝酸钴溶液各自对应的荧光发射光谱中410nm处的荧光强度的分析,可得如图3所示的钴离子浓度-荧光强度关系图。从图3中可以看出钴离子浓度与硫量子点的荧光强度之间存在线性关系:f0/f1=5.73194+9325c1,r=0.96102,由线性关系也可说明,随着钴离子浓度增加,硫量子点的荧光强度降低。并且,由于钴离子浓度与硫量子点的荧光强度之间存在良好的线性关系,则在利用硫量子点检测钴离子浓度时,可通过测定样品溶液的荧光强度,然后利用上述线性方程,求解出待测溶液中的钴离子浓度。由此可简便快捷地测试出待测溶液中的钴离子浓度。实验结果表面,硫量子点可在0~9×10-5mol/l范围内精确检测钴离子。
另外,利用uv-3100pc型紫外可见分光光度计分别对硝酸钴溶液和含有钴离子的样品溶液进行紫外吸收光谱测定。测定时,用蒸馏水做参比,对波长200~800nm进行紫外吸收光谱扫描,测定结果如图4所示。图4中标示的a对应硝酸钴溶液的紫外吸收光谱,图4中标示的b对应含有钴离子的样品溶液的紫外吸收光谱。从图4中可以看出,两条紫外光谱具有明显的差异,这也说明了硫量子点对钴离子的紫外吸收光谱有明显影响,它改变了钴离子的紫外吸收光谱,从而说明了硫量子点对钴离子的传感性。
实施例4:对硫量子点在不同酸碱环境下的荧光性能的检测
在比色皿中加入2ml蒸馏水和50μl的硫量子点,分别测定其在ph3~10时所对应的荧光光谱,以确定硫量子点在不同酸碱环境下的荧光性能,测定结果如图5所示。从图5中可以看出,ph=7时硫量子点的荧光强度最高,而ph=10时硫量子点的荧光强度最弱,且在ph=9时硫量子点的荧光强度已经较弱。因此,在使用硫量子点时,可将待测溶液的ph调节为7~8,使得硫量子点不会因为环境ph值急剧降低自身的荧光强度,从而有利于对待测溶液中传感离子的准确测定。
实施例5:确定硫量子点检测钴离子过程中的干扰离子
实施例5可以包括以下步骤:
步骤a5:分别配制浓度为0.001mol/l的氯化钙、硝酸镁、硫酸锌、硝酸铅、硝酸钠、硝酸铬、硝酸镉、氯化铵、硝酸锌、硝酸铜溶液。
针对配置出的每一种溶液,执行步骤b5,并且每检测完一种溶液,用蒸馏水清洗比色皿5次;
步骤b5:在比色皿中2ml蒸馏水、50μl的硫量子点和20μl硝酸钴溶液,再向比色皿中加入20μl步骤a5配制出的一种溶液。待体系平衡时测定在激发波长为360nm,发射波长为410nm的荧光强度。
实施例5的扫描结果如图6所示,从图6中可以看出,大多数金属离子几乎对钴离子的检测无干扰作用,但钙离子的影响较大,超过了其他金属离子对钴离子检测的影响。因此,在利用硫量子点对待测溶液中的钴离子进行检测时,可先检测待测溶液中是否存在钙离子,如果待测溶液中存在钙离子,则先将钙离子进行分离,以避免钙离子对硫量子点检测过程中的影响。例如,可采用向待测溶液中加入碳酸盐的方式分离钙离子。
另外,进一步扫描含有钴离子和硫量子点的氯化钙溶液其对应的荧光发射光谱,扫描时的激发波长设置,发射波长的起始值为390nm,终止值为440nm,得到的结果如图7所示,从图7中也可以看出钙离子的影响较大。
实施例6:硫量子点与钴离子的荧光可逆性检测
实施例6可以包括:循环执行5次以下步骤,每执行完一次则倾倒出比色皿中的溶液,并用蒸馏水清洗比色皿5次;
步骤a6:在比色皿中2ml蒸馏水和50μl的硫量子点,平衡5分钟后测测定其在360nm激发波长下的荧光强度,之后每隔5min测一次,共测定5次。
步骤b6:向步骤a6测量后的溶液中加入200μl钴离子溶液,平衡五分钟后测定其在360nm激发波长下的荧光强度,之后每隔五分钟测一次,共测定5次。
实施例6的测定结果如图8所示,在蒸馏水中每隔5min测得的硫量子点的荧光强度大致相同,加入钴离子之后,硫量子点的荧光强度明显下降,但每经过5min后测得硫量子点的荧光强度趋于稳定,重复操作一共五个循环,每次循环数据基本一致,说明硫量子点在检测钴离子时,其荧光强度不会随着时间的增加而出现较大浮动,所以钴离子对于硫量子点的响应具有可逆性。
从实施例6的检测结果可以看出,硫量子点在检测含钴离子的待测溶液后,其荧光强度降低,且不会随时间的增加而恢复,因此,为了恢复硫量子点的荧光强度,需向样本溶液中加入其他物质。
在本发明实施例中,通过向含有钴离子的样本溶液中加入诺氟沙星溶液,可恢复检测过钴离子溶液的硫量子点的荧光强度,使其能再次对co2+进行检测。具体地,取0.0319g的诺氟沙星胶囊配成0.001mol/l的溶液。在硫量子点与钴离子的体系中加入诺氟沙星溶液20μl,发现硫量子点的荧光强度增加,再依次加入20μl诺氟沙星溶液,测定其荧光发射光谱如图9所示。其中,图9中标识出的1到20对应的诺氟沙星的浓度(mol/l)依次为:0,10-5,2×10-5,3×10-5,4×10-5,5×10-5,6×10-5,7×10-5,8×10-5,9×10-5,10-4,1.1×10-4,1.2×10-4,1.3×10-4,1.4×10-4,1.5×10-4,1.6×10-4,1.7×10-4,1.8×10-4,1.9×10-4,2×10-4,即1对应的诺氟沙星的浓度为0。从图9可以看出,随着诺氟沙星浓度的增加,硫量子点与钴离子体系中的硫量子点的荧光强度逐渐增强,说明诺氟沙星能恢复硫量子点对co2+的检测活性。
另外,进一步对不同浓度的诺氟沙星对应的荧光光谱中410nm处的荧光强度的分析,可得如图10所示的诺氟沙星浓度-荧光强度关系图。从图10中可以看出诺氟沙星浓度与硫量子点的荧光强度之间存在线性关系:f2=359.79632+2.85108×10-6c2,其中,f2表征加入所述目标溶液后的样品溶液在360nm激发波长下的荧光强度,c2表征所述诺氟沙星溶液的浓度。从图10中也可以看出,随着诺氟沙星浓度的增加,硫量子点与钴离子体系中的硫量子点的荧光强度逐渐增强,这也说明诺氟沙星能恢复硫量子点的荧光强度。
由此,可利用硫量子点先检测钴离子,钴离子使得硫量子点的荧光猝灭,从而检测出钴离子。然后利用含有钴离子和硫量子点的溶液接力识别诺氟沙星,诺氟沙星可恢复硫量子点的荧光强度,从而识别出诺氟沙星。这可能是由于钴离子与诺氟沙星形成了配位键,使得钴离子与硫量子点之间的聚集诱导效应消失,从而使得硫量子点的荧光强度有所恢复,其反应机理如下所示。这也可以说明诺氟沙星可以作为硫量子点与钴离子组成的新型传感器的开关,由此可构建一种用于检测钴离子和诺氟沙星的新型“on-off-on”光学传感器,以弥补传统方法测量灵敏度低、耗时长、准确性差等缺陷。
根据上述方案,本发明至少具有如下有益效果:
1、在本发明实施例中,向待测溶液中加入硫量子点,形成样品溶液,然后通过对空白溶液和样品溶液分别进行荧光发射光谱扫描,当样品溶液的样品荧光发射光谱中未出现空白溶液的空白荧光发射光谱中出现的波峰时,即可确定待测溶液中含有钴离子。另外,na+、fe3+、cu2+、mg2+、zn2+、pb2+、cd2+、nh4+、ag+、ni2+和bi3+的荧光发射光谱均出现了空白荧光发射光谱中的波峰,由此说明硫量子点对钴离子具有特征传感性,能用于钴离子的检测。
2、在本发明实施例中,可直接利用硫量子点对待测溶液中的钴离子进行检测,而无需对待测溶液中的其他阳离子进行掩蔽或分离,从而缩短了钴离子的检测时长。
3、在本发明实施例中,通过将硫量子点溶解在不同钴离子浓度的溶液中,并分别检测溶液的荧光强度,以检测在不同钴离子浓度的影响下,硫量子点的荧光强度变化。检测结果表明,钴离子浓度与硫量子点的荧光强度具有良好的线性关系,可利用测得的线性关系直接计算待测溶液中的钴离子浓度,简化了钴离子浓度的检测过程。
4、在本发明实施例中,硫量子点对钴离子的传感具有良好的可逆性,可利用诺氟沙星恢复硫量子点对钴离子的检测活性,使得硫量子点可多次检测待测溶液。
5、在本发明实施例中,将诺氟沙星作为硫量子点与钴离子组成的新型传感器的开关,由此可构建一种用于检测钴离子和诺氟沙星的新型“on-off-on”光学传感器,弥补了传统方法测量灵敏度低、耗时长、准确性差等缺陷。
需要说明的是,在本文中,诸如第一和第二之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个······”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同因素。
最后需要说明的是:以上所述仅为本发明的较佳实施例,仅用于说明本发明的技术方案,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内所做的任何修改、等同替换、改进等,均包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!