一种荧光探针及其制备方法与流程
本发明涉及一种荧光探针及其制备方法,特别是涉及一种用于异氰酸酯检测的荧光探针及其制备方法,属于分析检测技术领域。
背景技术:
异氰酸酯是一大类含有(o=c=n-)的有机化合物,包括二异氰酸酯、单异氰酸酯和多异氰酸酯。因异氰酸酯基中碳原子的两个杂基双键连接着电负性极大氮氧原子,使得含有异氰酸酯基团的化合物均具备很高的化学活性,能够和绝大多数含有活泼氢基团的化合物发生反应,例如:羟基、胺基、羧基等。目前常见的有异氰酸酯有甲苯二异氰酸酯(tdi)、二苯基甲烷二异氰酸酯(mdi)、异佛尔酮二异氰酸酯(ipdi)、六亚甲基二异氰酸酯(hdi)等。
异氰酸酯是一种重要的工业原料,应用范围也非常广泛。但是脂肪族及芳香族的异氰酸酯类有机物均会对生物体造成严重的危害。在空气中,异氰酸酯会以蒸汽态和气溶胶态存在且极易挥发,并通过呼吸道、消化道、皮肤接触途径进入体内对人体造成不同程度的伤害。目前已知的异氰酸酯对人的眼睛、皮肤、喉咙、支气管及呼吸道粘膜等器官造成伤害的主要表现为:1)人体在接触0.35mg/m3~0.92mg/m3的甲苯二异氰酸酯(tdi)后,眼和鼻会受到刺激并引起流泪;眼睛接触异氰酸酯蒸气会因粘膜刺激而出现化学性结膜炎等症状,长时间接触如果不治疗,可能导致永久性损伤。2)皮
国外对异氰酸酯的检测开始于上世纪50年代,我国对于异氰酸酯的检测虽起步较晚但已逐渐发展出了较为成熟的方法如:化学分析法、分光光度法、色谱法、红外光谱法。1)目前国内外检测异氰酸酯最常用的方法是化学分析法,即采用二丁胺与-n=c=o基团的反应,将过量的二正定胺和异氰酸酯基反应得到脲,然后利用酸标准溶液对其进行滴定中和,从而得到待测物当中的-n=c=o含量,采用该方法进行-n=c=o含量检测虽操作简单,但该化学分析法通常会使用甲苯、二正丁胺等有毒化学试剂,产生大量的检测废液,对环境污染较大;同时检测耗时长,检测稳定性较差,从而会影响生产控制的稳定性;2)分光光度法是根据不同的样品浓度反应后表现出不同的颜色变化以及吸光度的不同进行测定。针对异氰酸酯类物质检测常用的分光光度法包括:正丁胺-孔雀绿分光光度法、对二甲氨基苯甲醛盐酸法、重氮偶合分光光度法。对二甲氨基苯甲醛盐酸法精确度、准确性较高,操作简单,分析成本低,时间短效率高,是目前应用最为广泛的比色方法。将反应产物静置显色20min后,在440nm处测其吸光度,通过浓度与吸光度之间的关系得到待测物中-n=c=o含量,该方法快速简便,标准偏差小于5%,而正丁胺-孔雀绿法灵敏度较高,但缺点是所使用的溶液和试剂处理复杂,过程繁琐,对实验要求过高,显色体系不稳定;重氮偶合法需要预先用乙酸-硫酸体系将异氰酸酯水解,然后再进行显色测定;如果溶解效果不好,也会导致水解反应不完全,对实验结果造成很大影响;3)利用液相色谱法检测异氰酸酯,利用异氰酸酯类物质易与水、醇类物质反应的特性,使用液相色谱法检测时需要将异氰酸酯衍生化为稳定的衍生物在进行测定。国外针对异氰酸酯的检测多采用液相色谱检测,选用c18色谱柱进行分离,通过荧光检测器、质谱仪和uv紫外检测器进行检测。张泉福等人在测定聚氨酯预聚体中游离tdi时,将甲醇与tdi反应生成相应的氨基甲酸甲酯,即进行封端处理,然后用lichrosorbrp-18柱(250mm×4.6mm)分离,检测极限为0.13mg/d。此种方法的优点是检测物质不受其分子量大小影响,并且可以选择多种溶剂做流动相,缺点是操作性要求高,成本高,非常不利于日常检测;4)气相色谱法简称gc(gaschromatography),相对来说是一种比较新型的检测方法,具有高灵敏度,高选择性,分析快以及应用范围为广泛等特点。气相色谱法是利用gc试样中不同组分在气相以及固定液相间的具有分配系数上的差异,将不同的组分在气液两相间重复分配,根据组分通过色谱柱来到检测器的时间长短来定性,该方法的缺点是在进行分析时必须利用已知色谱进行对照,并且通常会选择和质谱、光谱连用才能得到理想的效果;5)红外光谱法,操作简单,并且不会损害样品,也被广泛应用在异氰酸酯的检测当中。同时,其灵敏度也较高,能够用来检测不同化学反应的产物制备过程。
综上所述,虽然当前几种较成熟的方法已经有了较成熟的发展,但也都存在着不同的缺陷,如:分光光度法虽然操作简单且成本低,但准确性不高,同时使用效率低;气相色谱法和液相色谱法虽然具备优秀的检测效果,但操作过程复杂、成本较高,不易于长久的发展。
技术实现要素:
本专利发明的目的在于克服现有异氰酸酯检测方法的缺陷,而开发的一种能够高效,准确,简便,快捷低成本的检测异氰酸酯的荧光探针以及制备方法。
为能够高效检测异氰酸酯类化合物,本专利采取的技术方案为:
第一方面,本发明提供了一种荧光探针,结构式如(i)所示:
本发明的荧光探针为n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺,其分子式为c22h21no2,相对分子质量为371.1。该探针为橙色无味固体粉末,不溶于水,易溶于甲醇、乙醇、二氯甲烷等有机溶剂。
本发明的荧光探针会发生分子内的电荷转移,处于n-位置的供电子氨基会转移给6-位置上的吸电子羟基;该荧光探针6-位置的酚羟基在可见光区无吸收,该探针含有活泼氢,可作为识别基团。由于异氰酸基极易与醇羟基发生酯化反应,导致6-位置基团吸电子能力变强,原有探针内部的电荷转移发生改变,从而荧光发射波长发生蓝移,探针荧光从橙色变为浅绿色。异氰酸酯浓度越大,移动效果越明显,探针与异氰酸酯作用前后不同发射位置的荧光强度比值可作为检测信号,从而实现探针对异氰酸酯类化合物的比率型荧光检测。
研究表明,将探针溶于乙醇溶液,在420nm的激发光照射下,荧光探针的发射波长在570nm;当探针的羟基在三乙胺的作用下(由于探针上的羟基电负性较小,加入三乙胺后增加-oh的电负性,能够让酚羟基的活性增强,易与-n=c=o基团反应)与异氰酸酯反应后,产物的发射波长开始向着527nm处移动,且异氰酸酯浓度越大波长移动越快,溶液有橙色开始变为浅绿色,利用紫外光谱仪分析探针与异氰酸酯反应前后的激发波长位置发生改变,通过红外光谱仪分析探针与异氰酸酯反应前后重要官能团发生改变来说明探针对于异氰酸酯的检测效应。
基于本发明荧光探针的上述荧光性质,可用于特异性识别异氰酸酯类化合物,并针对不同环境下的异氰酸酯的含量进行检测分析,且本探针具备高效,准确,快捷检测的优点。
第二方面,本发明提供了一种上述荧光探针的制备方法,包括以下步骤:
(1)以4-溴-1,8萘酐与正丁胺为原料,利用正丁胺消除萘酐上的氧原子反应制备结构式如式(ii)所示的n-正丁基-4-溴-1,8-萘二酰亚胺;
(2)以步骤(1)制得的n-正丁基-4-溴-1,8-萘二酰亚胺与4-乙酰氧基苯乙烯为原料反应,制备结构式如(iii)所示的n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺;
(3)以步骤(2)制得的n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺为原料,利用氢氧化钾脱羧基,制备结构式如(i)所示的n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺即探针
作为本发明所述荧光探针的制备方法的优选实施方式,所述荧光探针的制备方法包括一下步骤:
如权利要求2所述的荧光探针的制备方法,其特征在于:包括以下步骤:
(1)将4-溴-1,8萘酐、正丁胺溶于无水乙醇溶液当中,在氮气保护气体作用下,在85℃油浴条件下反应3~8个小时后,将反应液冷却至室温;然后利用旋转蒸发器蒸发反应溶剂,经过纯化后再旋转蒸发流动相获得固体,得到n-正丁基-4-溴-1,8-萘二酰亚胺;
(2)将(1)所得的n-正丁基-4-溴-1,8-萘二酰亚胺与4-乙酰氧基苯乙烯、溶于三乙胺与乙腈混合溶剂当中,加入醋酸钯、三(2-甲苯基)磷两种催化剂,在氮气或者惰性气体的保护下,在105℃高压瓶内进行反应48小时;然后旋转蒸发反应产物,经过纯化后再利用旋转蒸发器蒸发流动相获得固体,得到n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺;
(3)将(2)所得到的n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺与氢氧化钾溶解于甲醇溶剂当中,常温条件下反应2小时;然后加入盐酸萃取收集有机相,再通过旋转蒸发器蒸发反应溶剂,经过纯化后再旋转蒸发流动相获得固体,得到n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺结构式如(i)所示的荧光探针。
作为本发明所述的荧光探针制备方法的优选实施方式,所述步骤(1)~(3)中,均采用硅胶层析柱进行纯化。
作为本发明所述的荧光探针制备方法的优选实施方式,所述步骤(1)中,每毫摩尔4-溴-1,8萘酐加入5~6ml无水乙醇的比例,将4-溴-1,8萘酐溶解于无水乙醇当中;所述(2)中,每毫摩n-正丁基-4-溴-1,8-萘二酰亚胺加入8~10ml的三乙胺与乙腈混合液的比例,将n-正丁基-4-溴-1,8-萘二酰亚胺溶解于三乙胺与乙腈混合溶剂当中;所述(3)中每毫摩n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺加入8~10ml甲醇的比例,将n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺溶解于甲醇溶剂当中。
与现有技术相比,本发明的有益效果为:
(1)本发明所提供的荧光探针(n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺)6-位置的酚羟基在可见光区无吸收,该探针含有活泼氢,可以特异性识别异氰酸酯。异氰酸基极易与醇羟基发生酯化反应,导致6-位置基团吸电子能力变强,原有探针内部的电荷转移发生改变,从而荧光发射波长发生蓝移,因此该探针可以实现对异氰酸酯类化合物的比率型荧光检测,用于对液体环境,空气环境以及化学样品中的异氰酸酯检测分析。对比只利用发射波长的荧光强度变化来检测异氰酸酯的开-关型荧光探针,本发明利用探针与异氰酸酯前后不同发射波长的荧光强度比值来检测异氰酸酯,具备更高的准确性与检测精确度,避免了因为检测溶液浓度差异、激发波长不稳定以及检测的系统误差所带来的精度影响。
(2)本发明的荧光探针具有稳定的光学以及化学特性,并且能够针对不同的异氰酸酯类化合物进行特异性、精确检测。
(3)本发明的荧光探针能够对异氰酸酯类化合物进行快速检测:较低浓度的异氰酸酯环境下,探针与异氰酸酯反应后的发射波长立即发生变化,随着异氰酸酯浓度的提高,波长变化的速度越快。探针的发射波长位置在570nm处,与异氰酸酯反应后,荧光波峰开始向着527nm处移动,根据不同的异氰酸酯反应浓度,固定检测时间,根据反应液在570nm与527nm处的荧光强度比值建立相关曲线,即可针对不同环境下的异氰酸酯进行浓度检测。
(4)本发明的荧光探针制备简单且耗时较少,并且探针针对异氰酸酯类化合物的检测准确度高,方便快捷,建立的检测体系可针对不同环境下的异氰酸酯类化合物进行检测。
附图说明
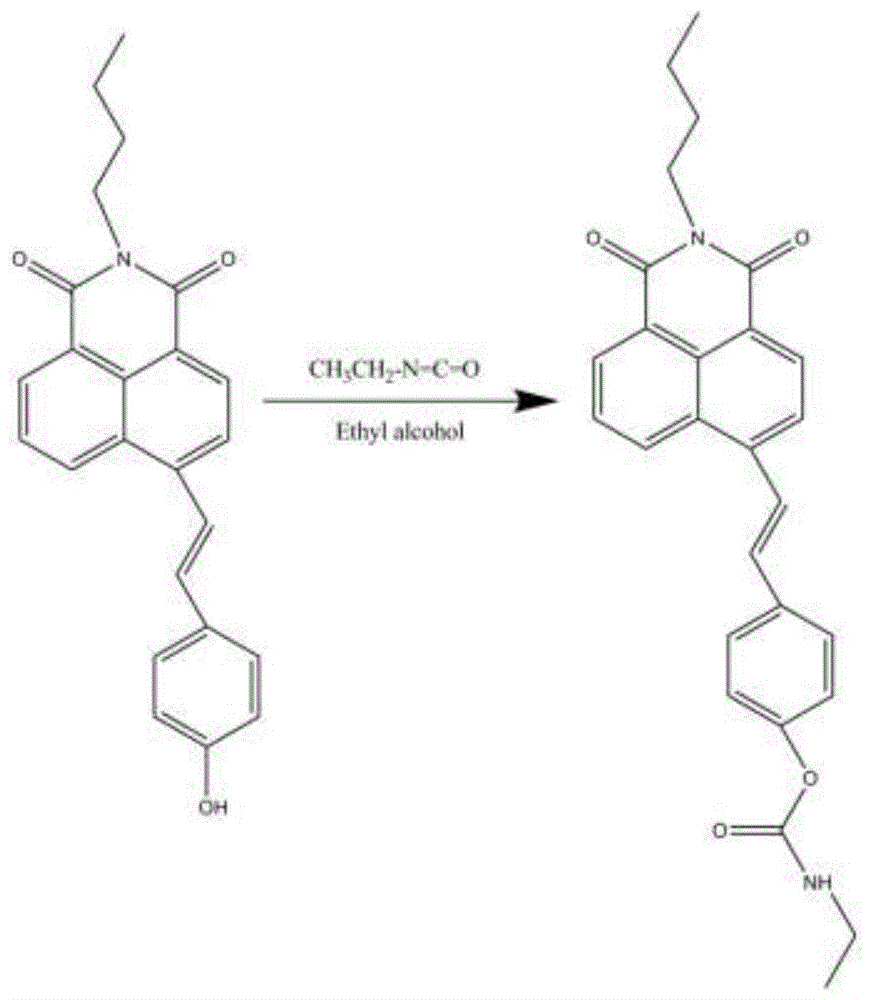
图1为本发明的荧光探针的合成路线图;
图2为本发明荧光探针n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺的核磁共振氢谱图;
图3为本发明荧光探针n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺的质谱图;
图4为荧光探针与异氰酸酯作用前后机理图;
图5为荧光探针的紫外荧光光谱图;
图6为荧光探针作用时间曲线;
图7为荧光探针针对不同异氰酸酯类化合物的检测图
图8为荧光探针对异氰酸酯的选择性检验图;
图9为荧光探针针对不同有机化合物的抗干扰图
图10为不同离子溶液对探针稳定性响应图;
图11为本发明荧光探针与不同反应浓度的异氰酸酯作用前后的荧光光变化图谱;
图12为本发明荧光探针与不同浓度的异氰酸酯反应后,在同一时间570nm与527nm处荧光强度比值的变化图谱;
图13为本发明荧光探针检测异氰酸酯的回归直线图。
具体实施方式
为了更好的说明本发明的目的、技术特点与优点,下面将附图对具体实施例进行进一步说明。
实施例1
本发明荧光探针及其制备方法的一种实施例,本实施例的荧光探针
为n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺,其结构式如式(i):
本实施例的荧光探针合成路线如图1所示,其具体制备方法如下:
1)在氮气保护和搅拌条件下,将4-溴-1,8萘酐(500mg,1.8mmol)与正丁胺(450μl,4.5mmol)搅拌溶解于无水乙醇(10~15ml)当中,利用油浴条件加热反应液至85℃,接通冷凝管形成回流,保持反应条件3~4个小时后,停止加热,待反应液冷却至室温后,取反应液至250ml烧瓶,然后利用旋转蒸发器蒸发反应溶剂,将所得产物经过硅胶层析柱纯化得到棕色固体n-正丁基-4-溴-1,8-萘二酰亚胺(478mg,1.74mmol)。
2)在氮气保护和搅拌条件下,将n-正丁基-4-溴-1,8-萘二酰亚胺(478mg,1.74mmol)与4-乙酰氧基苯乙烯(367μl,2.4mmol)搅拌溶解于15ml乙腈,5ml三乙胺当中,加入醋酸钯(2.24mg,0.01mmol)、三(2-甲苯基)磷(20.97mg,0.069mmol)做催化剂,利用油浴条件加热反应液至105℃,高压条件下保持反应48h,停止加热,待反应液冷却至室温后,取反应液至250ml烧瓶,然后利用旋转蒸发器蒸发反应溶剂,将所得产物经过硅胶层析柱纯化得到绿色产物n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺(73.9mg,0.179mmol)。
3)在氮气保护和搅拌条件下,将n-正丁基-4-(4-乙酰氧基苯乙烯基)-1,8-萘二酰亚胺(74mg,0.179mmol)与氢氧化钾(11mg,0.196mmol)溶解于甲醇(10ml)当中,常温条件下反应2个小时后,停止反应,然后加入盐酸经过萃取并且收集有机相至250ml烧瓶,利用旋转蒸发器蒸发反应溶剂,将所得产物经过硅胶层析柱纯化得到橙色产物n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺(55mg,0.148mmol)。通过核磁共振氢谱对其进行表征,结果如图2所示,具体分析如下:1hnmr(cdcl3,600mhz,ppm):1.00(t,j=6.0hz,3h),1.48(m,2h),1.75(m,2h),4.20(t,j=6.0hz,2h),6.93(d,j=6.0hz,1h),7.35(d,j=18.0hz,1h),7.56(d,j=12.0hz,1h),7.75(d,j=6.0hz,1h),7.81(t,j=6.0hz,1h),8.0(d,j=6.0hz,1h),8.60(d,j=6.0hz,1h),8.65(d,j=6.0hz,1h)。另外通过质谱进行辅助证明,结果如图3所示:ms(esi):m/z=370[m-h]-.通过分析可以确定所合成的即为目标产物。
实施例2荧光探针与异氰酸酯的作用机理图
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针与异氰酸酯之间的作用机理。荧光探针的检测基团为羟基,溶解于乙醇溶液当中,在三乙胺的条件下与异氰酸酯发生作用后,羟基反应后形成了氨基甲酸酯,荧光探针的乙醇溶液宏观上表现为橙色,与异氰酸酯发生作用后溶液变为浅绿色,具体变化如图4所示。
实施例3荧光探针的紫外荧光光谱性质
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针的紫外吸收与荧光光谱图。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl到比色皿当中,再加入2.7ml的无水乙醇制备成检测液,将检测液利用紫外分光光度计进行测试获得紫外吸收光谱图如图5所示,荧光探针在420nm处有强烈的吸收峰;另取300μl的母液至比色皿当中,再加入2.7ml的无水乙醇制备成检测液,将检测液进行荧光检测,获得荧光探针的荧光光谱图如9所示,荧光探针在570nm处有强烈的波峰;
实施例4荧光探针作用时间曲线
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针的紫外吸收与荧光光谱图。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl到比色皿当中,再加入2.7ml的无水乙醇制备成检测液,然后添加5μl的三乙胺和4μl的异氰酸酯溶液,分别测试0s,30s,60s,90s,120s,150s,180s,210s,240s,270s时刻的527nm与570nm处的荧光强度,根据i527/i570比值与时间建立关系如图6,当反应进形到0s时,i527/i570为0.6;当反应进行到30s时,比值约为1.4,说明探针已经开始和异氰酸酯发生作用,527nm处的荧光波峰不断增强;当反应进行到60s时,比值为2.2左右,荧光探针与异氰酸酯间的反应已经到达转折点,反应速率下降,异氰酸酯基本上已经被反应完全,表明该探针60s就可以达到对异氰酸酯的检测;当反应进行到180s时,i527/i570比值为2.3,再对之后的荧光比值进行检测,发现已经不发生变化,稳定在2.3左右,说明已经完全反应,表明荧光探针与异氰酸酯的反应在3min内就已经到达了终点。通过反应时间曲线的分析充分说明该荧光探针能够针对异氰酸酯类化合物迅速检测的目的。
实施例5荧光探针对不同异氰酸酯类化合物的检测
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针能够针对不同类的异氰酸酯化合物进行检测的目的。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl至比色皿当中,再加入2.7ml的无水乙醇制备成检测液。分别取4μl的二苯基甲烷二异氰酸酯(mdi)、异氰酸酯乙酯(eic)、甲苯二异氰酸酯(tdi)、六亚甲基二异氰酸酯(hdi)、异佛尔酮二异氰酸酯(ipdi)加入检测液当中,检测反应3min时i527/i570的比值,获得如下图7所示,其中mdi、tdi、hdi、ipdi的比值在1.6左右,而eic的比值在2.0左右,说明该荧光探针与不同种类的异氰酸酯化合物均发生作用,该探针可以用来检测不同种类的异氰酸酯化合物,针对异氰酸酯基团具备特异性检测的功能。
实施例6荧光探针对异氰酸酯的选择性检测
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针能够针对异氰酸酯化合物进行选择性检测的目的。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl到比色皿当中,再加入2.7ml的无水乙醇制备成检测液。分别加入4μl的氨水、苯、丙酮、二氯甲烷、甲醇、乙腈、异氰酸酯;另外一组仅用检测液作为对照,检测添加不同化合物的检测液在3min时i527/i570荧光强度比值。结果如图8所示,其中氨水、苯、丙酮、二氯甲烷、甲醇、乙腈的荧光强度i527/i570比值与空白对照组基本保持一致,这说明该荧光探针不与上述这些有机化合物发生作用,而加入异氰酸酯的实验组,i527/i570比值达到1.6,与其他实验组和空白对照组形成对比,充分说明了该探针针对异氰酸酯的特异性检测。
实施例7荧光探针检测针对不同有机化合物具备的抗干扰能力
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针检测异氰酸酯能够针对不同有机化合物具备的抗干扰能力。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl到比色皿当中,再加入2.7ml的无水乙醇制备成检测液。设置7组不同实验组,其中6组添加4μl的异氰酸酯,然后再分别加入4μl的氨水、苯、丙酮、二氯甲烷、甲醇、乙腈,第7组作为荧光探针的空白对照,测试检测液在3min时i527/i570荧光强度比值,结果如图9所示,空白组i527/i570的荧光强度比值为0.6左右,而其他六组的比值均发生明显变化,说明异氰酸酯与探针发生特异性反应;另外苯、丙酮、二氯甲烷、甲醇、乙腈设置组的比值在2.2左右,说明这几种有机化合物不会对探针检测异氰酸酯造成干扰,氨水这一组的比值略低于上述几组,是因为氨水溶液当中含有水分,水分极易与异氰酸酯基团发生作用,降低了异氰酸酯的浓度,造成比值有所减低,但是通过氨水组和空白组的对照,根据荧光强度的变化同样能够说明荧光探针能够对异氰酸酯进行检测。
实施例8不同离子溶液对探针稳定性响应图
本实施例测试了n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺探针在不同离子溶液条件下检测异氰酸酯的稳定性。具体方法如下:将4mg的纯探针溶于4ml的无水乙醇当中配制成标准探针溶液(母液),取300μl到比色皿当中,再加入2.7ml的无水乙醇制备成检测液。分别加入300μl不同的盐溶液包括:二水合氯化钡、碳酸钙、硫酸铜、磷酸二氢钾、硝酸钾、硫酸镁、氯化锰、氯化钠、硝酸钠、磷酸氢二铵,利用荧光光谱仪测试混合液在527nm与570nm处荧光强度比值,在和探针与异氰酸酯反应混合液做比较,结果如图10所示,所测试的不同盐溶液(即不同离子)对探针无影响,只有添加异氰酸酯后检测的比值发生了明显变化,说明该荧光探针的抗离子干扰稳定性良好。
实施例9n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针对液体环境中异氰酸酯含量的检测
以n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针(实施例1制备)对无水乙醇溶液当中的异氰酸酯含量进行检测分析。测试时探针的浓度稀释至4μm,分别加入不同的异氰酸酯量,记录探针与异氰酸酯反应后570nm与527nm处的荧光强度比值,结果如下表1所示。4μm的探针乙醇溶液与不同量的异氰酸酯后的荧光图谱变化如图11所示(图11中,曲线1-8依次代表加入0μmol、4μmol、8μmol、12μmol、16μmol、20μmol、24μmol、28μmol、32μm的异氰酸酯),i527/i570比值变化如图11所示。从图11可以看出,纯探针乙醇溶液在420nm激发光照射下在570nm处发射橙光,与异氰酸酯反应后,混合溶液呈现浅绿色,发射波长改变到527nm处,随着异氰酸酯量的增大,橙色波长荧光强度不断减弱,绿色波长荧光强度不断增强,波长蓝移越明显,以i527/i570荧光强度比值作为检测信号,可以实现对异氰酸酯的比率型荧光检测。从图12可以看出,在异氰酸酯浓度在5×10-6mol/ml以内,异氰酸酯与探针作用后在527nm处的荧光强度与探针在570nm处的荧光强度的比值(i527/i570)随着异氰酸酯浓度的升高而增大,且呈现线性关系,随着添加异氰酸酯量的上升曲线趋于平缓。
表1
实施例10n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针对异氰酸酯灵敏度的检测
本实施例考察了本发明制备的n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针检测异氰酸酯的灵敏度。具体考察方案如下:将荧光探针溶解稀释至4μm,分别加入不同量的异氰酸酯,以异氰酸酯浓度为横坐标,i527/i570荧光强度比值为纵坐标,绘制相关曲线如下图13所示。对浓度在5×10-6mol/ml以内的数据进行重新分析,得到拟合函数为y=1.13918+k×x(r=0.99),拟合程度极好;其中,y代表荧光强度比,k=0.15163。
检测极限lod=3×s.d./k,其中k是相关曲线的斜率,s.d.代表在没有添加异氰酸酯时探针的荧光强度比标准差。
lod=3×0.0057/0.15163nmol/l=112nmol/l,由该结果可见,本发明荧光探针检测异氰酸酯类化合物的灵敏度极高。
综上所述:本发明制备的n-正丁基-4-(4-酚羟基苯乙烯基)-1,8-萘二酰亚胺荧光探针可用于针对异氰酸酯类化合物检测分析。根据探针与不同浓度的异氰酸酯反应,拟合相关曲线可对不同环境下的异氰酸酯浓度进行检测分析。
最后应当说明的是,以上实施例仅用以说明本发明的技术方案而非本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可对本发明的技术方案进行修改或者同等替换,而不脱离发明技术方案的实质与范围。
- 还没有人留言评论。精彩留言会获得点赞!