一种基于纳米多孔金属膜的葡萄糖电化学微电极传感器的制作方法
本发明属于电化学生物传感器领域,涉及一种多孔结构金属膜的加工工艺,及基于多孔金属膜的微电极和电化学葡萄糖传感器,以及它们的制备方法。
背景技术:
糖尿病是严重威胁人类健康的常见慢性病之一,血糖的实时监测有利于患者和医生评估病情,制定合理科学的治疗方案或者对现有方案进行调整,因此,葡萄糖传感器也是生物传感器领域研究最多、商品化最早的生物传感器。葡萄糖传感器最为核心的部件是葡萄糖氧化酶(glucoseoxidase,god)有效固定在生物活性界面组成的酶电极。在实际应用中或者现有市场出售的血糖监测传感器一般都采用针式微电极,它们创伤小,可以减少人身生理上的免疫反应。如得到美国食品和药物管理局(fda)认证雅培公司(abbott)的辅理善瞬感葡萄糖监测系统传感器(freestylenavigator),传感器探头直径小于0.4毫米,插入皮肤下方5毫米,不用采集指尖血,通过监测组织液葡萄糖水平而得到血糖指标。但是由于电极微型化和尺寸限制,使得god可负载面积大大减小,负载的酶量不足,使传感器的线性范围,灵敏度等性能下降,甚至不能正常工作,根据临床的要求,葡萄糖传感器线性区域上限必须达到30mm。实验室中研究出来的性能优异的新材料也往往因无空间固定而不能得到应用。
在不增加微电极尺寸的要求下,为了解决负载god酶量的问题,主要有两种途径解决。一种是增加微电极的数量,如国内专利cn200910097842.2(授权公告号cn101530327b)和cn200410101080.6提及的皮下组织植入式实时监测用针状葡萄糖传感器,使用一或两个针状工作电极和一个参比电极组成两电极体系,植入时需要植入2-3个电极进行测量,国内专利cn201510783056.3(授权公告号cn105266826b)提及了一种皮下组织植入式针状葡萄糖传感器,在基座底部设有工作电极、对电极和参比电极的分体式三电极体系。这些方法会加大了创伤的面积。另一种方法是在微电极表面制备三维网状结构,增加电极活性表面的比表面积,如电极表面修饰物中掺杂零维的量子点、金属纳米颗粒,一维纳米管,或者二维的石墨烯、氧化锌等纳米片,这些方法具有良好性能,但是制备过程复杂,需要苛刻的加工条件和工艺。最简单的三维网状结构的获得是直接制备具三维结构表面膜的电极,如介孔碳膜电极,多孔硅膜电极、多孔金属膜电极等。国内专利cn201510750828.3发明了一种多孔活性石墨烯微电极,固定葡萄糖氧化酶后,实现了酶的直接电化学及对葡萄糖的快速电化学测定;国内专利cn201810700292使用中空管状石墨烯纤维填充葡萄糖氧化酶,葡萄糖氧化酶被包覆在连续的石墨烯内部,起到极好的酶保护作用,并且优异的石墨烯导电性使得电荷快速转移和传输;专利cn201710592096提供了一种表面粗糙化处理的金膜电极,并基于该金膜电极构建电化学过氧化氢传感器,该方法利用磁控溅射制备金薄膜层,然后采用化学蚀刻处理,使金膜表面粗糙化。但是,一般而言,电极表面的三维结构有厚度的限制,增加厚度会增加镀膜脱落的几率,影响传感器电极的持久性和稳定性,因此,需要发明一种可以获得镀膜牢固,不易脱落的方法,简单可靠的获得三维结构表面电极的方法。
纳米多孔金属膜是一种具有纳米级孔结构的金属材料,内部为大量三维相互贯通的纳米级尺度的孔隙和骨架,其不仅有金属的导电性、延展性等特性,也具有小尺寸效应、表面效应、量子尺寸效应和量子隧道效应等纳米材料特有的性质。另外,其多孔结构也使其具有比表面积高、密度低、通透性好、导电性高等特点。目前已被广泛应用于催化、传感、分离、过滤、生物材料、燃料电池等领域,多孔金属膜的高比表面积可以增加电极的活性面积和电活性物质的负载量,纳米级孔结构和金属导电性使其对某些物质具有高度催化活性,纳米多孔金膜还表现出很好的稳定性和再生性,易回收重复利用。
纳米多孔金属的制备方法主要包括去合金法、模板法和电化学法。模板法是将金属通过一定的技术负载在预先制定的模板上,然后通过物理、化学等方法将模板除去,从而获得多孔的目标金属,常用的模板有离子溶液聚合物、生物模板、多孔氧化铝等。模板法能较好地控制所得的纳米多孔金属的形态尺寸,但由于模板的束缚,调节多孔金属的结构或尺寸时只能通过重新调整模板来实现,同时还要采用适当的方法除去模板,因此操作较为复杂繁琐。电化学法,使用纯金属作为基底,通过在一定的溶液中持续施加电压,对金属进行阳极化处理,使表面上的部分金属逐渐溶解到电解液中,由此得到纳米多孔金属膜。该方法虽然应用较为普遍,但如上文提到的专利cn201710592096所述一样,得到的往往只是粗糙化的表面,孔隙不能达到很深的内部,且孔隙的孔径不易调节,腐蚀时横向和径向的速度很难控制,得到的孔径不理想,孔径过小(<5纳米)时,会导致god等蛋白无法进入孔隙,孔径过大(>200nm)时,固定的god容易脱落。另一方面,腐蚀而溶解到电解液中的金属很难回收利用,也造成了金属的浪费和环境的污染。去合金法是利用不同金属之间活性的差异,在腐蚀性溶液中将合金中的一种或多种金属选择性溶解,从而得到单一组分的纳米多孔金属。去合金法在au-ag合金体系研究较多,金与银能组成单相无限固溶体,两金属组分具有足够大的标准电极电势差,银原子可以被腐蚀溶解,残留的金原子在界面上扩散并聚集,形成纳米多孔金的骨架。去合金法总体上操作简单方便,制得的纳米结构比表面积高、结构均匀,能通过对腐蚀过程的动态调整控制获得的孔径,适合大规模的工业生产。但是使用此法时,需预先制备特定组成、晶相相同的合金,大部分金属较难找到适用的合金体系,适用范围窄,且金膜形成过程需要金组分重新凝结,原有刚性被破坏,膜的附着力下降,易变形脱落。
技术实现要素:
针对现有技术中微电极葡萄糖氧化酶传感器由于尺寸限制,负载酶量少而导致的传感器灵敏度低,线性范围窄等问题,本发明提供了一种基于三维多孔金属膜的微电极制备方法及葡萄糖传感器制备方法。本发明中多孔金属膜的制备无需模板,孔隙孔径易调,与衬底结合力强,不易脱落,方法适用范围广,包括金、铂等一系列金属都可通过此法获得多孔结构,用于大量负载葡萄糖氧化酶,提高传感器的灵敏度和增加线性范围。
本发明是通过如下技术方案实现的:
一种基于纳米多孔金属膜的葡萄糖电化学微电极传感器,包括:
聚酰亚胺衬底;
所述衬底上的纳米多孔金属膜;所述多孔金属膜的厚度为50-200nm;所述多孔金属膜的空隙为10-100nm;
所述多孔金属膜之上的修饰层及衬底上的修饰层;
所述衬底分a和b两面,a面制备多孔金属膜,金属膜孔隙内填充固定葡萄糖氧化酶后制成酶电极为传感器工作电极;多孔金属膜工作电极修饰层从内到外为酶膜传感层,限制扩散层,抗干扰亲水层;b面涂覆银/氯化银为对电极-参比电极,组成两电极电化学葡萄糖传感器。
一种基于纳米多孔金属膜的葡萄糖电化学微电极传感器,包括:
聚酰亚胺衬底;
所述衬底上的纳米多孔金属膜;所述多孔金属膜的厚度为50-200nm;所述多孔金属膜的空隙为10-100nm;
所述多孔金属膜之上的修饰层及衬底上的修饰层;
所述衬底分a和b两面,a面制备多孔金属膜,金属膜孔隙内填充固定葡萄糖氧化酶后制成酶电极为传感器工作电极;多孔金属膜工作电极修饰层从内到外为酶膜传感层,限制扩散层,抗干扰亲水层;涂覆银/氯化银的b面为参比电极,铂丝为对电极,组成三电极电化学葡萄糖传感体系。
所述聚酰亚胺衬底的厚度为0.5mm。
多孔膜的金属是金、铂、铱、铼、钨、钽、铪、银、钯、铑、钌和钛中的任意一种。
所述多孔金属膜工作电极修饰层还包括催化层,所述催化层设置在酶膜传感层和金属孔内壁之间。
所述催化层由铂纳米颗粒、铂黑、二茂铁或普鲁士蓝组成,通过电化学沉积的方法制备。
所述限制扩散层由nafion、聚氨酯、聚乙烯醇、聚碳酸酯或聚氯乙烯组成,通过浸泡或者滴涂方法制备。
所述抗干扰亲水层由nafion、聚乙烯醇、壳聚糖、改性壳聚糖、聚乙二醇或者低聚寡糖组成,通过浸泡或者滴涂方法制备。
1.本发明首选提供了一种多孔金属膜,其包括:
聚酰亚胺衬底;
所述衬底上的多孔金属膜;
所述多孔金属膜的厚度为50-200nm;
所述多孔金属膜的空隙为10-100nm;
适用的金属导电性好,化学性质稳定,室温不易氧化、生物相容性好等特点,可以是金、铂、铱、铼、钨、钽、铪、银、钯、铑、钌、钛中的任意一种,或由它们组成的合金;
多孔金属膜的支撑衬底聚酰亚胺衬底厚度可选0.05-1mm,优选0.5mm;
2.本发明提供了一种多孔金属膜的制备方法:
在聚酰亚胺衬底上,采用双靶磁控共溅射,沉积不同厚度、不同比例的金属和金属氧化物(如mgo、cao)混合物膜,经去离子水或弱酸溶液浸泡,使金属氧化物去除,留下三维多孔金属层。
优选的,磁控溅射金属与金属氧化物靶材为2吋标准尺寸,纯度99.999%;
优选的,磁控溅射衬底加热温度200℃;
优选的,金属和金属氧化物使用射频溅射电源;
磁控溅射气压为3-10毫托,优选5毫托,衬底转速10-30转/分钟,优选20转/分钟;
所述不同比例的金属和金属氧化物,其中金属氧化物所占比例可为:15%、30%、45%、60%、70%、80%,优选70%,金属氧化物占比越大,所制备金属膜的孔隙孔径越大,孔径从10-100nm可调。
所述金属和金属氧化物混合物膜不同厚度,可选50-200nm,优选100nm;
所述金属和金属氧化物混合物膜不同厚度,可选50-200nm,优选100nm;
所述溶液清洗持续时间10-60分钟,优选30分钟,反复三次;
3.基于多孔金属膜,本发明构建了一种微电极葡萄糖传感器,其包括:
聚酰亚胺衬底;
衬底上的多孔金属膜;
多孔金属膜之上的修饰层及衬底上的修饰层;
所述衬底分a和b两面,a面按照权利要求4和5制备多孔金属膜,金属膜孔隙内填充固定葡萄糖氧化酶后制成酶电极为传感器工作电极;b面涂覆银/氯化银为对电极-参比电极,组成两电极电化学葡萄糖传感器。
所述固定葡萄糖氧化酶的多孔金属面a面为工作电极,涂覆银/氯化银的b面为参比电极,铂丝为对电极,组成三电极电化学葡萄糖传感体系。
所述多孔金属膜工作电极修饰层从内到外为酶膜传感层,限制扩散层,抗干扰亲水层,可选设置催化层。
所述酶膜传感层包含:葡萄糖氧化酶、戊二醛交联剂,牛血清蛋白,可选纳米金、纳米铂、碳纳米管等纳米颗粒组分,通过滴涂或者浸泡或者喷涂方式固定god于金膜的孔隙内。
所述催化层设置在酶膜传感层和金之间,可选纳米铂等贵金属纳米颗粒、铂黑、二茂铁和普鲁士蓝等为代表的电子媒介体等,通过电化学沉积的方法制备。
所述限制扩散层可选聚氨酯、聚乙烯醇、聚碳酸酯或聚氯乙烯中的任意一种,通过浸泡或者滴涂方法制备。
所述抗干扰亲水层可选聚乙烯醇、壳聚糖或者改性壳聚糖、聚乙二醇或者低聚寡糖中的任意一种。
所述衬底b面的对电极-参比电极,包含银金属、氯化银、限制扩散层和抗干扰亲水层。银/氯化银利用磁控溅射法镀一层银,进行氯化形成后得到或者或者直接涂覆ag/agcl浆得到。
4.本发明提供了一种基于多孔金属膜的微电极葡萄糖传感器的制备方法和步骤,主要包括:
(1)清洁衬底并干燥:分别用乙醇和异丙醇超声清洗10分钟,氮气吹干;可选氧等离子体处理,增加衬底表面的亲水性,镀膜厚度更均匀,粗糙度更小;
(2)制备多孔金属膜:在清洁衬底上,磁控共溅射不同比例,不同厚度的金属和氧化镁混合膜,去离子水中清洗理,形成多孔金属膜;
(3)制备银/氯化银电极,首先在衬底多孔金属膜相反的一面,利用蒸镀或者磁控溅射一层50-200nm银金属,利用银浆或者焊接技术分别引出两侧金属面的导线,利用以下方法之一制得银/氯化银电极:
恒电流电镀技术,银金属膜为阳极,多孔金属膜为阴极,电流为0.1-0.3ma,浸渍在0.1mol/l盐酸溶液中,氯化2-6个小时,去离子水清洗;
采用恒电压法电镀,银金属膜为阳极,多孔金属膜为阴极,在电极两侧施加5v直流电压,电解液为0.1mol/l盐酸溶液,持续10-30分钟,去离子水清洗;
(4)多孔金属膜修饰催化层:在酶膜层和金属孔内壁之间的催化层,可选铂纳米颗粒、普鲁士蓝等,通过以下任一方法制备:
在氯铂酸溶液中直接恒电位法电沉积pt纳米颗粒:以多孔金膜电极为工作电极,铂丝为对电极,ag/agcl为参比电极,连接到电化学工作站,将电极浸入h2ptcl6溶液中,在-0.25v电位下,采用恒电位法沉积铂纳米颗粒,沉积时间120s,去离子水冲洗后在0.5mol/lh2so4溶液中扫描至稳定;
循环伏安法电沉积pt纳米颗粒:0.5-5.0mmol/l的hptcl4溶液中,于1.5-0.3v范围内,以扫速50-150mv/s循环伏安扫描5-50圈,一步法沉积pt纳米颗粒;
两步法循环伏安法电沉积pt纳米颗粒:将多孔金膜电极置于k2so4溶液中进行循环伏安法扫描,表面活化表面。将活化后的电极置于2mk2ptcl4和0.1mk2so4的混合溶液中进行循环伏安法扫描,所得电极置于h2so4溶液中进行循环伏安法扫描,使铂的配合物转化为铂纳米颗粒。
首先制备铂纳米溶胶然后通过浸泡吸附:将129.4毫克氯铂酸溶于91.5ml水中,将5mg聚乙烯吡咯烷酮(pvp)溶于5ml水后,两溶液混合后,边搅拌边缓慢加入1ml0.1mol/l硼氢化钠,所得混合液室温下静置24小时;将金膜电极浸入0.1wt%的十八烷基三甲基氯化铵(stac)溶液中,静置5秒后取出晾干,然后置于铂纳米溶胶中30分钟,静电吸附一层铂纳米颗粒催化层,取出后用去离子水冲洗,去除表面未固定化的铂纳米颗粒,晾干;
电沉积普鲁士蓝:以多孔金属膜的一面为工作电极,ag/agcl面为参比电极,pt丝为对电极,在含有kcl、k3[fe(cn)6]、fecl3和hcl的混合电解液中进行电化学沉积,使用恒定电压0.4v,沉积时间10-30s,获得普鲁士蓝修饰的多孔金属膜电极,
(5)固定葡糖糖氧化酶于工作电极:采用经典的化学交联的方法,以戊二醛(ga)为交联剂,将葡萄糖氧化酶(god)与牛血清蛋白(bsa)配制成氧化酶混合液,充分均匀混合后,滴涂到电极表面,4℃干燥,用去离子水冲洗为固定氧化酶,重复滴涂和冲洗,反复1-4次,干燥待用;
(6)微电极的工作电极和参比电极涂覆限制扩散层和抗干扰亲水层:限制扩散层聚合物可选nafion、聚氨酯、聚乙烯醇、聚碳酸酯或聚氯乙烯中的任意一种,通过浸泡或者滴涂方法制备。抗干扰亲水层可选nafion、聚乙烯醇、壳聚糖或者改性壳聚糖、聚乙二醇或者低聚寡糖中的任意一种,通过浸泡或者滴涂方法制备。
(7)采用激光切割,批量裁剪镀膜衬底成微电极所需尺寸。
与现有技术相比,本发明具有如下有益效果:
(1)多孔三维的金属膜提供了高比表面积的活性界面,可以作为进一步修饰的支撑基底,god负载量大大增加,进而使得制备的葡糖糖具有较宽的响应范围(0.025mmol/l-25.5mmol/l)和高灵敏度(8.20μa/mm);
(2)多孔金属膜既作为修饰层的支撑层,同时也是传感器的导电层,金属的良好导电性质,可以使电荷快速转移和传输;
(3)god深入多孔金属膜的孔隙中,对酶具有一定的保护作用,纳米尺寸的金属框架对检测的中间产物过氧化氢具有一定的催化效果,可以放大电流信号;
(4)多孔金属膜的制备无需模板,且方法适用范围广,本专利列举的金、铂、铱、铼、钨、钽、铪、银、钯、铑、钌、钛的金属或其合金都可以;
(5)多孔金属膜的制备可以通过调节共溅射mgo或cao的比例而对其孔隙孔径、密度进行调节,除负载god外,还可以负载不同尺寸的纳米颗粒等修饰物;
(6)传感器的工作电极和参比电极-对电极集成在单一微电极的两个表面,在植入时,可以减少创伤;
(7)本发明选用的衬底具有良好的刚性和韧性,植入时,不容易断裂,不需要另外附加导针;
(8)本发明的微电极葡萄糖电化学传感器制作方法镀膜简单易行,重复性好,可大规模批量制备,具有极大的应用价值和前景。
附图说明
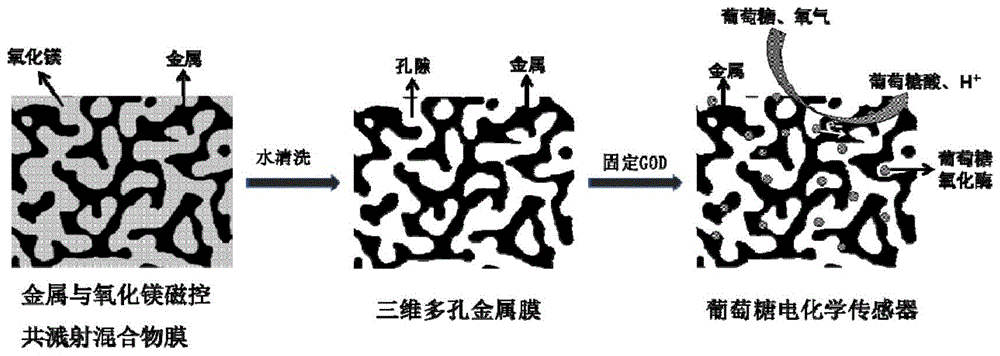
图1为多孔金属膜制备和固定葡萄糖氧化酶制备葡萄糖传感器的示意图;
图2为修饰普鲁士蓝、god酶层和nafion膜后多孔金膜电极的电子扫描显微镜图片;
图3为普鲁士蓝修饰多孔金god电极对不同葡萄糖浓度响应的计时电流曲线,在20mlph7.0磷酸缓冲液中测试,测试电位+0.6v,电磁搅拌,室温,箭头标注表示单次加样后葡萄糖总浓度。
图4为普鲁士蓝修饰多孔金葡萄糖生物传感器的工作曲线(n=5,rsd=3.2~4.7%)。插图为工作曲线线性拟合:线性范围:0.025–2.15mmol/l。
图5为普鲁士蓝修饰多孔金葡萄糖生物传感器对1mmol/l葡萄糖、0.1mmol/l抗坏血酸(aa)、0.5mmol/l尿酸(ua)和0.1mmol/l醋氨酚(ap)的时间电流响应。(+0.6vvs.ag/agcl;0.1mpbs,ph7.0)
图6为普鲁士蓝修饰多孔金葡萄糖生物传感器在45天内对1mmol/葡萄糖的响应电流(n=5),误差棒表示标准差。在20mlph7.0磷酸缓冲液中测试,+0.6vvs.ag/agcl;电磁搅拌,室温。
具体实施方式
为便于理解本发明,本发明列举实施例如下。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
实施例1
一种制备多孔金膜微电极的方法,以聚酰亚胺为衬底,磁控共溅射金和氧化镁,乙酸水溶液清洗去除mgo,得到多孔金膜表面,具体操作步骤如下:
(1)取商用聚酰亚胺衬底,长、宽、厚分别为8mm、2mm、0.5mm,用氧等离子体处理30min后,分别用水、乙醇和异丙醇清洗,氮气吹干后,待用;
(2)磁控共溅射金和mgo,金与氧化镁靶材纯度99.999%,2吋大小,磁控溅射时,压力5毫托,衬底转速20转/分钟,衬底加热至200℃。
(3)氧化镁使用150w,金使用不同功率得到不同比例的共溅射膜:
(4)所得镀膜与衬底置于去离子水中,浸泡30分钟后,更换去离子水,重新浸泡,进行三次此过程,取出氮气吹干待用;
(5)在衬底背面,采用磁控溅射镀金属银膜,厚度100nm,溅射过程中,衬底加热200℃,使银金属膜贴附衬底更加牢固;
(6)采用金线球焊技术,在多孔金和银金属表面引出两根金线电极,距离衬底末端1毫米;
(7)以银金属膜为阳极,金膜为阴极,两端施加0.25ma的直流电流,电解液为0.1mol/l盐酸,氯化5个小时后,用去离子水清洗3遍;
(8)所得一面为多孔金表面,另一面为银/氯化银表面的微电极。
实施例2
本发明第二实施例是基于第一实施例多孔金膜微电极制备的基础上,提供一种葡萄糖电化学生物传感器,具体操作步骤如下:
(1)选取溅射70%氧化镁比例,总厚度为100nm的样品进行此实施例,此条件下,孔隙孔径在20-100nm范围;
(2)在多孔金膜孔隙内修饰一层普鲁士蓝,方法为:
将微电极先浸入体积比为1:3:4的浓hno3:hcl:h2o溶液3分钟,用去离子水彻底清洗电极表面后,用乙醇和去离子水再反复清洗,氮气吹干;
以多孔金膜的一面为工作电极,ag/agcl面为参比电极,pt丝为对电极,连接电化学工作站,在含有0.1mol/lkcl、2.5mmol/lk3[fe(cn)6]、2.5mmol/lfecl3和hcl的混合电解液中进行电化学沉积,0.1mol/lhcl用来调节电解液ph至1.0-2.5之间,使用恒定电压0.4v,沉积时间10s,获得普鲁士蓝修饰的多孔金膜电极,普鲁士蓝成球形,厚度约15nm;
所得普鲁士蓝修饰电极在0.1mol/lhcl和0.1mol/lkcl混合液中进行活化,使用-50-350mv的电压循环伏安扫描,扫速50mv/s,循环50次;再在含有0.1mol/lkcl的0.1mol/lph6.8磷酸缓冲液中,使用-50mv的恒电位极化100s,去离子水冲洗,氮气吹干后,置于90℃的烘箱中,烘烤1小时,使修饰微电极完全干燥,待用;
(3)采用化学交联法固定葡糖糖氧化酶于普鲁士蓝修饰多孔金膜电极,方法步骤为:
用0.1mol/l磷酸缓冲液(ph7.0)配置4mg/mlgod酶液和4mg/ml牛血清蛋白溶液,取等体积两种溶液混合后,超声分散10分钟,取2-4μl所得混合液小心滴涂于普鲁士蓝修饰多孔金膜电极表面,晾干后,在酶膜表面滴涂1.5-4%(v/v)的戊二醛溶液进行交联固定30分钟,交联温度为35℃水浴。用0.1mol/l磷酸缓冲液反复冲洗电极表面,重新进行滴涂god和戊二醛的步骤2-4次,4℃晾干后,所得为固定葡萄糖氧化酶的多孔金膜工作电极。
(4)nafion上富含大量的亲水性磺酸基团,具有较好的水溶性,而且nafion膜也具有较好的阳离子选择性和生物相容性,本实施例中选择在微电极的工作电极和参比电极表面修饰一层nafion膜增加传感器的亲水性和抗干扰能力,以10:1的比例混合0.1mol/l磷酸缓冲液和5%nafion乙醇溶液配制稀释nafion溶液;取2-4μl上述nafion溶液滴涂与电极两侧,空气中干燥30分钟。
(5)所有电极测试前均置于0.1mol/lpbs(ph7.0)中在0-1.0v电压下扫描直至获得稳定的伏安图,测试后在0.1mol/lpbs(ph7.0)中,0-1.0v电压下循环伏安扫描20圈(扫描速率50mv/s)进行重建,电极闲置时,保持于4℃恒定湿度条件下,修饰表面水平向上,用烧杯扣罩防尘。
(6)多孔金膜葡萄糖电化学微电极传感器对不同浓度葡萄糖的响应。
采用常规的三电极测试系统,以构建的多孔金膜微电极为工作电极,以ag/agcl为参比电极,铂丝(直径1mm)为对电极,20mlpbs(ph7.0)缓冲液为电解液,在电极电位+0.6vvs.ag/agcl下测定酶电极对葡萄糖的响应电流,并在0~+0.6v电压下对酶电极进行循环伏安扫描。电流测量时利用磁力搅拌器缓慢搅拌,以使葡萄糖分子在缓冲液中均匀扩散。所有测试均在室温下进行。
葡萄糖溶液用去离子水配制,加入几滴0.1mol/lhcl调节ph至酸性,防止微生物生长,新配的葡萄糖溶液静置过夜以使α-葡萄糖充分转化为god的底物β-葡萄糖。
多孔金膜葡萄糖电化学微电极传感器对逐渐增加的葡萄糖浓度均产生了一定的电流响应,葡萄糖浓度依次为0.025、0.05、0.1、0.15、0.2、0.25、0.35、0.45、0.55、0.65、0.8、0.9、1.0、1.2、1.4、1.65、1.9、2.2、2.65、3.2、3.8、4.2、4.6、5.2、6.2、7.2、8.2、9.2、10.4、12.9、15.5、20.5、25.5mmol/l。
所述的修饰多孔金膜电极对葡萄糖具有快速灵敏的响应,达到最大响应电流95%的时间≤8s,说明h2o2在修饰薄膜中很容易扩散,葡萄糖浓度为0.025mm~2.15mm之间时符合线性方程:i(μa)=0.79525+8.19829c(mmol/l),相关系数为0.9983(rsd=3.2~4.7%,n=5),从公式中得到传感器的灵敏度为8.20μa/mm,检测限为8.2mol/l(s/n=3)。
(7)多孔金膜葡萄糖电化学微电极传感器抗干扰性能测试。
加入生理浓度的干扰物,普鲁士蓝修饰多孔金葡萄糖生物传感器对1mmol/l葡萄糖、0.1mmol/l抗坏血酸(aa)、0.5mmol/l尿酸(ua)和0.1mmol/l醋氨酚(ap)的时间电流响应显示电极具有良好的抗干扰能力,干扰物产生的电流对于葡萄糖的检测基本不会产生影响。
(8)多孔金膜葡萄糖电化学微电极传感器稳定性测试。
连续在45天时间内测定多孔金膜葡萄糖电化学微电极对1mmol/l葡萄糖的响应电流,电流随时间变化下降缓慢,45天后葡萄糖生物传感器响应电流相对于最大响应电流只下降了15.7%,表明金膜和金膜修饰物具有良好的亲水性和生物相容性,对酶起到保护作用,有利于酶活性的保持,使得电极具有良好的稳定性。
申请人声明,尽管本发明通过上述实施例详细说明了本发明的工艺设备和工艺流程,但本发明并不局限于上述详细工艺设备和工艺流程,即不意味着本发明必须依赖上述详细工艺设备和工艺流程才能实施,上述描述不应被认为是对本发明的限制。所属技术领域的技术人员阅读了上述内容后,对本发明的任何改进,修改和替代都将是显而易见的。因此,本发明的保护范围应由所附的权利要求来限定。
- 还没有人留言评论。精彩留言会获得点赞!