用于检测农药残留的MRM母子离子对的三重四极杆质谱仪的制作方法
本申请要求2018年1月23日提交的序列号62/620,961和2018年3月1日提交的序列号62/637,350的优先权,并通过引用将其整体并入本文。
本公开中所引用的每一篇参考文献均通过引用整体并入本文。
本公开总体上涉及使用质谱检测和/或定量农药的系统和方法。
背景技术:
质谱(ms)是用于确定未知样品物质的元素组成的分析技术,并且具有定量和定性应用。例如,ms可用于鉴定未知化合物、确定分子中元素的同位素组成,以及通过观察其裂解来确定特定化合物的结构,以及定量样品中特定化合物的量。质谱仪通常通过电离测试样品以形成带正电粒子的离子流来进行操作。然后,对离子流进行质量分化(在时间或空间上),以根据质荷比(m/z)来分离离子流中不同的粒子群。下游质量分析器可以检测质量分化的离子群的强度,以便计算感兴趣的分析数据,例如,不同离子群的相对浓度、产物或碎片离子的质荷比以及其他可能有用的分析数据。
感兴趣的离子(“分析物离子”)可以与和分析物离子具有基本相同的标称m/z比的其他不想要的离子群(“干扰离子”)在离子流中共存。在一些情况下,干扰离子的m/z比足够接近分析物离子的m/z比,以致于低于质量分析器的分辨率极限,因此无法区分分析物离子和干扰离子。提高质量分析器的分辨率是处理此类干扰(通常称为“同质异位素(isobaric)”或“光谱干扰”)的一种方法。但是,较高分辨率的质量分析器往往具有较低的提取速率和较高的离子信号损失,因此需要更灵敏的检测器。也可能会遇到可实现的分辨率的限制。
此外,某些样品(诸如大麻样品)中的农药分析受到基质干扰的阻碍。大麻含有不同类别的化合物诸如大麻素、萜烯、碳氢化合物、糖、脂肪酸、类黄酮等,这些化合物的存在导致可变的信号离子抑制和基质干扰,特别是因为农药水平与高浓度自然产生的大麻素和萜烯水平之间的巨大差异。
需要用于检测和定量农药的改进的系统和方法。
附图说明
图1a和图1b是用于检测和/或定量一组农药的过程的框图。
图2是使用空气作为雾化气体的大气化学电离(apci),通过串联质谱检测和/或定量农药的过程的框图。
图3是液相色谱和串联质谱系统的示意图。
图4是云计算环境的实例的框图。
图5是示例计算设备和示例移动计算设备的框图。
图6a-图6b是示出阿维菌素(abamectin)信号作为hsid(热表面诱导的去溶剂化)温度(图6a)和源温度(图6b)的函数的图。
图7a-图7d是使用385.2>189(图7a,7c)或385.2>343.1(图7b,7d)的多反应监测(mrm)母子离子对(transition)分析大麻样品中灭螨醌(acequin℃yl)的存在的色谱图。图7a和7b,包含100ppb(十亿分之一)灭螨醌的大麻样品。图7c和7d,空白大麻样品。nd,未检测到。s/n,信噪比。
图8是灭螨醌的前体(母体)离子质量扫描。
图9a-图9d是使用402.2>189(图9a,9c)或402.2>343.1(图9b,9d)的mrm母子离子对分析大麻样品中灭螨醌的存在的色谱图。图9a和9b,包含100ppb灭螨醌的大麻样品。图9c和9d,空白大麻样品。
图10a是阿维菌素的前体(母体)离子质量扫描。图10b-图10e是使用890.5>567.2(图10b,10d)或890.5>305.1(图10c,10e)的mrm母子离子对分析大麻样品中阿维菌素的存在的色谱图。图10b和图10c,包含100ppb阿维菌素的大麻样品。图10d和图10e,空白大麻样品。
图11a-图11d是包含100ppb涕灭威(aldicarb)的大麻样品并使用208>89(图11a)、208>116(图11b)、116>70(图11c)和116>89(图11d)的mrm母子离子对分析涕灭威的存在的色谱图。
图12a-图12b是使用163.1>88的mrm母子离子对分析大麻样品中灭多威(methomyl)的存在的色谱图。图12a,包含100ppb灭多威的大麻样品。图12b,空白大麻样品。
图13a-图13b是使用316.9>263.9的mrm母子离子对分析大麻样品中克菌丹(captan)的存在的色谱图。图13a,包含1000ppb克菌丹的大麻样品。图13b,空白大麻样品。
图14a是溴虫腈(chlorfenapyr)的前体(母体)离子质量扫描。
图14b-图14e是示出使用不同的mrm母子离子对获得的溴虫腈的铵([m+nh4]+)加合物的信号振幅的色谱图。图14b,426>59;图14c,426>271;图14d,426>376;图14e,426>409。
图14f-图14i是示出使用不同的mrm母子离子对获得的质子化溴虫腈([m+h]+)的信号振幅的色谱图。图14f,409>41;图14g,409>59;图14h,409>271;图14i,409>379。
图14j-图14k是包含100ppb溴虫腈的大麻样品且使用mrm母子离子对409>271(图14j)和409>379(图14k)获得的色谱图。
图14l-图14n是包含100ppb溴虫腈的大麻样品且使用mrm母子离子对409>59(图14l)、426>59(图14m)和426>409(图14n)获得的色谱图。
图15a-图15b是使用mrm母子离子对409.1>186(图15a)和409.1>206(图15b)分析大麻样品中肟菌酯(trifloxystrobin)的存在的色谱图。图15c是使用mrm母子离子对409.1>59分析肟菌酯和溴虫腈的存在的色谱图。
图16a是示出二溴磷(naled,也称“dibrom”或“dibrom”)的同位素分布的图。图16b是包含二溴磷的样品的前体(母体)质量扫描。图16c-图16f是包含100ppb二溴磷的大麻样品且使用mrm母子离子对380.8>127(图16c)、378.8>127(图16d)、380.8>109(图16e)和378.8>127(图16f)分析二溴磷的存在的色谱图。
图17a和图17b是显示丁酰肼(daminozide)的产物离子扫描的图。图17a,高碰撞能量(ce)=-30v。图17b,低ce=-15v。
图17c-图17e是包含100ppb丁酰肼的大麻样品且使用161.1>44(图17c)、161.1>101(图17d)和161.1>143(图17e)的mrm母子离子对分析丁酰肼的存在的色谱图。
图18a-图18b是使用mrm母子离子对184>143分析大麻样品中乙酰甲胺磷(acephate)的存在的色谱图。图18a,包含100ppb乙酰甲胺磷的大麻样品。图18b,空白大麻样品。
图19a-图19b是使用mrm母子离子对297>41分析大麻样品中抑霉唑(imazalil)的存在的色谱图。图19a,包含100ppb抑霉唑的大麻样品。图19b是空白大麻样品。
图20a和图20b是n-辛基双环庚烯二甲酰亚胺(mgk-264)的产物离子扫描。图20a,低ce=-25v。图20b,高ce=-50v。
图20c-图20e是包含100ppbmgk-264的大麻样品且使用mrm母子离子对276.2>98(图20c)、276.2>121(图20d)和276.2>210(图20e)分析mgk-264的存在的色谱图。
图21a-图21d是使用mrm母子离子对361.2>213(图21a,21c)和361.2>107(图21b,21d)分析大麻样品中瓜菊酯ii(cinerinii)的存在的色谱图。图21a和21b是包含1000ppb瓜菊酯ii的大麻样品。图21c和21d是空白大麻样品。
图22a-图22b是使用mrm母子离子对317.2>149分析大麻样品中瓜菊酯i的存在的色谱图。图22a,包含1000ppb瓜菊酯i的大麻样品。图22b,空白大麻样品。
图23a-图23f是使用mrm母子离子对302.1>88(图23a,23c)、302.1>256(图23b,23d)和302.1>116(图23e,23f)分析大麻样品中苯氧威(fenoxycarb)的存在的色谱图。图23a、23b和23e,包含100ppb苯氧威的大麻样品。图23c、23d和23e,空白大麻样品。
图24a-图24f是使用mrm母子离子对388.1>165(图24a,24d)、388.1>273(图24b,24e)和388.1>301(图24c,24f)分析大麻样品中烯酰吗啉(dimethomorph)的存在的色谱图。图24a、24b和24c是包含100ppb烯酰吗啉的大麻样品。图24d、24e和24f是空白大麻样品。
图25a-图25b是使用mrm母子离子对302.1>55分析大麻样品中环酰菌胺(fenhexamid)的存在的色谱图。图25a,包含100ppb环酰菌胺的大麻样品。图25b,空白大麻样品。
图26a-图26b是使用mrm母子离子对748.5>98分析大麻样品中乙基多杀菌素(spinetoram)的存在的色谱图。图26a是包含100ppb乙基多杀菌素的大麻样品。图26b是空白大麻样品。
图27a-图27c是总离子色谱图(tic)。图27a,使用通用液相色谱梯度(固定梯度率)获得的空白大麻样品的tic。图27b,包含100ppb农药的大麻样品的tic。图27c,使用实施例1中所述的条件获得的空白大麻样品的tic。另请参见实施例2。
图27d是示出各种类型的液相色谱(lc)柱的vandeemter曲线的图。
图27e和27f是示出流速对嘧菌酯(azoxystrobin)信号的影响的图。
图28a-图28c是包含100ppb马拉硫磷(malathion)的大麻样品且使用mrm母子离子对331>99(图28a)、331>285(图28b)和331>127(图28c)分析马拉硫磷的存在的色谱图。
图29a是使用2.1mm内径(id)lc柱分析大麻样品中螺环菌胺(spiroxamine)的存在的色谱图。图29b是使用4.6mmid柱分析大麻样品中螺环菌胺的存在的色谱图。
图30a是示出对于通过使用100%甲醇洗脱溶剂的lc方法处理的样品,与灭螨醌相关的mrm母子离子对的强度随时间变化的图。图30b是示出对于通过使用75%甲醇:25%乙腈洗脱溶剂的lc方法处理的样品,与灭螨醌相关的mrm母子离子对的强度随时间变化的图。图30c是示出灭螨醌和阿维菌素的mrm母子离子对信号强度与lc方法中使用的有机洗脱溶剂的甲醇浓度百分比的函数关系图。
图31是示出大麻样品中总农药回收率的图。
图32a-图32b是在大麻基质中(图32a)和在溶剂中(图32b)的嘧菌酯的校准曲线。
图33a是五氯硝基苯(pcnb;quintozene)的前体(母体)质量扫描。图33b是示出五氯硝基苯的同位素分布的图。
图34a是氯丹(chlordane)的前体(母体)质量扫描。图34b是示出氯丹的同位素分布的图。
图35a是包含氯丹且使用采用无添加剂的流动相的lc方法处理的样品的前体(母体)质量扫描。图35b是包含氯丹且使用采用含有甲酸的流动相的lc方法处理的样品的前体(母体)质量扫描。
图36是在负离子模式下使用apci源获得的五氯硝基苯的产物离子扫描。
图37a-图37d是使用mrm母子离子对275.8>35.1(图37a,37c)和273.8>35.1(图37b,37d)分析大麻样品中五氯硝基苯的存在的色谱图。图37a和37b是包含100ppb五氯硝基苯的大麻样品。图37c和37d是空白大麻样品。
图38a-图38d是使用mrm母子离子对439.8>35.1(图38a,38c)和441.8>35.1(图38b,38d)分析大麻样品中氯丹的存在的色谱图。图38a和38b是包含100ppb氯丹的大麻样品。图38c和38d是空白大麻样品。
图39是示出在负离子模式下使用apci源获得的背景光谱的图。
图40a是示出基于定量剂/定性剂mrm母子离子对两者的灵敏度计算的72种农药的定量限(loq)的图。图40b是示出仅基于定量剂mrm母子离子对的灵敏度计算的72种农药的loq的图。
图41a-图41d是使用mrm母子离子对161.1>143(图41a,41c)和161.1>44(图41b,41d)分析大麻样品中丁酰肼的存在的色谱图。图41a和41b是包含100ppb丁酰肼的大麻样品。图41c和41d是空白大麻样品。
图42a-图42d是使用mrm母子离子对237.1>72(图42a,42c)和237.1>90(图42b,42d)分析大麻样品中草氨酰(oxamyl)的存在的色谱图。图42a和42b是包含100ppb草氨酰的大麻样品。图42c和42d是空白大麻样品。
图43a-图43d是使用mrm母子离子对230.1>203(图43a,43c)和230.1>174(图43b,43d)分析大麻样品中氟啶虫酰胺(flonicamid)的存在的色谱图。图43a和43b是包含100ppb氟啶虫酰胺的大麻样品。图43c和43d是空白大麻样品。
图44a-图44d是使用mrm母子离子对184>143(图44a,44c)和184>49(图44b,44d)分析大麻样品中乙酰甲胺磷的存在的色谱图。图44a和44b是包含100ppb乙酰甲胺磷的大麻样品。图44c和44d是空白大麻样品。
图45a-图45d是使用mrm母子离子对163.1>88(图45a,45c)和163.1>106(图45b,45d)分析大麻样品中灭多威的存在的色谱图。图45a和45b是包含100ppb灭多威的大麻样品。图45c和45d是空白大麻样品。
图46a-图46d是使用mrm母子离子对292>211(图46a,46c)和292>181(图46b,46d)分析大麻样品中噻虫嗪(thiamethoxam)的存在的色谱图。图46a和46b是包含100ppb噻虫嗪的大麻样品。图46c和46d是空白大麻样品。
图47a-图47d是使用mrm母子离子对256.1>209(图47a,47c)和256.1>175(图47b,47d)分析大麻样品中吡虫啉(imidacloprid)的存在的色谱图。图47a和47b是包含100ppb吡虫啉的大麻样品。图47c和47d是空白大麻样品。
图48a-图48d是使用mrm母子离子对230>125(图48a,48c)和230>199(图48b,48d)分析大麻样品中乐果(dimethoate)的存在的色谱图。图48a和48b是包含100ppb乐果的大麻样品。图48c和48d是空白大麻样品。
图49a-图49d是使用mrm母子离子对225>127(图49a,49c)和225>109(图49b,49d)分析大麻样品中速灭磷(mevinphos)的存在的色谱图。图49a和49b是包含100ppb速灭磷的大麻样品。图49c和49d是空白大麻样品。
图50a-图50d是使用mrm母子离子对223.1>99(图50a,50c)和223.1>126(图50b,50d)分析大麻样品中啶虫脒(acetamiprid)的存在的色谱图。图50a和50b是包含100ppb啶虫脒的大麻样品。图50c和50d是空白大麻样品。
图51a-图51d是使用mrm母子离子对253>126(图51a,51c)和253>90(图51b,51d)分析大麻样品中噻虫啉(thiacloprid)的存在的色谱图。图51a和51b是包含100ppb噻虫啉的大麻样品。图51c和51d是空白大麻样品。
图52a-图52b是使用mrm母子离子对297>159分析大麻样品中抑霉唑的存在的色谱图。图52a是包含100ppb抑霉唑的大麻样品。图52b是空白大麻样品。
图53a-图53d是使用mrm母子离子对343.1>151(图53a,53c)和343.1>268(图53b,53d)分析大麻样品中甲基硫菌灵(thiophanate-methyl)的存在的色谱图。图53a和53b是包含100ppb甲基硫菌灵的大麻样品。图53c和53d是空白大麻样品。
图54a-图54d是使用mrm母子离子对208>89(图54a,54c)和208>116(图54b,54d)分析大麻样品中涕灭威的存在的色谱图。图54a和54b是包含100ppb涕灭威的大麻样品。图54c和54d是空白大麻样品。
图55a-图55d是使用mrm母子离子对210.1>168(图55a,55c)和210.1>111(图55b,55d)分析大麻样品中残杀威(propoxur)的存在的色谱图。图55a和55b是包含100ppb残杀威的大麻样品。图55c和55d是空白大麻样品。
图56a-图56d是使用mrm母子离子对220.9>109(图56a,56c)和220.9>127(图56b,56d)分析大麻样品中敌敌畏(dichlorvos)的存在的色谱图。图56a和56b是包含100ppb敌敌畏的大麻样品。图56c和56d是空白大麻样品。
图57a-图57d是使用mrm母子离子对222.1>123(图57a,57c)和222.1>165(图57b,57d)分析大麻样品中加保扶(carbofuran)的存在的色谱图。图57a和57b是包含100ppb加保扶的大麻样品。图57c和57d是空白大麻样品。
图58a-图58d是使用mrm母子离子对202.1>127(图58a,58c)和202.1>145(图58b,58d)分析大麻样品中甲萘威(carbaryl)的存在的色谱图。图58a和58b是包含100ppb甲萘威的大麻样品。图58c和58d是空白大麻样品。
图59a-图59d是使用mrm母子离子对298.3>100.1(图59a,59c)和298.3>144.1(图59b,59d)分析大麻样品中螺环菌胺的存在的色谱图。图59a和59b是包含100ppb螺环菌胺的大麻样品。图59c和59d是空白大麻样品。
图60a-图60d是使用mrm母子离子对380.8>109(图60a,60c)和380.8>127(图60b,60d)分析大麻样品中二溴磷(naled/”dibrom”)的存在的色谱图。图60a和60b是包含100ppb二溴磷的大麻样品。图60c和60d是空白大麻样品。
图61a-图61d是使用mrm母子离子对280.2>192.1(图61a,61c)和280.2>248.1(图61b,61d)分析大麻样品中甲霜灵(metalaxyl)的存在的色谱图。图61a和61b是包含100ppb甲霜灵的大麻样品。图61c和61d是空白大麻样品。
图62a-图62d是使用mrm母子离子对484>285.9(图62a,62c)和484>452.9(图62b,62d)分析大麻样品中氯虫酰胺(chlorantraniliprole)的存在的色谱图。图62a和62b是包含100ppb氯虫酰胺的大麻样品。图62c和62d是空白大麻样品。
图63a-图63d是使用mrm母子离子对318>133(图63a,63c)和318>160(图63b,63d)分析大麻样品中亚胺硫磷(phosmet)的存在的色谱图。图63a和63b是包含100ppb亚胺硫磷的大麻样品。图63c和63d是空白大麻样品。
图64a-图64d是使用mrm母子离子对264>124.9(图64a,64c)和264>231.9(图64b,64d)分析大麻样品中甲基对硫磷(methylparathion)的存在的色谱图。图64a和64b是包含100ppb甲基对硫磷的大麻样品。图64c和64d是空白大麻样品。
图65a-图65d是使用mrm母子离子对404.1>344(图65a,65c)和404.1>372(图65b,65d)分析大麻样品中嘧菌酯的存在的色谱图。图65a和65b是包含100ppb嘧菌酯的大麻样品。图65c和65d是空白大麻样品。
图66a-图66d是使用mrm母子离子对226.1>121(图66a,66c)和226.1>169(图66b,66d)分析大麻样品中甲硫威(methi℃arb)的存在的色谱图。图66a和66b是包含100ppb甲硫威的大麻样品。图66c和66d是空白大麻样品。
图67a-图67b是使用mrm母子离子对316.9>235.9分析大麻样品中克菌丹的存在的色谱图。图67a是包含1000ppb克菌丹的大麻样品。图67b是空白大麻样品。
图68a-图68d是使用mrm母子离子对343>140(图68a,68c)和343>272(图68b,68d)分析大麻样品中啶酰菌胺(boscalid)的存在的色谱图。图68a和68b是包含100ppb啶酰菌胺的大麻样品。图68c和68d是空白大麻样品。
图69a-图69d是使用mrm母子离子对247.1>126(图69a,69c)和247.1>180(图69b,69d)分析大麻样品中咯菌腈(fludioxonil)的存在的色谱图。图69a和69b是包含100ppb咯菌腈的大麻样品。图69c和69d是空白大麻样品。
图70a-图70d是使用mrm母子离子对294.1>125(图70a,70c)和294.1>70(图70b,70d)分析大麻样品中多效唑(paclobutrazol)的存在的色谱图。图70a和70b是包含100ppb多效唑的大麻样品。图70c和70d是空白大麻样品。
图71a-图71d是使用mrm母子离子对331>285(图71a,71c)和331>127(图71b,71d)分析大麻样品中马拉硫磷的存在的色谱图。图71a和71b是包含100ppb马拉硫磷的大麻样品。图71c和71d是空白大麻样品。
图72a-图72d是使用mrm母子离子对388.1>273(图72a,72c)和388.1>301(图72b,72d)分析大麻样品中烯酰吗啉的存在的色谱图。图72a和72b是包含100ppb烯酰吗啉的大麻样品。图72c和72d是空白大麻样品。
图73a-图73d是使用mrm母子离子对289.1>70(图73a,73c)和289.1>125(图73b,73d)分析大麻样品中腈菌唑(myclobutanil)的存在的色谱图。图73a和73b是包含100ppb腈菌唑的大麻样品。图73c和73d是空白大麻样品。
图74a-图74d是使用mrm母子离子对301.1>170(图74a,74c)和301.1>198(图74b,74d)分析大麻样品中联苯肼酯(bifenazate)的存在的色谱图。图74a和74b是包含100ppb联苯肼酯的大麻样品。图74c和74d是空白大麻样品。
图75a-图75b是使用mrm母子离子对302.1>55分析大麻样品中环酰菌胺的存在的色谱图。图75a,包含100ppb环酰菌胺的大麻样品。图75b,空白大麻样品。
图76a-图76d是使用mrm母子离子对435>250(图76a,76c)和435>330(图76b,76d)分析大麻样品中氟虫腈(fipronil)的存在的色谱图。图76a和76b是包含100ppb氟虫腈的大麻样品。图76c和76d是空白大麻样品。
图77a-图77d是使用mrm母子离子对374.2>216(图77a,77c)和374.2>302.1(图77b,77d)分析大麻样品中螺虫乙酯(spirotetromat)的存在的色谱图。图77a和77b是包含100ppb螺虫乙酯的大麻样品。图77c和77d是空白大麻样品。
图78a-图78d是使用mrm母子离子对243.1>131(图78a,78c)和243.1>173(图78b,78d)分析大麻样品中灭线磷(ethoprophos)的存在的色谱图。图78a和78b是包含100ppb灭线磷的大麻样品。图78c和78d是空白大麻样品。
图79a-图79d是使用mrm母子离子对302.1>256(图79a,79c)和302.1>116(图79b,79d)分析大麻样品中苯氧威的存在的色谱图。图79a和79b是包含100ppb苯氧威的大麻样品。图79c和79d是空白大麻样品。
图80a-图80d是使用mrm母子离子对314.1>222(图80a,80c)和314.1>235(图80b,80d)分析大麻样品中醚菌酯(kresoxim-methyl)的存在的色谱图。图80a和80b是包含100ppb醚菌酯的大麻样品。图80c和80d是空白大麻样品。
图81a-图81d是使用mrm母子离子对308>70(图81a,81c)和308>125(图81b,81d)分析大麻样品中戊唑醇(tebuconazole)的存在的色谱图。图81a和81b是包含100ppb戊唑醇的大麻样品。图81c和81d是空白大麻样品。
图82a-图82d是使用mrm母子离子对305.1>97(图82a,82c)和305.1>169(图82b,82d)分析大麻样品中二嗪磷(diazinon)的存在的色谱图。图82a和82b是包含100ppb二嗪磷的大麻样品。图82c和82d是空白大麻样品。
图83a-图83d是使用mrm母子离子对732.5>98(图83a,83c)和732.5>142(图83b,83d)分析大麻样品中多杀菌素a(spinosyna)的存在的色谱图。图83a和83b是包含100ppb多杀菌素a的大麻样品。图83c和83d是空白大麻样品。
图84a-图84d是使用mrm母子离子对363>226.9(图84a,84c)和363>306.9(图84b,84d)分析大麻样品中蝇毒磷(coumaphos)的存在的色谱图。图84a和84b是包含100ppb蝇毒磷的大麻样品。图84c和84d是空白大麻样品。
图85a-图85d是使用mrm母子离子对276.2>98(图85a,85c)和276.2>210.1(图85b,85d)分析大麻样品中mgk-264的存在的色谱图。图85a和85b是包含100ppbmgk-264的大麻样品。图85c和85d是空白大麻样品。
图86a-图86d是使用mrm母子离子对303>102(图86a,86c)和303>138(图86b,86d)分析大麻样品中四螨嗪(clofentezine)的存在的色谱图。图86a和86b是包含100ppb四螨嗪的大麻样品。图86c和86d是空白大麻样品。
图87a-图87d是使用mrm母子离子对342.1>69(图87a,87c)和342.1>159(图87b,87d)分析大麻样品中丙环唑(propiconazole)的存在的色谱图。图87a和87b是包含100ppb丙环唑的大麻样品。图87c和87d是空白大麻样品。
图88a-图88d是使用mrm母子离子对301.2>132.9(图88a,88c)和301.2>168.9(图88b,88d)分析大麻样品中炔丙菊酯(prallethrin)的存在的色谱图。图88a和88b是包含100ppb炔丙菊酯的大麻样品。图88c和88d是空白大麻样品。
图89a-图89d是使用mrm母子离子对746.5>98(图89a,89c)和746.5>142(图89b,89d)分析大麻样品中多杀菌素d的存在的色谱图。图89a和89b是包含100ppb多杀菌素d的大麻样品。图89c和89d是空白大麻样品。
图90a-图90d是使用mrm母子离子对451.1>191(图90a,90c)和451.1>434(图90b,90d)分析大麻样品中氟氯氰菊酯(cyfluthrin)的存在的色谱图。图90a和90b是包含1000ppb氟氯氰菊酯的大麻样品。图90c和90d是空白大麻样品。
图91a-图91d是使用mrm母子离子对409.1>186(图91a,91c)和409.1>206(图91b,91d)分析大麻样品中肟菌酯的存在的色谱图。图91a和91b是包含100ppb肟菌酯的大麻样品。图91c和91d是空白大麻样品。
图92a-图92b是使用mrm母子离子对748.5>142分析大麻样品中乙基多杀菌素的存在的色谱图。图92a是包含100ppb乙基多杀菌素的大麻样品。图92b是空白大麻样品。
图93a-图93d是使用mrm母子离子对426>409(图93a,93c)和426>59.1(图93b,93d)分析大麻样品中溴虫腈的存在的色谱图。图93a和93b是包含1000ppb溴虫腈的大麻样品。图93c和93d是空白大麻样品。
图94a-图94d是使用mrm母子离子对433.1>127(图94a,94c)和433.1>191.1(图94b,94d)分析大麻样品中氯氰菊酯(cypermethrin)的存在的色谱图。图94a和94b是包含1000ppb氯氰菊酯的大麻样品。图94c和94d是空白大麻样品。
图95a-图95d是使用mrm母子离子对408.1>183(图95a,95c)和408.1>355(图95b,95d)分析大麻样品中氯菊酯(permethrin)的存在的色谱图。图95a和95b是包含100ppb氯菊酯的大麻样品。图95c和95d是空白大麻样品。
图96a-图96b是使用mrm母子离子对361.2>149分析大麻样品中瓜菊酯ii的存在的色谱图。图96a是包含1000ppb瓜菊酯ii的大麻样品。图96b是空白大麻样品。
图97a-图97d是使用mrm母子离子对375.2>163(图97a,97c)和375.2>213(图97b,97d)分析大麻样品中茉莉菊酯ii(jasmolinii)的存在的色谱图。图97a和97b是包含100ppb茉莉菊酯ii的大麻样品。图97c和97d是空白大麻样品。
图98a-图98d是使用mrm母子离子对373.2>161(图98a,98c)和373.2>143(图98b,98d)分析大麻样品中除虫菊酯ii(pyrethrinii)的存在的色谱图。图98a和98b是包含1000ppb除虫菊酯ii的大麻样品。图98c和98d是空白大麻样品。
图99a-图99d是使用mrm母子离子对331.2>163(图99a,99c)和331.2>121(图99b,99d)分析大麻样品中茉莉菊酯i的存在的色谱图。图99a和99b是包含1000ppb茉莉菊酯i的大麻样品。图99c和99d是空白大麻样品。
图100a-图100b是使用mrm母子离子对317.2>107分析大麻样品中瓜菊酯i的存在的色谱图。图100a是包含1000ppb瓜菊酯i的大麻样品。图100b是空白大麻样品。
图101a-图101c是使用mrm母子离子对329.2>143(图101a)和329.2>161(图101b,101c)分析大麻样品中除虫菊酯i的存在的色谱图。图101a和101b是包含580ppb除虫菊酯i的大麻样品。图101c是空白大麻样品。
图102a-图102d是使用mrm母子离子对349.9>97(图102a,102c)和349.9>321.9(图102b,102d)分析大麻样品中毒死蜱(chlorpyrifos)的存在的色谱图。图102a和102b是包含100ppb毒死蜱的大麻样品。图102c和图102d是空白大麻样品。
图103a-图103d是使用mrm母子离子对356.2>119(图103a,103c)和356.2>177(图103b,103d)分析大麻样品中胡椒基丁醚(piperonylbutoxide)的存在的色谱图。图103a和103b是包含100ppb胡椒基丁醚的大麻样品。图103c和103d是空白大麻样品。
图104a-图104d是使用mrm母子离子对353.1>168(图104a,104c)和353.1>228(图104b,104d)分析大麻样品中噻螨酮(hexythiazox)的存在的色谱图。图104a和104b是包含100ppb噻螨酮的大麻样品。图104c和104d是空白大麻样品。
图105a-图105d是使用mrm母子离子对360.2>57.1(图105a,105c)和360.2>141(图105b,105d)分析大麻样品中乙螨唑(etoxazole)的存在的色谱图。图105a和105b是包含100ppb乙螨唑的大麻样品。图105c和105d是空白大麻样品。
图106a-图106d是使用mrm母子离子对273.1>187(图106a,106c)和273.1>255(图106b,106d)分析大麻样品中螺甲螨酯(spiromesifen)的存在的色谱图。图106a和106b是包含100ppb螺甲螨酯的大麻样品。图106c和106d是空白大麻样品。
图107a-图107d是使用mrm母子离子对422.2>135(图107a,107c)和422.2>366.1(图107b,107d)分析大麻样品中唑螨酯(fenpyroximate)的存在的色谱图。图107a和107b是包含100ppb唑螨酯的大麻样品。图107c和107d是空白大麻样品。
图108a-图108d是使用mrm母子离子对365.1>147(图108a,108c)和365.1>309(图108b,108d)分析大麻样品中哒螨灵(pyridaben)的存在的色谱图。图108a和108b是包含100ppb哒螨灵的大麻样品。图108c和108d是空白大麻样品。
图109a-图109d是使用890.5>305.1(图109a,109c)或890.5>567.2(图109b,109d)的mrm母子离子对分析大麻样品中阿维菌素的存在的色谱图。图109a和109b是包含100ppb阿维菌素的大麻样品。图109c和109d是空白大麻样品。
图110a-图110d是使用mrm母子离子对394.2>107.1(图110a,110c)和394.2>177.1(图110b,110d)分析大麻样品中依芬普司(etofenprox)的存在的色谱图。图110a和110b是包含100ppb依芬普司的大麻样品。图110c和110d是空白大麻样品。
图111a-图111d是使用mrm母子离子对402.2>189(图111a,111c)和402.2>343.1(图111b,111d)分析大麻样品中灭螨醌的存在的色谱图。图111a和111b是包含100ppb灭螨醌的大麻样品。图111c和111d是空白大麻样品。
图112a-图112d是使用mrm母子离子对440.1>166.1(图112a,112c)和440.1>181.1(图112b,112d)分析大麻样品中联苯菊酯(bifenthrin)的存在的色谱图。图112a和112b是包含100ppb联苯菊酯的大麻样品。图112c和112d是空白大麻样品。
图113a-图113d是使用mrm母子离子对380.8>127(图113a)、378.8>127(图113b)、382.8>127(图113c)和378.8>109(图113d)分析包含100ppb二溴磷(naled/dibrom)的大麻样品中二溴磷的存在的色谱图。
图114a-图114h是使用mrm母子离子对342>69(图114a,114c)、342>159(图114b,114d)、344>69(图114e,114g)和344>161(图114f,114h)分析大麻样品中丙环唑的存在的色谱图。图114a、114b、114e和114f是包含10ppb丙环唑的大麻样品。图114c、114d、114g和114h是空白大麻样品。
图114i-图114j是包含100ppb丙环唑的大麻样品且使用mrm母子离子对342>69(图114i)和342>159(图114j)分析丙环唑的存在的色谱图。
图114k-图114l是包含100ppb丙环唑的大麻样品且使用mrm母子离子对344>69(图114k)和344>161(图114l)分析丙环唑的存在的色谱图。
图115a-图115h是包含1000ppb溴虫腈的大麻样品且使用mrm母子离子对423.9>59(图115a)、406.9>59(图115b)、425.9>59(图115c)、425.9>408.9(图115d)、408.9>59(图115e)、423.9>406.9(图115f)、408.9>378.8(图115g)和408.9>270.9(图115h)分析溴虫腈的存在的色谱图。
图116a-图116f是包含1000ppb氟氯氰菊酯的大麻样品且使用mrm母子离子对451>191(图116a)、453>193(图116b)、451>127(图116c)、451>206(图116d)、451>434(图116e)和453>436(图116f)分析氟氯氰菊酯的存在的色谱图。
图117a-图117e是包含1000ppb氯氰菊酯的大麻样品且使用mrm母子离子对435.1>193.1(图117a)、433.1>191.1(图117b)、433.1>127(图117c)、435.1>127(图117d)和433.1>91(图117e)分析氯氰菊酯的存在的色谱图。
图118a,采用基于质子化分子离子的mrm母子离子对的大麻基质(左迹线)和以0.1μg/g水平加标到大麻基质中的灭螨醌(右迹线)的响应叠加图。
图118b,采用基于加合物离子的mrm母子离子对的大麻基质(下迹线)和以0.1μg/g的水平加标到大麻基质中的灭螨醌(上迹线)的响应叠加图。
图119a-图119f是以0.01μg/g的水平加标到大麻基质中的一组代表性农药的色谱图。图119a,草氨酰;图119b,甲霜灵;图119c,唑螨酯;图119d,腈菌唑;图119e,依芬普司;和图119f,嘧菌酯。
图120.以100ng/ml水平加标到包含100ng/ml的二嗪磷的大麻花基质提取物中的二嗪磷进样1周的长期稳定性数据。
图121a-图121d.示出大麻中农药的基质匹配校准曲线示例的图。图121a,腈菌唑;图121b,二嗪磷;图121c,甲霜灵;图121d,亚胺硫磷。
图122a-图122b是包含100ppb乙酰甲胺磷且使用两种提取法制备的大麻样品的色谱图。图122a,乙腈。图122b,50:50乙腈和甲醇。
图123a-图123b是包含100ppb溴虫腈且使用apci源电离的大麻样品的色谱图。图123a,mrm母子离子对346.9>79;图123b,mrm母子离子对348.09>81。
具体实施方式
农药的分析,例如,在植物类材料中,通常需要同时使用气相色谱质谱(gc-ms)和液相色谱质谱(lc-ms)方法,因为一些非极性和氯化农药很难使用lc-ms系统中的电喷雾离子源电离。本公开提供了简单、经济有效、快速且稳健的lc-ms/ms方法,所述方法为各组农药提供的定量限(loq)远低于例如州监管机构为例如大麻产品中的这些化合物设定的行动限。
实际上,所公开的方法和系统对于包含大麻植物材料的样品中农药的检测和/或定量特别有用。除非本公开中另外指明,否则“大麻(cannabis)”涵盖所有品种的大麻植物,包括但不限于含有相对较高水平的四氢大麻酚(thc)的大麻植物诸如大麻(marijuana);以及含有较低水平的thc和较高水平的大麻二酚(cbd)的大麻植物诸如火麻(hemp)。大麻植物材料包含复杂的基质,其中包括诸如大麻素、萜烯和其他非大麻素化合物的成分。大麻植物材料中存在的大麻素含量通常为10–20%(对应于百万分之100,000至200,000(ppm))。萜烯和其他非大麻素化合物存在的含量也很高,大约为10至5,000ppm。然而,为了确保人类食用的安全和/或遵守监管的行动限,需要检测出的农药水平范围为0.00001至0.0010%(相当于十亿分之100至1000(ppb))。因此,来自诸如大麻素、萜烯和其他化合物的基质成分的干扰会淹没并掩盖来自大麻样品中痕量农药的所需信号。而且,在某些实施方案中,包含大麻提取物的样品被稀释10倍(例如,以降低基质干扰的水平)。因此,要检测稀释样品中的诸如这些少量农药,就需要极其灵敏的技术。本文描述的方法提供了足够的灵敏度,从而在远低于俄勒冈州(oregon)和加州(california)监管机构规定的各种行动限的水平下检测和/或定量农药。
此外,尽管这些监管平台中规定的某些农药可以通过esi进行分析,该方法与基于lc的仪器中的lc分离相结合,但是有些农药则不能。具体而言,特别疏水的和/或氯化的农药(例如,五氯硝基苯(quintozene,也称为pentachloronitrobenzene)、氯丹、硫丹i、硫丹ii和氯唑灵(etridiazole))不能使用esi技术或其他常规的与lc兼容的电离方法来分析。相反,通常使用基于gc的技术来分析这些农药。因此,测试各组农药的样品通常需要在多个质谱仪(基于lc的仪器和基于gc的仪器)上进行多次运行,使样品的农药检测和/或定量既昂贵又费时。
本文描述的方法克服了与农药检测相关的许多挑战,所述挑战限制了准确性且使常规农药检测方法成为昂贵又费时的过程。首先,所述方法对每种农药使用一个或多个mrm母子离子对,几乎没有或没有基质干扰,从而使例如灭螨醌和丙环唑的loq分别提高了20和5倍。
其次,所公开的方法使得检测在大麻样品中通常具有低信号的农药(例如,阿维菌素、二溴磷、丁酰肼、mgk-264)成为可能。
第三,所述方法使用快速lc方法以实现高样品通量,并且可以将运行时间从30分钟减少到18.5分钟(包括平衡时间)。
第四,所公开的方法包括具有可接受的回收率的简单且快速的样品制备程序。
第五,所公开的方法可以检测具有低质子亲和力并因此具有低电离效率的农药(例如,氯氰菊酯、氟氯氰菊酯、克菌丹、二溴磷、氯菊酯和除虫菊酯)。
第六,所述方法使用apci源来电离高度氯化和非极性农药(例如pcnb、氯丹),从而无需使用gc-ms检测这些农药。这样就可以仅使用一种仪器(例如,perkinelmer
第七,即使对于通常使用esi源进行分析的溴虫腈,所公开的方法不仅提供了与esi源一起使用的推荐mrm母子离子对,还提供了可与apci源一起使用的mrm母子离子对以减少基质干扰和离子抑制,这在用于分析大麻基质中的该化合物时比esi源具有更好的灵敏度。
第八,在复杂基质中对农药进行测试,可能会诸如迅速污染常规的gc-ms和lc-ms系统,从而增加维护成本和停机时间,导致生产力下降。因此,在一些实施方案中,使用了qsight系统的staycleantm技术。该技术采用热表面诱导的去溶剂化(hsidtm),其中连续不断的热气流充当持续的清洗剂,以冲洗掉潜在的沉积物。离子从hsid界面转移到系统的层流离子导向器,然后由背景气体流移动到分析区域,并且不需要轴向电场。这意味着qsight系统不受电场波动的影响,因此,在分析这些复杂基质中的农药时,可以持续提供高水平的性能,而无需停机进行定期维护。
第九,利用apci或esi源的常规lcmsms方法使用的lc方法采用含有添加剂诸如甲酸、甲酸铵等的流动相。据信这些添加剂有助于样品中分析物的电离。然而,在某些实施方案中,本文描述的apci技术利用了令人惊讶的发现,即当使用不包括某些添加剂(例如,最多所有添加剂)的lc方法来产生用apci源电离的分离流时,某些农药的检测和/或定量限得到了提高。
具体来说,为了检测和/或定量某些特别疏水的和/或氯化的农药(例如,氯丹、五氯硝基苯、硫丹i、硫丹ii、氯唑灵),样品可以使用lc方法处理,所述方法采用不含酸性和/或中性添加剂(例如,不含任何添加剂)的流动相,并且随后用apci源对样品进行电离。在某些实施方案中,将采用包含中性添加剂(例如乙酸铵;例如甲酸铵)但不包含酸性添加剂的流动相的lc方法与apci结合使用。
不希望受限于特定的理论或观察,发现当使用apci源分析此类农药时,当使用采用无任何添加剂的流动相的lc方法时,观察到的信号最高。观察到添加中性添加剂诸如乙酸铵和甲酸铵可使信号降低到2到5分之一。当使用酸性添加剂诸如甲酸和乙酸时,发现用apci源电离的氯化农药的信号降低到20到50分之一。
mrm母子离子对
本公开为每种农药提供一个或多个特定的mrm母子离子对。在本公开中,mrm母子离子对由分别对应于第一m/z值和第二m/z值的两个数字标识,由“>”或“/”分隔(例如,385.2>343.1或385.2/343.1)。即,第一值对应于前体离子,而第二值对应于碰撞池中前体离子裂解后的产物离子。取决于质谱仪的灵敏度,本公开中提供的母子离子对可能存在一些可变性(例如,+0.1或+0.2)。因此,例如,“385.2>343.1”可能涵盖以下一项或多项:385.1>343.1、385.0>343.1、385.3>343.1、385.4>343.1、385.1>343.2、385.0>343.2、385.3>343.2、385.4>343.2、385.1>343.3、385.0>343.3、385.3>343.3、385.4>343.3、385.1>343.0、385.0>343.0、385.3>343.0、385.4>343.0、385.1>342.9、385.0>342.9、385.3>342.9和385.4>342.9。
表1列出了可以使用所公开的方法检测的农药,且包括通常使用gc-ms分析的农药(粗体显示)。表2a和表3提供了用于检测这些农药的独特mrm母子离子对。表4提供了用于检测真菌毒素的推荐mrm母子离子对。
表2a、2b、3和4使用了以下缩写:q1(第一四极杆)、q2(第二四极杆)、ce(碰撞能量)、ev(电子伏特)和ccl2(碰撞池透镜2)。在表2b、表3和表4中,标记为“expectedr.t.”(预期保留时间)、“δtime”(保留时间相对于预期保留时间的+-总变化)、“res”(四极杆1和2的分辨率设置),以及“res_diff”(当未使用默认单位/单位分辨率设置时不同的分辨率)的列是指使用perkinelmerqsightlc-ms/ms系统时的那些参数。
表1.农药和cas编号
表2a.esi-ms的推荐mrm母子离子对。
表2b.perkinelmerqsight的参数
表2c.挑战性农药和相关mrm母子离子对。以粗体强调的mrm母子离子对要么提供高信号和>,要么减少(例如,更少或没有)来自大麻基质的基质干扰。
表2d.提供高信号和>或减少(例如,更少或没有)来自大麻基质干扰的挑战性农药和相关mrm母子离子对。
表3.apci-ms的推荐mrm母子离子对
表4.真菌毒素的推荐mrm母子离子对
在下面的实施例中描述了使用所公开的系统和方法分析大麻样品(通常是含有相对高水平的thc的植物)中的农药。这些实施例证明了所述系统和方法在大麻提取物中在基质效应和同质异位素干扰(例如,参见实施例6,灭螨醌)方面的优势。但是,所公开的系统和方法可以应用于检测各种样品中的农药和真菌毒素,所述各种样品包括大麻(marijuana)和火麻(hemp)产品诸如花;浓缩物(例如,油、酊剂、馏出物);食用品诸如糖果(例如,软糖、巧克力)、食用油、烘焙食品、饮料、冰淇淋;局部用药(例如,凝胶、软膏、洗剂),植物类样品诸如其他可食用植物和植物产品(例如草药、蔬菜、水果、食用花卉、香料、橄榄油);其他药用植物和植物产品;其他可熏制的植物和植物产品(例如,烟草、薄荷、鼠尾草);环境样品(例如,水)和临床样品(例如,血清、尿液)。可以分析以上所公开的农药的任何组合。
大麻中的农药分析
在所公开的方法的实施方案中,使用结合稀释的简单有机溶剂提取法、推荐的mrm母子离子对和具有高效率超高效液相色谱(uhplc)柱的lc梯度,所公开的方法可以用来避免基质效应,从而允许在远低于美国各州诸如加州和俄勒冈州以及其他国家诸如加拿大为大麻产品(包括可吸入产品)制定的最低行动水平的低水平(例如,0.005至0.3μg/g)下检测大麻样品中的农药-包括通常使用gcms检测的非常疏水和氯化的农药。真菌毒素也可以被检测到。例如,在包含受管制农药和真菌毒素且使用简单乙腈提取法提取的大麻样品中,所有农药和真菌毒素的回收率在70-120%的可接受范围内,相对标准偏差(rsd)小于20%。
图119a-图119f显示在大麻花提取物中以0.01μg/g的低水平加标的一组代表性农药的样品mrm色谱图具有出色的信噪比。
如本公开中提供的数据所证明,对于加州当前监管文件中列出的所有ii类农药和真菌毒素,loq均远低于当前加州行动限的2至600倍。大麻基质中每种农药和真菌毒素在loq水平下的响应rsd均小于20%。每种分析物的保留时间可在24小时内的±0.1分钟内重现。这表明所述方法对大麻中的农药和真菌毒素分析在加州规定的监管限值下具有足够的灵敏度和重现性。
通常使用带有ei源的gc-ms分析的农药
许多农药(例如,溴虫腈、氯氰菊酯、氟氯氰菊酯、克菌丹、二溴磷、氯菊酯和除虫菊酯)具有低质子亲和力,这导致使用esi源时的低电离效率。通常使用带有电子电离(ei)源的gc-ms分析这些农药。如在qsightlc-ms/ms系统中,使用带有同轴加热气体的被加热电喷雾源来电离这些农药比没有加热气体的常规esi源电离效率高得多。使用推荐的mrm母子离子对和被加热的电喷雾源,这些农药的loq在10-25ppb的范围内,这远低于例如加州和其他州对大麻设定的行动限。
例如,除虫菊酯是一类衍生自除虫菊(chrysanthemumcinerariifolium)的有机化合物,它们通过靶向昆虫的神经系统而具有强杀虫活性。从菊花(chrysanthemum)花中提取的天然产生的除虫菊酯是第一菊酸(chrysanthemicacid)的酯(除虫菊酯i、瓜菊酯i和茉莉菊酯i)和第二菊酸(pyrethricacid)的酯(除虫菊酯ii、瓜菊酯ii和茉莉菊酯ii);它们的结构如下所示。
在美国,除虫菊提取物的标准为总除虫菊酯的45-55%重量/重量且在市售的除虫菊酯标准中,除虫菊酯i、除虫菊酯ii、瓜菊酯i、瓜菊酯ii、茉莉菊酯i和茉莉菊酯ii的百分比分别为约56.1%、27.8%、5.7%、3.8%、4%和2.6%。大麻中的许多化合物模仿除虫菊酯的结构,且因此由于基质干扰,大麻中除虫菊酯的分析非常困难。使用采用推荐mrm母子离子对和lc梯度的lc-ms/ms方法时,大麻花中除虫菊酯i、除虫菊酯ii、瓜菊酯i、瓜菊酯ii、茉莉菊酯i和茉莉菊酯ii的loq分别为0.1、0.1、0.01、0.03、0.025和0.01μg/g。
校准
在常规方法中,执行基质匹配校准以更准确地定量不同基质诸如食品基质中的农药和其他分析物。在某些实施方案中,使用不同浓度的基于溶剂的分析标准品更为实用和方便。具体来说,在不同食品基质中对农药进行定量具有挑战性,因为不含农药和其他分析物的标准食品基质可能难以获得和/或获得成本很高。
在某些实施方案中,一些农药可能由于基质效应而受到离子抑制,因此可以将同位素标记的内标的混合物加入基于溶剂的校准标样和样品中(参见实施例1)。这种方法可以减少由于离子抑制而导致的基质中农药和其他分析物的定量误差。
减少基质效应引起的离子抑制的另一种方法是用甲醇或乙腈进一步稀释样品提取物(例如,以1.5至50的倍数稀释)。这种方法可以减少离子抑制,但是也会通过增加不同食品基质中农药的定量限而降低灵敏度。在某些实施方案中,当lc使用甲醇作为强溶剂流动相时,用甲醇将乙腈提取物进一步稀释50%,以获得较早洗脱化合物的良好峰形。参见图125。
液相色谱法
采用apci和/或esi源的常规lc-ms/ms方法使用含有添加剂诸如甲酸、甲酸铵和其他添加剂的lc流动相来帮助样品中分析物的电离。但是,为了使用apci源帮助电离分析物诸如氯丹、五氯硝基苯、溴虫腈、氯唑灵、硫丹i、硫丹ii、氯唑灵、溴虫腈、氯唑灵和其他非常疏水或氯化的农药,不含添加剂的lc流动相提供更好的性能。然而,esi电离通常需要使用酸性添加剂诸如甲酸和乙酸和/或中性添加剂诸如甲酸铵和乙酸铵。
在某些实施方案中,可以使用两种按顺序的lc-ms/ms方法,其中第一lc分离方法用于产生采用esi源电离的第一分离流,而第二lc分离方法用于产生采用apci源电离的第二分离流。以此方式,第一lc分离方法可以采用使用酸性和/或中性添加剂的流动相以帮助esi电离,而第二lc方法可采用不含任何此类添加剂(例如,不含任何酸性和/或中性添加剂;不含任何添加剂)的流动相。
在某些实施方案中,使用单个lc-ms/ms的方法,该方法允许使用esi和apci电离(例如,在正离子和负离子模式下)同时电离和测量来自单次进样的样品。在这种方法中,使用的是单个lc方法,且样品中的lc柱洗脱液可以分为通过esi源电离的第一分离流和使用apci源电离的第二分离流。例如,可以使用t型接头将lc柱洗脱液转向到lc-ms/ms系统(例如,诸如perkinelmer'sqsight系统)中存在的esi和apci离子源中进行分析。所述lc-ms/ms系统可以在esi和apci两种模式下运行,而电离模式与极性之间的串扰或干扰可忽略不计。
如上所述,采用不含酸性和/或中性添加剂的流动相(例如,不含任何添加剂)的lc方法的使用允许使用apci源来分析分析物。具体来说,对于使用apci源分析各种氯化农药的情况,已经观察到,当不使用任何添加剂时信号最高,并且在添加中性添加剂诸如乙酸铵和甲酸铵时信号降低到2至5分之一。当添加酸性添加剂诸如甲酸和乙酸时,用apci源电离的氯化农药的信号下降到20至50分之一。因此,由于esi需要存在一些离子添加剂以辅助分析物的电离和分析,所以在某些实施方案中,可以使用采用含中性添加剂诸如乙酸铵或甲酸铵的流动相的单个lc方法。所述方法提供了一种折衷方案,其允许esi源和apci源两者与单个lc方法一起使用。通过只进行单次lc进样即可进行分析,该方法提高了通量。
实施方案的实施例
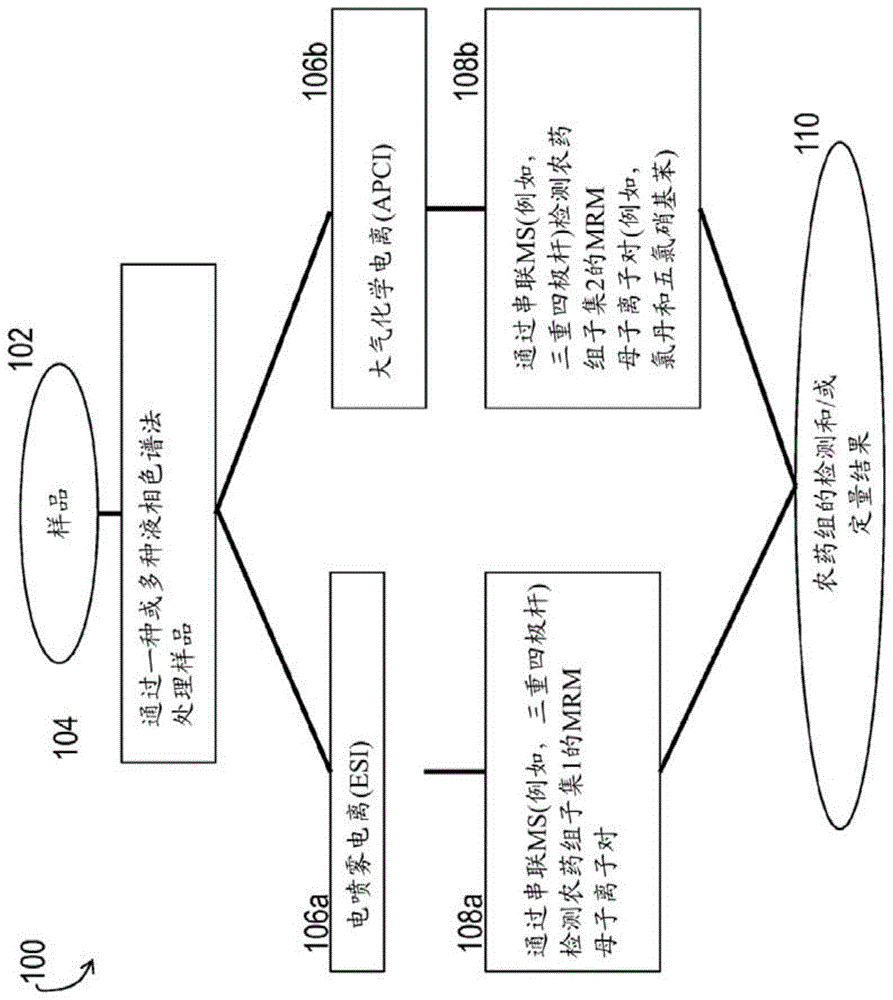
图1示出了用于根据本文所述方法在样品(例如,包含大麻植物材料)中检测和/或定量一组农药(例如72种农药)的示例过程100。在过程100中,样品102通过一种或多种lc方法104进行处理以产生第一分离流和第二分离流。使用esi源106a将第一分离流电离以产生第一电离样品流。串联质谱法(例如,三重四极杆质谱法)用于通过检测与第一子集108a的每种农药相关的mrm母子离子对的强度来检测和/或定量第一电离样品流中农药组的第一子集。使用apci源106b将第二分离流电离以产生第二电离样品流。串联质谱法用于通过检测与第二子集108b的每种农药相关的mrm母子离子对的强度来检测和/或定量第二电离样品流中农药组的第二子集。基于与农药相关的一个或多个mrm母子离子对的检测强度可以对每种农药进行检测(例如,鉴定为存在于样品中)和/或定量。通过以这种方式应用两个并行lc-ms/ms技术,获得全组110的检测和/或定量结果。
图2示出了用于使用含apci源的lc-ms/ms检测和/或定量样品中的一种或多种农药的示例过程200。在过程200中,样品202通过lc方法204进行处理以产生分离流。所述分离流使用apci源和空气作为雾化气体206进行电离。串联质谱法(例如,三重四极杆质谱法)用于检测与农药208相关的一个或多个mrm母子离子对的强度。相关的一个或多个mrm母子离子对的强度可以用来检测(例如,鉴定为存在于样品中)和/或定量农药210。
图3示出了在某些实施方案中用于执行本文所述lc-ms/ms技术的示例lc-ms/ms系统300。lc-ms/ms300包括lc阶段302、电离源(例如,esi源和/或apci源)304和两个质量过滤器306和310,其间串联有碰撞池308。在某些实施方案中,两个质量过滤器(q1和q2)是四极杆。在某些实施方案中,碰撞池是四极(q)(例如,rf四极)。在某些实施方案中,lc-ms/ms300是三重四极杆系统。lc-ms/ms300包括用于检测离子的检测器312。
在一个方面,一种用于通过液相色谱-串联质谱法(lc-ms/ms)检测和/或定量样品中农药组内的多种农药的方法,其包括:(a)使用一种或多种液相色谱法(lc)处理样品以产生第一分离流和第二分离流;(b)使用电喷雾电离(esi)源电离第一分离流以产生第一电离样品流;(c)使用大气化学电离(apci)源电离第二分离流以产生第二电离样品流;以及(d)通过串联质谱法(例如,使用三重四极杆系统)来检测:(i)对于组内第一子集的每种农药,使用第一电离样品流的与农药相关的一个或多个多反应监测(mrm)母子离子对的强度;和(ii)对于组内第二子集的每种农药,使用第二电离样品流的与农药相关的一个或多个多反应监测(mrm)母子离子对的强度,从而检测和/或定量农药组中的所述多种农药。
在某些实施方案中,所述样品包含大麻植物材料(例如,其中大麻植物材料被稀释例如10倍或更多倍)。在某些实施方案中,所述样品包含可食用材料(例如,食品)。在某些实施方案中,所述样品包含植物材料。
在某些实施方案中,所述样品包含提取物,并且所述方法包括使用提取程序产生所述样品提取物,所述提取程序包括将基础样品与一种或多种溶剂合并,并且在稀释所述基础样品之后,过滤所述稀释的基础样品。
在某些实施方案中,所述一种或多种溶剂包含甲醇。在某些实施方案中,所述一种或多种溶剂包含乙腈(例如,乙腈和/或乙腈与甲酸)。在某些实施方案中,所述提取程序还包括在将所述基础样品用一种或多种溶剂稀释后应用的分散固相提取程序(例如,使用psa(伯胺和仲胺)吸附剂、c18、氧化铝石墨化碳等;例如,以减少离子抑制和基质干扰)。
在某些实施方案中,所述方法包括,对于所述多种农药中的至少一部分的每种农药,基于检测到的与所述农药相关的一个或多个mrm母子离子对的强度,定量所述样品中所述农药的水平(例如,微克每克)(例如,其中所述样品包含大麻植物材料和/或其中所述农药的水平的loq低于加州和/或俄勒冈州行动水平例如2、10、20或50倍)。
在某些实施方案中,对于所述多种农药中的至少一种,定量所述样品中所述农药的水平包括使用基于溶剂的分析校准标准品(例如,同位素标记的内标)。在某些实施方案中,所述方法包括用内标混合物(参见表10)对所述校准标准品和/或所述样品加标。
在某些实施方案中,所述组包含72种农药。在一些实施方案中,例如,当所述样品是大麻样品时,第一子集包含70种农药且第二子集包含3种农药诸如氯丹、溴虫腈和五氯硝基苯(pcnb)。
在某些实施方案中,所述组的第一子集包含一种或多种高分子量和/或热不稳定的农药(例如,阿维菌素)。
在某些实施方案中,所述组的第一子集包含选自以下组成的组中的一种或多种2类农药:阿巴菌素、乙酰甲胺磷、灭螨醌、啶虫脒、嘧菌酯、联苯肼酯、联苯菊酯、啶酰菌胺、克菌丹、甲萘威、氯虫酰胺、瓜菊酯i、瓜菊酯ii、四螨嗪、氟氯氰菊酯、氯氰菊酯、二嗪磷、烯酰吗啉、乙螨唑、环酰菌胺、唑螨酯、氟啶虫酰胺、咯菌腈、噻螨酮、吡虫啉、茉莉菊酯i、茉莉菊酯ii、醚菌酯、马拉硫磷、甲霜灵、灭多威、腈菌唑、二溴磷、草氨酰、氯菊酯、亚胺硫磷、胡椒基丁醚、炔丙菊酯、丙环唑、除虫菊酯i、除虫菊酯ii、哒螨灵、乙基多杀菌素、多杀菌素、螺甲螨酯、螺虫乙酯、戊唑醇、噻虫嗪和肟菌酯。
在某些实施方案中,所述组的第一子集包含选自以下组成的组中的一种或多种1类农药:涕灭威、加保扶、溴虫腈、毒死蜱、蝇毒磷、丁酰肼、ddvp(敌敌畏)、乐果、灭线磷、依芬普司、苯氧威、氟虫腈、抑霉唑、甲硫威、甲基对硫磷、速灭磷、多效唑、残杀威、螺环菌胺、噻虫啉、mgk-264。
在某些实施方案中,所述组的第二子集包含一种或多种疏水的和/或氯化的农药。
在某些实施方案中,所述组的第二子集包含选自以下组成的组中的一种或多种农药:五氯硝基苯、氯丹、溴虫腈、硫丹i、硫丹ii和氯唑灵。
在某些实施方案中,所述组的第二子集包含氯丹、溴虫腈和/或五氯硝基苯(pcnb)。
在某些实施方案中,步骤(c)包括使用空气和/或其他气体诸如氮气、氩气和二氧化碳作为雾化气体(例如,以产生带负电荷的氧离子,所述带负电荷的氧离子充当试剂离子并帮助电离氯丹和/或五氯硝基苯)。
在某些实施方案中,步骤(a)包括使用单个lc方法处理所述样品(例如,且将所述单个lc方法的洗脱液分成所述第一分离流和所述第二分离流)。在某些实施方案中,所述单个lc方法采用含中性添加剂诸如乙酸铵、甲酸铵、氢氧化铵和碳酸铵的流动相。在某些实施方案中,所述单个lc方法采用不含酸性添加剂(例如,不含甲酸和/或不含乙酸)的流动相。在某些实施方案中,所述单个lc包括具有快速梯度(例如10–20%/分钟或更大有机变化)和慢速梯度[例如,1–10%/分钟(例如,5–6%)有机变化]的快速lc方法,以最大程度减少农药信号峰和基质干扰峰之间的重叠。
在某些实施方案中,步骤(a)包括使用第一lc方法处理所述样品以产生所述第一分离流和使用第二lc方法处理所述样品以产生所述第二分离流。在某些实施方案中,所述第二lc方法采用含中性添加剂诸如乙酸铵、甲酸铵、氢氧化铵和碳酸铵的流动相。在某些实施方案中,所述第二lc方法采用不含酸性添加剂(例如,不含甲酸和/或不含乙酸)的流动相。在一些实施方案中,所述第二lc方法使用不含任何中性和/或酸性添加剂的流动相。在某些实施方案中,所述第一lc方法和/或所述第二lc方法包括具有快速梯度(例如,10–20%/分钟或更大有机变化)和慢速梯度[例如,1–10%/分钟(例如,5–6%)有机变化]的快速lc方法,以最大程度减少农药信号峰和基质干扰峰之间的重叠。
在某些实施方案中,对于所述第一子集的每种农药和/或对于所述第二子集的每种农药,与所述农药相关的所述一个或多个mrm母子离子对的至少一部分与基质干扰明显不同。在一些实施方案中,所述样品包含大麻植物材料并且所述基质干扰是大麻基质干扰,诸如与大麻素、萜烯和/或其他非大麻素化合物相关的干扰。
在某些实施方案中,对于所述组的所述多种农药的至少一部分中的每一种,所述一个或多个相关mrm母子离子对包括表2a的一个或多个mrm母子离子对。
在某些实施方案中,对于所述组的所述多种农药的至少一部分中的每一种,所述一个或多个相关mrm母子离子对包括表2c的一个或多个mrm母子离子对。
在某些实施方案中,对于所述组的所述多种农药的至少一部分中的每一种,所述一个或多个相关mrm母子离子对包括表2d的一个或多个mrm母子离子对。
在某些实施方案中,对于所述组的所述多种农药的至少一部分中的每一种,所述一个或多个相关mrm母子离子对包括表3的一个或多个mrm母子离子对。
在一些实施方案中,一种用于使用lc-ms/ms检测和/或定量样品中一种或多种农药(例如,非常疏水的和/或氯化的农药)水平的方法包括:(a)使用液相色谱法(lc)处理所述样品以产生分离流;(b)使用空气和/或其他气体诸如氮气、氩气和二氧化碳作为雾化气体,使用apci源电离所述分离流以产生电离样品流;以及(d)通过串联质谱法(例如,使用三重四极杆系统),对于所述一种或多种农药中的每种农药,检测使用电离样品流的一个或多个多反应监测(mrm)母子离子对的强度,每个mrm母子离子对与所述农药相关,从而检测和/或定量所述一种或多种农药。
在某些实施方案中,所述样品包含大麻植物材料(例如,其中所述大麻植物材料被稀释例如10倍或更多倍)。在某些实施方案中,所述样品包含可食用材料(例如,食品)。在某些实施方案中,所述样品包含植物材料。
在某些实施方案中,所述样品是提取物,并且所述方法包括使用提取程序产生所述样品提取物,所述提取程序包括将基础样品与一种或多种溶剂合并(例如,稀释)[例如,并且在稀释所述基本样品之后,过滤所述稀释的基础样品。]在某些实施方案中,所述一种或多种溶剂包含甲醇。在某些实施方案中,所述一种或多种溶剂包含乙腈(例如,乙腈和/或乙腈与甲酸)。在某些实施方案中,当lc使用甲醇作为强溶剂流动相时,用甲醇将所述乙腈提取物进一步稀释50%或更多,以获得较早洗脱化合物的良好峰形。在某些实施方案中,所述提取程序还包括在将所述基础样品用一种或多种溶剂稀释后应用的分散固相提取程序(例如,使用psa(伯胺和仲胺)吸附剂、c18、氧化铝石墨化碳等;例如,以减少离子抑制和基质干扰)。
在某些实施方案中,所述方法包括对于所述一种或多种农药中的每种农药,基于检测到的与所述农药相关的一个或多个mrm母子离子对的强度,定量所述样品中所述农药的水平(例如,微克每克)[例如,其中样品包含大麻植物材料和/或其中所述农药的水平的定量限(loq)低于所述农药的加州行动水平和/或俄勒冈州行动水平(例如2、10、20或50倍]。
在某些实施方案中,对于所述农药中的至少一种,定量所述样品中所述农药的水平包括使用基于溶剂的分析校准标准品(例如,同位素标记的内标)。在某些实施方案中,所述方法包括用表6的内标混合物对所述校准标准品和/或所述样品加标。
在某些实施方案中,所述一种或多种农药包含一种或多种疏水的和/或氯化的农药。在某些实施方案中,所述一种或多种农药包含选自以下组成的组中的一种或多种农药:五氯硝基苯、氯丹、溴虫腈、硫丹i、硫丹ii和氯唑灵。在某些实施方案中,所述一种或多种农药包括氯丹和/或五氯硝基苯(quintozene,也称为pentachloronitrobenzene)。
在某些实施方案中,所述lc方法采用含中性添加剂诸如乙酸铵、甲酸铵、氢氧化铵和碳酸铵的流动相。在某些实施方案中,所述单个lc方法采用不含酸性添加剂(例如,不含甲酸和/或不含乙酸)的流动相。在某些实施方案中,所述单个lc方法采用不含任何中性和/或酸性添加剂(例如,不含任何添加剂)的流动相。
在某些实施方案中,对于所述一种或多种农药中的至少一部分的每种农药,与所述农药相关的所述一个或多个mrm母子离子对与基质干扰明显不同,诸如其中所述样品包含大麻植物材料而基质干扰是与大麻素、萜烯和/或其他非大麻素化合物相关的大麻基质干扰。
在某些实施方案中,所述一种或多种农药包括氯丹,并且步骤(d)包括检测与氯丹相关的一个或多个mrm母子离子对的强度,其中所述与氯丹相关的一个或多个mrm母子离子对包括一个或多个选自由439.8>35母子离子对和441.8>35母子离子对组成的组中的成员。
在某些实施方案中,所述一种或多种农药包括五氯硝基苯,并且步骤(d)包括检测与五氯硝基苯相关的一个或多个mrm母子离子对的强度,其中所述与五氯硝基苯相关的一个或多个mrm母子离子对包括一个或多个选自由275.8>35母子离子对、273.8>35母子离子对、275.8>201.8母子离子对和273.8>199.8母子离子对组成的组中的成员。
在某些实施方案中,所述一种或多种农药包括溴虫腈,并且步骤(d)包括检测与溴虫腈相关的一个或多个mrm母子离子对的强度,其中所述与溴虫腈相关的一个或多个mrm母子离子对包括一个或多个选自由346.9>79母子离子对和348.9>81母子离子对组成的组中的成员。
在某些实施方案中,所述一种或多种农药包括氯唑灵,并且步骤(d)包括检测与氯唑灵相关的一个或多个mrm母子离子对的强度,其中所述与氯唑灵相关的一个或多个mrm母子离子对包括一个或多个选自由216.8>35母子离子对和218.8>35母子离子对组成的组中的成员。
在某些实施方案中,所述lc方法是具有快速梯度(例如10–20%/分钟或更大有机变化)和慢速梯度[例如,1–10%/分钟(例如,5–6%)有机变化]的快速lc方法,以最大程度减少农药峰和基质干扰峰之间的重叠。
在另一方面,本公开提供一种用于执行本文描述的任何一种方法的系统,所述系统包括液相色谱串联质谱仪(例如,三重四极杆质谱lc质谱仪)。
本领域技术人员将理解,上述实施方案的许多变化和排列都落入所附权利要求的范围内。
实施例1
硬件和软件。在以下实施例中,色谱分离在
大麻样品的制备。将约5克的大麻花精细研磨,并将1克研磨混合物放入50ml离心管中,并且离心管中包含10μl的表6所示的内标溶液。将三个10mm钢球和5ml的lc-ms级乙腈一起添加到管中。将管加盖,置于多管涡旋混合仪上,且涡旋10分钟,然后以3000rpm离心10分钟。使用0.22微米尼龙注射器过滤器将溶剂过滤到5ml玻璃琥珀色小瓶中,将小瓶加盖并标记。
lc-ms/ms分析。将0.5ml提取的样品放入2mlhplc小瓶中,用0.5ml的lc-ms级乙腈稀释,并混合。进样3μl的这种样品,使用表5所示的lc方法和ms源条件,进行lc-ms/ms分析。
表5.lc方法和ms源条件
样品基质匹配校准标准品。基质匹配校准是定量的黄金标准,因为它补偿了基质效应。在复杂的基质诸如大麻中,基质效应对基于lcms的分析是常见的。响应的减少或增加归因于电离过程中由于共洗脱的基质化合物的存在而导致的分析物的离子抑制。由于样品基质效应,基质匹配校准曲线用于定量,并且是通过进样空白大麻花提取物和包含在0.1-1000ng/ml范围内至少七个或以上的不同浓度水平的变化浓度的农药和真菌毒素的空白大麻花提取物样品而生成的。
表6.示例内标混合物的组成
图121a-图121d示出了大麻提取物中的农药在四个数量级上的校准曲线的代表性示例。对于所有测试的分析物,所有农药和真菌毒素的校准曲线均为线性,校准拟合r2大于0.99。
实施例2.液相色谱法
图27a是示出使用通用(固定梯度率)液相色谱梯度在14分钟内获得的包含大麻植物材料的(空白)样品的总离子色谱图(tic)的图。图27b是示出包含大麻植物材料的包含100ppb农药的样品的tic的图。图27c是示出使用上述实施例1中所述的示例lc方法获得的tic的图。图27d是各种lc柱的vandeemter曲线。
柱内径。可以调整柱的内径(id)以提高响应和准确检测和/或定量植物类样品中各种农药的能力。图29a和图29b分别绘制了采用2.1mmid柱和4.6mmid柱测得的包含螺环菌胺(和大麻植物材料)的农药样品的mrm母子离子对的强度。数据表明较小id柱会扭曲峰形,被认为是由于较小id柱的大麻基质组分超载所致。
流速。流速是一个lc参数,会影响lc方法的性能以及在用于检测和/或定量特定农药的质谱测量中获得的信号。图27e和图27f是绘制用于测量包含嘧菌酯的样品的404.1>372.1mrm母子离子对的强度的图。图27e示出了当使用0.5ml>min流速时mrm母子离子对的强度。所获得的峰宽和信号振幅分别为0.19min和1.47×106。图27f示出了当使用0.8ml>min流速时mrm母子离子对的强度。所获得的峰宽和信号振幅分别为0.12min和2.41×106。0.5ml>min流速lc方法的峰宽是用0.8ml>min流速lc方法获得的峰宽的1.58倍,同时用0.8ml>min方法获得的信号振幅是0.5ml>min方法获得的信号振幅的1.64倍。因此,提高流速到0.8ml>min时,获得了更窄和更大振幅的峰。检测了流速对多种其他农药的信号的影响,并确定了对于本实施例中使用的4.6mmid柱,所有分析物的检测限均可提高约50%。
洗脱溶剂。图30a-图30c示出了关于在lc方法中使用的有机洗脱溶剂对各种农药的响应的影响的数据。图30a和图30b绘制了在使用两种不同有机溶剂组合物的lc方法分离之后所测量的包含灭螨醌的大麻提取物的mrm母子离子对的强度。图30a示出了当有机洗脱溶剂为100%甲醇溶剂时获得的mrm母子离子对的强度,且图30b示出了当有机洗脱溶剂为75%甲醇和25%乙腈时获得的mrm母子离子对的强度。图30c示出了有机洗脱溶剂中不同百分比的甲醇对观察到的对灭螨醌和阿维菌素响应的影响。
实施例3
使用本公开方法的实施方案演示了大麻样品中农药的检测和定量。结果显示在表7中鉴定的图中。另外的农药的检测和定量在实施例4-17中描述。
表7.示出大麻样品中农药的检测和定量的图
由于检测到的农药既包括极性化合物也包括非极性化合物,因此使用100%乙腈从样品提取物中提取所有分析物。大麻基质疏水性很强,并且用水性流动相进一步稀释大麻提取物以使其与反相lc相容,这导致一些农药由于沉淀而回收率较低。因此,将大麻提取物用乙腈稀释10倍以实现农药的高回收率并降低基质效应。但是,反相lc方法在lc运行开始时使用水性流动相,以帮助更好地将极性化合物保留在柱上。在lc上注入有机溶剂诸如乙腈样品提取物导致早期洗脱极性化合物的不良色谱峰。为克服此问题,在本实施例中报告的实验中使用了3微升的小样品进样量。
本实施例中描述的实验评估了用于检测和/或定量包含大麻植物材料的样品中不同农药的各个mrm母子离子对的性能。对于与特定农药相关的特定mrm母子离子对,通过测量两种不同样品的特定mrm母子离子对的强度变化(作为洗脱时间的函数)来评估性能:(i)包含大麻植物材料和所述特定农药(以特定浓度加标)的农药样品和(ii)包含大麻植物材料但不包含所述特定农药的空白大麻样品。通过将农药样品测量中观察到的一个或多个峰的振幅与空白大麻样品中的振幅波动进行比较,计算所述一个或多个峰中的每个峰的信噪比(s/n)。
对于各个mrm母子离子对,还计算了定量限(loq),并将其与州监管机构指定的与之相关的特定农药的行动限进行了比较。对于列出的所有ii类农药和真菌毒素,其loq远低于加州行动限2至600倍。大麻基质中每种农药和真菌毒素在其loq水平的响应相对标准偏差(rsd)均小于20%。每种分析物的保留时间可在24小时内的±0.1min内重现。这表明所述方法对大麻中的农药和真菌毒素分析在加州规定的监管限值下具有足够的灵敏度和重现性。
如上所述,大麻是一个具有挑战性的测试基质,而农药的低浓度水平使之更加复杂。为确保最高的分析置信度,为低水平检测确定了大麻基质中基质干扰最小时多种农药的多个mrm母子离子对。例如,灭螨醌在标准品中可以很容易地被电离为质子化的分子离子,但是基于大麻基质中质子化的分子离子的mrm母子离子对显示0.5–1μg/g的较差loq,是其加州行动限的约5-10倍。因此,确定了基于替代电离模式诸如加合物形成的mrm母子离子对,以减少基质干扰并实现例如大麻基质中灭螨醌的loq为0.025μg/g(行动限的四分之一)。
实施例4.阿维菌素
高分子量化合物诸如阿维菌素和一些早期洗脱的极性化合物诸如达米嗪等很难用gcms在低水平下测量,因为它们在高温下在gc进样器或gc柱温箱中分解。尽管这些化合物可以用esi源电离,但它们在esi源中也易于在高温下分解(例如,参见图6a,6b)。因此,确定了适合esi源的温度和hsid温度以使高分子量和极性农药的信号最大化。
阿维菌素还易于与从玻璃器皿浸入流动相中的钠和钾离子形成钠和钾加合物。由于浸出离子的量难以控制,因此将阿维菌素的钠加合物用作分析的q1质量会导致不可接受的响应变化。因此,为减少钠或钾加合物的形成,在流动相中加入受控量的铵盐(乙酸盐或甲酸盐)以形成阿维菌素的铵加合物。在流动相中并在正确的温度条件下使用铵盐,产生阿维菌素的良好且可重现的信号。
图10a是在q1扫描模式下阿维菌素的前体(母体)离子质量扫描。图10b-图10e和图109a-图109d是比较包含100ppb阿维菌素的大麻样品(图10b,10d;图109a,109b)和空白大麻样品(图10c,10e;图109c,109d)的与阿维菌素相关的两个不同mrm母子离子对的强度的色谱图。两个mrm母子离子对都使用对应于铵加合物代替钠加合物的前体(母体)质量。
使用890.5>567.2(图10b,10d;图109b,109d)的mrm母子离子对产生的信噪比(s/n)为41。使用890.5>305.1(图10c,10e;图109a,109c)的mrm母子离子对产生的s/n比为67。使用这些mrm母子离子对的阿维菌素的loq提高了大约十倍,达到约30ppb。
实施例5.乙酰甲胺磷
图18a-图18b和图44a-图44b是比较包含100ppb乙酰甲胺磷的大麻样品和空白大麻样品的与乙酰甲胺磷相关的两个不同mrm母子离子对的强度的色谱图。使用184>143mrm(图18a,18b)的mrm母子离子对提供了500的s/n比。使用184>49(图44a,44b)的mrm母子离子对提供了90的s/n比。这些mrm母子离子对可以将乙酸盐的loq提高到10ppb。
实施例6.灭螨醌
灭螨醌在溶剂标准品中可以很容易地被电离为质子化的分子离子,但是由于基质干扰,大麻基质中基于质子化的分子离子的mrm母子离子对的loq较差为0.5至1μg/g,是加州对灭螨醌的行动限的约5至10倍。如下所述,基于替代电离模式(例如加合物形成)的mrm母子离子对减少了基质干扰并实现了loq约为25ppb。
图7a-图7d是比较包含100ppb灭螨醌的大麻样品和空白大麻样品的与灭螨醌相关的两个不同mrm母子离子对的强度的四幅图。图7b和7d分别绘制了灭螨醌和空白大麻样品的mrm母子离子对385.2>343.1的强度。尽管在图7b的图中观察到大振幅强度峰,但同时在图7d所示的空白大麻样品数据中也出现了类似的峰。数据表明,这个mrm母子离子对由大麻基质干扰主导,因此不适合用于在大麻基质组分存在的情况下对灭螨醌的检测和/或定量。
图7a和图7b比较了灭螨醌和空白大麻样品的另一个mrm母子离子对385.2>189.1的强度。根据图7a和7b所示数据,对mrm母子离子对385.2>189.1,确定s/n比为24。这两个母子离子对确定可提供范围从0.5至1ppm的loq。
图8是示出灭螨醌的质量扫描的图,其显示了不同的前体(母体)离子质量。如图9和111呈现的数据所示,对应于402.2前体(母体)离子的mrm母子离子对为灭螨醌的检测和/或定量提供更高的s/n比。mrm母子离子对402.2>189(图9a,9c;图111a,111c)提供的s/n比为60。mrm母子离子对402.2>343.1(图9b,9d;图111b,111d)提供的s/n比为205,且loq提高到例如25或42ppb。
实施例7.溴虫腈
溴虫腈的结构如下:
esi电离源
图14a是示出溴虫腈的质量扫描的图,其显示了不同的前体(母体)离子质量。质量值为406.9和423.9的峰分别对应于质子化分子([m+h]+)和铵加合物([m+nh4]+)。
图14b-图14e绘制了mrm母子离子对的强度,其前体(母体)质量对应于溴虫腈的铵加合物([m+nh4]+)。mrm母子离子对426>59提供了1.2×105的信号振幅(图14b)。mrm母子离子对426>271提供了1.42×104的信号振幅(图14c)。mrm母子离子对426>379提供了1.99×104的信号振幅(图14d)。mrm母子离子对426>409提供了3.76×105的信号振幅(图14e)。
图14f-图14i绘制了mrm母子离子对的强度,其前体(母体)质量对应于质子化溴虫腈([m+h]+)。图14f绘制了mrm母子离子对409>41的强度,其提供了1.03×104的信号振幅。图14g绘制了mrm母子离子对409>59的强度,其提供了1.76×105的信号振幅。图14h绘制了mrm母子离子对409>271的强度,其提供了2.57×104的信号振幅。图14i绘制了mrm母子离子对409>379的强度,其提供了3.42×104的信号振幅。
图14j-图14n是包含1000ppb溴虫腈的大麻样品的色谱图。图14j和图14k中的色谱图是使用先前使用的mrm母子离子对409>271(图14j)和409>379(图14k)获得的,其中前者提供的s/n比为15,后者提供的s/n比为20。相比之下,图14l-图14n是使用本文公开的适当mrm母子离子对获得的色谱图,其可以将灵敏度提高3倍。mrm母子离子对409>59(图14l)提供的s/n比为55。mrm母子离子对426>59(图14m)提供的s/n比为78。mrm母子离子对426>409(图14n)提供的s/n比为37。
lc柱的类型会影响溴虫腈的鉴定。例如,使用联苯柱可能会导致将肟菌酯错误鉴定为溴虫腈,因为这两种化合物可能会共洗脱。使用c18柱代替联苯柱进行基线分离可解决此问题。图15a和图15b分别是使用mrm母子离子对409.1>186和409.1>206获得的色谱图。使用这些mrm母子离子对中的每一个都可获得单个峰。相比之下,使用mrm母子离子对409.1>59会出现两个峰(图15c);第一个(较早出现)对应于肟菌酯,而第二个(较晚出现)对应于溴虫腈。
图93a-图93d比较了包含100ppb溴虫腈的大麻样品与空白大麻样品测量结果的mrm母子离子对强度。图93a和93c分别比较了包含1000ppb溴虫腈的农药样品和空白大麻样品mrm母子离子对426>409的强度。图93b和93d分别比较了包含1000ppb溴虫腈的农药样品和空白大麻样品mrm母子离子对426>59.1的强度。loq为约650ppb。
图115a和图115b示出了与溴虫腈相关并避免基质干扰的其他mrm母子离子对的强度测量结果。图115a绘制了包含100ppb溴虫腈的农药样品和空白大麻样品mrm母子离子对423.9>59的强度。图115b绘制了包含1000ppb溴虫腈的农药样品和空白大麻样品mrm母子离子对406.9>59的强度。对于这两个mrm母子离子对,在农药样品测量结果中均观察到峰,而空白大麻样品测量结果的强度则相对平坦。mrm母子离子对423.9>59提供的s/n比为51,而mrm母子离子对406.9>59提供的s/n比为145。使用这些母子离子对的loq为100ppb。
图115c-图115f示出了与溴虫腈有关但受到基质干扰的各个mrm母子离子对的强度测量结果,尤其是mrm母子离子对425.9>59(图115c)、mrm母子离子对425.9>408.9(图115d)、mrm母子离子对408.9>59(图115e)和mrm母子离子对423.9>406.9(图115f)。图115g和图115h比较了包含100ppb的大麻样品与空白大麻样品测量结果的两个不同mrm母子离子对的强度。确定这些mrm母子离子对提供的灵敏度要低于图115a和115b所示的灵敏度。图115g中所示的mrm母子离子对408.9>378.8提供的s/n比为30。图115h绘制了mrm母子离子对408.9>270的强度,其提供了最小的s/n比。使用这些母子离子对获得的loq为1000ppb。
apci电离源
通常使用esi源分析溴虫腈,但使用apci源和mrm母子离子对346.9>79和348.9>81实现了更好的电离,并且基质干扰更少,从而将检测限提高到约25ppb。参见图123a-图123b。
实施例8.瓜菊酯i
图22a-图22b和图100a-图100b比较了包含1000ppb瓜菊酯i的大麻样品和空白大麻样品的与瓜菊酯i相关的两个不同mrm母子离子对的强度。使用mrm母子离子对317.2>149(图22a,22b),s/n比为180。使用mrm母子离子对317.2>107(图100a,11b),s/n比为38。loq为约10ppb。
实施例9.瓜菊酯ii
对表8中所示的瓜菊酯ii的六个mrm母子离子对进行了基质干扰评估。
表8.在空白大麻提取物以及纯溶剂中和大麻基质中加标值为40ppb的瓜菊酯ii的六个mrm母子离子对的信号
按常规,产生溶剂样品的最高信号振幅(“溶剂中的信号”列)的mrm母子离子对会(在这种情况下是mrm3)将被用于瓜菊酯ii的检测和/或定量。尽管mrm6在溶剂中的信号最低,但mrm6(375.2>213.1)和mrm5(375.2>149.1)一样减少了基质干扰。
图21a-图21b和图96a-图96b比较了包含1000ppb瓜菊酯ii的大麻样品和空白大麻样品的与瓜菊酯ii相关的两个不同mrm母子离子对的强度。mrm母子离子对361.2>213的s/n比为23(图21a,21b)。mrm母子离子对361.2>149的s/n比为36(图96a,96b)。loq为约30ppb。
图21e和图21f示出了对于某些母子离子对存在的挑战性的基质干扰效应。图21e和图21f分别绘制了包含1000ppb瓜菊酯ii的大麻样品和空白大麻样品mrm母子离子对361.2>107的强度。这两个强度图几乎无法区分,表明这个母子离子对是由来自大麻基质的基质干扰主导的。因此,这个母子离子对不能用于大麻样品中瓜菊酯ii的低水平分析。
实施例10.氟氯氰菊酯
图116a-图116f是使用与氟氯氰菊酯相关的各个mrm母子离子对获得的色谱图。图116a和图116b示出了与氟氯氰菊酯相关但受到基质干扰的各个mrm母子离子对的强度测量结果。图116a绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对451>434的强度。图116b绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对453>436的强度。这些mrm母子离子对受到基质干扰(即,农药样品测量结果中存在的峰也存在于空白大麻样品测量结果中)。mrm母子离子对451>434提供的s/n比为10。loq为约1000ppb。
图116c和图116d示出了与氟氯氰菊酯相关并避免基质干扰、但提供低信号振幅的两个mrm母子离子对的强度测量结果。图116c绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对451>127的强度。图116d绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对451>206的强度。这些mrm母子离子对提供的振幅峰值比451>191和453>193低,但仍避免了基质干扰(空白大麻样品测量结果的强度相对平坦)。mrm母子离子对451>127提供的s/n比为25,而mrm母子离子对451>206提供的s/n比为16。loq为约400ppb。
图116e绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对451>191的强度。图116f绘制了包含1000ppb氟氯氰菊酯的农药样品和空白大麻样品mrm母子离子对453>193的强度。对于这两个mrm母子离子对,在农药样品测量结果中均观察到峰,而空白大麻样品测量结果的强度则相对平坦。mrm母子离子对451>191提供的s/n比为66,而mrm母子离子对453>193提供的s/n比为33。通过这些mrm母子离子对获得的loq约为150ppb。
图90a-图90d也比较了包含1000ppb氟氯氰菊酯的大麻样品与空白大麻样品测量结果的mrm母子离子对强度。图90a和90c比较了451.1>191mrm母子离子对的强度,且90b和90d比较了451.1>434mrm母子离子对的强度。loq为约600ppb。
实施例11.氯氰菊酯
图94a-图94d比较了包含1000ppb氯氰菊酯的大麻样品和空白大麻样品测量结果的mrm母子离子对强度。图94a和94c分别比较了包含1000ppb氯氰菊酯的农药样品和空白大麻样品mrm母子离子对433.1>127的强度。图94b和94d分别比较了包含1000ppb氯氰菊酯的农药样品和空白大麻样品mrm母子离子对433.1>191.1的强度。loq为约150ppb。
图117a-图117d绘制了为空白大麻样品与包含100ppb氯氰菊酯的大麻样品测量的与氯氰菊酯相关的mrm母子离子对的强度。图117a-图117d所示的mrm母子离子对避免了来自大麻基质组分的基质干扰,并提供了100ppb的loq。图117a绘制了mrm母子离子对435.1>193.1的强度,其提供的s/n比为105。图117b绘制了mrm母子离子对433.1>191.1的强度,其提供的s/n比为100。图117c绘制了mrm母子离子对433.1>127的强度,其提供的s/n比为110。图117d绘制了mrm母子离子对435.1>127的强度,其提供的s/n比为39。图117e绘制了包含1000ppb浓度氯氰菊酯的农药样品mrm母子离子对433.1>91的强度。mrm母子离子对433.1>91受到基质干扰并提供了20的s/n比。此母子离子对的loq为500ppb。
实施例12.丁酰肼
图17a-图17b是对丁酰肼的产物离子扫描,其前体(母体)离子质量约为161。图17a示出了-30v的高碰撞能量(ce)的产物离子扫描。图17b示出了-15v的低ce的产物离子扫描。
图17c-图17e绘制了包含100ppb丁酰肼(100ppb浓度)的大麻样品三个不同mrm母子离子对的强度。图17c绘制了mrm母子离子对161.1>44的强度,其s/n比确定为180。图17d绘制了mrm母子离子对161.1>101的强度,其s/n比确定为42。图17e绘制了mrm母子离子对161.1>143的强度,其s/n比确定为390。因此,通过使用适当的mrm母子离子对,可以将对丁酰肼的测量灵敏度提高4倍。确定的loq低至11ppb。
图41a-图41d比较了包含100ppb丁酰肼的大麻样品与空白大麻样品测量结果的mrm母子离子对强度。图41a和41c分别比较了包含100ppb丁酰肼的农药样品和空白大麻样品mrm母子离子对161.1>143的强度。图41b和41d分别比较了包含100ppb丁酰肼的农药样品和空白大麻样品mrm母子离子对161.1>44的强度。loq为约10.8ppb。
实施例13.烯酰吗啉
图24a-图24f和图72a-图72d所示的色谱图比较了含有100ppb烯酰吗啉(100ppb浓度)的大麻样品和空白大麻样品的与烯酰吗啉相关的不同mrm母子离子对的强度。对于这些母子离子对的每一个,在包含100ppb烯酰吗啉的大麻样品的强度图中均观察到两个峰(图24a-图24c,图72a、72b)。图24a和24d分别绘制了包含烯酰吗啉的农药样品和空白大麻样品mrm母子离子对388.1>165的强度。第一个较早出现的峰受到基质干扰(即,空白大麻样品的强度图中大约同时出现一个对应的峰;图24d),并且提供的s/n比(约15)比第二个较晚出现的峰提供的s/n比361低。
图24b和24e以及图72a和72c分别绘制了含有烯酰吗啉的农药样品和空白大麻样品mrm母子离子对388.1>273的强度。两个峰均不受基质干扰。对于第一个(较早出现的)峰,s/n比确定为210;且对于第二个(较晚出现的)峰,s/n比为255。
图24c和24f以及图72b和72d分别绘制了含有烯酰吗啉的农药样品和空白大麻样品mrm母子离子对388.1>301的强度。两个峰均不受基质干扰。对于第一个(较早出现的)峰,s/n比为807;且对于第二个(较晚出现的)峰,s/n比为1251。通过使用适当的mrm母子离子对,对烯酰吗啉的检测限提高了10倍,达到了10ppb的loq。
实施例14.二溴磷(naled,“dibrom”)
图16a是示出计算出的二溴磷同位素分布的图,其结构如下所示:
图16b是包含二溴磷的样品的前体(母体)质量扫描。在图16b中,m(378.7峰)、m+2(380.7峰)、m+4(382.7峰)和m+6个(384.7峰)离子的相对丰度分别是42%、100%、91%和36%。
图16c-图16f和图113是包含100ppb二溴磷的大麻样品使用与二溴磷相关的不同mrm母子离子对获得的色谱图。mrm母子离子对380.8>127(图16c)提供了1.44×104的信号(峰)振幅和255的s/n比。mrm母子离子对378.8>127(图16d)提供了5.46×103的信号振幅和96的s/n比。mrm母子离子对380.8>109(图16e)提供了3.57×103的信号振幅和60的s/n比。mrm母子离子对382.8>127(图113)提供了1.38x104的信号和300的s/n比。mrm母子离子对378.8>109(图16f)提供了1.6×103的信号和1230的s/n比。
图60a和60c分别比较了包含二溴磷(100ppb浓度)的农药样品和空白大麻样品mrm母子离子对380.8>109的强度。图60b和60d分别比较了包含100ppb二溴磷的大麻样品和空白大麻样品mrm母子离子对380.8>127的强度。
loq低至约23ppb。
实施例15.n-辛基双环庚烯二甲酰亚胺(“mgk-264”)
图20a和图20b是mgk-264的产物离子扫描。图20a示出了-25v的低碰撞能量的产物离子扫描。图20b示出了-50v的高碰撞能量的产物离子扫描。观察到质量为210.1和质量为98的主要碎片离子。图20c-图20e绘制了包含100ppbmgk-264的大麻样品三个不同mrm母子离子对的强度。使用mrm母子离子对276.2>98(图20c)提供的s/n比为300。使用mrm母子离子对276.2>121(图20d)提供的s/n比为5。使用mrm母子离子对276.2>210(图20e)提供的s/n比为1500。因此,通过使用适当的mrm母子离子对可以使s/n比提高10倍或更多倍。
图85a-图85d比较了包含100ppbmgk-264的大麻样品与空白大麻样品测量结果的mrm母子离子对强度。图85a和85c比较了mrm母子离子对276.2>98的强度,且图85b和85d比较了mrm母子离子对276.2>210.1的强度。loq为约10ppb。
实施例16.丙环唑
对于基于标称q1质量约342da的mrm母子离子对,一些大麻植物提取物的基质干扰水平低于其他一些的基质干扰水平。此实施例提供了可用于检测两种类型的提取物中的丙环唑的mrm母子离子对。
图87a-图87d比较了包含100ppb丙环唑的基质干扰相对较低的大麻样品与空白大麻样品测量结果的mrm母子离子对强度。图87a和87c比较了mrm母子离子对342.1>69的强度,且图87b和87d比较了mrm母子离子对342.1>159的强度。loq为约19ppb,是加州最低行动限100ppb的5.3分之一。
图114a-图114d是四幅比较了在基于标称q1质量342的mrm母子离子对的情况下具有较高基质干扰并包含10ppb丙环唑的大麻样品所测量的两个不同mrm母子离子对的强度与空白大麻样品的测量结果的图。图114a绘制了mrm母子离子对342>69的强度,图114b绘制了mrm母子离子对342>159的强度,且图114d绘制了空白大麻样品mrm母子离子对342>69的强度。如图114c和图114d所示,对于342>69和342>159两个mrm母子离子对,空白大麻样品测量结果中都存在基质干扰峰。
图114e-图114h(10ppb丙环唑)示出了不受基质干扰的两个mrm母子离子对344>69和344>161的强度。图114e和图114f绘制了mrm母子离子对344>69的强度,且图114g和114h绘制了mrm母子离子对344>161的强度。在对应的空白大麻样品测量结果(图114g和图114h)中未观察到农药样品测量结果(图114e和图114f)中存在的强度峰。loq为约10ppb。
图114i-图114l比较了包含100ppb丙环唑的大麻样品的四个mrm母子离子对强度测量结果与空白大麻样品测量结果。图114i-图114l中的每个图绘制了特定mrm母子离子对的强度测量结果。具体来说,mrm母子离子对342>69、342>159、344>69和344>161的测量结果分别在图114i、图114j、图114k和图114l中示出。在图114i-图114l的每个图中,第一迹线绘制了对包含100ppb丙环唑的农药样品测得的mrm母子离子对强度,第二迹线绘制了mrm母子离子对强度。如图114i和图114j所示,mrm母子离子对342>69和342>159受到基质干扰,因为农药样品测量结果中存在的强度峰在空白大麻样品中也存在。相比之下,mrm母子离子对344>69和344>161不受基质干扰。如图114k和图114l所示,在农药样品测量结果中观察到大的信号峰,而空白大麻样品的强度相比之下变化很小。
实施例17.五氯硝基苯(pcnb)和氯丹的apci方法
传统上通过gc-ms分析两种非常疏水且氯化的农药(五氯硝基苯和氯丹),因为它们无法通过带esi源的lc-ms充分电离。此实施例描述了使用apci源来电离五氯硝基苯和氯丹。这种方法也可用于电离溴虫腈。
五氯硝基苯的结构如下所示。
五氯硝基苯不包含任何氢原子,且因此难以使用与lc-ms兼容的技术进行电离,在该技术中质子要么获得要么失去以形成离子。五氯硝基苯也不会形成加合物,且不能获得或失去质子。相反,常规方法依靠具有电子电离(ei)的gcms进行五氯硝基苯的检测和/或定量。
氯丹高度氯化且蛋白质亲和力很低。存在两种形式的氯丹:顺式和反式。这两种形式的氯丹的化学结构如下所示。
在此实施例中,使用apci源以空气作为雾化气体电离五氯硝基苯和氯丹。但是也可以使用空气和/或其他气体诸如氮气、氩气和二氧化碳。
使用具有短lc梯度的快速6分钟lc-ms/ms方法和qsightlc-ms/ms的apci源,在包含100ppb任一农药的大麻样品中,五氯硝基苯和氯丹的loq分别为10和33ppg。
图33a和图33b示出了经由apci形成的五氯硝基苯离子的同位素分布。图33a示出了以负模式经由apci获得的五氯硝基苯的前体(母体)质量扫描。在图33a中,最低质量(273.9)峰对应于[m-cl+o]-。对应于273.9峰、275.9峰、277.8峰和279.9峰的离子相对丰度分别是80.4%、100%、51%和12%。图33b示出了计算出的同位素分布。
图34a和图34b示出了经由apci形成的氯丹离子的同位素分布。图34a示出了经由apci获得的氯丹的前体(母体)质量扫描。在图34a中,对应于437.7峰(m)、439.7峰(m+2)、441.6峰(m+4)、443.8峰(m+6)和445.7峰(m+8)的离子相对丰度分别是34.5%、88.8%、100%、64.4%和25.9%。图34b示出了计算出的分布。
如本文所述,lc方法使用的流动相中添加剂的存在会影响通过公开的apci技术电离的分子所获得的信号水平。在此实施例中,lc方法中添加剂存在对氯丹的影响如图35a和图35b所示。图35a绘制了包含氯丹且使用采用无添加剂的流动相的lc方法分离的样品的前体(母体)质量扫描。图35b绘制了包含氯丹且使用采用含甲酸的流动相的lc方法分离的样品的前体(母体)质量扫描。无添加剂的lc方法观察到良好的信号(图35a),而含添加剂的lc方法未观察到氯丹的信号(图35b)。
图36是示出五氯硝基苯的产物离子扫描的图。图中的各个峰对应于以下离子(相关峰列于括号中):cl35-(35.1)、cl37-(37.1)、[m-cl-c-no2+o-o]-(201.8)、[m-cl-c-no2+o]-(271.8)、[m-cl-no2+o]-(229.9)、[m-cl-cl+o]-(240.9)、[m-cl-no+o]-(245.9)、[m-cl+o]-(275.9),其中m代表五氯硝基苯(quintozene/pentachloronitrobenzene)。
图39是示出在15-100的低质量范围内以负离子模式进入apci源的流动相的背景光谱的图。
不希望受任何特定理论的束缚,我们认为五氯硝基苯在apci源下电离的机理如下:
o2+e-→o2-
m+o2→[m–cl+o]--+clo,其中m代表五氯硝基苯。
不希望受任何特定理论的束缚,我们认为氯丹在apci源下电离的机理如下:
o2+e-→o2-
m+o2→[m+2]-,其中m代表氯丹。
图37a-图37b是使用mrm母子离子对275.8>35.1(图37a,37c)和273.8>35.1(图37b,37d)分析大麻样品中五氯硝基苯的存在的色谱图。图37a和37b是包含100ppb五氯硝基苯的大麻样品。图37c和37d是空白大麻样品。
图38a-图38b是使用mrm母子离子对275.8>35(图38a,38c;定性剂)和273.8>35(图38b,38d;定量剂)分析大麻样品中氯丹的存在的色谱图。图38a和38b是包含100ppb氯丹的大麻样品。图38c和38d是空白大麻样品。
实施例18.长期稳定性
使用配备有双重电喷雾电离源和大气化学电离源(apci)的三重四极杆质谱仪,并结合具有层流接口的被加热的自清洁保持清洁源(self-cleaningstaycleansource),收集了用于大麻中农药和真菌毒素分析的长期稳定性数据。
图120显示了包含100ng/ml二嗪磷的大麻提取物的长期响应(1周)。大麻中农药分析的长期稳定性数据表明,大多数农药和真菌毒素在1周内的响应rsd介于1.5%至20%之间。这些结果证明,lc-ms/ms系统中的被加热的自清洁保持清洁源减少了在脏基质诸如大麻的农药和真菌毒素分析中基于lc-ms/ms方法的维护需求。文献中发表的大多数lc-ms/ms方法和市场上的其他lcms系统都没有显示长期的稳定性数据,也没有说明必须每天或在批量后清洁电喷雾源以保持质谱仪的灵敏度(geis-asteggiante等,j.chromatogr.a,1258,43-54,2012)。此外,在最初的几分钟内以及最后一个峰洗脱后,它们将lc流从ms中转向离开,以减少来自lc柱中未保留和晚洗脱的基质化合物对ms的污染。在这项研究中,获得了出色的长期稳定性数据,而在最初的几分钟内以及运行结束和定期清洁离子源的过程中,没有将lc流从ms中转向。
实施例19.溶剂提取的回收研究
quechers是一种从含水量较高的水果和蔬菜基质中提取低水平污染物诸如农药的方法(anastassiades等,j.aoacint.86(2),412-31,2003)。它能够从这些食品基质中提取多种农药,且有效地去除水果和蔬菜中的糖和其他化合物(chung&chanj.chromatogr.a,1217,4815-24,2010;cunha等,j.sep.sci.30(4),620-26,2007;sapozhinikova,j.agric.foodchem.62,3684-89,2014;wang&cheung,j.aoacint.99(2),539-57,2016;villar-pulido等,talanta85,1419-27,2011)。它不适用于极性极强的农药诸如丁酰肼,丁酰肼已包括在加州和其他州的大麻监测清单中。丁酰肼极性太强,无法用quechers提取程序有效地提取,因为它保留在水相中,并且在盐析步骤中不会分配到有机溶剂中。据报道,用quechers提取法从大麻基质中回收的丁酰肼少于10%(stenerson&oden,cann.sci.&tech.1(1),48-53,2018)。此外,大麻基质中主要含有疏水性化合物诸如大麻素和萜烯,因此quechers提取方法在盐析步骤中不会去除大量基质化合物。不同的小组已尝试采用d-spe步骤开发先进的quechers方法,所述d-spe步骤利用psa和其他吸附剂从大麻提取物中去除基质(例如kowlaski等,lcgc35(5)8-22,2017;wang等,lcgc34(10),20-7,2016)。这些化合物在d-spe步骤中与psa吸附剂结合,且因此回收率较差。
由于quechers方法从大麻基质中提取农药的上述缺点,我们采用了一种简单的基于乙腈的溶剂提取法从大麻基质中提取农药。产生了强化的大麻花样品,以确定农药和黄曲霉毒素(aflatoxin)的回收率。对大麻花样品进行了测试以确认其在用农药加标之前不含这些农药。五个大麻花样品加标了2个水平(低和高)的所有农药(0.1和1μg/g)和真菌毒素(0.02和0.1μg/g)标准品。根据加州和其他州的监管限值,针对大麻中的农药和真菌毒素选择了这两个水平。表9、10和11表明,在2个不同水平下,5个大麻花样品所有66种农药和5种真菌毒素的绝对回收率在70%-120%的可接受范围内,rsd小于20%。对于3种农药,低加标值没有报告回收率值,因为它低于其loq值。
表9.采用乙腈溶剂提取法在2个不同水平从大麻中回收ii类农药
表10.采用乙腈溶剂提取法在2个不同水平从大麻中回收ii类真菌毒素
表11.采用乙腈溶剂提取法在2个不同水平从大麻中回收i类农药
实施例20.定量
图31是示出所分析农药的总体回收范围的条形图。如图所示,93%的农药的总回收率值在80%至120%之间(72种农药中49种总回收率值在80%至120%之间,72种农药中18种总回收率值在60%至80%之间)。这些计算是基于仅10种内标的混合物的使用。使用本说明书中公开的内标混合物有可能将其余5种农药(总回收率值低于60%的那些)的回收率提高到60%至120%范围内的值。例如,图32a和图32b分别示出了(i)包含大麻植物材料(大麻基质)的样品和(ii)溶剂(不含大麻植物材料)中浓度范围为0.1-120ppb的嘧菌酯的校准曲线。
上表9-表11以及图40a和图40b总结了本公开中分析的农药的检测和/或定量结果。图40a和图40b绘制了获得不同范围内loq的各种农药数量。在图40a中,loq是使用定量剂和定性剂母子离子对来确定的,而在图40b中,loq仅基于定量剂母子离子对来确定。
表12、13和14总结了大麻提取物中epaii类农药(中度毒性和中度刺激性)、epai类农药(剧毒和强刺激性)和真菌毒素中每一者的定量限(loq)和在loq水平上的响应重现性。通过同时考虑定量剂和定性剂离子的信号(两者的信噪比s/n>10)并确保产物离子比率在预期比率的20%公差窗口内来确定loq。
表12.ii类农药的loq。
*通常使用gc-ms/ms分析。
表13.ii类真菌毒素的loq
表14.i类农药的loq
*通常使用gc-ms/ms分析。
实施例21.计算机系统与网络环境
在图4中,示出并描述了用于提供本文所述的系统和方法的网络环境400的实现。现在参考图4,在简要概述中示出并描述了示例性云计算环境400的框图。云计算环境400可以包括一个或多个资源提供者402a、402b、402c(统称为402)。每个资源提供者402可以包括计算资源。在一些实现方式中,计算资源可以包括用于处理数据的任何硬件和/或软件。例如,计算资源可以包括能够执行算法、计算机程序和/或计算机应用程序的硬件和/或软件。在一些实现方式中,示例性计算资源可以包括具有存储和检索功能的应用程序服务器和/或数据库。每个资源提供者402可以连接到云计算环境400中的任何其他资源提供者402。在一些实现方式中,资源提供者402可以通过计算机网络408连接。每个资源提供者402可以通过计算机网络408连接到一个或多个计算设备404a、404b、404c(统称为404)。
云计算环境400可以包括资源管理器406。资源管理器406可以通过计算机网络408连接到资源提供者402和计算设备404。在一些实现方式中,资源管理器406可以促进一个或多个资源提供者402向一个或多个计算设备404提供计算资源。资源管理器406可以从特定的计算设备404接收对计算资源的请求。资源管理器406可以标识能够提供计算设备404所请求的计算资源的一个或多个资源提供者402。资源管理器406可以选择资源提供者402以提供计算资源。资源管理器406可以促进资源提供者402与特定的计算设备404之间的连接。在一些实现方式中,资源管理器406可以建立特定的资源提供者402与特定的计算设备404之间的连接。在一些实现方式中,资源管理器406可以使用所请求的计算资源将特定的计算设备404重定向到特定的资源提供者402。
图5示出了可用于实现本公开中描述的技术的计算设备500和移动计算设备550的实例。计算设备500旨在代表各种形式的数字计算机,诸如膝上型计算机、台式计算机、工作站、个人数字助理、服务器、刀片服务器、大型机和其他适当的计算机。移动计算设备550旨在代表各种形式的移动设备,诸如个人数字助理、蜂窝电话、智能手机和其他类似的计算设备。此处显示的组件、它们的连接和关系以及它们的功能仅是示例性实例,而非限制性的。
计算设备500可以包括处理器502、存储器504、存储设备506、连接到存储器504和多个高速扩展端口510的高速接口508,以及连接到低速扩展端口514和存储设备506的低速接口512。处理器502、存储器504、存储设备506、高速接口508、高速扩展端口510和低速接口512中的每一者可以使用各种总线互连,并且可以安装在共同主板上或以其他适当方式互连。处理器502可以处理用于在计算设备500内执行的指令,包括存储在存储器504中或存储设备506上的指令,以将图形用户界面(gui)的文本和/或图形信息显示在外部输入/输出设备(诸如耦接至高速接口508的显示器516)上。在其他实现方式中,可以适当地使用多个处理器和/或多个总线,以及多个存储器和存储器类型。并且,可以连接多个计算设备,每个设备提供必要操作的一部分(例如,作为服务器阵列(serverbank)、一组刀片服务器或多处理器系统)。因此,当本文使用术语时,在多个功能被描述为由“处理器”执行的情况下,这涵盖了其中所述多个功能由任意数量的计算设备(一个或多个)的任意数量的处理器(一个或多个)执行的实施方案。此外,在将一种功能描述为由“处理器”执行的情况下,这涵盖了其中该功能由任意数量的计算设备(一个或多个)(例如,在分布式计算系统中)的任意数量的处理器(一个或多个)执行的实施方案。
存储器504将信息存储在计算设备500内。在一些实现方式中,存储器504是一个或多个易失性存储单元。在一些实现方式中,存储器504是一个或多个非易失性存储单元。存储器504也可以是另一种形式的计算机可读介质,诸如磁盘或光盘。
存储设备506能够为计算设备500提供大容量存储。在一些实施方式中,存储设备506可以是或包含计算机可读介质诸如软盘设备、硬盘设备、光盘设备或磁带设备、闪存或其他类似的固态存储设备,或设备阵列(包括存储区域网络或其他配置中的设备)。指令可以存储在信息载体中。指令在由一个或多个处理设备(例如,处理器502)执行时,执行一种或多种诸如上述方法的方法。指令也可以由一个或多个存储设备诸如计算机或机器可读介质(例如,存储器504、存储设备506或处理器502上的存储器)存储。
高速接口508可以管理计算设备500的带宽密集型操作,而低速接口512可以管理较低带宽密集型操作。这种功能分配仅是一个实例。在一些实现方式中,高速接口508可以耦接到存储器504、显示器516(例如,通过图形处理器或加速器),并且可以耦接到可以接受各种扩展卡(未示出)的高速扩展端口510。在一些实现方式中,低速接口512可以耦接到存储设备506和低速扩展端口514。可以包括各种通信端口(例如,usb、
如图所示,可以以多种不同形式来实现计算设备500。例如,它可以被实现为标准服务器520,或者在一组这样的服务器中多次实现。另外,它可以在诸如膝上型计算机522的个人计算机中实现。它也可以被实现为机架服务器系统524的一部分。或者,来自计算设备500中的组件可以与诸如移动计算设备550的移动设备(未示出)中的其他组件组合。每一个这样的设备都可以包含计算设备500和移动计算设备550中的一者或多者,并且整个系统可以由彼此通信的多个计算设备组成。
移动计算设备550可以包括处理器552、存储器564、输入/输出设备诸如显示器554、通信接口566和收发器568,以及其他组件。移动计算设备550也可提供有存储设备诸如微驱动器或其他设备,以提供附加的存储。处理器552、存储器564、显示器554、通信接口566和收发器568中的每一者可以使用各种总线互连,并且这些组件中的几个可以被安装在共同主板上,或以其他合适的方式互连。
处理器552可以在移动计算设备550内执行指令,包括存储在存储器564中的指令。处理器552可以被实现为芯片组,其包括单独的以及多个模拟和数字处理器。处理器552可以提供例如用于移动计算设备550的其他组件的协调,诸如对用户接口、由移动计算设备550运行的应用程序以及由移动计算设备550进行的无线通信的控制。
处理器552可以通过耦接到显示器554的控制接口558和显示接口556与用户通信。显示器554可以是例如tft(薄膜晶体管液晶显示器)显示器或oled(有机发光二极管)显示器或其他适当的显示技术。显示接口556可以包括用于驱动显示器554以向用户呈现图形和其他信息的适当电路。控制接口558可以接收来自用户的命令并且将它们转换以提交给处理器552。另外,外部接口562可以提供与处理器552的通信,以便实现移动计算设备550与其他设备的近区域通信。外部接口562可以在一些实现方式中提供例如有线通信,或者在其他实现方式中提供无线通信,并且也可以使用多个接口。
存储器564将信息存储在移动计算设备550内。存储器564可以被实现为计算机可读介质、易失性存储单元或非易失性存储单元中的一者或多者。也可以提供扩展存储器574,并通过扩展接口572将其连接到移动计算设备550,所述扩展接口572可以包括例如sd卡和/或simm(单列直插式内存模块)卡接口。扩展存储器574可以为移动计算设备550提供额外的存储空间,或者也可以为移动计算设备550存储应用程序或其他信息。具体地说,扩展存储器574可以包括用于执行或补充上述过程的指令,并且也可以包括安全信息。因此,例如,扩展存储器574可以被提供作为用于移动计算设备550的安全模块,并且可以用允许安全使用移动计算设备550的指令来编程。此外,可以经由simm卡提供安全的应用程序以及其他信息,诸如以不可破解的方式将标识信息放在simm卡上。
存储器可以包括例如闪存和/或nvram存储器(非易失性随机存取存储器),如下面所讨论。在一些实现方式中,指令被存储在信息载体中。指令在由一个或多个处理设备(例如,处理器552)执行时,执行一种或多种诸如上述方法的方法。指令也可以由一个或多个存储设备诸如一个或多个计算机或机器可读介质(例如,存储器564、扩展存储器574或处理器552上的存储器)存储。在一些实现方式中,可以例如通过收发器568或外部接口562在传播的信号中接收指令。
移动计算设备550可以通过通信接口566进行无线通信,所述通信接口566在必要处可以包括数字信号处理电路。通信接口566可以提供各种模式或协议下的通信,诸如gsm语音呼叫(全球移动通信系统)、sms(短消息服务)、ems(增强消息服务)或mms消息(多媒体消息服务)、cdma(码分多址)、tdma(时分多址)、pdc(个人数字蜂窝)、wcdma(宽带码分多址)、cdma2000或gprs(通用分组无线业务)等。例如,可以使用射频通过收发器568进行这种通信。此外,可能会发生短距离通信,诸如使用
移动计算设备550也可以使用音频编解码器560在听觉上进行通信,所述音频编解码器560可以从用户接收口语信息并将其转换为可用的数字信息。音频编解码器560同样可以为用户生成可听见的声音,诸如通过扬声器,例如,在移动计算设备550的听筒中。这样的声音可以包括来自语音电话呼叫的声音,可以包括录制的声音(例如,语音消息、音乐文件等),并且也可以包括由在移动计算设备550上运行的应用程序生成的声音。
如图所示,可以以多种不同形式来实现移动计算设备550。例如,它可以被实现为蜂窝电话580。它也可以被实现为智能手机582、个人数字助理或其他类似移动设备的一部分。
此处描述的系统和技术的各种实现方式可以通过数字电子电路、集成电路、专门设计的asic(专用集成电路)、计算机硬件、固件、软件和/或其组合来实现。这些各种实现方式可以包括在一个或多个计算机程序中的实现方式,所述一个或多个计算机程序在包括至少一个可编程处理器的可编程系统上是可执行的和/或可解释的,所述可编程处理器可以是专用的或通用的,其被耦接以从存储系统、至少一个输入设备和至少一个输出设备接收数据和指令以及向其发送数据和指令。
这些计算机程序(也称为程序、软件、软件应用程序或代码)包括用于可编程处理器的机器指令,并且可以使用高级过程式和/或面向对象的编程语言和/或使用汇编/机器语言来实现。如本文所使用的术语机器可读介质和计算机可读介质是指用于向可编程处理器提供机器指令和/或数据的任何计算机程序产品、装置和/或设备(例如磁盘、光盘、内存、可编程逻辑器件(pld)),其包括接收机器指令作为机器可读信号的机器可读介质。术语机器可读信号是指用于向可编程处理器提供机器指令和/或数据的任何信号。
为了提供与用户的互动,这里描述的系统和技术可以在计算机上实现,所述计算机具有向用户显示信息的显示设备(例如,crt(阴极射线管)或lcd(液晶显示器)监视器)以及用户可以通过其向计算机提供输入的键盘和指点设备(例如,鼠标或轨迹球)。其他类型的设备也可用来提供与用户的互动;例如,提供给用户的反馈可以是任何形式的感官反馈(例如,视觉反馈、听觉反馈或触觉反馈);并且来自用户的输入可以以任何形式被接收,包括声音、语音或触觉输入。
本文描述的系统和技术可以在计算系统中实现,所述计算系统包括后端组件(例如,作为数据服务器),或包括中间件组件(例如,应用程序服务器),或包括前端组件(例如,具有图形用户界面或网页浏览器的客户端计算机,用户可以通过其与本文描述的系统和技术的实现方式互动),或这种后端、中间件或前端组件的任何组合。系统的组件可通过任何形式或介质的数字数据通信(例如,通信网络)互连。通信网络的实例包括局域网(lan)、广域网(wan)和互联网。
所述计算系统可包括客户端和服务器。客户端和计算机一般相互是远程且通常通过通信网络进行交互。客户端和服务器的关系通过在各自计算机上运行且使相互具有客户端服务器关系的计算机程序而产生。
在一些实现方式中,各种模块可以被分开、组合或并入单个或组合的模块中。图中描绘的任何模块都不旨在将本文描述的系统限于其中示出的软件架构。
- 还没有人留言评论。精彩留言会获得点赞!