液相色谱串联质谱对血液中环孢素A浓度的检测方法与流程
液相色谱串联质谱对血液中环孢素a浓度的检测方法
技术领域
1.本发明涉及生物检测技术领域,尤其涉及一种采用液相色谱串联质谱对血液中环孢素a浓度的检测方法。
背景技术:
2.环孢素a(cyclosporin,csa,别名环孢霉素a,环孢菌素a,环孢多肽a,环孢灵等等)由11个氨基酸组成的环状多肽组成,属于强效免疫抑制剂。临床上主要用于肝、肾以及心脏移植的抗排异反应,也可与肾上腺皮质激素同用,治疗免疫性疾病。ca作为一种强效免疫抑制剂,近年来人们对它的研究越来越多,发现它还可用来治疗自身免疫性疾病、血液病及抗寄生虫病等。
3.治疗药物监测(therapeutic drug monitoring, tdm)是在药物动力学原理的指导下,应用现代先进的分析技术,测定血液中或其他体液中药物浓度,用于设计或调整给药方案,同时也有助于解释为什么某种药物在常用量时不能产生疗效或发生意外中毒,从而把经验式临床用药提高到科学性较高的水平,以提高药物的疗效和减少不良反应的发生。tdm既是保证治疗充分的重要手段,又是避免过度药物暴露、减少药物相关不良反应的重要措施。液相色谱串联质谱(lc-ms/ms)方法具有特异性强、准确度高、快速测定的特点,常被用来进行药物浓度测定。
4.然而,环孢素a服用剂量过高会产生很多副作用,如下所示:一、肾毒性是环孢素a最为重要的毒副作用,其表现多样,可表现为短时性、功能性和急性器质性病变,在临床上表现为慢性非进行性或慢性进行性肾功能不全。环孢素a可引起轻度肝功能损害,肝功能损害的程度同环孢素a剂量有关,减量或停药后可恢复正常。环孢素a引起的高胆红素血症可能因胆汁排出受阻引起的。
5.二、由于服用环孢素a引起胆汁增多,胆囊结石的发生率增高。环孢素a可对神经系统产生毒性,最常见的是不自主的震颤,发生率约为22%,常是环孢素a过量的表现。
6.三、环孢素a导致的电解质异常主要包括高钾血症、高氯血症、低镁血症和钠排减少等。其原因主要是由于环孢素a对肾小管的毒性引起。环孢素a还可以引发高血压、高脂血症、高尿酸血症及多毛症。另外牙龈增生的出现率较高等。
技术实现要素:
7.基于上述问题,本发明所要解决的问题在于提供一种基于液相色谱串联质谱(lc-ms/ms)方法对于人体血液中环孢素a浓度的检测方法,该方法能够准确、快速的对血液中环孢素a浓度进行有效检测,为后续临床用药提供的合理性参考。
8.本发明的技术方案如下:一种采用液相色谱串联质谱对血液中环孢素a浓度的检测方法,其特征在于, 包括如下步骤:获取含环孢素a的待检测血液样本;
分别对液相色谱和质谱进行液相色谱串联质谱参数的设置及优化;将待测血液样本溶液进样至液相色谱仪串联质谱仪中,随流动相流动并进行检测分析,获得待测血液样本中的环孢素a浓度曲线;采用标准曲线法,根据待测血液样本中的环孢素a峰面积/内标峰面积比值,计算出血液中环孢素a浓度。
9.一实施例,所述检测方法中,所述待检测血液样本由以下步骤制得:将装有全血样本的采集管上下颠倒,量取血液,并制作空白全血;取同浓度的环孢素a标准品储备液和环孢素a质控品储备液分别加入所述空白全血中,混匀,制备得到环孢素a标准品和质控品工作液;量取环孢素a标准品和质控品工作液加入离心管底部,再往离心管中加入超纯水,经涡旋、超声后,加入环孢素a_d12内标工作液,再次涡旋、离心处理后取上清液并加入萃取剂,继续涡旋、离心处理,再取上层液体加入复溶液,继续涡旋、冷冻离心处理后,将上清液移转至进样瓶中,获得待检血样样本。
10.一实施例,所述检测方法中,所述环孢素a标准品和质控品工作液制备步骤中还包括如下步骤:将环孢素a与甲醇混匀,配置成两份同浓度的储备液,一份作为环孢素a标准品储备液,一份作为环孢素a质控品储备液;分别量取所述环孢素a标准品储备液、环孢素a质控品储备液与空白全血混匀,制得所述环孢素a标准品和质控品工作液。
11.一实施例,所述检测方法中,所述环孢素a标准品和质控品工作液制备步骤中,所述环孢素a标准品储备液、所述环孢素a质控品储备液的体积数分别与空白全血的体积数之比为1:19。
12.一实施例,所述检测方法中,所述环孢素a_d12内标工作液采用如下步骤制得:移取环孢素a_d12内标准品,加入甲醇,混匀,配制成环孢素a_d12内标准品储备液;移取所述环孢素a_d12内标准品储备液,加入甲醇沉淀剂ii及0.1m浓度的硫酸锌溶液沉淀剂ⅰ,混匀,配制成所述环孢素a_d12内标工作液,备用。
13.一实施例,所述检测方法中,所述环孢素a_d12内标工作液涡旋、离心处理过程中,加入的萃取剂为正己烷与乙酸乙酯混合溶液。
14.一实施例,所述检测方法中,所述液相色谱串联质谱参数设置和优化步骤中,质谱条件为:正离子模式工作,cad为2-5,cur为15-25,gs1为40-55,gs2为40-55,is为4000-6000,tem为300-500
°
c;及液相色谱条件为:色谱柱:phenomenex kinetex
®
xb-c18柱,5μm,150mm * 4.6 mm,柱温:60
°
c。
15.一实施例,所述检测方法中,所述液相色谱串联质谱检测分析步骤中,在液相色谱仪中进行流动的流动相采用如下步骤制得:配制流动相a:2 mm乙酸铵水溶液含0.1%甲酸;配制流动相b:2 mm乙酸铵甲醇溶液含0.1%甲酸;将所述流动相a和流动相b混合,制得流动相;优选地,所述流动相的速度为0.6ml/min;每次过渡的驻留时间为30-45ms。
16.一实施例,所述检测方法中,移取体积比3:7的所述流动相a和流动相b,混匀,获得所述复溶液,置于常温保存15天备用。
17.一实施例,所述检测方法中,采用标准曲线法时,还需要制作环孢素a的标准曲线,其步骤如下:将环孢素a加入甲醇中,配制7个不同浓度:25ng/ml,50 ng/ml,100ng/ml,250ng/ml,500ng/ml,1000ng/ml,2000ng/ml的标准曲线,制备三份;随后分三个批次进样到液相色谱-质谱中,绘制出环孢素a的标准曲线。
18.本发明提供的采用液相色谱串联质谱对血液中环孢素a浓度的检测方法,具有如下有点:1、检测前处理方法相对简单,一天可以同时处理多批样本;2、仪器上机时间短,分析一针样本只需6.5分钟,一天可以分析上百个样本;3、可以满足大量样本的同时检测,时效性更短;4、在25-2000 ng/ml,检测范围比较广,满足所有血液中环孢素a样本的检测。
附图说明
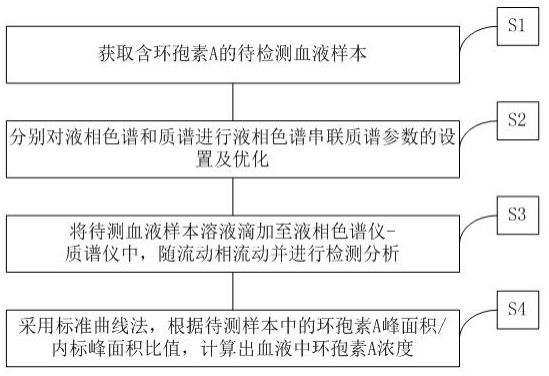
19.图1为本发明提供的血液中环孢素a浓度的检测工艺流程图;图2是本发明实施例环孢素a标准曲线。
具体实施方式
20.下面结合附图,对本发明的较佳实施例作进一步详细说明。
21.如图1所示,一种采用液相色谱串联质谱对血液中环孢素a浓度的检测方法,包括如下工艺步骤:s1、获取含环孢素a的待检测血液样本;s2、分别对液相色谱和质谱进行液相色谱串联质谱参数的设置及优化;s3、将待测血液样本溶液进样至液相色谱仪串联质谱仪中,随流动相流动并进行检测分析,获得待测血液样本中的环孢素a浓度曲线;s4、采用标准曲线法,根据待测样本中的环孢素a峰面积/内标峰面积比值,计算出血液中环孢素a浓度。
22.具体操作中,上述采用液相色谱串联质谱检测环孢素a血液药物浓度的方法,具体工艺步骤如下:(1)、标准曲线配制:配制7个浓度的环孢素a:25ng/ml,50 ng/ml,100ng/ml,250ng/ml,500ng/ml,1000ng/ml,2000ng/ml的标准曲线,制备三份;随后分三个批次进样到液相色谱-质谱中,绘制出环孢素a的标准曲线。
23.(2)、使用采集管,采集正常人血液后,将装有全血样本的采集管上下颠倒,量取血液,并制作空白全血。
24.(3)、环孢素a标准品储备液、质控品储备液的配制:量取20 μl 1mg/ml的环孢素a与甲醇混匀,配制成40 μg/ml的环孢素a标准品储备液;
量取20 μl 1mg/ml的环孢素a与甲醇混匀,制备成40 μg/ml的环孢素a质控品储备液。
[0025] (4)、环孢素a标准品和质控品工作液的配制:分别量取步骤(3)中得到的同浓度的环孢素a标准品储备液、环孢素a质控品储备液与步骤(2)得到的空白全血混匀,制得所述环孢素a标准品和质控品工作液;其中,量取同浓度的环孢素a标准品储备液、环孢素a质控品储备液的体积数分别为10 μl,量取空白全血的体积数为190 μl。
[0026]
(5)、硫酸锌溶液沉淀剂i的配制:称取1.438 g znso4·
7h2o于玻璃试剂瓶中,用50 ml超纯水溶解,配制成100 mm的硫酸锌水溶液,置于常温保存1个月。
[0027]
(6)、甲醇沉淀剂ii的配制:量取50 ml甲醇于玻璃试剂瓶中,置于常温保存1个月。
[0028]
(7)、环孢素a_d12内标工作液的配制:移取100 μl 0.1 mg/mlcsa_d12内标准品,加入甲醇,混匀,配制成10 μg/ml环孢素a _d12内标准品储备液,即ss1溶液;再移取100 μl环孢素a _d12内标准品储备液,加入体积量比为2:1的19900 μl甲醇沉淀剂ii与0.1m硫酸锌混合溶液沉淀剂i,混匀,配制成50 ng/ml的环孢素a _d12的内标工作液,转入棕色滴瓶中,备用。
[0029] (8)、萃取剂的配制:量取50 ml正己烷,乙酸乙酯于玻璃试剂瓶中,置于常温保存1个月;(9)、流动相的配制: a. 流动相a:2 mm乙酸铵的水溶液加0.1%的甲酸。
[0030]
称取0.154 g乙酸铵置于标配的流动相试剂瓶a中,用1000 ml超纯水溶解,加入1 ml甲酸。上下颠倒10次,混合均匀,超声脱气5 min,室温下可保存15天。
[0031] b. 流动相b:2 mm乙酸铵的甲醇溶液加0.1%的甲酸。
[0032]
称取0.154 g乙酸铵置于标配的流动相试剂瓶b中,用1000 ml甲醇溶解,加入1 ml甲酸,上下颠倒10次,混合均匀,超声脱气5 min,室温下可保存30天。
[0033]
(10)、复溶液的配制:移取6 ml流动相a和14 ml流动相b,混匀,得到复溶液,置于常温保存15天。
[0034]
(11)、待检测血液样本预处理:a.取样前,将装有全血样本的采集管上下颠倒5次。
[0035]
b.移取环孢素a标准品和质控品工作液200 μl于1.5 ml离心管底部中,再加入200 μl超纯水,涡旋10 s,放入到小离心机中瞬离5 s;c.离心后,使用浮漂将环孢素a标准品和质控品工作液放置在超声仪中,超声30 s;d.超声完成后,加入400 μl环孢素a_d12内标工作液,涡旋1 min,常温静置15 min,然后再涡旋1 min;e.然后放置在冷冻离心机中,13000 rpm,4℃离心15 min;f.离心完成后,取上清500 μl至2 ml离心管中,加入1000 μl萃取剂,涡旋2 min;
然后放置在冷冻离心机中,13000 rpm,4℃离心10 min;g.离心完成后,取800 μl上层液体至1.5 ml离心管中,氮气吹干;h.加入200 μl复溶液,涡旋1 min,放置在冷冻离心机中,13000 rpm,4℃离心5 min;i.取上清液150 μl,获得待检测血液样本,到装有内插管的1.5 ml进样瓶中,备用。
[0036]
(12)、设置液相色谱-质谱条件:按照液相色谱条件和质谱条件,进行液相色谱串联质谱参数的设置和优化;将30 μl待测血液样本溶液进样至液相色谱仪串联质谱仪中,随流动相流动并进行检测分析。
[0037]
(13)、待检测血液样本中环孢素a血药浓度计算:采用标准曲线法,根据待测样本中的免疫抑制剂环孢素a峰面积/内标峰面积比值即可计算出全血中免疫抑制剂环孢素a的药物浓度。
[0038]
进一步的,所述步骤(12)中质谱条件为:正离子模式工作,cad为2-5,cur为15-25,gs1为40-55,gs2为40-55,is为4000-6000,tem为300-500
°
c;进一步的,所述步骤(12)中液相色谱条件为:色谱柱:phenomenex kinetex
®
xb-c18柱,5μm,150mm * 4.6 mm,柱温:60
°
c。
[0039]
进一步的,所述步骤(12)中液相色谱的流动相a:2 mm乙酸铵水溶液含0.1%甲酸;流动相b:2 mm乙酸铵的甲醇溶液中含0.1%甲酸;梯度洗脱;流动液相的流速:0.6ml/min。
[0040]
进一步的,lc-ms/ms条件中,即使用液相色谱仪和质谱仪进行检测分析时,每次过渡的驻留时间为20ms,并通过多反应监测(mrm)。
[0041]
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
[0042]
实施例:人类血液样本中环孢素a血药浓度的测定方法:1.药品和试剂:环孢素a(c-093,supelco)、环孢素a_d12(cms-m1102)购自上海谱芬生物科技有限公司,znso4
·
7h2o(z165065-500g)、正己烷(h109655-500ml)、乙酸乙酯(e116136-500ml)、乙酸铵(色谱纯)、甲酸(色谱纯 )、甲醇(色谱纯)、乙腈(色谱纯)、异丙醇(色谱纯)购自上海阿拉丁生化科技股份有限公司。
[0043]
2.仪器和条件:色谱柱kinetex
®ꢀ5µ
m xb-c18 100
ꢀå
, lc column 150 * 4.6 mm(00f-4605-e0,phenomenex),进样瓶套装购自上海恬甜生物技术有限公司。
[0044]
液相设置条件:色谱柱采用kinetex
®ꢀ
xb-c18 100
ꢀå
, lc column(5
µ
m,150*4.6 mm);流动相a:2 mm乙酸铵水溶液含0.1%甲酸;流动相b:2 mm乙酸铵的甲醇溶液中含0.1%甲酸;进样体积为30
ꢀµ
l;梯度洗脱程序如表1所示。
[0045]
表1 梯度洗脱时间程序表
质谱设置条件:使用带有esi源的ab sciex 3200md质谱仪,采用正离子mrm模式进行扫描。具体参数如下:cad为3,cur为20,gs1为45,gs2为45,is为5000,tem为400
°
c。
[0046]
3. 环孢素a标准品储备液、质控品储备液配制:移取20 μl 1mg/ml的环孢素a加入甲醇,混匀,配制成40 μg/ml的环孢素a标准品储备液;移取20 μl 1mg/ml的环孢素a加入甲醇,混匀,配制成40 μg/ml的环孢素a质控品储备液。
[0047]
4. 环孢素a标准品和质控品工作液配制:取相同浓度的环孢素a标准品储备液、环孢素a质控品储备液各10 μl,加入190 μl空白全血,混匀,制备得到环孢素a标准品和质控品工作液。
[0048]
5. 环孢素a_d12内标工作液配制:移取100 μl 0.1 mg/ml环孢素a_d12内标准品,加入甲醇,混匀,配制成10 μg/ml环孢素a_d12的内标准品储备液;再移取100 μl环孢素a _d12内标准品储备液,加入体积量比为2:1的19900 μl甲醇沉淀剂ii与0.1m硫酸锌混合溶液沉淀剂i,混匀,配制成50 ng/ml的环孢素a _d12的内标工作液,转入棕色滴瓶中,备用。
[0049]
6.方法学验证:6.1 线性:配制7个浓度的环孢素a:25ng/ml,50 ng/ml,100ng/ml,250ng/ml,500ng/ml,1000ng/ml,2000ng/ml的标准曲线,制备三份,分三个批次进样。
[0050]
结果:从图2中可以看到,环孢素a的标准曲线线性 y=0.0108x+0.0108(r=0.9982),在环孢素a 25-2000 ng/ml的线性范围内,三批线性准确度基本都在标示值的85%-115%,相关系数r》0.995,线性良好。所以确定环孢素a标准曲线的线性范围为25-2000 ng/ml。
[0051]
6.2残留:配制双空白样品及标准曲线样品,在标准曲线最高点进样后,再进双空白样品。
[0052]
结果:环孢素a残留为lloq面积的0.12%。内标残留为内标响应的0.01%,符合残留要求,如表2所示。
[0053]
表2 环孢素a残留结果表
6.3 lloq确定:配制标准曲线最低点样本,10个平行进行分析。
[0054]
结果:环孢素a分析物浓度为25 ng/ml,测定浓度平均值为25.75ng/ml,lloq样本的准确度为103%,精密度cv为7.14%,所以确定环孢素a的lloq确定为25 ng/ml。
[0055]
6.4 准确度及精密度:使用空白基质配制低、中、高质控样本,每个浓度6个平行,3个分析批次,3天进行。
[0056]
结果:环孢素aqcl,qcm,qch的批内批间准确度都在93%-103%,批内批间精密度cv都小于7%,准确度及精密度良好,如表3所示。
[0057]
表3 环孢素a批内批间准确度及精密度6.5 提取回收率:空白全血添加待测药物配制成低、中、高浓度样本,加入内标进行处理,采集数据,计算其峰面积a1;空白全血提取后添加待测药物与内标配制成与上述样本浓度一致的样本,采集数据,计算峰面积a2,提取回收率=a1/a2*100%;每个浓度样本平行三份。
[0058]
结果:环孢素a分析物和内标的回收率分别为75%和71%,回收率一致。精密度cv都小于15%,说明内标适用,如表4所示。
[0059]
表4 环孢素a提取回收率结果
6.6基质效应:使用六批不同供体的空白基质配制低浓度样品及高浓度样品,低浓度和高浓度样品比较分析物及内标的基质因子。
[0060]
结果:经过内标归一化的环孢素a六批基质因子的cv小于15%,如表5所示。
[0061]
表5 环孢素a基质效应结果7. 商用质控验证:检测2次商用质控,2次商用质控测定的环孢素a的值都在商用质控范围内,即第一次商用质控测定浓度为101ng/ml,第二次商用质控测定浓度为100ng/ml,在商用质控范围84.2-126ng/ml之间,说明本方法可以准确检测样本。
[0062]
本发明开发了一种检测人体血液中环孢素a药物浓度的方法。该方法操作简单,可在3个小时内完成检测实验,测量结果准确度高,能够准确快速的对血药浓度环孢素a进行有效监测。
[0063]
同时该方法相对简单,一天可以同时处理多批样本。仪器上机时间短,分析一针样本只需6.5分钟,一天可以分析上百个样本。所以本方案可以满足大量样本的同时检测,时效性更短,得到检测结果后,医生即可及时高效的调整用药方案,既能有效控制病情的发作与恶化,又能减少不良反应或其他毒副作用的发生。
[0064]
应当理解的是,上述针对本发明较佳实施例的表述较为详细,并不能因此而认为是对本发明专利保护范围的限制,本发明的专利保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1