用于LAM化学发光免疫的检测试剂盒及方法与流程
用于lam化学发光免疫的检测试剂盒及方法
技术领域
1.本发明属于检测领域,具体涉及一种用于lam化学发光免疫的检测试剂盒及方法。
背景技术:
2.脂阿拉伯甘露聚糖(lipoarabinomannan,lam)是结核分枝杆菌细胞壁中的重要组成部分,达15毫克/g 细菌总重量,包含9个单克隆抗体结合表位,属结合分枝杆菌特异性抗原。lam可通过肾脏过滤,可从尿液中检测到,尿液无菌且易获得,且lam是一种具有热稳定性的抗原,即使在煮沸的尿液中,也可以通过敏感的免疫学技术检测到。研究表明,尿液lam检测可以提高活动性结核病的诊断的准确性。现有通过检测hiv患者尿液中的lam抗原来诊断结核病的方法先后获得多个科学家和who的认可,全球范围内已有比较成熟的产品包括美国的 alere determined
ꢀ™ꢀ
tb lam ag 和日本的fujifilm silvamp tb lam 。alere determined
ꢀ™ꢀ
tb lam ag产品基于胶体金方法学,在hiv感染者组中当cd4细胞》200个/ul,检测的敏感性和特异性分别为4%和99%(alere产品说明书)。fujifilm silvamp tb lam产品基于免疫层析及胶体金方法学,在hiv感染者组中当cd4细胞》200个/ul,灵敏度为36%,特异性99%(li z,tong x,liu s,et al.the value of fujilam in the diagnosis of tuberculosis: a systematic review and meta-analysis.[j].front public health,2022,:757133.)。现有的这两款检测患者尿液中的lam抗原来诊断结核病的产品也只推荐用于艾滋病患者的结核病筛查,不能用于非艾滋病患者的结核病筛查。现有市面上对于非艾滋病患者病人的结核病筛查,除了常规痰涂、痰培、gene xpert等常规检测方法外,并没有基于尿液lam对于未感染hiv人群的结核病筛查项目。基于尿液中lam的结核病筛查,已有注册产品均应用于hiv阳性患者中。因尿液中lam含量较低,对于检测该指标的试剂灵敏度要求较高,同时因尿液样本中盐、尿素、脂肪、糖类等物质的存在会对检测结果造成一定的影响。现有结核杆菌检测方法,周期长、操作繁琐、且收费昂贵,样本来源为血液、痰或其他组织液,均为有创获取。除此之外,市面上的尿液检测产品主要应用于hiv+患者人群,检测方法为胶体金,该两种产品均应用于辅助诊断活动性结核患者,但检测灵敏度偏低、在hiv+患者中阳性检出率也较低,此外检验人群限定为hiv阳性患者,尤其是并发hiv感染和低cd4+t淋巴细胞计数的重症患者(传染病医院或者icu)等问题。化学发光免疫分析是一种成熟的检测技术,cn110988330a、cn106645729a等均公开了基于化学发光免疫分析检测结核分枝杆菌的技术,通过对γ干扰素进行定量分析实现检测。化学免疫发光主要包括捕获磁珠,利用磁珠上偶联的抗体实现对样本的富集,之后再进一步进行化学发光检测。虽然化学发光免疫分析具有较好的灵敏度,但是其对样本也有一定的要求。由于尿液样本中富含盐、尿素、脂肪及糖类等物质,对样本中lam进行测定时对信号值产生干扰。同时其中lam的含量较低,这导致基于lam的结核分析杆菌检测技术存在相当的难度,现有技术中未见相关技术的报导。
技术实现要素:
[0003]
本发明的目的在于克服现有技术的至少一个不足,提供一种用于lam化学发光免疫的检测试剂盒及方法。
[0004]
本发明所采取的技术方案是:本发明的第一个方面,提供:一种用于lam化学发光免疫检测的试剂盒,包括:磁珠试剂,其中的磁珠上修饰有lam捕获抗体;发光试剂,包括修饰有发光试剂的lam检测抗体;样本稀释液,由10~200mm tris-hcl缓冲液,ph6.0~8.0,0.1~0.5m nacl,0.01~0.5wt.% tween-20,0.1~5 wt.%bsa和0.5~5 wt.%peg组成。
[0005]
在一些试剂盒的实例中,所述的磁珠试剂为包被lam捕获抗体的磁珠,通过lam捕获抗体上的氨基与磁珠上的羧基共价偶联获得。
[0006]
在一些试剂盒的实例中,抗体与磁珠的偶联比为10~50ug抗体每mg磁珠。
[0007]
在一些试剂盒的实例中,磁珠试剂的工作浓度为0.5~2mg/ml。
[0008]
在一些试剂盒的实例中,所述的发光试剂为标记吖啶酯的lam检测抗体,通过吖啶酯上的羧基与lam检测抗体上的氨基共价偶联获得。
[0009]
在一些试剂盒的实例中,吖啶酯与抗体的偶联比为20~100ug吖啶酯每mg抗体。
[0010]
在一些试剂盒的实例中,所述发光试剂的工作浓度为0.5~2ug/ml。
[0011]
在一些试剂盒的实例中,所述peg为peg6000。
[0012]
本发明的第二个方面,提供:一种确定尿液样本中lam含量的方法,包括如下步骤:在待测尿液样本中加入本发明第一个方面所述的磁珠试剂,搅拌条件下孵育0.5~3小时;分离磁珠,使用本发明第一个方面所述的样本稀释液重悬磁珠,涡旋混匀,取涡旋液加入本发明第一个方面所述的发光试剂,上机检测,确定lam含量。
[0013]
在一些的实例中,样本稀释液与磁珠的用量比为(50ug-300ug):(0.2~0.4) ml。
[0014]
本发明的有益效果是:本发明一些实例的检测试剂盒,可以有效地减少与非lam特异性物质结合,且可以提高检测系统灵敏度与信号值,对于反应系统的提升有优化效果,且该试剂盒特异性高。
附图说明
[0015]
图1是lam捕获抗体对lam的亲和力检测结果。
[0016]
图2是lam检测抗体对lam的亲和力检测结果。
[0017]
图3是最佳约登指数处的roc曲线。
[0018]
图4是采用本发明方法检测健康人(n=106)和tb患者(n=80)尿液样本中lam浓度结果对比图。
具体实施方式
[0019]
本发明的第一个方面,提供:
一种用于lam化学发光免疫检测的试剂盒,包括:磁珠试剂,其中的磁珠上修饰有lam捕获抗体;发光试剂,包括修饰有发光试剂的lam检测抗体;样本稀释液,由10~200mm tris-hcl缓冲液,ph6.0~8.0,0.1~0.5m nacl,0.01~0.5wt.% tween-20,0.1~5 wt.%bsa和0.5~5 wt.%peg组成。
[0020]
在一些试剂盒的实例中,所述样本稀释液由50mm tris-hcl缓冲液,ph7.4,0.15m nacl,0.1wt.% tween-20,1wt.%bsa和1wt.%peg组成。
[0021]
磁珠试剂可以按现有方法制备得到。在一些试剂盒的实例中,所述的磁珠试剂为包被lam捕获抗体的磁珠,通过lam捕获抗体上的氨基与磁珠上的羧基共价偶联获得。
[0022]
抗体和磁珠的偶联比可以根据偶联效率等进行相应的调整,以保证磁珠上偶联有足够量的抗体,以保护捕获效果。在一些试剂盒的实例中,抗体与磁珠的偶联比为10~50ug抗体每mg磁珠。
[0023]
磁珠试剂的工作浓度可以根据检测的需要进行相应的调整。在一些试剂盒的实例中,磁珠试剂的工作浓度为0.5~2mg/ml。
[0024]
发光试剂可以按现有方法制备得到。在一些试剂盒的实例中,所述的发光试剂为标记吖啶酯的lam检测抗体,通过吖啶酯上的羧基与lam检测抗体上的氨基共价偶联获得。
[0025]
吖啶酯与抗体的偶联比可以根据偶联效果进行相应的调整,使抗体上偶联有充分的发光试剂且不影响特异性识别能力为宜。在一些试剂盒的实例中,吖啶酯与抗体的偶联比为20~100ug吖啶酯每mg抗体。
[0026]
发光试剂的工作浓度可以根据检测的需要进行相应的调整。在一些试剂盒的实例中,所述发光试剂的工作浓度为0.5~2ug/ml。
[0027]
在一些试剂盒的实例中,所述peg为peg6000。
[0028]
本发明的第二个方面,提供:一种确定尿液样本中lam含量的方法,包括如下步骤:在待测尿液样本中加入本发明第一个方面所述的磁珠试剂,搅拌条件下孵育0.5~3小时;分离磁珠,使用本发明第一个方面所述的样本稀释液重悬磁珠,涡旋混匀,取涡旋液加入本发明第一个方面所述的发光试剂,上机检测,确定lam含量。
[0029]
在一些的实例中,样本稀释液与磁珠的用量比为(50ug-300ug):(0.2~0.4) ml。具体的量可以根据检测的具体情况进行相应的调整。
[0030]
下面结合实例,进一步说明本发明的技术方案。以下实施中,如无特别说明,百分比均为质量百分比。
[0031]
1、采用化学发光平台检测尿液样本中lam抗原的双抗体夹心免疫学定量检测方法,检测过程均基于全自动化学发光免疫分析仪中进行,该方法包括下列步骤:(1)结核分枝杆菌lam捕获抗体对微球进行包被,为磁珠试剂;(2)结核分枝杆菌lam检测抗体进行吖啶酯标记,为发光试剂;(3)结核分支杆菌lam进行梯度稀释,为校准品曲线;(4)取一定体积的尿液样本/校准品加入磁珠试剂,孵育后清洗;(5)加入一定体积的缓冲液重悬磁珠作为样品,上机;
(6)加入一定体积的发光试剂,孵育后清洗;(7)加入一定体积的预激发液和激发液;(8)获得发光信号值(rlu)并分析数据判定结果。2、磁珠上包被的lam捕获抗体与尿液样本中lam进行孵育结合后,与发光试剂中标记有吖啶酯的lam检测抗体进行双抗夹心复合物。孵育方法为:(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清,并用10mmpbs(ph7.2)清洗3次;(4)磁珠重悬后,立即上机检测。3、检测尿液中lam含量的为化学发光检测平台。结核分枝杆菌脂阿拉伯甘露聚糖(lam)试剂的制备及空白限检测1、主要材料:1.1 lam抗原、磁珠,从有资质的供应商处购买。lam捕获抗体、lam检测抗体根据现有方法制备得到,当然,也可以采用商品化的lam捕获抗体、lam检测抗体。本发明所使用的lam捕获抗体对lam的亲和力如图1所示,lam检测抗体对lam的亲和力如图2所示。lam捕获抗体、lam检测抗体均具有良好的亲和力。
[0032]
2、方法:2.1 lam捕获抗体包被磁珠s1) 将140mg磁珠用binding buffer(ph 6.0)在磁分离架中清洗3次(保持磁珠浓度为20mg/ml,且加入的binding buffer至少应超过磁力架磁铁所在位置);最后一次,将反应瓶置于磁力架上,待磁珠凝聚完毕,小心移去上清;s2) 加入适量binding buffer将磁珠重新悬浮,并按每10mg磁珠加入5μl edc和50ul nhs,补加binding buffer保持磁珠浓度为20mg/ml;室温旋转反应30min,结束后用binding buffer(ph 6.0)在磁力架中清洗1次;最后一次,将反应瓶置于磁力架上,待磁珠凝聚完毕,小心移去上清;s3) 加入适量binding buffer(ph6.0),按照投料比(抗体:磁珠=1:40的质量比)加入包被抗体,再补加适量binding buffer(ph6.0),保持磁珠浓度为20mg/ml,室温旋转反应过夜;s4) 按体积比15μl/ml的比例,在磁珠中加入105μl乙醇胺,旋转反应30分钟;s5) 吸附磁珠,移去上清,加入磁珠试剂封闭液(tbs+1%bsa)至20mg/ml,旋转反应3小时;s6) 用磁珠洗涤缓冲液清洗3次,最后一次,将反应瓶置于磁分离架上,待磁微球凝聚完毕,小心移去上清,用磁珠试剂稀释液将磁珠稀释至20mg/ml。2.2 lam检测抗体标记吖啶酯紫外分光光度计测定抗体浓度a280,计算标记前抗体浓度。标记抗体加入到偶联缓冲碳酸氢钠溶液(0.1m)中(抗体终浓度1mg/ml)。使用dmf溶解吖啶酯,终浓度为1mg/ml。按一定投料比将溶解有吖啶酯的dmf溶液加入到标记抗体稀释液中,室温避光震荡40min,转速160rpm/min。加入6ul的10%甘氨酸终止反应,室温避光震荡30min,转速160rpm/min。放置ph6.8的pbs缓冲液中透析2-3天。加入10%bsa、丙三醇(甘油)至标记产物中,使得终浓度
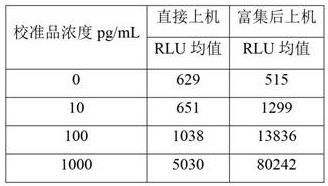
1%bsa,40%甘油,-20℃保存使用。2.3 lam校准曲线配置lam抗原使用校准品稀释液进行梯度稀释0pg/ml,10pg/ml,100pg/ml,1000pg/ml,分别同时直接上机检测和富集后上机检测。2.4 直接上机检测(1)在全自动化学放光免疫分析仪上,仪器自动取100ul待测尿液样本,加入10ug-60ug的磁珠试剂;(2)37℃,孵育5~15min;(3)仪器自动清洗4~8次;(4)加入50ul吖啶酯标记抗体;(5)37℃,孵育5~15min;(6)仪器自动清洗4~8次;(7)加入100ul预激发液和激发液,读取发光值(rlu)。
[0033]
2.5富集后上机检测(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清;(4)用0.3ml稀释液(50mm tbs+0.15m nacl + 0.1% tween 20 + 1%bsa,ph7.4)重悬磁珠,涡旋混匀,立即上机检测。3、结果检测结果如表1所示。
[0034]
表1由表1的数据可知,通过使用磁珠富集后,检测系统灵敏度明显提升,检出限可达2.6pg/ml。
[0035]
不同组成样本稀释液对检测结果的影响1.主要材料:1.1磁珠稀释液:对照组:50mm tbs +0.15mnacl+ 0.1% tween 20 + 1%bsa,ph7.4;实验组: 50mm tbs +0.15m nacl+ 0.1% tween 20 + 1%bsa + 1% peg6000,ph7.4。
[0036]
对比例1:50mm tbs +0.15m nacl+ 0.1% tween 20 + 1%bsa,ph7.4对比例2:50mm tbs +0.15m nacl+1%bsa + 1% peg6000,ph7.4
对比例3:50mm tbs +0.15m nacl + 0.1% tween 20 + 1% peg6000,ph7.4实施例1:50mm tbs +0.15m nacl + 0.1% tween 20 + 1%bsa + 1% peg6000,ph7.41.2校准曲线、发光试剂、磁珠试剂。
[0037]
2.方法:(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清;(4)分别用对照组和实验组的磁珠稀释液重悬磁珠,涡旋混匀,立即上机检测。3.结果检测结果如表2所示。
[0038]
表2由表2的数据可知,对比例2的稀释液重悬磁珠,与对比例1相比,检测系统灵敏度有所提升;对比例3的稀释液与对比例1分别重悬磁珠后相比,灵敏度有提升,但检测本底值偏高;通过使用实施例1与对比例1相比,检测灵敏度提升,且本底信号值无明显变化。说明bsa、吐温和peg对lam的检测具有难以预见的影响。实施例1的样本稀释液具有最佳的效果。
[0039]
特异性实验1、主要材料:1.1 校准曲线、发光试剂、磁珠试剂1.2 临床样本:健康人尿液样本2、方法:lam富集(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清;(4)使用实施例1的样本稀释液将磁珠重悬后,立即上机检测。3.结果检测结果如表3所示所示。
[0040]
表3
由表3可知,以60例健康人尿液样本的97.5%为切值,只有1例样本呈现假阳性,特异性为98.33%。准确性测定实验1、主要材料:1.1 校准曲线、发光试剂、磁珠试剂1.2 临床样本:17例菌阳患者尿液样本(以菌培作为金标准)2、方法:lam富集(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清;(4)使用实施例1的样本稀释液磁珠重悬后,立即上机检测。3、结果17例样品中检测出15例阳性,检出率为88.24%,准确度性高。该定性产品在临床中应用1、主要材料:1.1校准曲线、发光试剂、磁珠试剂1.2切值建立临床样本:50例肺结核样本,60例健康人样本进行该试剂盒检测系统切值水平的建立。
[0041]
1.3 临床验证样本:切值水平为判断标准,在临床80例临床诊断为肺结核患者尿液样本,106例健康人尿液样本进行特异性及准确性的临床验证。
[0042]
2、方法:lam富集(1)取1-10ml待测尿液样本,加入50ug-300ug的磁珠试剂;(2)室温旋转孵育1-5h;(3)使用磁分离器进行分离,弃上清;(4)使用实施例1的样本稀释液磁珠重悬后,立即上机检测。
3、结果3.1 在最佳约登指数处,roc曲线auc面积为0.799,p《0.0001,灵敏度为72.0%(图3),特异性为93.8%,为了保证产品特异性。选定定性产品切值为0.97,特异性为100%,进行大临床样本验证。
[0043]
3.2 选用的临床验证样本:80例临床诊断为肺结核患者尿液样本,106例健康人尿液样本验证结果如下:80例肺结核样本中lam阳性检出率为55%,106例健康人样本中阳性检出率为0%(图4)。
[0044]
以上是对本发明所作的进一步详细说明,不可视为对本发明的具体实施的局限。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的简单推演或替换,都在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1