含有TARC的组合物、稀释剂、减少TARC残留的方法、吸附抑制剂和连续分析方法与流程
本发明涉及含有tarc的组合物和用于含有tarc的组合物的稀释剂。本发明还涉及减少tarc残留的方法,以及用于防止tarc吸附的吸附抑制剂。本发明还涉及连续分析含有tarc的两个或更多个样品的方法。
背景技术:
1、胸腺活化调节趋化因子(以下可称为tarc)是c-c趋化因子配体17(ccl17),是一种具有白细胞迁移活性的趋化因子。tarc将淋巴细胞之一的th2细胞吸引到病变部位,引起ige的产生和嗜酸性粒细胞的浸润/活化。据认为,tarc通过以这种方式增强过敏反应来加剧特应性皮炎的症状(非专利文献1)。
2、对特应性皮炎炎症进行及时可靠的镇静被认为是重要的。与特应性皮炎疾病状态的其他指标如血清ige水平、外周血嗜酸性粒细胞计数和血清ldh水平相比,tarc与特应性皮炎的严重程度很好地匹配,这被认为更敏感地反映疾病状态(非专利文献2)。因此,使用tarc作为生物标志物可以在选择或更换特应性皮炎的治疗剂时客观快速地掌握严重程度,以确定其效果。
3、为了测量样品中的成分,需要使用校准样品。校准样品是含有待测量成分的样品,用于内标或浓度校准标准(校准器)等应用。为了便于操作,校准样品优选为流体溶液(以下可称为“液体”)的形式。在这种情况下,校准样品所需物质的实例包括维持生物学活性(如对特定抗体的抗原性、对抗体和凝集素的特定结合配偶体的结合活性、肽激素的生理活性、酶活性以及作为支持每种活性的蛋白质的三维结构)、防止对容器的吸附和保持防腐能力。
4、已知作为用于免疫测定的液态校准样品的储存方法,已知稳定校准样品中与酪蛋白和/或乳清蛋白共存的抗原的方法(专利文献1),已知稳定胰岛素与胆汁酸酰胺衍生物共存的方法(专利文献2),已知稳定可溶性白细胞介素-2受体(sil-2r)与螯合剂共存的方法(专利文献3)。对于tarc,本发明人进一步研究了使用阳离子表面活性剂或阴离子表面活性剂的方法(专利文献4),该方法使用一种或多种选自糖脂肪酸酯型非离子表面活性剂,聚氧乙烯-聚氧丙烯嵌段共聚物型非离子表面活性剂,和聚氧乙烯烷基胺型非离子表面活性剂(专利文献5),以及使用具有2-甲基丙烯酰氧乙基磷酰胆碱作为结构单元的聚合物的方法(专利文献6)。
5、引文列表
6、专利文献
7、专利文献1
8、日本专利公开号08-005634
9、专利文献2
10、日本专利公开号08-012593
11、专利文献3
12、日本专利公开号2010-230660
13、专利文献4
14、日本专利申请号2020-119024
15、专利文献5
16、日本专利申请号2020-119025
17、专利文献6
18、日本专利申请号2020-119026
19、非专利文献
20、非专利文献1
21、j allergy clin immunol 107:535-541,2001
22、非专利文献2
23、journal of the japanese dermatological association 116(1):27-39,2006
技术实现思路
0、发明概述
1、技术问题
2、当使用自动分析仪测量样品中的成分时,使用样品探针将样品分配到稀释池或反应池中。具体而言,样品探针是一种微毛细管,用于吸收所需量的样品(校准样品,样品或用稀释剂稀释的样品)并将样品放入反应池中。样品探针根据每个自动分析仪的特定程序进行操作。对于浓度校准,从较低浓度侧进行采样,因此许多仪器都有用于对每个样品用水冲洗样品探针但不用于用洗涤剂洗涤的程序。有些仪器有只有在完成所有标准物质的校准取样后才能用洗涤剂冲洗或洗涤的程序,这种情况是即使用水也不冲洗每个样品的样品探针而进行的。因此,在对高浓度校准样品进行取样时,或在取样后、冲洗或清洗前,由于误差等原因需要再次进行浓度校准时,无需清洗已抽吸用于校准的高浓度标准物质的样品探针,可对零浓度或低浓度的校准样品进行取样。高浓度校准样品中含有的抗原很可能粘附在样品探针上,当没有用水彻底冲洗时,这种成分会污染下一个样品,即发生残留。因此,在浓度校准期间发生的残留未能构建准确的校准曲线,从而造成无法获得样品的准确测量值的问题。
3、此外,在样品测量过程中,系统通常涉及用水冲洗每个样品的样品探针,因此很可能会出现与校准样品一样的残留,但是可以通过添加仪器设置(避免残留设置)来避免残留,这样就可以在取样前用洗涤剂清洗样品探头。另一方面,有些自动分析仪没有加载上述洗涤机制,因此存在因样品探针清洗而导致处理能力下降的缺点。
4、问题的解决方案
5、本发明人发现,当连续定量tarc时,tarc抗原吸附在样品探针上,从而导致残留到随后的样品中,然后再进行定量。本发明者对不会发生残留的方法进行了大量研究。结果,本发明者发现,如果采用以下结构时,可以防止发生残留,从而实现本发明。
6、具体而言,本发明如下所述。
7、<1>组合物,其包括:
8、(a)tarc(胸腺活化调节趋化因子);和
9、(b)一种或多种成分,其选自由酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物,及其盐组成的组,且
10、呈液态。
11、<2>根据<1>所述的组合物,其中所述组合物是用于测量tarc的校准样品溶液。
12、<3>根据<1>或<2>所述的组合物,进一步包括:
13、(c)缓冲液。
14、<4>根据<1>至<3>中任一项所述的组合物,其中所述酸性聚合物及其盐为聚磺苯乙烯钠、萘磺酸缩合物、聚丙烯酸钠或聚丙烯酸。
15、<5>根据<1>至<4>中任一项所述的组合物,其中,相对于组合物,成分(b)的浓度为0.0001至20质量%。
16、<6>用于含有tarc的样品的稀释剂,其包括:
17、(b)一种或多种成分,其选自由以下组成的组
18、酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物,及其盐。
19、<7>根据<6>所述的稀释剂,其中所述酸性聚合物及其盐为聚磺苯乙烯钠、萘磺酸缩合物、聚丙烯酸钠或聚丙烯酸。
20、<8>根据<6>或<7>所述的稀释剂,进一步包括:
21、(c)缓冲液。
22、<9>根据<6>至<8>中任一项所述的稀释剂,其中,相对于稀释剂,成分(b)的浓度为0.0001至20质量%。
23、<10>用于减少tarc残留的方法,其包括将
24、(a)tarc和
25、(b)一种或多种成分,其选自由酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物,及其盐组成的组
26、在溶液中接触。
27、<11>根据<10>所述的用于减少tarc残留的方法,其中所述酸性聚合物及其盐为聚磺苯乙烯钠、萘磺酸缩合物、聚丙烯酸钠或聚丙烯酸。
28、<12>根据<10>或<11>所述的用于减少tarc残留的方法,其中所述溶液是缓冲液。
29、<13>根据<10>至<12>中任一项所述的用于减少tarc残留的方法,其中所述残留是样品探针中的残留。
30、<14>根据<10>至<13>中任一项所述的用于减少tarc残留的方法,其中,相对于溶液,成分(b)的浓度为0.0001至20质量%。
31、<15>吸附抑制剂,其用于防止含有tarc的溶液中的tarc吸附到样品探针上,所述吸附抑制剂包括:
32、(b)一种或多种成分,其选自酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物,及其盐组成的组。
33、<16>根据<15>所述的吸附抑制剂,其中所述酸性聚合物及其盐为聚磺苯乙烯钠、萘磺酸缩合物、聚丙烯酸钠或聚丙烯酸。
34、<17>连续分析含有tarc的两个或更多个样品的方法,该方法包括:
35、(a)使用样品探针抽吸含有tarc的第一样品,
36、(b)从样品探针中排出第一样品,
37、(c)测量第一样品的信号强度,
38、(d)用冲洗溶液冲洗样品探针的壁表面,
39、(e)使用样品探针抽吸含有tarc的第二样品,和
40、(f)测量第二样品的信号强度,
41、其中,第一样品和第二样品包括(b)相对于第一样品和第二样品,0.0001质量%至20质量%的选自由酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物,及其盐组成的组的一种或多种成分,以及
42、含有tarc的第一样品的tarc浓度高于含有tarc的第二样品的tarc浓度。
43、发明的有利效果
44、本发明可以提供不容易导致tarc抗原残留的校准样品和样品的稀释剂。因此,本发明能够准确定量生物样品中的tarc,并准确掌握特应性皮炎的严重程度。
45、实施方案的描述
46、以下,将详细描述本发明。本说明书按本发明的不同方面进行描述,但在各方面描述的章节、术语定义和实施方案也适用于其他方面。
47、1.含有tarc的组合物
48、(成分(a):tarc)
49、在本描述中,“tarc”是指胸腺活化调节趋化因子(ccl17)。tarc是一种具有白细胞迁移活性的趋化因子。tarc具有将淋巴细胞之一的th2细胞吸引到病变部位,引起ige的产生和嗜酸性粒细胞的浸润/活化的功能。使用tarc作为生物标志物可以在选择或更换特应性皮炎的治疗剂时客观快速地掌握严重程度。
50、tarc可以通过如免疫学技术等已知方法进行测定。免疫技术的实例包括elisa,酶免疫测定,表面等离子体共振,乳胶凝集免疫测定(ltia,乳胶比浊免疫测定),化学发光免疫测定,电化学发光免疫测定,荧光抗体法,放射免疫测定,蛋白质印迹,免疫层析和高效液相色谱(hplc)。
51、包含在本发明组合物中的tarc可以是市售产品或自行生产或纯化的产品。包含在本发明组合物中的tarc可以在体外产生或从活体中提取。
52、(tarc的浓度)
53、包含在本发明组合物中的tarc的浓度不限于以下实例,但相对于组合物,优选为10pg/ml至1μg/ml,更优选50pg/ml至500ng/ml,进一步优选100pg/ml至100ng/ml,最优选100pg/ml至50ng/ml。
54、(成分(b))
55、本发明的组合物包括一种或多种成分(以下简称成分(b)),其选自由酸性氨基酸,碱性氨基酸,平均分子量为4000至1200000的酸性聚合物及其盐组成的组。这些成分在水溶液中离子化并显示正电荷或负电荷。在水溶液中离子化并显示负电荷是指具有比碱性官能团(例如氨基)更多的酸性官能团(例如磺基),并且溶解在水中时显示负电荷。在水溶液中离子化并显示正电荷是指具有比酸性官能团更多的碱性官能团,并且溶解在水中时显示正电荷。
56、酸性官能团的实例包括磺基,磷酸基团和羧基。优选磺基或羧基。
57、碱性官能团的实例包括氨基,例如伯氨基、仲氨基、叔氨基、季铵盐、酰胺基、吡啶(pyridyl)基、吡啶(pyridine)基、吡咯烷酮基、咪唑基和亚胺基。优选氨基。
58、对于酸性氨基酸,可使用重均分子量为4000至1200000的酸性聚合物或其盐、l-谷氨酸、l-天冬氨酸、聚磺苯乙烯钠(cas注册号25704-18-1)、聚丙烯酸钠(cas注册号9003-04-7)、萘磺酸缩合物(cas注册号9084-06-4),或聚丙烯酸(cas注册号9003-01-4)。可用的萘磺酸缩合物由kao corporation以demol(注册商标)rn生产和销售。本说明书中所述的氨基酸可以是作为生物体结构单元的α-氨基酸,也可以是非天然氨基酸。在本说明书中,氨基酸包括l型,d型及其混合物。
59、(碱性氨基酸或其盐)
60、对于碱性氨基酸或其盐,可以使用l-赖氨酸,l-精氨酸或其盐。
61、只要可以获得本发明的效果,酸性氨基酸盐、碱性氨基酸盐或重均分子量为4000至1200000的酸性聚合物盐不受限制,并且实例包括由无机酸或有机酸(例如盐酸盐、硫酸氢盐和乙酸盐)形成的盐,和由碱形成的盐,如钠盐和钾盐。
62、酸性氨基酸,碱性氨基酸或重均分子量为4000至1200000的酸性聚合物优选为l-谷氨酸、l-天冬氨酸、聚磺苯乙烯钠、萘磺酸缩合物或聚丙烯酸,更优选为l-谷氨酸、l-天冬氨酸、聚磺苯乙烯钠或萘磺酸缩合物(demol rn)。可用的酸性聚合物是平均分子量(平均分子量:重均分子量)为例如4000至1200000,且优选5000至1000000的那些。此外,重均分子量(mw)优选为70000至1000000。可以使用尺寸排阻色谱(sec)测量重均分子量(mw)。酸性聚合物可以不受限制地使用,只要它是通过聚合具有酸性基团的单体而获得的聚合物即可。酸性聚合物优选是通过聚合具有羧基或磺基的单体而获得的酸性聚合物。
63、成分(b)的浓度为例如相对于组合物的0.0001至20质量%,优选0.001至10质量%。
64、当使用酸性氨基酸或其盐时,浓度更优选为相对于组合物的0.05至10质量%,进一步优选为0.1至5质量%,最优选为0.5至1质量%。
65、当使用酸性聚合物或其盐时,浓度更优选为相对于组合物的0.001至1质量%,进一步优选为0.001至0.5质量%,并且最优选为0.002至0.1质量%。
66、当使用碱性氨基酸或其盐时,例如,浓度为相对于组合物的1至20质量%,优选3至18质量%,更优选5至15质量%,最优选5至10质量%。
67、在本实施方案的组合物中,只要可以获得本发明的效果,添加成分(b)和tarc的顺序不受特别限制。
68、(成分(c):缓冲液)
69、在此描述中,“缓冲液”是指具有ph缓冲作用的溶液。
70、对于本发明中使用的缓冲液,可以适当使用已知的缓冲液,例如pbs(磷酸盐缓冲盐水),mes(2-(n-吗啉代)乙磺酸),pipes(哌嗪-n,n'-双(2-乙磺酸),aces(n-(2-乙酰胺基)-2-氨基乙磺酸),ada(n-(2-乙酰胺基)亚氨基二乙酸),bis-tris(2,2-双(羟乙基)-(亚氨基)-(羟甲基)-甲烷),tris(三(羟甲基)氨基甲烷),mops(3-吗啉代丙烷磺酸),hepes(4-(2-羟乙基)-1-哌嗪乙磺酸),柠檬酸盐缓冲液,甘氨酸缓冲液,硼酸盐缓冲液或磷酸盐缓冲液,但不限于此。本发明中使用的缓冲液优选pbs。
71、只要可以获得本发明的效果,缓冲液的浓度不受特别限制,例如1至500mm,5至400mm,10至300mm或50至200mm。
72、本发明中使用的缓冲液ph值例如为4.0至11.0、5.0至10.0、6.0至9.0、6.5至8.0或7.0至8.0。可以使用本领域技术人员已知的用于ph调节的试剂(例如氢氧化钠或盐酸)调节ph。
73、本发明组合物中的缓冲液的含量为,例如,相对于组合物的90质量%或更高、92质量%或更高、95质量%或更高、97质量%或更高或99质量%或更高。
74、(存储容器)
75、本发明的组合物优选填充在储存容器中。储存容器的材料不受具体限制,只要可以获得本发明的效果,并且可以实现密封,但与组合物的至少部分或全部接触区域是塑料[例如烯烃树脂、苯乙烯树脂、丙烯酸树脂、聚酯树脂、聚碳酸酯树脂、氟树脂、氯化树脂(例如聚氯乙烯)、聚酰胺树脂、聚缩醛树脂、聚苯醚树脂(例如改性聚苯醚),聚丙烯酸酯(polyarylate),聚苯乙烯砜,聚酰亚胺树脂,纤维素树脂(例如醋酸纤维素)和烃树脂(包括卤素取代的产物)],金属(例如铝),玻璃等。其中,考虑到校准样品的生产、运输和储存,优选塑料或玻璃,塑料中优选烯烃树脂,更优选聚丙烯。
76、储存容器可以由单一材料或两种或多种材料制成,但最好由单一材料制成。存储容器可以包括容器体和盖。在这种情况下,容器体和盖子可以由不同的材料制成。另外,储存容器,特别是主体部分,优选具有透明性,使得可以从外部看到液体内容物。
77、储存容器的形式可以是硬式或软式,其实例包括安瓿、小瓶、软袋、注射器式容器和玻璃瓶。为了便于使用和tarc的稳定性,储存容器优选为塑料滴管瓶的形式,特别是圆柱形滴管瓶的形式,包括容器体和盖子。
78、(组合物)
79、本发明的组合物可以用作tarc测量中的校准样品溶液。在本说明书中,校准样品溶液是指用于准确测量待测物质并含有一定浓度的待测物质的样品溶液。其中实例包括标准物质、校准器、对照品和内标物质。本发明组合物的供应形式的实例包括通过将溶剂与tarc和成分(b)混合而预先制备的溶液状态。
80、在tarc测量中,“使用组合物”是指使用组合物以便准确测量tarc。例如,这意味着使用含有tarc的液体组合物作为校准样品溶液(如标准物质、校准器、对照品和内标物质)。
81、本发明中组合物的ph值例如为4.0至11.0、5.0至10.0、6.0至9.0、6.5至8.0或7.0至8.0。
82、可以使用本领域技术人员已知的ph调节试剂例如氢氧化钠或盐酸调节ph。
83、只要不损害本发明的效果,发明的组合物可以具有没有特别限制的任何组合物。当通过免疫测定法测量tarc时,该组合物是合适的,只要它不损害本发明的效果并且不阻止构成测定系统的全部或部分反应例如抗原抗体反应和酶反应即可。通常用于免疫测定的各种成分可以根据目的适当地选择和使用,包括例如促进抗原抗体反应的成分(例如,聚合物如聚乙二醇和聚乙烯吡咯烷酮)、糖蛋白和肽(例如,bsa和酪蛋白)、氨基酸、盐类(例如,氯化钠和氯化钾)、糖类(如蔗糖和环糊精)、防腐剂(如叠氮化钠和proclin 300)和其他吸附抑制剂(如lipidure)。
84、在本说明书中,“残留”是指当分离第一样品时,样品中的tarc抗原吸附并驻留在样品探针等的壁表面上,并且源自第一样品的tarc抗原流入第二样品的反应池中,随后进行采样。当残留发生时,第二样品及其后的信号强度相对高于最初获得的信号强度,从而无法获得准确的定量值。如前所述,本发明人发现,当tarc与样品探针接触时,即使仅接触很短时间,也会发生残留。当使用本发明的组合物时,可以防止残留,并且可以提高tarc测量的精度。
85、在本说明书中,样品探针是指用于从诸如抽血管的容器中抽吸所需量的样品并将样品放入反应池中的微毛细管。样品探针既包括用于自动测量装置的样品探针,也包括用于手动使用的样品探针。样品探针优选地由金属制成,更优选地由不锈钢制成。
86、(用于tarc测量的样品)
87、用于tarc测量的样品没有特别限制,只要可以测量tarc即可,但优选使用血液、血清或血浆。可以根据需要对样品进行适当的预处理。该样品优选地是从人类采集的生物样品。
88、(tarc试剂盒)
89、本发明的组合物可以以tarc试剂盒的形式提供,该试剂盒包括本发明的成分和其他试剂。试剂盒的实例包括使用免疫学技术的试剂盒。免疫技术的实例包括elisa,酶免疫测定,表面等离子体共振,乳胶凝集免疫测定(ltia,乳胶比浊免疫测定),化学发光免疫测定,电化学发光免疫测定,荧光抗体法,放射免疫测定,蛋白质印迹,免疫层析和高效液相色谱(hplc)。
90、试剂盒可用于选择特应性皮炎的治疗方法或药物,并用于在确定治疗效果时掌握特应性皮肤炎的严重程度。
91、试剂盒还可以包括使用说明书等。试剂盒可以包含可选的成分,例如稳定剂、ph调节剂和反应容器。
92、2.含有tarc的样品的稀释剂
93、(含有tarc的样品)
94、本发明的稀释剂可用于稀释含有tarc的样品。含有tarc的样品的实例包括用于测量tarc的样品(例如血液,血清或血浆),标准物质,校准品,对照和内标物质。如前所述,除tarc外的其他成分与“1.含有tarc的组合物”相同。
95、可以使用本发明的稀释剂,以使稀释后的tarc浓度优选为10pg/ml至1μg/ml,更优选50pg/ml至500ng/ml,进一步优选100pg/ml至100ng/ml,最优选100pg/ml至50ng/ml。
96、3.减少tarc残留的方法
97、本发明减少tarc残留的方法包括使tarc与成分(b)在溶液中接触。可以在将成分(b)添加到溶液中后添加tarc,也可以在将tarc添加到溶液中后添加成分(b)。该溶液优选为缓冲液,更优选为pbs。
98、残留包括由样品探针引起的残留。只要可以获得本发明的效果,tarc作为成分(a)和本技术中发现的化合物作为成分(b)可以在样品探针中相互接触,或者将成分(a)与成分(b)接触后制备的含有tarc的组合物转移到样品探针中。
99、本发明减少tarc残留的方法可以包括将含有tarc的制备的组合物保持在样品探针中。“将含有tarc的制备的组合物保持在样品探针中”是指含有tarc的组合物只能与样品探针的壁表面接触,并且可以同时进行其他动作,例如移动样品探针进行分配。
100、只要可以获得本发明的效果,tarc在样品探针中的保持时间不受限制,例如,下限可以是0.1秒或更长,0.2秒或更长,或0.5秒或更长。上限可以是1小时或更少、30分钟或更少、15分钟或更少、10分钟或更少、5分钟或更少、1分钟或更少、30秒或更少、10秒或更少、5秒或更少、3秒或更少、或2秒或更少。特定的保持时间范围为0.1秒至1小时、0.1秒至30分钟、0.1秒至15分钟、0.1秒至10分钟、0.1秒至1分钟、0.2秒至30秒、0.2秒至10秒、0.5秒至5秒或0.5秒至3秒。
101、本发明减少tarc残留的方法还可以任选地包括以下一个或多个步骤:
102、(a)使用样品探针抽吸含有tarc的第一样品,
103、(b)从样品探针中排出第一样品,
104、(c)测量第一样品的信号强度,
105、(d)用冲洗溶液冲洗样品探针的壁表面,
106、(e)使用样品探针抽吸含有tarc的第二样品(以及之后的样品),
107、(f)从样品探针中排出第二样品(及其后的样品),
108、(g)测量第二样品及其后样品的信号强度。
109、在步骤(a)中,含有tarc的第一样品和含有tarc的第二样品以及之后的样品都包括成分(b)。包含在第一样品中的成分(b)和包含在第二样品中的成分(b)优选地相同。第一样品和第二样品可以在测量之前将成分(b)作为样品稀释剂添加到其中,或者也可以从一开始就包括成分(b)。第一样品和第二样品可以是用于测量tarc的任何样品(例如血液,血清或血浆)或校准样品(例如标准物质,校准品,对照)。第一样品和第二样品优选为用于测量tarc的校准样品(例如,标准物质、校准器、对照)。
110、步骤(a)和(e)中的“使用样品探针抽吸”包括通过分析仪手动抽吸第一样品,以及在分析仪开关打开时使用自动分析仪自动抽吸第一样品。这也适用于(a)以外的步骤。可用的自动分析仪包括用于进行乳胶免疫浊度法(ltia法,乳胶免疫比浊法),电化学发光免疫测定法(ecl法),酶免疫测定法(elisa),化学发光免疫测定法,荧光抗体法等的自动分析仪。
111、在步骤(a)至(g)中,按照所列顺序执行步骤(a)、(b)、(d)、(e)和(f)。执行(c)和(g)的时间可以根据所用自动分析仪的程序需要进行设置。
112、可以根据分析方法的种类适当选择产生信号的物质。产生信号的物质的实例包括金属络合物、酶、不溶性颗粒、荧光物质、化学发光物质、生物素、抗生物素蛋白、放射性同位素、金胶体颗粒、乳胶颗粒和有色乳胶。只要可以基于信号的强度测量样品中的tarc浓度,信号就不受限制,并且可以根据分析方法的种类从荧光、吸光度、散射光强度等中适当地选择。
113、在步骤(b)中,当第一样品不包括成分(b)时,在排出第一样品后,tarc抗原已经粘附到样品探针的壁表面。因此,当在排出第一样品后没有提供使用洗涤剂等的洗涤步骤时,第二样品和随后要测量的样品会发生tarc抗原残留。
114、在步骤(d)中,“冲洗样品探针的壁表面”是指用冲洗溶液运行时产生的摩擦力、剪切应力等冲洗样品探针的壁表面,而不利用诸如使用刷子的摩擦和抛光等的作用。冲洗溶液通常基本上仅由水制成,更优选地基本上不含洗涤剂。这是因为,当冲洗溶液包括洗涤剂时,残留在样品探针中的洗涤剂需要用水进一步冲洗,从而延长冲洗步骤所需的时间。不一定排除冲洗溶液包括洗涤剂,但冲洗溶液中洗涤剂的含量优选为0.1质量%或更少,更优选为0.01质量%或更少,进一步优选为0.001质量%或更少,最优选不含洗涤剂。
115、洗涤剂是指能够基于化学作用从样品探针的壁表面分离蛋白质的物质。洗涤剂具体包括酸、碱、表面活性剂、酶等。
116、在步骤(e)中,含有tarc的第一样品的tarc浓度优选高于第二样品和其后含有tarc的样品的tarc浓度。当含有tarc的第一样品的tarc浓度高于含有tarc的第二样品的tarc浓度时,由于tarc抗原残留的影响,第二样品及其后的样品的信号强度相对高于原始获得的信号强度,因此可能无法获得准确的定量值。
117、即将从样品探针排出之前的第一样品的tarc浓度例如为500pg/ml或更高,1000pg/ml或更高,5000pg/ml或更高,10000pg/ml或更高,15000pg/ml或更高,或20000pg/ml或更高。
118、即将从样品探针排出之前的第二样品的tarc浓度可能低于第一样品的tarc浓度,例如为0pg/ml至10000pg/ml,0pg/ml至5000pg/ml,0pg/ml至1000pg/ml,0pg/ml至700pg/ml,0pg/ml至600pg/ml,0pg/ml至500pg/ml,0pg/ml至300pg/ml,或0pg/ml至100pg/ml。当加入样品稀释剂时,上述浓度是稀释后的浓度。
119、在步骤(g)中,当第一样品包括成分(b)时,可以防止tarc抗原残留对第二样品及其后的样品的影响。因此,可以以高精度测量tarc浓度。
120、在本发明用于减少tarc抗原残留的方法中,还可以任选地包括以下一个或多个步骤:
121、-根据第一样品和第二样品以及之后的样品的信号强度,分别计算第一样品和第二样品以及其后的样品的tarc浓度
122、-基于包含第一样品和第二样品的样品的信号强度构建校准曲线
123、-在样品分析开始和/或样品分析完成时,使用含有洗涤剂的洗涤液洗涤样品探针。
124、“样品分析完成时”是指所有待分析样品的分析完成的时间。
125、4.用于防止tarc抗原吸附的吸附抑制剂
126、本发明用于防止tarc抗原吸附的吸附抑制剂包括显示正电荷或负电荷的化合物作为活性成分。本发明用于防止tarc抗原吸附的吸附抑制剂的实施方案与前面描述的实施方案相同。
127、5.连续分析含有tarc的两个或更多个样品的方法
128、本说明书中的“连续分析两个或更多个样品的方法”是指使用全自动分析仪连续分析两个或更多个样品。
129、在本发明用于连续分析含有tarc抗原的两个或更多个样品的方法中,优选在每个样品的分析之间不包括使用洗涤剂等的洗涤步骤而分析两个或更多个样品。也就是说,在本发明用于连续分析含有tarc抗原的两个或更多个样品的方法中,优选在每个样品的分析之间用水冲洗样品探针的壁表面,并且在分析的开始和完成时包括使用洗涤剂等的洗涤步骤。在连续分析两个或更多个样品的方法中,不一定排除在每个样品的分析之间用洗涤剂洗涤样品探针壁表面的系统。
130、本发明的用于连续分析含有tarc抗原的两个或更多个样品的方法可以任选地包括将tarc作为成分(a)与成分(b)在溶液中接触。该步骤可以是例如用含有成分(b)的样品稀释剂稀释第一和/或第二样品以及其后含有tarc的样品的步骤。
131、将通过实施例具体描述本发明,但这些并不限制本发明的范围。除非另有说明,否则在本说明中,%指质量百分数。实施例中使用的添加剂的产品名称、成分名称和经销商如下。
132、-lipidure(r)系列,可从nof公司获得
133、-acetamin(r)24成分名称:椰子胺乙酸酯,可从kao公司获得
134、-demol(r)rn-l成分名称:β萘磺酸缩合物钠盐,可从kao公司获得
135、-enagicol(r)l-30an成分名称:β月桂酰基甲基丙氨酸钠,可从lion公司获得
136、-blockmaster(r)ce系列,可从mbl life science获得
137、其他通用试剂适当地从试剂制造商购买并使用。
138、实施例
139、1.测量方法
140、1-1.测量试剂
141、制备了由以下第一试剂和第二试剂组成的用于tarc测量的ltia测量试剂。
142、(1)第一试剂
143、100mm mops-naoh(ph 7.5)
144、500mm nacl
145、0.5% bsa
146、(2)第二试剂
147、抗人tarc单克隆抗体致敏乳胶(两种类型)
148、5mm mops-naoh(ph 7.0)
149、抗人tarc单克隆抗体是通过本领域技术人员熟知的方法,使用市售tarc抗原获得的。市售tarc抗原的实例包括ccl17,胸腺活化调节趋化因子(shenandoah biotechnology,inc.),ccl17/tarc,人(lifespan bioscience,inc.)和人tarc(ccl17)(abeomics,inc.)。此外,还通过本领域技术人员熟知的方法,选择了能对tarc抗原进行夹心检测的单克隆抗体组合。抗人tarc单克隆抗体致敏胶乳参照日本专利公开号2017-181377中所述方法制备。
150、1-2.样品
151、将tarc抗原溶解在具有以下组成的稀释剂中,以制备低浓度样品(样品a,800pg/ml水平)和高浓度样品(样品b,20000pg/ml水平)。此外,分别制备了盐水。
152、稀释剂
153、-pbs(ph 7.2)
154、-0.5% lipidure(前提是这与表5所示的成分不同)
155、-添加剂(浓度和成分名称见表2至表6)
156、1-3.测量程序
157、组合第一试剂和第二试剂,使用日立自动分析仪3500(样品探针由不锈钢制成)测量样品的tarc浓度。具体而言,将120μl第一试剂加入至2.4μl样品中,并在37℃下加热5分钟,随后加入40μl第二试剂并搅拌。此后,在570nm的主波长和800nm的次波长下测量5分钟内团聚形成的吸光度变化。根据获得的吸光度变化计算测量灵敏度。
158、1-4.分析方法
159、使用每种添加剂的各自稀释剂,在用水冲洗样品探针但不使用洗涤剂洗涤后,总共进行12次取样,包括两次盐水,五次样品a(=第一组),两次样品b,五次样品a(=第二组),并连续测量。从每次测量的测量灵敏度中,减去两次盐水测量的平均测量灵敏度。计算第一组五次测量的平均测量灵敏度,并计算第二组每个测量灵敏度与第一组平均测量灵敏度的相对比率(%)。在每次测量中,样品探针中的保持时间为约1至2秒。
160、2.结果
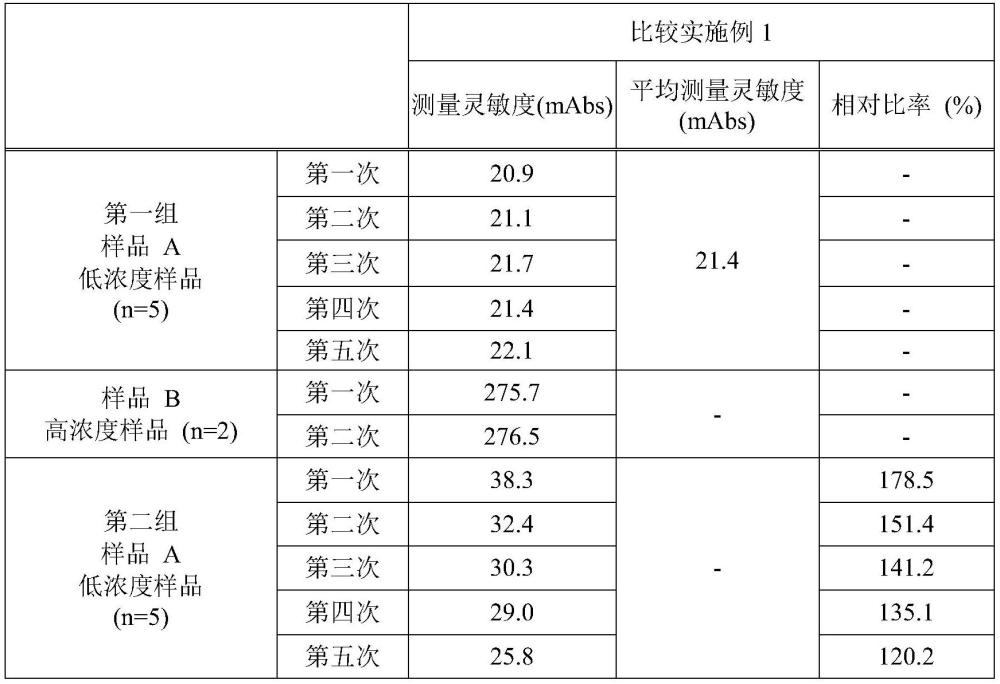
161、表1显示了未将成分(b)添加到校准稀释剂中时获得的结果。第一组样品a(800pg/ml水平)的五次测量的测量灵敏度范围为20.9至22.1mabs,平均测量灵敏度为21.4mabs。随后,测量样品b(20000pg/ml水平)两次,然后再次测量样品a五次(第二组)。第二组的第一次测量灵敏度为38.3mabs,该值显著高于第一组的平均测量灵敏度,相对比率差至178.5%。原因可能是样品b中含有的tarc抗原吸附在样品探针上,出现了引入第二组测量中的残留。在第二组中,随着第二次和第三次重复测量,测量灵敏度降低,但即使在第五次,相对比率也为120.2(%),表明残留的影响。
162、[表1]
163、
164、然后,表2至表6显示了当将各种添加剂添加到稀释剂中以达到表中所示的最终浓度时获得的结果。在表格中,摘录并显示了第二组的每个测量灵敏度与第一组五个测量的平均测量灵敏度的相对比率。
165、[表2]
166、添加酸性氨基酸时的结果
167、
168、[表3]
169、添加碱性氨基酸和中性氨基酸时的结果
170、
171、
172、首先,描述表2和表3。表2显示了添加酸性氨基酸时获得的结果,表3显示了添加碱性氨基酸或中性氨基酸时获得的结果。在“判定”栏下,“a”表示第二组第一次的相对比率在90%至110%之间,因此是很好的结果,“b”表示第二组第一次的相对比率偏离为90%至110%,但第二次的相对比率偏离为90%至110%之内,因此是好的结果,“c”表明,第二组第一次和第二次的相对比率偏离为90%至110%,但第三次为80%至120%,因此是不充分的但与不添加相比是有效的,“d”表明没有发现任何效果。
173、表2显示,当添加0.5%至1.0%的谷氨酸(一种酸性氨基酸)时(实施例1、2),第二组第一次测量灵敏度与第一组五次测量的平均测量灵敏度的相对比率为102.6%至108.1%,减少了样品b的残留。当添加0.5%的天冬氨酸(一种酸性氨基酸)时,第二组第一次测量灵敏度与第一组五次测量的平均测量灵敏度的相对比率为104.2%,与谷氨酸一样,减少了残留(实施例3)。
174、进一步如表3显示,当以高浓度(5.0%,10%)添加精氨酸(一种碱性氨基酸)时,发现了减少残留的趋势(实施例4,5)。与精氨酸一样,当以高浓度添加赖氨酸(一种碱性氨基酸)时,发现了减少残留的趋势(实施例6、7)。另一方面,当添加中性氨基酸时,未发现与酸性氨基酸相同的减少残留的作用(比较实施例2至12)。
175、上述发现表明,当向稀释剂中添加酸性氨基酸时,即使酸性氨基酸浓度低至约0.5%至1.0%,稀释剂能够减少由吸附在样品探针上的tarc抗原引起的残留。因此,认为当添加酸性氨基酸时,即使在测量具有高浓度tarc抗原的样品后立即测量具有低浓度tarc抗原的样品,也可以以高精度测量具有低浓度tarc抗原的样品。
176、类似地表明了,当碱性氨基酸以高达5.0%至10%的浓度添加到稀释剂中时,碱性氨基酸对tarc抗原吸附到样品探针上时引起的残留具有减少作用。
177、[表4]
178、添加酸性聚合物和表面活性剂时的结果
179、(以聚磺苯乙烯钠、聚丙烯酸钠和聚丙烯酸的名称显示的数值显示了每种化合物的重均分子量)
180、
181、然后,将描述当添加高分子化合物和表面活性剂时获得的结果(表4)。在“判定”栏下,“a”表示第二组第一次的相对比率在90%至110%之内,因此是很好的结果,“b”表示第二组第一次的相对比率偏离为90%至110%,但第二次的相对比率在90%至110%之内,因此是好的结果,“c”表明,第二组第一次和第二次的相对比率偏离为90%至110%,但第三次为90%至110%,因此在一定程度上有效,“d”表明没有发现任何作用。
182、当使用聚磺苯乙烯钠(其中具有磺基的单体聚合的高分子化合物)(实施例8:mw70000,实施例9:mw 200000,实施例10:mw 1000000)和demol rn(实施例11)时,第二组第一次测量灵敏度与第一组五次测量的平均测量灵敏度的相对比率为99.1至104.9%,减少了样品b的残留。使用聚丙烯酸钠(实施例12,分子量22000至70000)和聚丙烯酸(实施例13至15,分子量5000至1000000)这些具有羧基的单体聚合而成的高分子化合物时,也在一定程度上发现了这种作用。当优化分子量,浓度和溶液条件时,预计会获得更好的结果。另一方面,胆酸钠,十二烷基硫酸钠(sds)和enagicol l-30an未显示减少残留作用(比较实施例14至16)。
183、上述发现表明,当加入酸性聚合物聚磺苯乙烯钠(分子量70000至1000000),萘磺酸缩合物(demol rn),聚丙烯酸钠(分子量22000至70000)和聚丙烯酸(分子量5000至1000000)时,稀释剂能够减少tarc抗原吸附在样品探针上时引起的残留。因此,认为当向稀释剂中加入酸性聚合物时,即使在测量具有高浓度tarc抗原的样品后立即测量具有低浓度tarc抗原的样品,也可以以高精度测量具有低浓度tarc抗原的样品。
184、demol rn也具有表面活性剂作用,但在本说明书中被认为是酸性聚合物,因为它在分子中含有磺酸。
185、[表5]
186、添加在分子中具有正电荷的化合物时的结果
187、
188、
189、表5显示了对分子中带有正电荷的例如氨基或季铵盐的化合物的研究结果。评价标准与表2和表3相同,但与不添加(比较实施例1)相比,添加后都没有作用。
190、[表6]
191、酸性聚合物添加浓度的研究(与化合物名称一起显示的数值显示了每种化合物的重均分子量)
192、
193、然后,将描述当聚磺苯乙烯钠(一种酸性聚合物)的添加浓度改变时获得的结果(表6)。在“判定”栏下,“a”显示第二组第一次的相对比率在90%至110%之内,因此是非常好的结果。
194、当聚磺苯乙烯钠的添加浓度从0.002%变为0.050%(实施例16至20:mw 70000,实施例21至25:mw 200000,实施例26至30:mw 1000000)时,第二组第一次测量灵敏度与第一组五次测量的平均测量灵敏度的相对比率为93.8至106.4%,聚磺苯乙烯钠的添加浓度为0.002%至0.050%可减少样品b的残留。
195、工业实用性
196、本发明可以提供不容易导致tarc抗原残留的校准样品和样品的稀释剂。
- 还没有人留言评论。精彩留言会获得点赞!