一种免疫层析试纸盒及其制备方法和应用与流程
1.本发明属于免疫层析技术领域,涉及一种免疫层析试纸盒及其制备方法和应用,尤其涉及一种用于消除动物粪便样本非特异性干扰的免疫层析试纸盒及其制备方法和应用。
背景技术:
2.动物体外诊断试剂需要用到粪便样本的项目有猫瘟病毒(猫泛白细胞减少症病毒)等,但是动物粪便成分中粪胆色素、尿胆素、重金属、细菌蛋白、脱落细胞蛋白等成分会影响到实验检测的结果。以细菌蛋白和脱落细胞蛋白为例,动物粪便中含有大量且多种细菌,比如猫的粪便里细菌有巴东氏杆菌、沙门氏菌病,还可能携带一些寄生虫,如弓形虫、钩虫等,这些生物含有的蛋白质(比如细菌蛋白、脱落细胞蛋白等)很多会作为干扰性抗体,交联捕获抗体和检测抗体,导致分析中的高读数,从而导致假阳性结果等问题。
3.免疫层析技术中对于样本的处理方法有:添加样本稀释液;将阻断剂包被于nc膜上形成一条阻断线;在样品垫的处理配方中添加阻断剂等。市面上大多数样本稀释液成分为糖、盐、封闭剂等;处理样品垫的配方为封闭剂、表面活性剂、缓冲液等,例如处理样品垫的现有技术常规配方为bsa、吐温、pvp-k30等,置于37℃烘干15h,取出后与反应膜和金标垫组装;这种常规技术不能实现宠物体外诊断检测粪便样本的假阳性问题。宠物粪便中的干扰成分为:尿胆素、重金属、细菌蛋白、脱落细胞蛋白等,原有的技术并不能很好的封闭以上干扰物质,在加样检测时会导致干扰物质与反应膜上包被抗体结合,产生假阳性问题。
4.综上,非常有必要提供一种免疫层析试纸盒及其制备方法和应用。
技术实现要素:
5.为了解决现有技术中存在的技术问题,本发明提供了一种免疫层析试纸盒及其制备方法和应用。本发明中的免疫层析试纸盒通过采用合适配方的样品稀释液和样品垫处理液相配合,可以有效地封闭粪便中的干扰因素,可以消除免疫层析检测中动物粪便样本非特异性干扰,有效提升检测的灵敏性和准确度。
6.本发明在第一方面提供了一种免疫层析试纸盒,所述免疫层析试纸盒包括免疫层析试纸条和样品稀释液;所述样品稀释液含有0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.05~0.15w/v%表面活性剂、0.05~0.15w/v%生物防腐剂和0.15~0.25w/v%硫化钠;所述免疫层析试纸条的样品垫经过样品垫处理液处理;所述样品垫处理液含有0.45~0.55w/v%牛血清白蛋白、0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.8~1.5w/v%异嗜性抗体阻断剂、0.8~1.5w/v%树脂和0.45~0.55w/v%兔抗人多克隆抗体。
7.优选地,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2)。
8.优选地,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体
阻断剂、树脂和兔抗人多克隆抗体的质量比为5:2:1:10:10:5;和/或所述样品稀释液含有0.2w/v%硫化钠。
9.优选地,所述样品稀释液和/或所述样品垫处理液中含有的吐温为吐温20;所述样品稀释液和/或所述样品垫处理液中含有的聚乙二醇为聚乙二醇20000;所述表面活性剂为乙二胺四乙酸;所述生物防腐剂为液体生物防腐剂proclin300;和/或所述树脂为聚甲基丙烯酸羟乙酯。
10.优选地,所述样品稀释液采用浓度为0.01~0.03mol/l、ph为7.4的pb缓冲液作为溶剂配制而成;和/或所述样品垫处理液采用浓度为0.08~0.12mol/l、ph为7.4的tris-hcl缓冲液作为溶剂配制而成。
11.优选地,所述免疫层析试纸条为胶体金免疫层析试纸条,所述胶体金免疫层析试纸条包括底板和设置在所述底板上的胶条;所述胶条包括顺次搭接的样品垫、胶体金标记的结合垫、包被有抗体的反应膜和吸水垫;所述反应膜包括检测线t线和质控线c线。
12.本发明在第二方面提供了一种本发明在第一方面所述的免疫层析试纸盒的制备方法,其特征在于,所述方法包括如下步骤:(1)配制所述样品稀释液;(2)配制所述样品垫处理液;(3)提供样品垫,然后将样品垫在所述样品垫处理液中进行浸泡,再经烘干,得到经过样品垫处理液处理的样品垫;(4)将经过样品垫处理液处理的样品垫与结合垫、反应膜、吸水垫以及底板组装形成免疫层析试纸条,由此得到包括免疫层析试纸条和样品稀释液的免疫层析试纸盒。
13.优选地,进行浸泡的时间为2~8h;所述烘干为在37℃烘干15~20h;提供的所述样品垫采用的材质为玻璃纤维;所述反应膜为硝酸纤维素膜;和/或所述底板为聚氯乙烯底板。
14.本发明在第三方面提供了本发明在第一方面所述的免疫层析试纸盒在消除免疫层析检测中动物粪便样本非特异性干扰中的应用。
15.本发明在第四方面提供了本发明在第一方面所述的免疫层析试纸盒在检测猫泛白细胞减少症病毒中的应用。
16.本发明与现有技术相比至少具有如下有益效果:(1)动物粪便成分中的粪胆色素、尿胆素、重金属、细菌蛋白、脱落细胞蛋白等成分会影响到实验检测的结果;现有技术不能很好地解决这种非特异性吸附造成的假阳性结果;本发明中的免疫层析试纸盒通过采用合适配方的样品稀释液和样品垫处理液相配合,特别是其中的na2s、树脂、hbr、rbc等成分缺一不可,如此才可以有效地封闭粪便中的干扰因素如粪胆色素、尿胆素、重金属、细菌蛋白、脱落细胞蛋白等,可以消除免疫层析检测中动物粪便样本非特异性干扰,有效提升检测的灵敏性和准确度,使得样品符合率可以高达90%以上。
17.(2)本发明在一些优选实施方案中发现,所述样品稀释液含有0.19~0.22w/v%硫化钠与所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2)相配合,如此才能最大可能地封闭粪便中的干扰因素如粪胆色素、尿胆素、重金属、细菌蛋白等,更加明显地消除免疫层析检测中动物粪便样本非特异性干扰,有效提升检测的
灵敏性和准确度,能够使得样品符合率达到95%以上。
附图说明
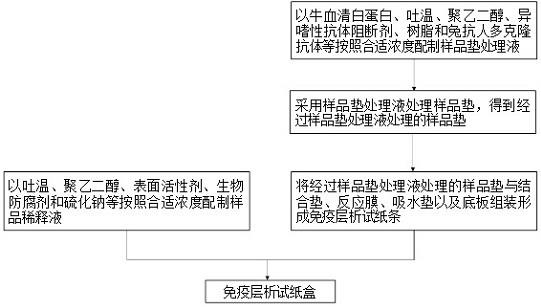
18.图1是本发明一些具体实施方式中制备免疫层析试纸盒的流程图。
19.图2是以10份对比例1中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的假阳性结果图。
20.图3是以10份对比例1中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的阳性结果图。
21.图4是以10份对比例2中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的假阳性结果图。
22.图5是以10份对比例2中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的阳性结果图。
23.图6是以10份对比例3中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的假阳性结果图。
24.图7是以10份对比例3中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的阳性结果图。
25.图8是以10份实施例1中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的阴性结果图。
26.图9是以10份实施例1中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的阳性结果图。
27.在图2至图9中,从右往左的方向为层析方向。
具体实施方式
28.为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述。显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
29.本发明在第一方面提供了一种免疫层析试纸盒,所述免疫层析试纸盒包括免疫层析试纸条和样品稀释液;所述样品稀释液含有0.15~0.25w/v%(例如0.15w/v%、0.16w/v%、0.17w/v%、0.18w/v%、0.19w/v%、0.2w/v%、0.21w/v%、0.22w/v%、0.23w/v%、0.24w/v%或0.25w/v%)吐温、0.05~0.15w/v%(例如0.05w/v%、0.06w/v%、0.07w/v%、0.08w/v%、0.09w/v%、0.1w/v%、0.11w/v%、0.12w/v%、0.13w/v%、0.14w/v%或0.15w/v%)聚乙二醇(peg)、0.05~0.15w/v%(例如0.05w/v%、0.06w/v%、0.07w/v%、0.08w/v%、0.09w/v%、0.1w/v%、0.11w/v%、0.12w/v%、0.13w/v%、0.14w/v%或0.15w/v%)表面活性剂、0.05~0.15w/v%(例如0.05w/v%、0.06w/v%、0.07w/v%、0.08w/v%、0.09w/v%、0.1w/v%、0.11w/v%、0.12w/v%、0.13w/v%、0.14w/v%或0.15w/v%)生物防腐剂和0.15~0.25w/v%(例如0.15w/v%、0.16w/v%、0.17w/v%、0.18w/v%、0.19w/v%、0.2w/v%、0.21w/v%、0.22w/v%、0.23w/v%、0.24w/v%或0.25w/v%)硫化钠(na2s);所述免疫层析试纸条的样品垫经过样品垫处理液处理,即所述免疫层析试纸条的样品垫经样品垫处理液处理后得到;所述样品垫处理液含有0.45~0.55w/v%(例如0.45w/
v%、0.46w/v%、0.47w/v%、0.48w/v%、0.49w/v%、0.5w/v%、0.51w/v%、0.52w/v%、0.53w/v%、0.54w/v%或0.55w/v%)牛血清白蛋白(bsa)、0.15~0.25w/v%(例如0.15w/v%、0.16w/v%、0.17w/v%、0.18w/v%、0.19w/v%、0.2w/v%、0.21w/v%、0.22w/v%、0.23w/v%、0.24w/v%或0.25w/v%)吐温、0.05~0.15w/v%(例如0.05w/v%、0.06w/v%、0.07w/v%、0.08w/v%、0.09w/v%、0.1w/v%、0.11w/v%、0.12w/v%、0.13w/v%、0.14w/v%或0.15w/v%)聚乙二醇(peg)、0.8~1.5w/v%(例如0.8w/v%、0.9w/v%、1w/v%、1.1w/v%、1.2w/v%、1.3w/v%、1.4w/v%或1.5w/v%)异嗜性抗体阻断剂(hbr)、0.8~1.5w/v%(例如0.8w/v%、0.9w/v%、1w/v%、1.1w/v%、1.2w/v%、1.3w/v%、1.4w/v%或1.5w/v%)树脂和0.45~0.55w/v%(例如0.45w/v%、0.46w/v%、0.47w/v%、0.48w/v%、0.49w/v%、0.5w/v%、0.51w/v%、0.52w/v%、0.53w/v%、0.54w/v%或0.55w/v%)兔抗人多克隆抗体(rbc);在本发明中,所述树脂为沸点不大于95℃,与水混溶的液态树脂;本发明中的样品垫处理液采用异嗜性抗体阻断剂(hbr)进行封闭,hbr作为异嗜性抗体阻断剂的优势在于只需要小量蛋白质作封闭,不减弱检信号,hbr比传统方法能阻断更多假阳性;hbr可阻断抗所有种属(比如anti-rabbit, anti-goat, anti-sheep, and anti-mouse等),可阻断抗鼠单克隆抗体的所有亚型(比如anti-mouseigg1,anti-mouse igg2等),rbc也是在消除动物性蛋白的干扰上有很大的作用;本发明对吐温、聚乙二醇(peg)、牛血清白蛋白(bsa)、表面活性剂、生物防腐剂、牛血清白蛋白(bsa)、异嗜性抗体阻断剂(hbr)、树脂以及兔抗人多克隆抗体(rbc)等的来源不做具体的限定,采用市面上可以直接购买的产品或者通过现有方法合成的产品均可;在本发明中,“w/v%”表示的是样品稀释液、样品垫处理液中含有的组分的浓度(终浓度)的单位,表示的是单位“g/100ml”。
30.本发明中的免疫层析试纸盒通过采用合适配方的样品稀释液和样品垫处理液相配合,特别是其中的na2s、树脂、hbr、rbc等成分缺一不可,且除了样品稀释液中的na2s的浓度对结果影响较大之外,样品垫处理液中含有的各成分之间需要具有合适的浓度配比,特别是树脂、hbr、rbc、牛血清白蛋白之间需要具有合适的浓度配比,这些成分的共同作用,才可以有效地封闭粪便中的干扰因素如粪胆色素、尿胆素、重金属、细菌蛋白、脱落细胞蛋白等,从而可以有效消除免疫层析检测中动物粪便样本非特异性干扰,有效提升检测的灵敏性和准确度,而在本发明的研究过程中,本发明发现样品垫处理液各组分之间的浓度配比的选择并没有任何具有指导性的规律可循,特别是牛血清白蛋白、hbr、树脂、rbc中任一种组分或者两种以上组分的浓度不合适,均可能会对检测结果产生比较大的影响,本发明是经过大量创造性试验,给出了样品垫处理液中各组分的合适浓度配比;此外,本发明发现,硫化钠(na2s)需要加入到样品稀释液中,所述硫化钠在样品稀释液中才能保持硫离子的活性,而树脂、hbr、rbc则需要加入到所述样品垫处理液中,树脂与hbr、rbc一起加入才具有好的效果,本发明将硫化钠与树脂、hbr、rbc分开加入,如此能够保证有效地封闭粪便中的干扰因素。
31.根据一些优选的实施方式,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.5~5.5):(1.5~2.5):(0.5~1.5):(9~12):(9~12):(4.5~5.5),优选为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2),更优选为(4.8~5.2):(1.5~2):(1~1.2):(9~10):(9~10):(5~5.2)。
32.根据一些优选的实施方式,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为5:2:1:10:10:5;和/或所述
样品稀释液含有0.2w/v%硫化钠。
33.本发明在一些优选实施方案中发现,所述样品稀释液含有0.19~0.22w/v%硫化钠更优选为0.2w/v%与所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2)更优选为质量比为5:2:1:10:10:5相配合,如此才能最大可能地封闭粪便中的干扰因素如粪胆色素、尿胆素、重金属、细菌蛋白等,更加明显地消除免疫层析检测中动物粪便样本非特异性干扰,有效提升检测的灵敏性和准确度,使得样品符合率达到95%以上,甚至可以使得样品符合率高达98%以上。
34.根据一些优选的实施方式,所述样品稀释液和/或所述样品垫处理液中含有的吐温为吐温20;所述样品稀释液和/或所述样品垫处理液中含有的聚乙二醇为聚乙二醇20000;所述表面活性剂为乙二胺四乙酸(edta);所述生物防腐剂为液体生物防腐剂proclin300;和/或所述树脂为聚甲基丙烯酸羟乙酯;在本发明中,液体生物防腐剂proclin300即指的是proclin300,本发明对proclin300、聚甲基丙烯酸羟乙酯的来源不做具体的限定,采用市面上可以直接购买的产品或者通过现有方法合成的产品均可。
35.根据一些优选的实施方式,所述样品稀释液采用浓度为0.01~0.03mol/l(例如0.01、0.02或0.03mol/l)、ph为7.4的pb缓冲液作为溶剂配制而成;和/或所述样品垫处理液采用浓度为0.08~0.12mol/l(例如0.08、0.09、0.10、0.11或0.12mol/l)、ph为7.4的tris-hcl缓冲液作为溶剂配制而成;本发明对pb缓冲液和tris-hcl缓冲液不做具体的限定,可以采用市面上可以直接购买的产品或者通过现有方法配制而成均可,只要pb缓冲液的浓度为0.01~0.03mol/l,ph为7.4,tris-hcl缓冲液的浓度为0.08~0.12mol/l、ph为7.4即可。
36.在本发明中,优选的是,所述样品稀释液采用0.01~0.03mol/l、ph为7.4的pb缓冲液作为溶剂配制而成,所述样品垫处理液采用0.08~0.12mol/l、ph为7.4的tris-hcl缓冲液作为溶剂配制而成,与样品稀释液、样品垫处理液的各组分更匹配的溶剂的使用,可以更加有效地封闭粪便中的干扰因素如粪胆色素、尿胆素、重金属、细菌蛋白、脱落细胞蛋白等,更有效提升检测的灵敏性和准确度;本发明发现,若样品稀释液采用tris-hcl缓冲液作为溶剂,样品垫处理液采用pb缓冲液,则会降低试纸盒的检测灵敏性和准确度,导致出现较高的假阳性。
37.根据一些优选的实施方式,所述免疫层析试纸条为胶体金免疫层析试纸条,所述胶体金免疫层析试纸条包括底板和设置在所述底板上的胶条;所述胶条包括顺次搭接的样品垫、胶体金标记的结合垫、包被有抗体的反应膜和吸水垫;所述反应膜包括检测线t线和质控线c线;在本发明中,也可以将样品垫记作加样垫,所述免疫层析试纸条也可以存在于检测板中,即例如所述免疫层析试纸盒还包括密封扣合的上盖和下盖,所述上盖上设有加样孔和检测窗,所述下盖上设有卡槽,所述卡槽内放置有免疫层析试纸条,所述免疫层析试纸条的反应膜的位置与所述检测窗的位置相对应,所述免疫层析试纸条的样品垫(加样垫)的位置与加样孔相对应。
38.在本发明中,所述免疫层析试纸盒例如可以以猫泛白细胞减少症病毒作为检测对象,采用的胶体金标记的结合垫和包被有抗体的反应膜为本领域的常规技术,胶体金标记的标记抗体与反应膜的检测线t线包被抗体配对使用,没有特别的要求,只要适用于猫泛白细胞减少症病毒检测即可;在本发明的一些具体实施例以及对比例中,所述反应膜的检测
线t线包被的抗体为猫泛白细胞减少症病毒单克隆抗体7e3(产品名称简记为:fpv-7e3),该产品购买自郑州凌思生物科技有限责任公司,批次为20220416,所述胶体金标记的标记抗体为猫泛白细胞减少症病毒单克隆抗体5g6(产品名称简记为:fpv-5g6),该产品购买自郑州凌思生物科技有限责任公司,批次为20220221,fpv-7e3与fpv-5g6配对使用,所述反应膜的质控线c线包被的抗体为羊抗鼠抗体(羊抗鼠igg抗体)。
39.本发明在第二方面提供了一种本发明在第一方面所述的免疫层析试纸盒的制备方法,其特征在于,所述方法包括如下步骤:(1)配制所述样品稀释液;(2)配制所述样品垫处理液;(3)提供样品垫,然后将样品垫在所述样品垫处理液中进行浸泡,再经烘干(即烘烤),得到经过样品垫处理液处理的样品垫;在本发明中,例如可以以玻璃纤维为材质得到样品垫,本发明对玻璃纤维不做具体的限定,例如可以采用密度为0.15~0.65g/cm3的玻璃纤维,本发明采用玻璃纤维制成玻璃纤维膜作为样品垫为本领域的常规技术;具体地,将玻璃纤维制成玻璃纤维膜裁切成合适的尺寸大小,得到整张样品垫(该整张样品垫可以裁成用于免疫层析试纸条的多条样品垫),然后将整张样品垫在所述样品垫处理液中进行浸泡,本发明在浸泡时,对样品垫处理液的用量不做具体的限定,为本领域的常规技术,使得整张样品垫完全浸没在所述样品垫处理液中即可,在一些具体的实施例中,例如将一整张样品垫浸泡在样品垫处理液中,以免疫层析试纸条中,每条样品垫对应的样品垫处理液的用量例如可以为3~6ml优选为5ml为标准进行整张样品垫对应的样品垫处理液用量的计算;然后,将浸泡后的样品垫置于37℃烘箱中,并使所述样品垫在烘箱中15-20h后,使得样品垫达到稳定的状态,从而得到经过样品垫处理液处理的样品垫;在未使用样品垫的情况下,可以将经过样品垫处理液处理的样品垫放入密封袋加入干燥剂保存,从而延长样品垫的使用时效。
40.(4)将经过样品垫处理液处理的样品垫与结合垫、反应膜、吸水垫以及底板组装形成免疫层析试纸条;优选的是,所述结合垫为胶体金标记的结合垫;在本发明中,将胶体金标记的结合垫也记作金标垫,本发明对结合垫(例如采用玻璃纤维膜制成的结合垫)进行胶体金标记为本领域的常规技术,例如可以是将胶体金溶液(例如可以采用100od值胶体金溶液)、缓冲液和标记抗体混匀后偶联2h后封闭1h,离心复溶后将溶液喷到结合垫上放入烘箱4h后裁切得到胶体金标记的结合垫(金标垫);在本发明中,所述反应膜为包被有抗体的反应膜,所述反应膜包括检测线t线和质控线c线,包被有抗体的反应膜的制备为本领域的常规技术,例如可以是配制包被溶液后,使用划膜仪将包被的c线和t线抗体划上,烘干备用。
41.根据一些优选的实施方式,进行浸泡的时间为2~8h(例如2、3、4、5、6、7或8h);优选的是,在室温(例如室温15~30℃)下进行浸泡2~8h;所述烘干为在37℃烘干15~20h(例如15、16、17、18、19或20h);提供的所述样品垫采用的材质为玻璃纤维;所述反应膜为硝酸纤维素膜(nc膜);和/或所述底板为聚氯乙烯底板(pvc底板)。
42.本发明在第三方面提供了本发明在第一方面所述的免疫层析试纸盒在消除免疫层析检测中动物粪便样本非特异性干扰中的应用;优选的是,对于每一份免疫层析试纸盒,配制的样品稀释液为400~600μl,将动物粪便样本稀释于400~600μl的样品稀释液得到检测样本,对于每条免疫层析试纸条,检测样本的用量为55~65μl,更优选的是,对于每一份免疫
层析试纸盒,配制的样品稀释液为500μl,对应的检测样本用量为60μl/条;本发明对稀释前,动物粪便样本的取量不做具体的限定,按照本领域的常规操作取用即可,例如用棉签蘸取适量动物粪便即可。
43.本发明在第四方面提供了本发明在第一方面所述的免疫层析试纸盒在检测猫泛白细胞减少症病毒中的应用。
44.本发明还提供了一种用于处理免疫层析试纸盒的样品垫的样品垫处理液,所述样品垫处理液含有0.45~0.55w/v%牛血清白蛋白、0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.8~1.5w/v%异嗜性抗体阻断剂、0.8~1.5w/v%树脂和0.45~0.55w/v%兔抗人多克隆抗体;所述样品垫处理液与样品稀释液配合使用,所述样品稀释液含有0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.05~0.15w/v%表面活性剂、0.05~0.15w/v%生物防腐剂和0.15~0.25w/v%硫化钠;优选的是,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2),更优选为5:2:1:10:10:5;优选的是,所述样品稀释液含有0.2w/v%硫化钠;优选的是,所述样品稀释液和/或所述样品垫处理液中含有的吐温为吐温20;所述样品稀释液和/或所述样品垫处理液中含有的聚乙二醇为聚乙二醇20000;所述表面活性剂为乙二胺四乙酸;所述生物防腐剂为液体生物防腐剂proclin300;所述树脂为聚甲基丙烯酸羟乙酯;所述样品稀释液采用浓度为0.01~0.03mol/l、ph为7.4的pb缓冲液作为溶剂配制而成;和/或所述样品垫处理液采用浓度为0.08~0.12mol/l、ph为7.4的tris-hcl缓冲液作为溶剂配制而成。
45.本发明还提供了一种用于免疫层析试纸盒的样品稀释液,所述样品稀释液含有0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.05~0.15w/v%表面活性剂、0.05~0.15w/v%生物防腐剂和0.15~0.25w/v%硫化钠(na2s);所述样品稀释液与用于处理免疫层析试纸盒的样品垫的样品垫处理液配合使用,所述样品垫处理液含有0.45~0.55w/v%牛血清白蛋白、0.15~0.25w/v%吐温、0.05~0.15w/v%聚乙二醇、0.8~1.5w/v%异嗜性抗体阻断剂、0.8~1.5w/v%树脂和0.45~0.55w/v%兔抗人多克隆抗体;优选的是,所述样品垫处理液中含有的牛血清白蛋白、吐温、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体的质量比为(4.8~5.2):(1.5~2.5):(0.8~1.2):(9~12):(9~12):(5~5.2),更优选为5:2:1:10:10:5;优选的是,所述样品稀释液含有0.2w/v%硫化钠;优选的是,所述样品稀释液和/或所述样品垫处理液中含有的吐温为吐温20;所述样品稀释液和/或所述样品垫处理液中含有的聚乙二醇为聚乙二醇20000;所述表面活性剂为乙二胺四乙酸;所述生物防腐剂为液体生物防腐剂proclin300;所述树脂为聚甲基丙烯酸羟乙酯;所述样品稀释液采用浓度为0.01~0.03mol/l、ph为7.4的pb缓冲液作为溶剂配制而成;和/或所述样品垫处理液采用浓度为0.08~0.12mol/l、ph为7.4的tris-hcl缓冲液作为溶剂配制而成。
46.下文将通过举例的方式对本发明进行进一步的说明,但是本发明的保护范围不限于这些实施例。本发明还可有其它多种实施例,在不背离本发明精神及其实质的情况下,熟悉本领域的技术人员可根据本发明作出各种相应的改变和变形,但这些相应的改变和变形都应属于本发明所附的权利要求的保护范围。
47.实施例1一种免疫层析试纸盒,所述免疫层析试纸盒包括免疫层析试纸条和样品稀释液;
其中,用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)、生物防腐剂(proclin300)和na2s配制成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)、0.1w/v%生物防腐剂(proclin300)和0.2w/v%硫化钠(na2s),配方如下表1所示。
48.表1所述免疫层析试纸条的制备包括:
①
用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白(bsa)、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.5w/v%兔抗人多克隆抗体(rbc),配方如下表2所示。
49.表2
②
采用玻璃纤维制成玻璃纤维膜,即得到样品垫;将样品垫在所述样品垫处理液中进行浸泡5h,浸泡每条样品垫所需的样品垫处理液的用量为5ml,然后将浸泡后的样品垫置于37℃烘箱中,并将所述样品垫在烘箱中烘干(烘烤)15h,使得样品垫达到稳定的状态,得到经过样品垫处理液处理的样品垫。
50.③
以猫泛白细胞减少症病毒检测为实验对象,制造出胶体金标记的结合垫和包被有抗体的nc膜;所述nc膜包括检测线t线和质控线c线;将经过样品垫处理液处理的样品垫与胶体金标记的结合垫、包被有抗体的nc膜、吸水垫以及底板(pvc底板)组装形成免疫层析试纸条。
51.实施例2实施例2与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白、0.15w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.45w/v%兔抗人多克隆抗体(rbc)。
52.实施例3实施例3与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.55w/v%牛血清白蛋白、0.2w/v%吐温20、0.15w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.55w/v%兔抗人多克隆抗体(rbc)。
53.实施例4实施例4与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.48w/v%牛血清白蛋白、0.15w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)、0.9w/v%树脂(聚甲基丙烯酸羟乙酯)和0.5w/v%兔抗人多克隆抗体(rbc)。
54.实施例5实施例5与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.52w/v%牛血清白蛋白、0.2w/v%吐温20、0.12w/v%聚乙二醇(peg20000)、0.9w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.52w/v%兔抗人多克隆抗体(rbc)。
55.实施例6实施例6与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.3w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.5w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.3w/v%兔抗人多克隆抗体(rbc)。
56.实施例7实施例7与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液
中含有0.4w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.8w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.4w/v%兔抗人多克隆抗体(rbc)。
57.实施例8实施例8与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.6w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1.5w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.5w/v%兔抗人多克隆抗体(rbc)。
58.实施例9实施例9与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.35w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.5w/v%异嗜性抗体阻断剂(hbr)、0.5w/v%树脂(聚甲基丙烯酸羟乙酯)和0.6w/v%兔抗人多克隆抗体(rbc)。
59.实施例10实施例10与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)、生物防腐剂(proclin300)和硫化钠(na2s)配制成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)、0.1w/v%生物防腐剂(proclin300)和0.15w/v%硫化钠(na2s)。
60.实施例11实施例11与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)、生物防腐剂(proclin300)和硫化钠(na2s)配制成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)、0.1w/v%生物防腐剂(proclin300)和0.25w/v%硫化钠(na2s)。
61.对比例1对比例1与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)和生物防腐剂(proclin300)配制成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)和0.1w/v%生物防腐剂(proclin300)。
62.用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20和聚乙二醇配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白、0.2w/v%吐温20和0.1w/v%聚乙二醇(peg20000)。
63.对比例2
对比例2与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20和聚乙二醇配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白、0.2w/v%吐温20和0.1w/v%聚乙二醇(peg20000)。
64.对比例3对比例3与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)和生物防腐剂(proclin300)配制成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)和0.1w/v%生物防腐剂(proclin300)。
65.对比例4对比例4与实施例1基本相同,不同之处在于:用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)、生物防腐剂(proclin300)和na2s配制而成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)、0.1w/v%生物防腐剂(proclin300)和0.2w/v%硫化钠(na2s)。
66.用浓度为0.02mol/l、ph=7.4的pb缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白(bsa)、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)和0.5w/v%兔抗人多克隆抗体(rbc)。
67.对比例5对比例5与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)、生物防腐剂(proclin300)、na2s和树脂配制而成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)、0.1w/v%生物防腐剂(proclin300)、0.2w/v%硫化钠(na2s)和1w/v%树脂(聚甲基丙烯酸羟乙酯)。
68.用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂和兔抗人多克隆抗体配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/v%异嗜性抗体阻断剂(hbr)和0.5w/v%兔抗人多克隆抗体(rbc)。
69.对比例6对比例6与实施例1基本相同,不同之处在于:用浓度为0.02mol/l、ph=7.4的pb缓冲液将吐温20、聚乙二醇(peg20000)、表面活性剂(edta)和proclin300配制而成样品稀释液,所述样品稀释液中含有0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、0.1w/v%表面活性剂(edta)和0.1w/v%生物防腐剂(proclin300)。
70.用浓度为0.1mol/l、ph=7.4的tris-hcl缓冲液将牛血清白蛋白、吐温20、聚乙二醇、异嗜性抗体阻断剂、树脂、兔抗人多克隆抗体和硫化钠配制成样品垫处理液,所述样品垫处理液中含有0.5w/v%牛血清白蛋白、0.2w/v%吐温20、0.1w/v%聚乙二醇(peg20000)、1w/
v%异嗜性抗体阻断剂(hbr)、1w/v%树脂(聚甲基丙烯酸羟乙酯)、0.5w/v%兔抗人多克隆抗体(rbc)和0.2w/v%硫化钠(na2s)。
71.性能检测一检测方法:以猫泛白细胞减少症病毒检测为实验对象,每份检测样本均是采用猫的粪便样本稀释于500μl样品稀释液中,得到检测样本,每条免疫层析试纸条对应的检测样本用量为60μl,等待15min后判定结果。
72.以10份对比例1中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的结果均为假阳性,结果如图2所示。
73.以10份对比例1中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的结果均为阳性,结果如图3所示。
74.以10份对比例2中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的结果均为假阳性,结果如图4所示。
75.以10份对比例2中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的结果均为阳性,结果如图5所示。
76.以10份对比例3中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的结果均为假阳性,结果如图6所示。
77.以10份对比例3中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的结果均为阳性,结果如图7所示。
78.以10份实施例1中的免疫层析试纸盒测试10份阴性样本,10条免疫层析试纸条显示的结果均为阴性,结果如图8所示。
79.以10份实施例1中的免疫层析试纸盒测试10份阳性样本,10条免疫层析试纸条显示的结果均为阳性,结果如图9所示。
80.性能检测二检测方法:以猫泛白细胞减少症病毒检测为实验对象,每份检测样本均是采用猫的粪便样本稀释于500μl样品稀释液中,得到检测样本,每条免疫层析试纸条对应的检测样本用量为60μl,等待15min后判定结果,具体是以实施例1~11以及对比例1~6中的免疫层析试纸盒各100份测试100份阴性样本,阴性样本来自宠物医院pcr检测(病毒核酸检测)为阴性的猫个体,得到假阳率的结果如表3所示,与核酸检测结果符合率结果如表3所示。
81.表3
本发明未详细说明部分为本领域技术人员公知技术,本领域技术人员可以根据需要进行选择。
82.最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1