正极材料和电池的制作方法
1.本公开涉及正极材料和电池。
背景技术:
2.专利文献1公开了一种全固体锂电池,其含有以硫化物为主体的锂离子传导性固体电解质、以及表面由锂离子传导性氧化物被覆了的活性物质。
3.非专利文献1记载了在使用硫化物固体电解质的电池中,在初期充电后,在正极材料与硫化物固体电解质的界面形成界面层,电池的电阻增加。
4.在先技术文献
5.专利文献1:国际公开第2007/004590号
6.非专利文献1:chemistry ofmaterials,am.chem.soc.2010,vol.22,3,949-956
技术实现要素:
7.发明要解决的课题
8.本公开提供一种能够降低电池电阻、进而提高充放电效率的正极材料。
9.用于解决课题的手段
10.本公开的正极材料,包含第1固体电解质、正极活性物质、以及被覆所述正极活性物质的表面的被覆材料。
11.所述第1固体电解质由下述组成式(1)表示。
12.liambocxd···
式(1)
13.在所述组成式(1)中,a、b、c和d是正实数,m是选自ta和nb中的至少一种,并且x是选自cl、br和i中的至少一种。
14.发明的效果
15.本公开提供一种能够降低电池电阻、进而提高充放电效率的正极材料。
附图说明
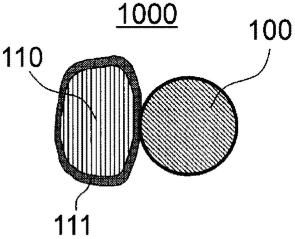
16.图1是表示实施方式1中的正极材料的大致结构的剖视图。
17.图2是表示实施方式2中的电池的大致结构的剖视图。
18.图3是表示实施例1中的电池的3.7v的奈奎斯特线图的图。
19.图4a是表示实施例1中使用的活性物质的x射线光电子能谱法的o1s光谱的图。
20.图4b是表示实施例1中使用的活性物质的x射线光电子能谱法的o1s光谱、和没有由被覆材料被覆表面的活性物质的x射线光电子能谱法的o1s光谱的图。
具体实施方式
21.(成为本公开的基础的见解)
22.专利文献1公开了一种全固体理电池,其含有以硫化物为主体的锂离子传导性固
体电解质、以及表面由锂离子传导性氧化物被覆了的活性物质。专利文献1记载了特别是通过使用铌酸锂(即linbo3)作为锂离子传导性氧化物,能够抑制在硫化物固体电解质与正极活性物质表面之间生成高电阻层,显著提高输出特性。
23.非专利文献1记载了在硫化物固体电解质与正极活性物质表面之间生成高电阻层的原因在于,正极活性物质中所含的金属元素和构成固体电解质的硫元素(即s)的相互扩散。即、上述那样的高电阻层的生成是由于作为固体电解质的构成元素的s。
24.根据由专利文献1和非专利文献1记载的发明而得到的见解,在电池使用硫化物作为固体电解质的情况下,如果不利用例如锂离子传导性氧化物这样的被覆材料被覆活性物质的表面来充分抑制活性物质与固体电解质的接触,则活性物质与固体电解质的界面的电阻变高,极化增大,因此实质上难以作为电池进行工作。另一方面,在电池使用不含s的固体电解质的情况下,即使不利用锂离子传导性氧化物被覆活性物质的表面,也能够作为电池进行工作。
25.但是,本发明人等进行了深入研究,结果发现即使在使用不含s的固体电解质作为正极材料中所含的固体电解质的情况下,通过由被覆材料被覆活性物质的表面,电池的电阻也会降低。其理由尚不明确,认为是被覆材料的耐电压性、作为电池的固体电解质而使用的锂离子传导性固体电解质的耐氧化性、被覆材料与活性物质的反应性、被覆材料与固体电解质的反应性、以及活性物质与固体电解质的物理接触性等各种因素的综合贡献。
26.例如,在作为电池的固体电解质而使用的锂离子传导性固体电解质为卤化物的情况下,如果在电池的充电过程中正极的电位变高,则会诱发固体电解质中所含的卤素的氧化。通过这样的卤素的氧化而发生固体电解质的分解。另外,如果发生卤素的氧化反应,则会产生卤素气体,从而在活性物质与固体电解质的接触界面产生间隙,减少有效的反应面积。由此,电池的电阻增大。通过使被覆活性物质表面的被覆材料介于活性物质与固体电解质之间,能够抑制固体电解质与高电位的活性物质接触,因此能够抑制卤素的氧化。基于这些理由,认为能够降低电池的电阻。
27.根据以上见解,本发明人实现了能够降低电池电阻的以下的本公开的正极材料。
28.(本公开涉及的一个技术方案的概要)
29.本公开的第1技术方案涉及的正极材料,包含第1固体电解质、正极活性物质、以及被覆所述正极活性物质的表面的被覆材料。
30.在此,所述第1固体电解质由下述组成式(1)表示。
31.liambocxd···
式(1)
32.在所述组成式(1)中,a、b、c和d是正实数,m是选自ta和nb中的至少一种,并且x是选自cl、br和i中的至少一种。
33.第1技术方案涉及的正极材料中,被覆材料介于正极活性物质与作为卤化物固体电解质的第1固体电解质之间。通过该被覆材料,即使在电池的充电过程中正极的电位变高的情况下,也能够抑制相对于卤化物固体电解质的电子授受。因此,卤化物固体电解质中的卤素的氧化反应得到抑制,从而抑制了第1固体电解质的分解,并且也抑制了卤素气体的产生。其结果,抑制了第1固体电解质的劣化,并且也抑制了正极活性物质与第1固体电解质的有效反应面积的减少。基于这些理由,第1技术方案涉及的正极材料能够降低电池的电阻。其结果,第1技术方案涉及的正极材料也能够提高电池的充放电效率。
34.本公开的第2技术方案中,例如在第1技术方案涉及的正极材料的基础上可以设为:所述被覆材料包含o。
35.第2技术方案涉及的正极材料,能够更有效地降低电池的电阻,进一步提高充放电效率。
36.本公开的第3技术方案中,例如在第1或第2技术方案涉及的正极材料的基础上可以设为:所述被覆材料包含f。
37.第3技术方案涉及的正极材料,能够更有效地降低电池的电阻。
38.本公开的第4技术方案中,例如在第1~第3技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含选自b、n、p、s和si中的至少一种。
39.通过被覆材料包含选自b、n、p、s和si中的至少一种,能够在正极活性物质表面形成电子传导性低的被覆物。因此,第4技术方案涉及的正极材料能够进一步减少第1固体电解质的氧化反应。另外,b、n、p、s和si这样的元素与氧形成强的共价键。因此,被覆材料中的电子离域化,从而使由被覆材料构成的被覆物的电子传导性变低。所以,即使在正极活性物质的表面上的被覆材料的厚度变薄的情况下,也能够阻断正极活性物质与第1固体电解质的电子的授受,从而能够更有效地抑制第1固体电解质的氧化反应。因此,第4技术方案涉及的正极材料能够更有效地降低电池的电阻,进一步提高充放电效率。
40.本公开的第5技术方案中,例如在第1~第4技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含以非金属或半金属为阳离子的含氧酸盐。
41.第5技术方案涉及的正极材料,能够更有效地降低电池的电阻。
42.本公开的第6技术方案中,例如在第1~第5技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含玻璃形成氧化物。
43.第6技术方案涉及的正极材料,能够提高被覆材料中的锂离子传导率。具体而言,通过被覆材料含有磷酸或硅酸这样的被称为玻璃形成氧化物的氧化物的锂化合物,使得被覆物的一部分非晶质化,离子传导路径变宽。因此,认为能够提高被覆材料中的锂离子传导率。由此,第6技术方案涉及的正极材料能够更有效地降低电池的电阻。
44.本公开的第7技术方案中,例如在第1~第6技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含中间氧化物。
45.第7技术方案涉及的正极材料,能够提高被覆材料中的锂离子传导率。具体而言,通过被覆材料含有铌酸这样的被称为中间氧化物的氧化物的锂化合物,使得被覆物的一部分非晶质化,离子传导路径变宽。因此,认为能够提高被覆材料中的锂离子传导率。由此,第6技术方案涉及的正极材料能够更有效地降低电池的电阻。
46.本公开的第8技术方案中,例如在第1~第7技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含li。
47.第8技术方案涉及的正极材料,能够提高正极活性物质与第1固体电解质的界面的载流子浓度、即li浓度。因此,第8技术方案涉及的正极材料能够更有效地降低电池的电阻。
48.本公开的第9技术方案中,例如在第1~第8技术方案中任一方案涉及的正极材料的基础上可以设为:所述被覆材料包含选自磷酸锂、铌酸锂、氟磺酸锂和双(氟磺酰)亚胺锂中的至少一种。
49.磷酸锂和铌酸锂能够提高被覆材料的锂离子传导率。另外,氟磺酸锂和双(氟磺
酰)亚胺锂能够形成正极活性物质与第1固体电解质的良好的界面、即电阻低的界面。由此,第9技术方案涉及的正极材料能够更有效地降低电池的电阻。
50.本公开的第10技术方案中,例如在第1~第9技术方案中任一方案涉及的正极材料的基础上可以设为:所述x包含cl。
51.第10技术方案涉及的正极材料中,能够进一步提高第1固体电解质的离子导电率。由此,第10技术方案涉及的正极材料能够进一步提高电池的充放电效率。
52.本公开的第11技术方案中,例如在第1~第10技术方案中任一方案涉及的正极材料的基础上可以设为:所述正极活性物质包含含锂的过渡金属氧化物。
53.第11技术方案涉及的正极材料,能够提高电池的能量密度。
54.本公开的第12技术方案涉及的电池,具备正极、负极、以及配置于所述正极与所述负极之间的电解质层,所述正极包含第1~第11技术方案中任一方案涉及的正极材料。
55.第12技术方案涉及的电池,能够降低电阻,进一步提高充放电效率。
56.本公开的第13技术方案中,例如在第12技术方案涉及的电池的基础上可以设为:所述电解质层包含硫化物固体电解质。
57.在第13技术方案涉及的电池中,能够降低电阻,进一步提高充放电效率。
58.以下,参照附图对本公开的实施方式进行说明。
59.(实施方式1)
60.图1是表示实施方式1中的正极材料1000的大致结构的剖视图。实施方式1中的正极材料1000包含第1固体电解质100、正极活性物质110、以及被覆正极活性物质110表面的被覆材料111。如图1所示,第1固体电解质100和正极活性物质110可以是粒子状。另外,被覆材料111既可以被覆正极活性物质110的整个表面,也可以部分地被覆正极活性物质110的表面。即、被覆材料111只要被覆正极活性物质110的表面的至少一部分即可。换言之,正极活性物质110和第1固体电解质100由被覆材料111隔开,存在相互不接触的部分。正极活性物质110和第1固体电解质100也可以存在相互接触的部分。
61.第1固体电解质100由下述组成式(1)表示。
62.liambocxd···
式(1)
63.在上述组成式(1)中,a、b、c和d是正实数。m是选自ta和nb中的至少一种。x是选自cl、br和i中的至少一种。
64.在本实施方式的正极材料1000中,被覆材料111介于正极活性物质110与作为卤化物固体电解质的第1固体电解质100之间。通过该被覆材料111,即使在电池的充电过程中正极的电位变高的情况下,也能够抑制相对于卤化物固体电解质的电子授受。因此,抑制了第1固体电解质100中的卤素的氧化反应,从而抑制了第1固体电解质100的分解,并且也抑制了由氧化反应引起的卤素气体的产生。其结果,抑制了第1固体电解质100的劣化,并且也抑制了正极活性物质110与第1固体电解质100的有效反应面积的减少。基于这些理由,本实施方式中的正极材料1000能够降低电池的电阻。其结果,第1技术方案涉及的正极材料1000也能够提高电池的充放电效率。
65.如上所述,被覆材料111可以同样地被覆正极活性物质110的整个表面。由此,能够抑制正极活性物质110与第1固体电解质100的直接接触,更切实地抑制第1固体电解质100的氧化反应。因此,能够进一步提高电池的充放电特性,并且抑制电池的反应过电压的上
升。
66.或者,被覆材料111也可以被覆正极活性物质110的表面的一部分。多个正极活性物质110的粒子彼此经由未被被覆材料111被覆的部分而直接接触,由此正极活性物质110的粒子间的电子传导性提高。因此,能够实现电池的高输出工作。
67.被覆材料111例如可以使用电子传导性低的材料。作为被覆材料111,例如可以使用含有o的材料。例如,含有o的材料的例子有氧化物材料或氧化物固体电解质。
68.可用于被覆材料111的氧化物材料例如有sio2、al2o3、tio2、b2o3、nb2o5、wo3或zro2等。可用于被覆材料111的氧化物固体电解质例如有li3po4等li-p-o化合物、linbo3等li-nb-o化合物、libo2、li3bo3等li-b-o化合物、lialo2等li-al-o化合物,li4sio4等li-si-o化合物、li2so4、li4ti5o
12
等li-ti-o化合物、li2zro3等li-zr-o化合物、li2moo3等li-mo-o化合物、liv2o5等li-v-o化合物、或li2wo4等li-w-o化合物等。
69.被覆材料111可以包含氧化物固体电解质。氧化物固体电解质的离子导电率高且高电位稳定性高。因此,通过使用氧化物固体电解质,能够进一步提高充放电效率。
70.被覆材料111可以包含含氧酸盐。通过被覆材料111含有含氧酸盐,能够更有效地降低电池的电阻。含氧酸盐可以是以非金属或半金属为阳离子的含氧酸盐。如上所述,“半金属元素”是指b、si、ge、as、sb和te。“非金属元素”是指n、p、s、cl、br和i。即、这些元素是与氧结合而生成含氧酸的元素组。
71.被覆材料111可以含有选自b、n、p、s和si中的至少一种。
72.通过被覆材料111含有选自b、n、p、s和si中的至少一种,能够在正极活性物质110的表面形成电子传导性低的被覆物。因此,实施方式1中的正极材料1000能够进一步减少第1固体电解质100的氧化反应。此外,b、n、p、s和si这样的元素与氧形成强的共价键。因此,被覆材料111中的电子离域化,从而由被覆材料111构成的被覆物的电子传导性变低。所以,即使在正极活性物质110的表面上的被覆材料111的厚度变薄的情况下,也能够阻断正极活性物质111与第1固体电解质100的电子的授受,从而能够更有效地抑制第1固体电解质100的氧化反应。因此,通过被覆材料111含有选自b、n、p、s和si中的至少一种,正极材料1000能够更有效地降低电池的电阻,进一步提高充放电效率。
73.被覆材料111可以含有li。根据该结构,能够提高正极活性物质110与第1固体电解质100的界面处的载流子浓度,从而能够更有效地降低电池的电阻。
74.在被覆材料111含有li的情况下,被覆材料111中的锂与其他阳离子的摩尔比li/(其他阳离子)可以为0.2以上且3.6以下,也可以为0.2以上且3.0以下。通过摩尔比li/(其他阳离子)为0.2以上且3.6以下,能够提高被覆材料111中的锂离子传导率。由此,能够更有效地降低电池的电阻。
75.被覆材料111可以包含磷酸或硅酸这样的玻璃形成氧化物。在此,玻璃形成氧化物是指即使单独也能够形成玻璃的网眼形成氧化物。成为能够形成玻璃形成氧化物的阳离子的元素、即被称为网眼形成体的元素,例如有si、p、b、ge和v等。通过被覆材料111含有玻璃形成氧化物,能够提高被覆材料111中的锂离子传导率。具体而言,通过被覆材料111含有磷酸或硅酸这样的被称为玻璃形成氧化物的氧化物的锂化合物,使得被覆物的一部分非晶质化,离子传导路径变宽。因此,能够提高被覆材料111中的锂离子传导率,能够更有效地降低电池的电阻。
76.被覆材料111可以包含铌酸这样的中间氧化物。在此,中间氧化物是指不能单独形成玻璃(即、不能单独形成玻璃的网眼),但根据组成能够形成玻璃或进入玻璃的网眼的氧化物。成为能够形成中间氧化物的阳离子的元素例如有nb、ti、zn、al和zr等。通过被覆材料111含有中间氧化物,能够提高被覆材料111中的锂离子传导率。具体而言,通过被覆材料111含有铌酸这样的被称为中间氧化物的氧化物的锂化合物,使得被覆物的一部分非晶质化,离子传导路径变宽。因此,能够提高被覆材料111中的锂离子传导率,能够更有效地降低电池的电阻。
77.被覆材料111可以含有选自磷酸锂、铌酸锂、氟磺酸锂和双(氟磺酰)亚胺锂中的至少一种。
78.磷酸锂和铌酸锂能够提高被覆材料111的锂离子传导率。另外,氟磺酸锂和双(氟磺酰)亚胺锂能够形成正极活性物质110与第1固体电解质100的良好的界面、即电阻低的界面。由此,本实施方式的正极材料1000能够更有效地降低电池的电阻。
79.被覆材料111含有选自磷酸锂、铌酸锂、氟磺酸锂和双(氟磺酰)亚胺锂中的至少一种作为主要成分,并且还含有不可避免的杂质或者在形成被覆材料111时使用的起始原料、副产物和分解产物等。即、被覆材料111例如可以合计含有以相对于被覆材料111整体的质量比例计为50%以上(50质量%以上)的磷酸锂、铌酸锂、氟磺酸锂和双(氟磺酰)亚胺锂。被覆材料111例如也可以除了不可避免混入的杂质以外,合计含有以相对于被覆材料111整体的质量比例计为100%(100质量%)的磷酸锂、铌酸锂、氟磺酸锂和双(氟磺酰)亚胺锂。
80.另外,在实施方式1中,被覆材料111可以是linbo3。linbo3的离子导电率高且高电位稳定性更高。因此,通过使用linbo3,能够进一步提高电池的充放电效率。
81.在正极活性物质110与第1固体电解质100直接接触的状态下,如果对电池进行充电而使正极的电位变高,则从第1固体电解质100抽出电子,发生第1固体电解质100的氧化。为了防止这种情况,使被覆材料111介于正极活性物质110与第1固体电解质100之间是有效的。但是,被覆材料111有时也会遮断正极活性物质110与导电助剂或正极活性物质110之间的电子接触。该情况下,从电池的集电体到各正极活性物质110的粒子的电子路径被切断,孤立的正极活性物质110有时对充放电反应没有贡献。即,由于表观上的活性物质量减少,反应面积减少,因此难以充分降低电阻。与此相对,通过不利用被覆材料111覆盖正极活性物质110的表面的一部分而是使其露出,能够同时实现第1固体电解质100的氧化反应的抑制和电子路径的确保。因此,正极活性物质110的表面的一部分可以不被被覆材料111覆盖而露出。
82.为了进一步抑制第1固体电解质100的氧化反应,更有效地降低电池的电阻,由被覆材料111被覆了的正极活性物质111的被覆表面积相对于正极活性物质110的总表面积的比例即被覆率可以为47%以上。为了更有效地降低电池的电阻,上述被覆率可以为60%以上,也可以为100%。
83.上述被覆率可以通过将x射线光电子能谱法(xps)中的o1s的峰进行分离而求出。例如,在使用li(ni,co,mn)o2作为正极活性物质110并且使用磷酸锂作为被覆材料111的情况下,将以529ev附近为峰顶的来自正极活性物质的o1s峰的面积、除以在532ev附近出现的o1s峰减去在531ev附近出现的来自碳酸的o1s峰而得到的面积,由此求出被覆比例。
84.在难以采用上述方法正确地求出被覆比例的情况下,作为替代方法,可以通过xps
测定,求出活性物质110中的金属例如ni、co和mn的元素量以及被覆材料111中的阳离子种类例如p或si的元素量,根据它们的比率求出被覆率。
85.被覆材料111可以含有含氧酸盐。通过被覆材料111含有含氧酸盐,能够更有效地降低电池的电阻。含氧酸盐可以是以非金属或半金属为阳离子的含氧酸盐。如上所述,“半金属元素”是指b、si、ge、as、sb和te。“非金属元素”是指n、p、s、cl、br和i。即、这些元素是与氧结合而生成含氧酸的元素组。
86.被覆材料111相对于正极活性物质110的质量比率可以为2.0质量%以下,也可以为1.1质量%以下。根据该结构,能够增加正极中的活性物质110或第1固体电解质100的比例,从而能够增加电池的能量密度。
87.被覆材料111相对于正极活性物质110的质量比率可以为0.1质量%以上,也可以为0.2质量%以上。根据该结构,能够有效地抑制活性物质110与第1固体电解质100的副反应,从而能够更有效地降低电池的电阻。
88.被覆材料111相对于正极活性物质110的质量比率的求法,例如可以将正极用酸等溶解而制成水溶液后,通过电感耦合等离子体(icp)发射光谱分析对所含的元素进行定量,求出质量比率。此时,可以根据仅包含在正极活性物质110和被覆材料111的任意一方中的元素的定量值,假定为化学计量组成而求出。例如,在linio2被li3po4被覆的情况下,可以根据ni和p的定量值,假定linio2和li3po4以化学计量组成存在,求出被覆材料111的质量比率。
89.在上述组成式(1)中,x可以含有cl。根据该结构,能够进一步提高第1固体电解质100的离子导电率。由此,能够进一步提高电池的充放电效率。
90.正极活性物质110例如是具有吸藏和释放金属离子(例如锂离子)的特性的材料。正极活性物质的例子有含锂的过渡金属氧化物、过渡金属氟化物、聚阴离子材料、氟化聚阴离子材料、过渡金属硫化物、过渡金属氧硫化物或过渡金属氧氮化物等。含锂的过渡金属氧化物的例子有li(ni,co,al)o2、li(ni,co,mn)o2或licoo2等。作为正极活性物质,例如在使用含锂的过渡金属氧化物的情况下,能够降低正极的制造成本,提高平均放电电压。
91.为了提高电池的能量密度,正极活性物质110可以是镍钴锰酸锂。例如,正极活性物质110可以是li(ni,co,mn)o2。
92.根据以上的结构,能够进一步提高电池的能量密度和充放电效率。
93.被覆材料111的厚度可以为1nm以上且100nm以下。
94.通过使被覆材料111的厚度为1nm以上,能够抑制正极活性物质110与第1固体电解质100的直接接触,抑制第1固体电解质的副反应。因此,能够提高充放电效率。
95.另外,通过使被覆材料111的厚度为100nm以下,被覆材料111的厚度不会变得过厚。因此,能够充分减小电池的内部电阻。其结果,能够提高电池的能量密度。
96.被覆材料111的厚度可以为2nm以上且40nm以下。
97.通过使被覆材料111的厚度为2nm以上,能够更好地抑制正极活性物质110与第1固体电解质100的直接接触,抑制第1固体电解质100的副反应。因此,能够更好地提高充放电效率。
98.另外,通过使被覆材料111的厚度为40nm以下,能够进一步减小电池的内部电阻。其结果,能够提高电池的能量密度。
99.对于测定被覆材料111的厚度的方法没有特别限定,例如可以通过使用透射型电子显微镜等直接观察被覆材料111的厚度来求出。另外,也可以一边通过ar溅射削去被覆层一边测定xps,根据来自活性物质的光谱的变化而求出。
100.对于实施方式1中的第1固体电解质100的形状没有特别限定,例如可以是针状、球状、椭圆球状等。例如,第1固体电解质100的形状可以是粒子状。
101.例如,在实施方式1中的第1固体电解质100的形状为粒子状(例如球状)的情况下,中位直径可以为100μm以下。如果中位直径为100μm以下,则正极活性物质110和第1固体电解质100在正极材料1000中成为良好的分散状态,因此充放电特性提高。另外,在实施方式1中,中位直径也可以为10μm以下。
102.根据以上的结构,在正极材料1000中,正极活性物质110和第1固体电解质100能够形成良好的分散状态。
103.另外,在实施方式1中,第1固体电解质100可以比正极活性物质110的中位直径小。
104.根据以上的结构,在电极中,第1固体电解质100和正极活性物质110能够形成更良好的分散状态。
105.正极活性物质110的中位直径可以为0.1μm以上且100μm以下。
106.如果正极活性物质110的中位直径为0.1μm以上,则在正极材料1000中,正极活性物质110和第1固体电解质100在正极材料1000中成为良好的分散状态,因此电池的充放电特性提高。另外,如果正极活性物质110的中位直径为100μm以下,则正极活性物质110内的锂的扩散快,因此电池在高输出下的工作变得更容易。
107.正极活性物质110的中位直径可以大于第1固体电解质100的中位直径。由此,正极活性物质110和第1固体电解质100能够形成良好的分散状态。
108.中位直径是指体积基准的粒度分布中的累积体积等于50%时的粒径。体积基准的粒度分布例如通过激光衍射式测定装置或图像解析装置来测定。
109.另外,在实施方式1的正极材料1000中,如图1所示,第1固体电解质100和被覆材料111可以相互接触。
110.实施方式1中的正极材料1000可以包含多个粒子状的第1固体电解质100和多个粒子状的正极活性物质110。
111.另外,实施方式1的正极材料1000中的第1固体电解质100的含量和正极活性物质110的含量可以彼此相同,也可以不同。
112.<第1固体电解质的制造方法>
113.实施方式1中的第1固体电解质例如可以通过下述方法制造。
114.准备成为目标组成的配合比的原料粉并混合。原料粉的例子是氧化物、氢氧化物、卤化物或酰卤。例如,在制作由li、ta、o和cl构成的固体电解质的情况下,以1:1的摩尔比准备lioh和tacl5。
115.此时,通过选择原料粉的种类,能够确定上述组成式(1)中的“m”。另外,通过调整原料、配合比和合成工艺,能够调整上述的值“a”、“b”、“c”和“d”。
116.将原料粉充分混合后,采用机械化学研磨的方法将原料粉彼此混合、粉碎并使其反应。或者,也可以将原料粉充分混合后,在真空中烧结。
117.由此,得到第1固体电解质。
118.<由被覆材料被覆了的正极活性物质的制造方法>
119.可以采用下述方法制造由被覆材料111被覆了的正极活性物质110。
120.首先,准备正极活性物质110的粉末。正极活性物质110的粉末例如采用共沉淀法制作。在共沉淀法中,制作由金属氧化物构成的前体,将该前体与锂源一起烧成,由此可制作正极活性物质110。另外,各种组成的正极活性物质110的粉末在市场上有售,可以容易地得到它们。
121.接着,在正极活性物质110的粒子的表面形成被覆材料111。对于形成被覆材料111的方法没有特别限定。作为形成被覆材料111的方法,可举出液相被覆法和气相被覆法。
122.例如,在液相被覆法中,将被覆材料111的前体溶液涂布在正极活性物质110的表面。在形成包含磷酸锂的被覆材料111的情况下,前体溶液可以是溶剂、氢氧化锂和磷酸三乙酯的混合溶液。
123.另外,原料只要溶解或分散在溶剂中即可,没有任何限定。锂源的例子有叔丁基锂之类的烷基锂、甲醇锂、乙醇锂、异丙醇锂、叔丁醇锂之类的醇锂、碘化锂、溴化锂、氯化锂、碳酸锂、硝酸锂、硫酸锂或金属锂。磷酸源的例子有磷酸三甲酯、磷酸三丙酯、磷酸三丁酯、磷酸、磷酸二氢一铵、磷酸一氢二铵或磷酸三铵。也可以使用含有磷酸和锂的原料。
124.溶剂例如是乙醇等醇。但是,溶剂只要能够使原料溶解或分散即可,没有任何限定,可以根据原料选择各种溶剂。溶剂的例子有甲醇、丙醇、异丙醇、丁醇、碳酸二甲酯、碳酸二乙酯、碳酸甲乙酯、二甲基亚砜、四氢呋喃、己烷、苯、甲苯、二氯甲烷、丙酮或乙腈。
125.根据被覆材料111的目标组成,调整氢氧化锂和磷酸三乙酯的量。根据需要,可以向前体溶液中加入水。前体溶液即可以是酸性也可以是碱性。
126.(实施方式2)
127.以下,对实施方式2进行说明。适当省略与实施方式1重复的说明。
128.图2是表示实施方式2中的电池2000的大致结构的剖视图。
129.实施方式2中的电池2000具备正极201、电解质层202和负极203。
130.正极201包含实施方式1中的正极材料1000。
131.电解质层202配置于正极201与负极203之间。
132.根据以上的结构,能够提高电池2000的电池的充放电效率。
133.关于正极201中所含的正极活性物质110与第1固体电解质100的体积比率“v1:100-v1”,可以满足30≤v1≤95。在此,v1表示将正极201中所含的正极活性物质110和第1固体电解质100的合计体积设为100时的正极活性物质110的体积比率。在满足30≤v1的情况下,容易确保充分的电池2000的能量密度。在满足v1≤95的情况下,电池2000的高输出下的工作变得更容易。
134.正极201的厚度可以为10μm以上且500μm以下。另外,在正极201的厚度为10μm以上的情况下,容易确保充分的电池2000的能量密度。另外,在正极201的厚度为500μm以下的情况下,电池2000在高输出下的工作变得更容易。
135.电解质层202配置于正极201与负极203之间。
136.电解质层202是包含电解质材料的层。该电解质材料例如是固体电解质(即、第2固体电解质)。即、电解质层202也可以是固体电解质层。
137.作为电解质层202中所含的第2固体电解质,可举出上述实施方式1中说明的第1固
体电解质。即、电解质层202可以包含上述实施方式1中说明的第1固体电解质。
138.根据以上的结构,能够进一步提高电池2000的充放电效率。
139.作为电解质层202中所含的第2固体电解质,可以是与上述实施方式1中说明的第1固体电解质不同的卤化物固体电解质。即、电解质层202可以包含与上述实施方式1中说明的第1固体电解质不同的卤化物固体电解质。
140.根据以上的结构,能够提高电池2000的输出密度和充放电效率。
141.电解质层202中所含的卤化物固体电解质可以含有y作为金属元素。
142.根据以上的结构,能够进一步提高电池2000的输出密度和充放电效率。
143.作为电解质层202中所含的第2固体电解质,可以使用硫化物固体电解质。即、电解质层202可以包含硫化物固体电解质。
144.根据以上的结构,由于含有还原稳定性优异的硫化物固体电解质,因此能够使用石墨或金属锂等低电位负极材料,能够提高电池2000的能量密度。
145.硫化物固体电解质的例子有li2s-p2s5、li2s-sis2、li2s-b2s3、li2s-ges2、li
3.25
ge
0.25
p
0.75
s4、或li
10
gep2s
12
等。另外,可以在它们中添加lix2、li2o、m2oq、li
p
m2oq等。其中,x2是选自f、cl、br和i中的1种或2种以上的元素。另外,m2是p、si、ge、b、al、ga、in、fe和zn中的任一种。另外,p和q各自独立地为自然数。
146.作为电解质层202中所含的第2固体电解质,可以使用氧化物固体电解质、高分子固体电解质或络合氢化物固体电解质。
147.作为氧化物固体电解质,例如可以使用以liti2(po4)3及其元素置换体为代表的nasicon型固体电解质、(lali)tio3系的钙钛矿型固体电解质、以li
14
znge4o
16
、li4sio4、ligeo4及其元素置换体为代表的lisicon型固体电解质、以li7la3zr2o
12
及其元素置换体为代表的石榴石型固体电解质、li3n及其h置换体、li3po4及其n置换体、以libo2、li3bo3等li-b-o化合物为基础而添加了li2so4、li2co3等的玻璃、玻璃陶瓷等。
148.作为高分子固体电解质,例如可以使用高分子化合物和锂盐的化合物。高分子化合物可以具有环氧乙烷结构。通过具有环氧乙烷结构,能够含有较多的锂盐,能够进一步提高离子导电率。作为锂盐,可以使用lipf6、libf4、lisbf6、liasf6、liso3cf3、lin(so2cf3)2、lin(so2c2f5)2、lin(so2cf3)(so2c4f9)、lic(so2cf3)3等。作为锂盐,可以单独使用选自它们中的一种锂盐。或者,作为锂盐,可以使用选自它们中的2种以上的锂盐的混合物。
149.作为络合氢化物固体电解质,例如可以使用libh
4-lii、libh
4-p2s5等。
150.另外,电解质层202可以含有第2固体电解质作为主要成分。即、电解质层202例如可以含有以相对于电解质层202整体的质量比例计为50%以上(50质量%以上)的第2固体电解质。
151.根据以上的结构,能够进一步提高电池2000的充放电特性。
152.另外,电解质层202例如可以含有以相对于电解质层202整体的质量比例计为70%以上(70质量%以上)的第2固体电解质。
153.根据以上的结构,能够进一步提高电池2000的充放电特性。
154.另外,电解质层202可以含有第2固体电解质作为主要成分,并且还含有不可避免的杂质、或者合成第2固体电解质时使用的起始原料、副产物和分解产物等。
155.另外,电解质层202中,例如除了不可避免的杂质以外,可以含有以相对于电解质
层202整体的质量比例计为100%(100质量%)的第2固体电解质。
156.根据以上的结构,能够进一步提高电池2000的充放电特性。
157.如上所述,电解质层202可以仅由第2固体电解质构成。
158.另外,电解质层202可以含有作为第2固体电解质列举的材料中的2种以上。例如,固体电解质层可以包含卤化物固体电解质和硫化物固体电解质。
159.电解质层202的厚度可以为1μm以上且300μm以下。在电解质层202的厚度为1μm以上的情况下,正极201和负极203短路的可能性变低。另外,在电解质层202的厚度为300μm以下的情况下,高输出下的工作变得容易。即、如果适当地调整电解质层202的厚度,则能够确保电池2000的充分的安全性,并且能够使电池2000以高输出进行动作。
160.负极203包含具有吸藏和释放金属离子(例如锂离子)的特性的材料。负极203例如包含负极活性物质。
161.负极活性物质可以使用金属材料、碳材料、氧化物、氮化物、锡化合物或硅化合物等。金属材料可以是单质的金属。或者,金属材料也可以是合金。作为金属材料的例子可举出锂金属或锂合金等。作为碳材料的例子可举出天然石墨、焦炭、石墨化中间碳、碳纤维、球状碳、人造石墨或非晶质碳等。从容量密度的观点出发,可以使用硅(si)、锡(sn)、硅化合物或锡化合物。
162.负极203可以包含第3固体电解质。根据以上的结构,能够提高负极内部的锂离子传导性,进行高输出下的工作。作为负极203中所含的第3固体电解质,可以使用作为电解质层202的第2固体电解质的例子列举的材料。
163.负极活性物质粒子的中位直径可以为0.1μm以上且100μm以下。如果负极活性物质粒子的中位直径为0.1μm以上,则在负极203中,负极活性物质粒子和第3固体电解质成为良好的分散状态,由此电池2000的充放电特性提高。另外,如果负极活性物质粒子的中位直径为100μm以下,则负极活性物质粒子内的锂的扩散快,因此电池在高输出下的工作变得更容易。
164.负极活性物质粒子的中位直径可以大于第3固体电解质的中位直径。由此,能够形成负极活性物质粒子和固体电解质的良好的分散状态。
165.关于负极203中所含的负极活性物质粒子与固体电解质的体积比率“v2:100-v2”,可以满足30≤v2≤95。在满足30≤v2的情况下,容易确保充分的电池2000的能量密度。在满足v2≤95的情况下,电池2000的高输出下的工作变得更容易。
166.负极203的厚度可以为10μm以上且500μm以下。在负极203的厚度为10μm以上的情况下,容易确保充分的电池2000的能量密度。在负极203的厚度为500μm以下的情况下,电池2000在高输出下的工作变得更容易。
167.为了提高粒子之间的密合性,选自正极201、电解质层202和负极203中的至少一者可以含有粘结剂。粘结剂用于提高构成电极和电解质层的材料的粘结性。作为粘结剂,可以举出聚偏氟乙烯、聚四氟乙烯、聚乙烯、聚丙烯、芳纶树脂、聚酰胺、聚酰亚胺、聚酰胺酰亚胺、聚丙烯腈、聚丙烯酸、聚丙烯酸甲酯、聚丙烯酸乙酯、聚丙烯酸己酯、聚甲基丙烯酸、聚甲基丙烯酸甲酯、聚甲基丙烯酸乙酯、聚甲基丙烯酸己酯、聚乙酸乙烯酯、聚乙烯吡咯烷酮、聚醚、聚醚砜、六氟聚丙烯、丁苯橡胶、羧甲基纤维素等。另外,作为粘结剂,可以使用选自四氟乙烯、六氟乙烯、六氟丙烯、全氟烷基乙烯基醚、偏二氟乙烯、氯三氟乙烯、乙烯、丙烯、五氟
丙烯、氟甲基乙烯基醚、丙烯酸、己二烯中的2种以上材料的共聚物。另外,也可以将选自它们中的2种以上混合,作为粘结剂使用。
168.为了提高电子导电性,正极201和负极203中的至少一方可以含有导电助剂。作为导电助剂,例如可以使用天然石墨或人造石墨等石墨类、乙炔黑或科琴黑等炭黑类、碳纤维或金属纤维等导电性纤维类、氟化碳、铝等金属粉末类、氧化锌或钛酸钾等导电性晶须类、氧化钛等导电性金属氧化物、聚苯胺、聚吡咯或聚噻吩等导电性高分子化合物等。在使用碳导电助剂的情况下,能够谋求低成本化。
169.另外,实施方式2的电池2000可以构成为硬币型、圆筒型、方型、片型、纽扣型、扁平型、层叠型等各种形状的电池。
170.实施方式2的电池2000例如可以通过下述方式制造:分别准备实施方式1的正极材料1000、电解质层形成用的材料、负极形成用的材料,采用公知的方法,制作由正极、电解质层和负极依次配置而成的层叠体。
171.实施例
172.以下,参照实施例和比较例对本公开进行更详细的说明。
173.《实施例1》
174.[由被覆材料被覆了表面的正极活性物质的制作]
[0175]
在露点为﹣60℃以下的氩气气氛的氩气手套箱内,将9.5mg的氢氧化锂、24.0mg的磷酸三乙酯溶解于适量的超脱水乙醇(和光纯药制)中,制作了被覆材料溶液。在被覆材料溶液中,锂与磷的摩尔比率为3:1。
[0176]
在玛瑙研钵上准备2g作为正极活性物质的li(ni,co,mn)o2(以下记为ncm)后,一边向其中缓慢添加制作好的被覆材料溶液,一边搅拌。
[0177]
将被覆材料溶液全部添加后,进行搅拌直至目视能够确认干固。
[0178]
将干固后的粉末放入氧化铝制坩埚中,在氧气气氛下以400℃进行3小时的热处理。
[0179]
将热处理后得到的粉末用玛瑙研钵再粉碎,由此得到由被覆材料被覆了表面的实施例1的正极活性物质。该被覆材料是磷酸锂(li3po4)。
[0180]
[第1固体电解质的制作]
[0181]
在露点为﹣30℃以下的干燥气氛中,作为原料粉末将lioh和tacl5以lioh:tacl5=1:1的摩尔比进行称量。将这些原料粉末用研钵粉碎并混合,得到混合粉末。使用行星式球磨机(friich公司制,p-7型)对所得到的混合粉末以600rpm研磨处理24小时。接着,在200℃下对混合粉烧成6小时。通过以上,得到由li、ta、o和cl构成的实施例1的固体电解质的粉末。
[0182]
由此,得到由li、ta、o和cl构成的实施例1的第1固体电解质的粉末。以下将由li、ta、o和cl构成的实施例1的固体电解质记为“ltoc”。关于所得到的实施例1的第1固体电解质的组成,采用icp发射光谱分析法测定li和ta,采用离子色谱法测定cl,采用惰性气体熔融-红外线吸收法测定o。用于测定组成的装置有icp发射光谱分析装置(“icap7400”(thermo fisher scientific公司制))、离子色谱装置(“ics-3000”(thermo fisher scientific公司制))、氧分析装置(“emga-920”(堀场制作所公司制))。在实施例1的第1固体电解质中,摩尔比li/ta为1.20,摩尔比o/cl为0.35。
[0183]
[第2固体电解质的制作]
[0184]
在露点为﹣60℃以下的氩气气氛中,作为原料粉将licl、ycl3和ybr3以licl:lycl3:ybr3=3.000:0.333:0.666的摩尔比进行准备。将它们用研钵粉碎后混合。接着,将所得到的原料粉的混合物在氩气气氛中使用电炉以500℃烧成3小时。将所得到的材料用研杵和研钵进行粉碎。通过以上,得到含有li、y、br和cl的第2固体电解质的粉末。以下将实施例1的第2固体电解质记载为“lybc”。
[0185]
[电池的制作]
[0186]
在露点为﹣60℃以下的氩气气氛中,将由作为被覆材料的磷酸锂被覆了的正极活性物质、作为第1固体电解质的ltoc、以及作为导电助剂的气相生长碳纤维(vgcf),以正极活性物质:ltoc:vgcf=77:21:2的质量比率进行准备。将它们在玛瑙乳钵中混合,由此制作了正极合剂。
[0187]
在绝缘性外筒中,将硫化物固体电解质li6ps5cl(80mg)、lybc粉末(20mg)、以及上述正极合剂(18.2mg)依次层叠。对其施加720mpa的压力,得到了正极和电解质层。
[0188]
接着,在电解质层的与接触正极侧相反的一侧层叠li箔。对其施加80mpa的压力,制作了正极、电解质层以及负极的层叠体。由li箔形成了负极。
[0189]
接着,在层叠体的上下配置不锈钢制的集电体,在集电体上设置集电引线。最后,使用绝缘性套圈,将绝缘性外筒的内部与外部气体气氛隔绝且密闭。
[0190]
通过以上,制作了实施例1的电池。
[0191]
[充放电试验]
[0192]
将实施例1的电池放置在25℃的恒温槽中。对于电池以成为0.140ma的电流值进行恒流充电,在电压4.3v结束充电。接着,同样以成为0.140ma的电流值进行放电,在电压2.5v结束放电。将此时的放电容量相对于充电容量的比率作为充放电效率。实施例1中的电池的充放电效率为96%。
[0193]
[电阻测定]
[0194]
图3是表示实施例1中的电池的3.7v的奈奎斯特线图的图。将实施例1的电池配置在25℃的恒温槽中。接着,与搭载了频率响应分析器的恒电位仪连接。然后,对于电池以成为0.140ma的电流值进行恒流充电,在电压3.7v结束充电。然后,采用交流阻抗法评价电阻成分的频率依赖性。此时,通过曲线拟合将在10
5-102hz附近出现的电阻成分分离,作为来自活性物质-固体电解质界面的电阻。根据该测定,估算实施例1的电池的电阻为7ohm。
[0195]
[被覆率的测定]
[0196]
图4a是表示实施例1中使用的活性物质的xps法的o1s光谱的图。采用xps法得到由磷酸锂被覆的正极活性物质表面的o1s光谱。作为xps的射线源使用al-kα射线。
[0197]
观测到了以528ev为中心的峰和以532ev为中心的峰。528ev的峰是来自正极活性物质中的m-o(ni-o、mn-o、co-o)的峰。另外,532ev的峰是作为表面的杂质的碳酸锂中的c-o的峰与磷酸锂中的p-o的峰重叠的峰。通过从被覆了的活性物质的532ev附近的峰面积中减去在氧气气氛下以400℃对没有由被覆材料被覆的活性物质进行烧成而得到的物质中检测出的532ev附近的峰面积,除去来自碳酸锂的影响,计算出来自被覆材料的峰面积。图4b是表示实施例1中使用的活性物质的xps法的o1s光谱、和没有由被覆材料被覆表面的活性物质的xps法的o1s光谱的图。图4b所示的表面没有由被覆材料被覆的活性物质的xps法的o1s
光谱,也是表示比较例1中使用的活性物质的xps法的o1s光谱的图。因此,在图4b中,表面没有由被覆材料被覆的活性物质的xps法的o1s光谱表示为比较例1中使用的活性物质的光谱。
[0198]
根据这些峰,求出o1s中的m-o和p-o的比例,推定被覆率。推定实施例1中使用的活性物质的磷酸锂的被覆率为47%。
[0199]
《实施例2》
[0200]
[由被覆材料被覆了表面的正极活性物质的制作]
[0201]
在氩气气氛中,将5.95g的乙氧基锂(高纯度化学制)和36.43g的五乙氧基铌(高纯度化学制)溶解于500ml的超脱水乙醇(和光纯药制)中,制作了被覆材料溶液。
[0202]
在正极活性物质ncm上形成被覆材料时,使用转动流动造粒涂布装置(powrex制,fd-mp-01e)。正极活性物质的投入量、搅拌转速、被覆材料溶液的送液速率分别设为1kg、400rpm、6.59g/分钟。
[0203]
将处理后的粉末放入氧化铝制坩埚中,在大气气氛下取出。
[0204]
接着,在大气气氛下以300℃进行了1小时的热处理。
[0205]
将热处理后的粉末用玛瑙研钵再粉碎,由此得到由被覆材料被覆了表面的实施例2的正极活性物质。该被覆材料是铌酸锂(linbo3)。
[0206]
[电池的制作]
[0207]
除了使用实施例2的正极活性物质以外,采用与实施例1同样的方法制作了电池。
[0208]
[充放电试验]
[0209]
采用与实施例1相同的方法进行了电池的充放电试验。
[0210]
[电阻测定]
[0211]
采用与实施例1同样的方法进行了电池的电阻测定。
[0212]
[被覆率的测定]
[0213]
来自铌酸锂的nb-o的o1s峰出现在530ev附近。根据该值与实施例1同样地求出被覆率。实施例2中使用的活性物质的被覆率大致为100%。
[0214]
《实施例3》
[0215]
[由被覆材料被覆了表面的正极活性物质的制作]
[0216]
在露点为﹣50℃以下的氩气气氛的氩气手套箱内,将0.2g的双(氟磺酰)亚胺锂(lin(so2f)2)粉末溶解于19.80g的碳酸二甲酯中,制作了1.0质量%的被覆材料溶液。双(氟磺酰)亚胺锂以下记为“lifsi”。
[0217]
然后,在聚烯烃制容器上,准备2g作为正极活性物质的ncm后,将制作好的被覆材料溶液缓缓滴下0.5g并搅拌。然后,以100℃进行真空干燥,得到了由被覆材料被覆了表面的实施例3的正极活性物质。该被覆材料是氟磺酸锂。
[0218]
[电池的制作]
[0219]
除了使用实施例3的正极活性物质以外,采用与实施例1同样的方法制作了电池。
[0220]
[充放电试验]
[0221]
采用与实施例1同样的方法进行了电池的充放电试验。
[0222]
[电阻测定]
[0223]
采用与实施例1同样的方法进行了电池的电阻测定。
[0224]
《实施例4》
[0225]
[由被覆材料被覆了表面的正极活性物质的制作]
[0226]
在露点为﹣50℃以下的氩气气氛的氩气手套箱内,将0.25g的氟磺酸锂(liso3f)粉末溶解于19.75g的碳酸二甲酯中,制作了1.25质量%的被覆材料溶液。
[0227]
然后,在聚烯烃制容器上,准备2g作为正极活性物质的ncm后,将制作好的被覆材料溶液缓缓滴下1.3g并搅拌。然后,以100℃进行真空干燥,得到了由被覆材料被覆了表面的实施例4的正极活性物质。该被覆材料是lifsi。
[0228]
[电池的制作]
[0229]
除了使用实施例4的正极活性物质以外,采用与实施例1同样的方法制作了电池。
[0230]
[充放电试验]
[0231]
采用与实施例1同样的方法进行了电池的充放电试验。
[0232]
[电阻测定]
[0233]
采用与实施例1同样的方法进行了电池的电阻测定。
[0234]
《比较例1》
[0235]
[正极活性物质的准备]
[0236]
将实施例1~4中作为正极活性物质使用的ncm,不用被覆材料被覆表面而作为比较例1的正极活性物质使用。
[0237]
[电池的制作]
[0238]
除了使用比较例1的正极活性物质以外,采用与实施例1同样的方法制作了电池。
[0239]
[充放电试验]
[0240]
采用与实施例1同样的方法进行了电池的充放电试验。
[0241]
[电阻测定]
[0242]
采用与实施例1同样的方法进行了电池的电阻测定。
[0243]
《比较例2》
[0244]
[由被覆材料被覆了表面的正极活性物质的制作]
[0245]
采用与实施例1同样的方法,制作了由被覆材料被覆了表面的正极活性物质。即、使用由磷酸锂(li3po4)被覆了表面的ncm作为比较例2的正极活性物质。
[0246]
[硫化物固体电解质的制作]
[0247]
在露点为﹣60℃以下的氩气气氛中的氩气手套箱内,将li2s和p2s5以li2s:p2s5=75:25的摩尔比进行称量。将这些用研钵粉碎并混合。然后,使用行星式球磨机(friich公司制,p-7型)以510rpm进行10小时研磨处理,得到玻璃状的固体电解质。对于玻璃状的固体电解质,在惰性气氛中以270℃进行2小时热处理。由此,得到了玻璃陶瓷状的固体电解质li2s-p2s5。li2s-p2s5以下记为“lps”。
[0248]
[电池的制作]
[0249]
在露点为﹣60℃以下的氩气气氛中,将由作为被覆材料的磷酸锂被覆了的正极活性物质和作为硫化物固体电解质的lps以正极活性物质:lps=85:15的质量比率进行准备。将它们用玛瑙研钵混合,由此制作了正极合剂。此后,与实施例1同样地制作了电池。
[0250]
[充放电试验]
[0251]
采用与实施例1同样的方法进行了电池的充放电试验。
[0252]
[电阻测定]
[0253]
采用与实施例1同样的方法进行了电池的电阻测定。
[0254]
[考察1]
[0255]
表1示出实施例1~4、比较例1和比较例2中使用的正极活性物质的被覆材料、正极材料中使用的固体电解质、电池的电阻、以及电池的充放电效率。
[0256]
将实施例1~4的电池与比较例1的电池的电阻和充放电效率进行比较可知,在使用ltoc作为正极材料中所含的固体电解质的情况下,如果正极活性物质的表面被磷酸锂、铌酸锂、双(氟磺酰)亚胺锂和氟磺酸锂这样的被覆材料被覆,则能够降低电池的电阻,进而能够提高充放电效率。
[0257]
将实施例1的电池与比较例2的电池的电阻和充放电效率进行比较可知,即使使用相同的由磷酸锂被覆了的正极活性物质,使用ltoc作为正极材料中所含的固体电解质的实施例1的电池的电阻和充放电效率也更优异。
[0258]
《实施例5》
[0259]
[由被覆材料被覆了表面的正极活性物质的制作]
[0260]
采用与实施例1同样的方法,制作了由被覆材料被覆了表面的正极活性物质。即、使用由磷酸锂(li3po4)被覆了表面的ncm作为实施例5的正极活性物质。
[0261]
[第1固体电解质的制作]
[0262]
在露点为﹣30℃以下的干燥气氛中,作为原料粉将li2o2和nbcl5以li2o2:nbcl5=1:2的摩尔比进行称量。将它们用研钵粉碎并混合,得到混合粉。使用行星式球磨机(friich公司制,p-7型)对所得到的混合粉以600rpm进行24小时研磨处理。接着,以200℃对混合粉烧成6小时。由此,得到了由li、nb、o和cl构成的固体电解质的粉末。以下将所得到的由li、nb、o和cl构成的实施例5的第1固体电解质记为“lnoc”。在所得到的lnco中,摩尔比li/nb为1.2,摩尔比o/cl为0.35。另外,关于实施例5的第1固体电解质的组成,采用icp发射光谱分析法测定li和nb,采用离子色谱法测定cl,采用惰性气体熔融-红外线吸收法测定o。用于测定组成的装置有icp发射光谱分析装置(“icap7400”(thermo fisher scientific公司制))、离子色谱装置(“ics-3000”(thermo fisher scientific公司制))、氧分析装置(“emga-920”(堀场制作所公司制))。
[0263]
[电池的制作]
[0264]
除了使用实施例5的正极活性物质和第1固体电解质以外,采用与实施例1同样的方法制作了电池。
[0265]
[充放电试验]
[0266]
采用与实施例1同样的方法进行了电池的充放电试验。其中,放电的截止电压、即结束放电的电压被设定为3v。
[0267]
[电阻测定]
[0268]
采用与实施例1同样的方法进行了电池的电阻测定。
[0269]
[被覆率的测定]
[0270]
采用与实施例1同样的方法进行了被覆率的电阻测定。推定实施例5中使用的活性物质的磷酸锂的被覆率为47%。
[0271]
《比较例3》
[0272]
[正极活性物质的准备]
[0273]
将实施例5中作为正极活性物质使用的ncm,不用被覆材料被覆表面而作为比较例3的正极活性物质使用。
[0274]
[电池的制作]
[0275]
除了使用比较例3的正极活性物质以外,采用与实施例5同样的方法制作了电池。
[0276]
[充放电试验]
[0277]
采用与实施例5同样的方法进行了电池的充放电试验。
[0278]
[电阻测定]
[0279]
采用与实施例5同样的方法进行了电池的电阻测定。
[0280]
[考察2]
[0281]
表1示出实施例5和比较例3中使用的正极活性物质的被覆材料、正极材料所使用的固体电解质、电池的电阻、以及电池的充放电效率。
[0282]
在实施例5和比较例3的电池中,使用相同的lnoc作为正极材料中所含的固体电解质。其结果,可确认即使在使用lnoc作为固体电解质的情况下,通过用被覆材料被覆正极活性物质,也使电池的电阻降低,进而电池的充放电效率提高。由该结果可知,与构成固体电解质的金属种类的区别无关,通过用被覆材料被覆正极活性物质的表面,可得到电池的电阻降低、进而充放电效率提高的效果。
[0283]
表1
[0284][0285]
产业可利用性
[0286]
本公开的电池例如可用作全固体锂二次电池等。
[0287]
附图标记说明
[0288]
1000 正极材料
[0289]
100 第1固体电解质
[0290]
110 正极活性物质
[0291]
111 被覆材料
[0292]
2000 电池
[0293]
201 正极
[0294]
202 电解质层
[0295]
203 负极
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1