匹诺塞林在制备预防和/或治疗肺动脉高压中的药物用途的制作方法
本发明涉及创新药物匹诺塞林(Pinocembrin)的新药理作用,以及匹诺塞林在制备预防、缓解和/或治疗肺动脉高压及其并发症产品中的用途,属创新药物技术领域。
技术背景
原发性肺动脉高压是一种较少见但却非常严重的疾病。其发病人群年龄偏低,约75%患者集中于20-40岁年龄段,且有约15%患者年龄在20岁以下。目前针对肺动脉高压的发病原因仍没有明确的结论,肺部小动脉原发性增生病变导致血管闭塞可能是其发病的主要原因。
当肺动脉高压发生时,病人表现出呼吸困难、心悸、胸痛、咳血、晕厥等症状,晚期会出现缺氧、右心肥大甚至右心衰竭症状,严重时会发生死亡。目前针对这一疾病的治疗手段和药物仍旧十分欠缺,预后情况很差,仅20%患者能够得到较为有效的控制,多数病人在疾病确诊后2-3年内就可能死亡。目前临床上治疗肺动脉高压的一线药物是波生坦,但其治疗效果不尽人意。开发新的能够有效治疗肺动脉高压的药物是一项十分重要和迫切的工作。
在本实验室前期工作中通过高通量筛选发现一种作用机制新颖的新型脑卒中治疗药物,通过结构比较发现其是从传统药物蜂胶中分离得到的一种天然黄烷酮类化合物,名为匹诺塞林(经中华人民共和国药典委员会正式命名为匹诺塞林,曾别称生松素,乔松素)。匹诺塞林是蜂胶中含量最高的黄酮类化合物,自80年代起,国内外研究发现其抗菌、抗病毒、抗氧化、抗炎等方面药理活性。筛选中心在整合靶点理论指导下,以网点式高通量药物筛选新模式,发现了匹诺塞林防治脑缺血性疾病的新用途,并证明匹诺塞林对多种脑卒中动物模型有显著而突出的抗脑缺血作用,获得了知识产权保护,作为1.1类化学新药进入临床研究。
目前针对匹诺塞林的研究主要集中在神经保护方面。通过查阅文献,发现至今没有文献报道这一化合物在肺动脉高压治疗方面的作用。
技术实现要素:
本发明的目的可以通过如下技术方案来实现。采用一次性皮下注射野百合碱建立大鼠肺动脉高压模型,在模型建立一周后开始给药,连续给予18天匹诺塞林。通过在实验终点观察动物死亡情况、心电图变化、主动脉压力及肺动脉压力变化、各脏器指数变化、测定动物血清酶、组织损伤情况及组织形态学变化,判定匹诺塞林对大鼠肺动脉高压的预防、缓解和治疗作用。
本发明的特点与优势在于,本发明研发的药物匹诺塞林作为具有自主知识产权的化学药,该化合物具有物质来源可靠、生产成本较低、作用机制新颖、市场前景好等特点,而且前期研究工作基础扎实、药物疗效确切,降低了后续开发的风险。另外,匹诺塞林作为来源于天然产物具有广泛活性的单体化合物,具有舒张肺动脉血管、降低肺动脉压力、保护肺动脉高压所致的肺血管损伤、恢复肺组织功能、修复心脏和肝脏等器官损伤、显著降低肺动脉高压动物的死亡率、预防和治疗肺动脉高压疾病的药理作用;具有减轻组织器官水肿,减少组织器官损伤,改善组织器官功能,防治右心室肥厚的作用,可应用于制备预防、缓解和/或治疗肺动脉高压及其导致的慢性阻塞性肺气肿、慢性肺源性心脏病、右心衰竭、肝功能损伤等并发症的产品。
本发明的另一方面,涉及一种用于预防和/或治疗肺动脉高压及其并发症的药物组合物,其含有预防、缓解和/或治疗有效量的匹诺塞林,以及任选的药学可接受的载体和/或辅料。
在本发明中,根据施用途径,所述匹诺塞林药物组合物可呈选自如下剂型:溶液、混悬液、冻干粉针、乳剂、丸剂、胶囊、粉末、控制释放或持续释放制剂。
本发明的匹诺塞林药物组合物可以用已知的方法配制,使用几种途径对受试者施用,包括但不限于肠胃外、经口、局部、皮内、肌肉内、腹膜内、皮下、静脉、鼻内途径。
本发明中匹诺塞林可通过已知方法制备得到。
本发明的匹诺塞林药物组合物任选的可以通过任何常规方法用一种或多种药学可接受的载体和/或赋形剂来配制。因此,匹诺塞林和它药学可接受的衍生物可特别配制为例如吸入或吹入(通过口或鼻)或经口、含化、肠胃外或直肠给药。
匹诺塞林的药物组合物也可以采用溶液、混悬液、乳剂、丸剂、胶囊、粉末、控制释放或持续释放制剂。这些制剂将含有治疗有效量的匹诺塞林,优选为纯化形式,以及适量的载体,以提供对患者适当给药的形式。
在本发明中,所述纯化形式的匹诺塞林是指基本上纯的匹诺塞林,尤其是纯度大于80%,优选的大于85%,特别优选的大于90%,甚至更优选的大于95%的匹诺塞林。所述纯化形式的匹诺塞林纯度范围可以是例如80-98%。
所述的产品包括药品、食品、保健品。
附图说明
图1.匹诺塞林对肺动脉高压大鼠体重的影响。
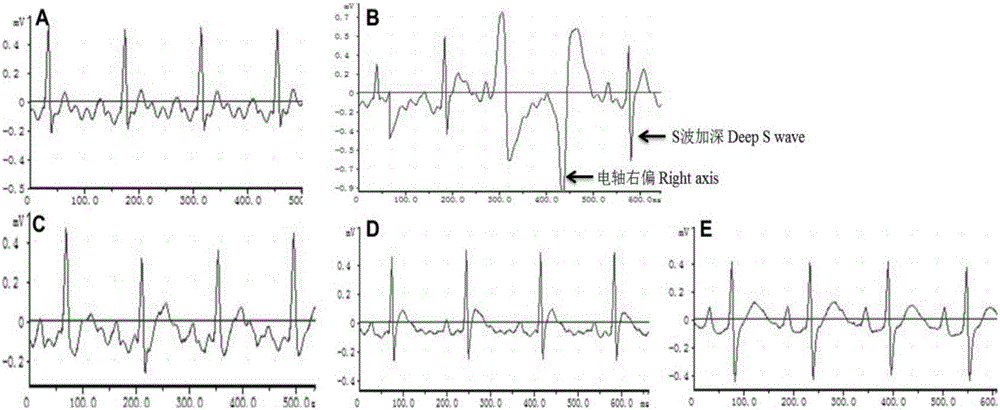
图2.匹诺塞林对肺动脉高压大鼠心电图的改善作用。A-正常,B-模型,C-波生坦,D-法舒地尔,E-匹诺塞林(30mg/kg)。
图3.匹诺塞林对肺动脉高压大鼠主动脉压力的影响。A-主动脉收缩压,B-主动脉舒张压,C-大鼠心率。
图4.匹诺塞林降低肺动脉高压大鼠右心室收缩压。图5、匹诺塞林对肺动脉高压大鼠脏器指数的影响。A-肺脏,B-心脏,C-肝脏。
图5.匹诺塞林对肺动脉高压大鼠脏器指数的影响。A-肺脏,B-心脏,C-肝脏。
图6.匹诺塞林对肺动脉高压大鼠右心室肥厚的抑制作用。
图7.匹诺塞林对肺动脉高压大鼠血清中各种酶活性的抑制作用。A-天门冬氨酸氨基转移酶(aspartate aminotransferase,AST),B-乳酸脱氢酶(lactate dehydrogenase,LDH),C-谷丙转氨酶(Alanine aminotransferase,ALT)。
图8.匹诺塞林对肺动脉高压大鼠血清中NT-proBNP含量的抑制作用。
图9.匹诺塞林对肺动脉高压大鼠肺组织中ET-1含量的抑制作用。
图10.组织病理切片(HE染色)观察匹诺塞林对肺动脉高压大鼠右心室保护作用。A-正常,B-模型,C-波生坦,D-法舒地尔,E-匹诺塞林(30mg/kg)。
图11.组织病理切片(Masson染色)观察匹诺塞林对肺动脉高压大鼠肺部组织、肺部血管保护作用。A-正常,B-模型,C-波生坦,D-法舒地尔,E-匹诺塞林(30mg/kg)。
图12.组织病理切片(HE染色)观察匹诺塞林对肺动脉高压大鼠肺动脉主干血管壁增厚的治疗作用。A-正常,B-模型,C-波生坦,D-法舒地尔,E-匹诺塞林(30mg/kg)。
图13.匹诺塞林体外舒张肺动脉血管的作用。
具体实施方式
下面结合本发明进一步说明匹诺塞林在体内对预防、缓解和/或治疗抗肺动脉高压及其并发症的药理作用与药物用途。
下述实施例更详细地举例说明本发明,并不是对本发明的任何限制。
实施例1:大鼠肺动脉高压模型的建立。
野百合碱是从野百合种子中提取的一种吡咯烷生物碱,它在大鼠体内被肝脏的混合功能氧化酶转化为野百合吡咯,野百合吡咯损伤肺血管内皮细胞,从而引起肺动脉平滑肌细胞进行性增殖,导致肺动脉压进行性增高,造成大鼠肺动脉高压模型。在模型建立一周后开始给药,连续给予18天匹诺塞林。本实施例通过观察大鼠心电图,测定大鼠主动脉压力及肺动脉压力(右心室压力),测定实验大鼠各脏器指数、右心室增厚程度、血清酶及肺动脉高压标志物、组织炎症因子以及组织形态学变化,判定匹诺塞林对大鼠肺动脉高压的保护作用及在制备预防和治疗肺动脉高压及其并发症产品中的用途。
实施例动物选用SD大鼠75只,体重170-190g,随机分成5组,每组15只:正常对照组、肺动脉高压模型对照组、阳性药波生坦(30mg/kg,灌胃给药)组、阳性药法舒地尔(10mg/kg,腹腔注射给药)组、匹诺塞林(30mg/kg,腹腔注射给药)组。在实验开始除正常组给予等剂量生理盐水,其它动物一次性皮下注射给予50mg/kg野百合碱制备大鼠肺动脉高压模型。造模后第7天开始给药,连续给予18天,每天一次,且每天监测大鼠体重变化,绘制体重曲线(附图1),在第18天统计各组大鼠的死亡情况(附表1)。
表1.匹诺塞林对肺动脉高压大鼠生存率的影响。
末次给药后各组大鼠均禁食过夜,于第二天戊巴比妥钠50mg/kg麻醉,前后肢皮下插入针状电极记录II导联心电图,观察S波加深及R波倒置情况。通过左颈动脉插管和右颈静脉插管分别测量大鼠主动脉压力和肺动脉压力(右心室压力)。实验结束后,腹主动脉取血用于各指标检测,取心、肺、肝称重,计算脏器指数。部分心脏、肺、肺动脉用于病理检测。
实施例2:匹诺塞林对肺动脉高压大鼠心电图的改善作用。
上述各组大鼠于末次给药后均禁食过夜,于第二天戊巴比妥钠50mg/kg麻醉,前后肢皮下插入针状电极,记录大鼠Ⅱ导联心电图,观察心电图S波加深情况和R波倒置情况。结果显示(附图2),正常大鼠心电图呈正常状态,注射野百合碱造模后引起大鼠心电图电轴右偏致R波倒置及S波加深,出现右心功能不全改变。波生坦、法舒地尔两个阳性药物,能够明显改善野百合碱引起的大鼠心电图变化,匹诺塞林能够在一定程度上改善野百合碱引起的大鼠心电变化,改善右心衰竭症状,说明匹诺塞林对野百合碱所致肺动脉高压引起的右心功能损伤具有良好的改善作用。
实施例3:匹诺塞林对肺动脉高压大鼠主动脉压力及心率的影响
沿正中线剪开大鼠颈部皮肤,钝性分离颈部肌肉,在气管斜下方仔细分离出左颈总动脉。结扎远心端,近心端用止血钳暂时止血,做一v形切口,将预先充满肝素生理盐水的PE导管插入颈动脉中,并用缝合线固定,此时松开止血钳,使血流畅通,观察颈动脉压力,即主动脉收缩压、舒张压及心率。结果显示(附图3),由于肺动脉高压导致心功能不全,因此导致主动脉压力代偿性升高。给予阳性药波生坦,对这一现象改善较少;另一阳性药法舒地尔能够明显降低主动脉压力的升高。给予匹诺塞林同样降低肺动脉高压所导致的主动脉压力增高,但以上三种药物对肺动脉高压大鼠的心率变化影响并不明显。
实施例4:匹诺塞林对肺动脉高压大鼠肺动脉压力(右心室内压)的降低作用。
由于大鼠肺动脉压与右心室收缩压基本一致,且肺动脉压较难测量,因此本实施例用右心室内压代替肺动脉压来进行药效评价。首先沿大鼠右肩剪开皮肤,暴露右颈静脉。然后钝性分离,仔细分离出右颈静脉,结扎远心端后做v形切口,将预先充满肝素生理盐水的弯头PE导管插入静脉中,用缝合线将导管与血管稍作固定以减少出血。将导管缓慢推进,沿上腔静脉插入至右心室中,注意避免插入腋静脉、右心房及下腔静脉中。调整导管头部角度,当出现稳定的右心室压力波形后观察并记录右心室压力。结果显示(附图4),野百合碱造模后大鼠右心室压力显著升高,阳性药波生坦和法舒地尔可以显著降低肺动脉高压大鼠的右心室压力,匹诺塞林对肺动脉高压大鼠右心室压力的降低作用也十分显著。
实施例5:匹诺塞林对肺动脉高压大鼠脏器指数的改善作用。
压力检测完毕后,开大鼠腹腔胸腔,分离并剪下肺、心、肝,用生理盐水洗净余血后,滤纸将多余液体吸干,称量各脏器重量,与体重相比计算脏器指数。结果显示(附图5),野百合碱造成大鼠肺动脉高压模型后,大鼠的肺脏、心脏及肝脏重量明显增加,脏器指数升高。阳性药物波生坦对于心脏和肺脏的水肿具有较好的改善作用,而对于肝脏水肿没有明显作用;另一阳性药法舒地尔对心脏和肝脏脏器指数增高具有一定的治疗作用,而对肺脏的作用并不明显;匹诺塞林对肺脏、心脏及肝脏的脏器指数增高均具有很好的治疗作用。
实施例6:匹诺塞林对肺动脉高压大鼠右心室肥厚的改善作用。
测量心脏重量后,沿心耳下缘将整个心房部分剪下,留下心室。沿室间隔边缘将右心室壁剪下,称量右心室壁重量,计算右心室壁与整个左心室及室间隔的重量比值,以此评价右心室肥厚程度。结果显示(附图6),阳性药波生坦能够明显改善肺动脉高压所致的右心室肥厚,法舒地尔有一定的改善作用,匹诺塞林降低肺动脉高压大鼠右心室壁肥厚、改善心功能的作用十分明显。
实施例7:匹诺塞林对肺动脉高压大鼠血清中ALT、AST及LDH含量的改善作用。
大鼠压力检测后,开腹腔进行腹主动脉取血,室温凝聚,离心分离血清,利用东芝全自动生化仪测定血清中所含表征心肌损伤情况的天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)和乳酸脱氢酶(lactate dehydrogenase,LDH),以及表征肝脏损伤情况的谷丙转氨酶(Alanine aminotransferase,ALT)。结果显示(附图7),肺动脉高压模型组的大鼠血清的心肌损伤标志酶AST和LDH以及肝脏损伤标志酶ALT显著升高(P<0.05)。血清中AST、LDH或ALT活性间接反映了心肌或肝脏的损伤程度,当心肌细胞或肝脏细胞受损时,细胞膜通透性增加,细胞内物质外漏而致血中AST、LDH、ALT升高。给予匹诺塞林可以明显减少心肌损伤及肝脏损伤标志酶的漏出,降低其在血清中的含量,表明匹诺塞林对于肺动脉高压所引起的心肌损伤和肝脏损伤具有保护作用,改善心功能和肝功能。
实施例8:匹诺塞林对肺动脉高压大鼠血清中NT-proBNP含量的改善作用。
同实施例7获得血清,利用ELISA的方法检测血清中NT-proBNP的含量。B型脑钠肽前体(proBNP)是心脏为弥补收缩无力而增大时,心壁被拉伸时由心脏释放到血液中的化学物质。也就是说proBNP的释放水平与心肌负担水平有直接相关性,在肺动脉高压中,由于右心室负担加重,室壁肥厚,患者血液中的proBNP含量相应增加。当proBNP从心脏释放到血液中,proBNP就会分割成为NT-proBNP和BNP。目前普遍认为,NT-proBNP更加稳定,易于追踪,使用简便高效,因此其已成为更灵敏、更广泛使用的表征肺动脉高压的指标。
本实施例利用酶联免疫吸附法来检测肺动脉高压大鼠血清中NT-proBNP的含量,具体步骤为:往包被抗NT-proBNP抗体的微孔板中依次加入样品血清或标准品、生物素化的抗NT-proBNP抗体、HRP标记的亲和素,经过彻底洗涤后用底物TMB显色;TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下最终转化成黄色,颜色的深浅和样品中的NT-proBNP呈正相关;用酶标仪在450nm波长下测定吸光度(OD值),计算血清中该物质浓度。结果显示(附图8),肺动脉高压模型动物血清中NT-proBNP含量明显增高,给予匹诺塞林可以在一定程度上减少proBNP的释放,证明匹诺塞林对肺动脉高压具有防治作用。
实施例9:匹诺塞林对肺动脉高压大鼠肺组织中ET-1含量的改善作用。
给予大鼠野百合碱会导致肺动脉内皮受损,此时受损的内皮大量释放内皮素1(Endothelium,ET-1)。随着肺动脉高压的发生发展,肺组织中聚集大量ET-1,使肺部血管进一步收缩,导致疾病加重。因此ET-1成为判断肺动脉高压疾病严重程度的重要指标。取肺动脉高压大鼠新鲜肺组织,按0.1g组织加入1mL PBS,对其进行匀浆,通过反复冻融2次达到使组织细胞破裂的目的。14000g低温离心20分钟,取上清,得到肺组织匀浆液,对其中ET-1含量用ELISA方法进行检测。
具体步骤为:往包被抗ET-1抗体的微孔板中依次加入肺组织匀浆样品或标准品、生物素化的抗ET-1抗体、HRP标记的亲和素,经过彻底洗涤后用底物TMB显色;TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下最终转化成黄色,颜色的深浅和样品中的ET-1呈正相关;用酶标仪在450nm波长下测定吸光度(OD值),计算组织中该物质浓度。结果显示(附图9),肺动脉高压模型大鼠肺组织中ET-1含量显著升高,给予匹诺塞林可以显著降低肺部ET-1含量,证明匹诺塞林可以有效防治肺动脉高压。
实施例10:病理组织学观察匹诺塞林对肺动脉高压大鼠心脏、肺脏及肺动脉的保护作用。
取心脏中下1/3处的部分心肌,用4%的多聚甲醛固定,石蜡包埋后连续切片,HE染色,光镜下观察右心室壁病理改变,CCD记录图像。结果显示(附图10),肺动脉高压发生时,右心室负荷加重导致右心室壁肥厚,心肌横切面显示心肌细胞排列致密,细胞肥大。给予匹诺塞林后,改善心肌细胞肥大现象。
取大鼠肺脏左肺上叶,用生理盐水将余血冲洗干净,用4%的多聚甲醛固定,石蜡包埋后连续切片,Masson染色,光镜下观察肺部组织中肺泡及肺血管病理改变,CCD记录图像。结果显示(附图11),肺动脉高压发生时,肺泡间隙水肿、间质增厚、充血,肺部小血管肌化、血管壁增厚。给予匹诺塞林后,改善肺部损伤情况。
取大鼠肺动脉主干,小心将其与心脏、肺脏及气管分开。用4%的多聚甲醛固定,石蜡包埋后连续切片,HE染色,光镜下观察肺动脉主干血管壁增厚情况,CCD记录图像。结果显示(附图12),肺动脉高压发生时,由于血管内皮脱落,造成肺动脉平滑肌细胞增殖,管壁变厚。给予匹诺塞林后,逆转肺动脉血管增厚情况。
实施例11:匹诺塞林体外舒张肺动脉血管作用。
取两个培养皿,倒入少量配制好的K-H液,通入95%O2和5%CO2混合气预饱和,并将培养皿置于冰上预冷。断头处死大鼠,迅速取出心肺,置于其中一个培养皿,轻轻摇动,去除血液残留后置于第二个培养皿中。小心剪去多余组织后,将心肺同针成三角形固定在带硅胶的平皿中,完全撑开后暴露肺动脉主干及左右分支,将分支血管剪成长度约为3mm的肺动脉环。
小心用两个不锈钢三角环插入到血管环中,将一端固定于浴槽底部,另一端连于张力换能器,浴槽中加入8mL KH液,维持37℃,充入95%O2和5%CO2的混合气体。血管张力由MP100A记录。调节初始张力为0.7g,并不断调节一维位移微调器,使血管环张力稳定在初始张力附近,稳定1h,期间每隔30min换一次K-H液。随后给予两次高钾K-H(60mmol·L-1KCl)液刺激收缩。升高0.7g以上的血管环可用。血管活性评价后,用普通KH液将其平衡至基础值,随后用60mM高钾KH液预收缩血管,约20min后达到平台,浓度累积加入匹诺塞林(0.3μM-100μM),加药间隔为5min,观察其对血管舒张作用。结果显示(附图13),加入匹诺塞林后,高钾预收缩的离体肺动脉血管明显舒张,证明匹诺塞林具有舒张肺动脉的作用。
整体动物实验结果表明,与肺动脉高压模型组比较,在肺动脉高压发病早期给予匹诺塞林(30mg/kg)能够明显改善肺动脉高压发病过程中的体重降低现象,降低肺动脉高压的动物死亡率,改善肺动脉高压大鼠的心电图,证明其能够减轻肺动脉高压造成的心脏损伤。给予匹诺塞林后,肺动脉高压大鼠的右心室收缩压明显降低,即肺动脉压力降低,并且对代偿性的主动脉压力升高具有良好的控制作用。给予匹诺塞林能够降低肺动脉高压引起的血清AST、LDH和ALT的升高,保护动物心脏和肝脏,使组织损伤降低,肺、心、肝脏器指数也明显降低。匹诺塞林对肺动脉高压所引起的右心室肥厚也有明显的抑制作用,右心室指数明显降低,改善心功能。另外给予大鼠匹诺塞林对肺组织中的ET-1和血清中的NT-proBNP也起到明显的降低作用,说明其改善受损心肺功能。
综上所述,匹诺塞林具有预防、缓解和/或治疗肺动脉高压的作用;显著降低肺动脉高压的动物死亡率;改善心电图,降低肺动脉压和主动压;减轻脏器水肿,降低心脏和肝脏损伤;改善右心室肥厚症状,有效对抗肺动脉高压造成的右心衰竭。匹诺塞林为天然产物中的单体,且目前已实现全合成,具有毒性低、合成工艺简单等优点;具有很好的应用与开发前景,是一种治疗肺动脉高压及其并发症的理想的新型的小分子化合物,可应用于制备预防、缓解和/或治疗肺动脉高压及其导致的慢性阻塞性肺气肿、慢性肺源性心脏病、心力衰竭、肝功能损伤等并发症的产品。
- 还没有人留言评论。精彩留言会获得点赞!