用于肋骨结构特征缺损的修复材料及制备方法和制造模具与流程
本发明涉及医疗器械技术领域,尤其涉及用于肋骨结构特征缺损的修复材料及制备方法和制造模具。
背景技术:
目前,骨缺损在临床上发病率较高,其治疗仍是骨科目前较为棘手的问题。骨缺损治疗虽可采用骨移植、组织工程技术、膜引导性组织再生技术和基因疗法等多种方式,但自体骨移植仍然为骨缺损修复的“金标准”。自体骨因其组织来源一致,具有完整骨质结构以及转导、诱导成骨潜能,仍是异源性转导成骨生物材料和其他合成材料无法比拟的。临床上常用自体肋骨为移植骨源修复下颌骨缺损,恢复其容貌及功能,提高患者的生存质量。由于肋骨弹性好易于弯曲、固定,且易于取材,操作简单,术后并发症少,临床上亦有采用自体肋骨修复大而复杂颅骨缺损。
但是目前取自体肋骨的规范尚缺乏科学数据支撑,且肋骨缺损后通常不进行修复。肋骨缺损不修复会带来许多后遗症。临床研究发现,骨性结构的缺损会导致胸壁缺乏有效的立体结构支撑,外观形态会发生明显的改变,同时也会导致胸壁顺应性的下降,从而影响呼吸和运动的功能。因此,对肋骨缺损的治疗及重建十分重要,亟待开发一种用于肋骨结构特征缺损的修复材料。尽管现有技术中存在用于骨修复的材料,然而,这些材料的力学性能特征以及降解性能并不适用于肋骨部位。
技术实现要素:
本发明要解决的技术问题是,针对现有技术中骨修复材料不适用 于肋骨部位修复的缺陷,提供一种用于肋骨结构特征缺损的修复材料及制备方法和制造模具。
为了解决上述技术问题,本发明提供了一种用于肋骨结构特征缺损的修复材料,所述修复材料包括内部的疏松层以及外部的致密层;所述致密层采用矿化胶原粉体冷压成型,密度为1.5~1.9g/cm3;所述疏松层由填充在所述致密层内部的矿化胶原溶液冷冻干燥而成,密度为0.15~0.4g/cm3。
在根据本发明所述的用于肋骨结构特征缺损的修复材料中,所述致密层采用的矿化胶原粉体由仿生矿化胶原粉和钙磷盐混合而成,其中仿生矿化胶原粉与钙磷盐的质量比为2:1~3:1;所述疏松层采用的矿化胶原溶液由仿生矿化胶原粉和钙磷盐混合后分散在介质中,其中仿生矿化胶原粉与钙磷盐的质量比为4:1~5:1。
在根据本发明所述的用于肋骨结构特征缺损的修复材料中,所述钙磷盐为羟基磷灰石,β-磷酸三钙,磷酸四钙或磷酸八钙。
在根据本发明所述的用于肋骨结构特征缺损的修复材料中,所述疏松层的孔隙率为70%~95%,孔径为50~500μm。
在根据本发明所述的用于肋骨结构特征缺损的修复材料中,所述修复材料呈弧形条状,圆弧角度为7°~18°,修复材料的长度为1~100mm,宽度为5~20mm,厚度为1~6mm。
在根据本发明所述的用于肋骨结构特征缺损的修复材料中,所述修复材料的致密层和疏松层的横截面为同中心的两个椭圆形,外部椭圆形的长半轴为2.5~10mm,短半轴为0.5~3mm;内部椭圆形的长半轴为1.2~6mm,短半轴为0.3~1.6mm。
本发明还提供了一种用于肋骨结构特征缺损的修复材料的制备方法,包括以下步骤:
S1、制备矿化胶原粉体和矿化胶原溶液;
S2、将矿化胶原粉体冷压成型为中空的弧形条状,以制备致密层;
S3、在所述致密层内部灌注所述矿化胶原溶液,通过冷冻干燥形 成疏松层,得到所述用于肋骨结构特征缺损的修复材料。
在根据本发明所述的用于肋骨结构特征缺损的修复材料的制备方法中,所述步骤S1具体包括:
步骤S1-1、将胶原溶于盐酸、硝酸或醋酸中的任何一种,配制成胶原的酸溶液,其中胶原浓度为5.0×10-5~5.0×10-3g/mL;
步骤S1-2、持续搅拌步骤S1-1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.4~0.8mol;
步骤S1-3、持续搅拌步骤S1-2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤S1-2中钙离子加入量的摩尔比为Ca/P=1/1~2/1;
步骤S1-4、持续搅拌步骤S1-3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合体系出现白色悬浊液;
步骤S1-5、将步骤S1-4所得混合体系静置24~120小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉;
步骤S1-6、在步骤S1-5所得仿生矿化胶原粉中加入钙磷盐颗粒,其中仿生矿化胶原粉与钙磷盐的质量比为2:1~3:1,将上述混合物混合均匀后得到用于制备致密层的矿化胶原粉体;
步骤S1-7、在步骤S1-5所得仿生矿化胶原粉中加入钙磷盐颗粒,其中仿生矿化胶原粉与钙磷盐的质量比为4:1~5:1,将上述混合物分散在水中搅拌24~72小时,用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层的矿化胶原溶液。
在根据本发明所述的用于肋骨结构特征缺损的修复材料的制备方法中,所述步骤S2具体为:在制造模具中加入矿化胶原粉体,向制造模具施加压力,使施加在矿化胶原粉体上的压强达到400~600MPa,保压400~600秒,得到致密层。
本发明还提供了一种用于肋骨结构特征缺损的修复材料的制造模 具,其特征在于,包括:成型模、底座和压柱,所述底座上具有型芯,所述成型模与底座合模后形成一用于容纳矿化胶原粉体的型腔,所述压柱的截面形状与所述型腔的截面形状一致,用于压入所述型腔中对矿化胶原粉体进行施压。
本发明的上述技术方案具有如下优点:本发明采用矿化胶原粉体冷压成型制成致密层,并在内部填充矿化胶原溶液冷冻干燥制成疏松层,该双层结构的肋骨修复材料与肋骨缺损部位的结构和外形相似,降解速率与肋骨的愈合时间相匹配,且力学性能也能符合肋骨部位要求。
附图说明
图1为根据本发明的用于肋骨结构特征缺损的修复材料的俯视图;
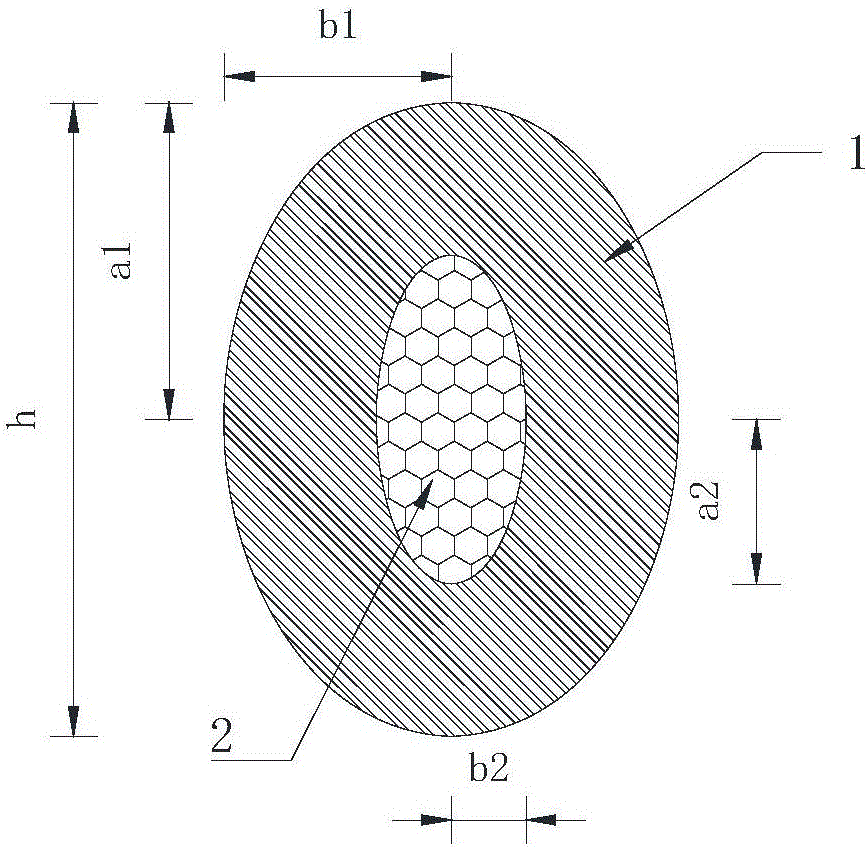
图2为图1中A-A处的剖面图;
图3为根据本发明的用于肋骨结构特征缺损的修复材料的立体图;
图4为根据本发明的用于肋骨结构特征缺损的修复材料的制备方法流程图;
图5a-5c为根据本发明用于肋骨结构特征缺损的修复材料的制造模具的第一实施例结构图;
图6a-6b为第一实施例制造模具的装配图;
图7a-7c为根据本发明用于肋骨结构特征缺损的修复材料的制造模具的第二实施例结构图;
图8a-8b为第二实施例制造模具的装配图;
图9a-9c分别为植入修复材料的术后4周、8周和12周的影像学分析结果图;
图10为植入修复材料的术后12周HE染色结果图;
图11a和11b分别为植入修复材料的术后12周马松染色的组织学结果图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
请参阅图1,为根据本发明的用于肋骨结构特征缺损的修复材料的俯视图。图2为图1中A-A处的剖面图。图3为根据本发明的用于肋骨结构特征缺损的修复材料的立体图。如图1-3所示,该实施例提供的用于肋骨结构特征缺损的修复材料宏观的外形为弧形条状,长度L为1~100mm,宽度为h为5~20mm,厚度s为1~6mm。该弧形条状的圆弧角度为θ为7°~18°。虽然该实施例中将用于肋骨结构特征缺损的修复材料设计成弧形条状,但是本领域基础技术人员在肋骨缺损不大于3cm时,也可以将该修复材料设计成直条形,以便于制作。例如,修复材料的长度L为1~30mm,宽度为h为5~20mm,厚度s为1~6mm。
本发明的用于肋骨结构特征缺损的修复材料包括内部的疏松层2以及外部的致密层1。其中致密层1采用矿化胶原粉体冷压成型,密度为1.5~1.9g/cm3。疏松层2由填充在致密层1内部的矿化胶原溶液冷冻干燥而成,密度为0.15~0.4g/cm3。疏松层的孔隙率为70%~95%,孔径为50~500μm,其微观结构单元为有序排列的纳米钙磷盐与胶原纤维。
如图2所示,在本发明的优选实施例中,该修复材料的致密层1和疏松层2的横截面为同中心的两个椭圆形,其中外部椭圆形的长半轴a1为2.5~10mm,短半轴b1为0.5~3mm;内部椭圆形的长半轴a2为1.2~6mm,短半轴为b2为0.3~1.6mm。
在本发明的优选实施例中,可以根据所修复肋骨的部位,设计相应的修复材料尺寸,如表格1所示。
表格1
本发明用于肋骨结构特征缺损的修复材料是基于仿生矿化胶原粉 来制备的。并且,本发明还根据肋骨的结构特点、力学性能特征以及愈合时间等参数对采用的原料成分进行了改进。致密层1采用的矿化胶原粉体是由仿生矿化胶原粉和钙磷盐混合而成,其中仿生矿化胶原粉与钙磷盐的质量比为2:1~3:1。疏松层2采用的矿化胶原溶液由仿生矿化胶原粉和钙磷盐混合后分散在介质中,其中仿生矿化胶原粉与钙磷盐的质量比为4:1~5:1。所述仿生矿化胶原粉是基于体外仿生矿化技术,在仿生矿化溶液中利用胶原分子调控钙、磷离子自组装成纳米羟基磷灰石而构建的一种微观结构有序排列的胶原/纳米钙磷盐复合材料。所述钙磷盐包括但不限于:羟基磷灰石(HA),β-磷酸三钙(β-TCP),磷酸四钙(TTCP)和磷酸八钙(OCP)。
本发明并没有直接使用仿生矿化胶原粉制备修复材料,这是因为仿生矿化胶原粉中钙磷盐比例通常较低,并且仿生矿化形成的钙磷盐结晶度弱,在体内降解快。本发明在仿生矿化胶原粉中添加了适当比例的钙磷盐颗粒。由于通过机械混合方式直接添加的钙磷盐颗粒结晶度较高,降解速度慢,因而可以延长修复材料的整体降解时间,并且力学性能也能符合肋骨部位要求。
下文将参照附图对用于肋骨结构特征缺损的修复材料的制备方法及制造模具的实施例进行详细说明。
请参阅图4,为根据本发明优选实施例的用于肋骨结构特征缺损的修复材料的制备方法流程图。如图4所示,该实施例提供的用于肋骨结构特征缺损的修复材料的制备方法包括以下步骤:
首先,在步骤S1中,制备矿化胶原粉体和矿化胶原溶液。
该步骤S1进一步包括以下步骤:
步骤S1-1、将胶原溶于盐酸、硝酸或醋酸中的任何一种,配制成胶原的酸溶液,其中胶原浓度为5.0×10-5~5.0×10-3g/mL。
步骤S1-2、持续搅拌步骤S1-1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.4~0.8mol。该含钙离子的溶液包括但不限于氯化钙、硝酸钙和醋酸钙的水溶液。
步骤S1-3、持续搅拌步骤S1-2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤S1-2中钙离子加入量的摩尔比为Ca/P=1/1~2/1。该含磷酸根离子的溶液包括但不限于磷酸、磷酸氢二钠、磷酸二氢钠、磷酸氢二铵和磷酸二氢铵的水溶液。
步骤S1-4、持续搅拌步骤S1-3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合体系出现白色悬浊液。
步骤S1-5、将步骤S1-4所得混合体系静置24~120小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉。该步骤中还可以对冷冻干燥的产物研磨后过筛,筛选出粒径小于200μm的仿生矿化胶原粉使用。
步骤S1-6、在步骤S1-5所得仿生矿化胶原粉中加入钙磷盐颗粒。其中仿生矿化胶原粉与钙磷盐的质量比为2:1~3:1,将上述混合物混合均匀后得到用于制备致密层1的矿化胶原粉体。
步骤S1-7、在步骤S1-5所得仿生矿化胶原粉中加入钙磷盐颗粒,其中仿生矿化胶原粉与钙磷盐的质量比为4:1~5:1,将上述混合物分散在纯化水中搅拌24~72小时。因为胶原在水中具有一定的溶胀性,胶原与钙磷盐分散在水中后形成类似胶状液。随后用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层2的矿化胶原溶液。
本申请在制备仿生矿化胶原粉时,加入的钙离子含量相对较高,由此制得的仿生矿化胶原粉中钙磷盐比例也较高,可延长修复材料的降解时间。但是,该钙磷盐比例仍然不能满足肋骨部位的要求,因此在步骤S1-6和步骤S1-7中以机械混合的方式添加了适量的结晶度较高的钙磷盐,使其降解时间与肋骨部位的愈合时间相匹配。
在步骤S2中,将矿化胶原粉体冷压成型为中空的弧形条状,以制备致密层1。该步骤具体为:在制造模具中加入如步骤S1-6制得的矿化胶原粉体,并向制造模具施加压力,使施加在矿化胶原粉体上的压强达到400~600MPa,保压400~600秒,得到致密层1。请结合参阅图 5a-5c,为根据本发明用于肋骨结构特征缺损的修复材料的制造模具的第一实施例结构图。其中图5a、5b和5c分别为该制造模具中成型模3、底座4和压柱5的立体结构图。如图所示,本发明还相应提供了一种用于肋骨结构特征缺损的修复材料的制造模具,包括成型模3、底座4和压柱5。底座4上具有型芯41。请参阅图6a-6b,为第一实施例的制造模具装配图。如图6a中所示,成型模3与底座4合模后形成一型腔31,用于装填前述制得的矿化胶原粉体。如图6b中所示,在完成矿化胶原粉体的装填后,将压柱5压入型腔31中向矿化胶原粉体施加压力,该压柱5的截面形状与型腔31的截面形状一致。
在该第一实施例中,模具整体呈弧形,使得型腔31的形状与本发明中用于肋骨结构特征缺损的修复材料的形状相匹配,且该模具的弧形角度与修复材料的圆弧角度相同,即7°~18°。型腔31的长度优选为1~100mm。型腔31还可以在开口部位保留一定的直口部位,以便于压柱5进入。型腔31的横截面同样为同中心的两个椭圆形,外部椭圆形的长半轴为2.5~10mm,短半轴为0.5~3mm;内部椭圆形的长半轴为1.2~6mm,短半轴为0.3~1.6mm。图7a-7c为为根据本发明用于肋骨结构特征缺损的修复材料的制造模具的第二实施例结构图。图8a-8b,为第二实施例的制造模具装配图。该第二实施例与第一实施例基本相同,不同之处在于:模具整体呈直线型,不存在弧度。第二实施例的制造模具可以适用于尺寸较小的肋骨缺损,比如不大于3cm的缺损,由于肋骨弧度体现的非常不明显,不带有弧度的直条形修复材料也能满足要求。并且,使用该直线型模具加工的材料成品率高,操作成本低。
该步骤S2中基于上述模具的具体加工过程可包括:
步骤S2-1、根据待制造的致密层的体积计算需要使用的矿化胶原粉体的质量,准确称取粒径<200μm的矿化胶原粉体,装入成型模3与底座4合模后形成的型腔31内,如图6a。矿化胶原粉体装填过程中可以通过压力机手动将粉末压紧,以便于粉末的装填。
步骤S2-2、完成矿化胶原粉体的装填后,将压柱5放入装料模34的型腔31中,如图6b所示。再将整套制造模具放入压力机中,向制造模具施加压力,使施加在矿化胶原粉体上的压强达到400~600MPa,保压400~600秒后卸去压力。该步骤中保压时间非常关键,保压时间太短不利于矿化胶原粉体紧密结合,影响肋骨材料的机械强度,也容易导致器件表面产生掉粉、遇水溶胀、体内降解过快等不良后果,保压时间太长将使成型器件内部应力过大,可能导致应力开裂,保压时间太长也降低了生产效率。
在步骤S3中,在致密层1内部灌注如步骤S1-7制得的矿化胶原溶液,进行充分冷冻干燥,形成疏松层2,得到用于肋骨结构特征缺损的修复材料。将所获得的干燥修复材料包装并辐照灭菌后即可作为肋骨缺损修复产品。
使用本发明工艺步骤和原料配比制备的用于肋骨结构特征缺损的修复材料具有与人体肋骨相似的化学组成和微观结构,其钙磷盐晶体为纳米尺寸,具有良好的生物活性,生物相容性和生物降解性,可促进骨再生,并随新骨的生成最终降解。该修复材料在肋骨修复中可达到自体骨的效果,具有优异的骨诱导活性,并且可通过开放手术的方式植入到骨缺损部位,可用于非承重部位骨缺损。
实例1
1、将胶原溶于盐酸,配制成胶原的酸溶液,其中胶原浓度为5.0×10-5g/mL。
2、持续搅拌步骤1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.4mol。
3、持续搅拌步骤2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤2中钙离子加入量的摩尔比为Ca/P=2/1。
4、持续搅拌步骤3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合 体系出现白色悬浊液。
5、将步骤4所得混合体系静置48小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉。
6、在步骤5所得仿生矿化胶原粉中加入羟基磷灰石颗粒。其中仿生矿化胶原粉与羟基磷灰石的质量比为3:1,将上述混合物混合均匀后得到用于制备致密层的矿化胶原粉体。
7、在步骤5所得仿生矿化胶原粉中加入羟基磷灰石颗粒,其中仿生矿化胶原粉与羟基磷灰石的质量比为5:1,将上述混合物溶于纯化水中搅拌分散48小时,用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层的矿化胶原溶液。
8、在制造模具中加入步骤6所得矿化胶原粉体,并向制造模具施加压力,使施加在矿化胶原粉体上的压强达到400MPa,保压600秒,得到致密层。
9、在致密层内部灌注步骤7制得的矿化胶原溶液,进行充分冷冻干燥,形成疏松层,灭菌后得用于肋骨结构特征缺损的修复材料。
该实例1的修复材料长度为10mm,宽度为12mm,厚度为5mm。圆弧角度为15°,修复材料中致密层的密度为1.6g/cm3;疏松层的密度为0.28g/cm3。疏松层的孔隙率为85%。
实例2
1、将胶原溶于硝酸,配制成胶原的酸溶液,其中胶原浓度为5.0×10-4g/mL。
2、持续搅拌步骤1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.6mol。
3、持续搅拌步骤2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤2中钙离子加入量的摩尔比为Ca/P=1/1。
4、持续搅拌步骤3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合 体系出现白色悬浊液。
5、将步骤4所得混合体系静置24小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉。
6、在步骤5所得仿生矿化胶原粉中加入β-磷酸三钙颗粒。其中仿生矿化胶原粉与β-磷酸三钙的质量比为2:1,将上述混合物混合均匀后得到用于制备致密层的矿化胶原粉体。
7、在步骤5所得仿生矿化胶原粉中加入β-磷酸三钙颗粒,其中仿生矿化胶原粉与β-磷酸三钙的质量比为4:1,将上述混合物溶于纯化水中搅拌分散72小时,用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层的矿化胶原溶液。
8、在制造模具中加入步骤6所得矿化胶原粉体,并向制造模具施加压力,使施加在矿化胶原粉体上的压强达到600MPa,保压500秒,得到致密层。
9、在致密层内部灌注步骤7制得的矿化胶原溶液,进行充分冷冻干燥,形成疏松层,灭菌后得用于肋骨结构特征缺损的修复材料。
该实例2的修复材料长度为1mm,宽度为5mm,厚度为1mm。圆弧角度为7°,修复材料中致密层的密度为1.9g/cm3;疏松层的密度为0.4g/cm3。疏松层的孔隙率为70%。
实例3
1、将胶原溶于醋酸,配制成胶原的酸溶液,其中胶原浓度为5.0×10-3g/mL。
2、持续搅拌步骤1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.8mol。
3、持续搅拌步骤2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤2中钙离子加入量的摩尔比为Ca/P=3/2。
4、持续搅拌步骤3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合 体系出现白色悬浊液。
5、将步骤4所得混合体系静置120小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉。
6、在步骤5所得仿生矿化胶原粉中加入磷酸四钙颗粒。其中仿生矿化胶原粉与磷酸四钙的质量比为5:2,将上述混合物混合均匀后得到用于制备致密层的矿化胶原粉体。
7、在步骤5所得仿生矿化胶原粉中加入磷酸四钙颗粒,其中仿生矿化胶原粉与磷酸四钙的质量比为14:3,将上述混合物溶于纯化水中搅拌分散48小时,用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层的矿化胶原溶液。
8、在制造模具中加入步骤6所得矿化胶原粉体,并向制造模具施加压力,使施加在矿化胶原粉体上的压强达到500MPa,保压600秒,得到致密层。
9、在致密层内部灌注步骤7制得的矿化胶原溶液,进行充分冷冻干燥,形成疏松层,灭菌后得到用于肋骨结构特征缺损的修复材料。
该实例3的修复材料长度为100mm,宽度为20mm,厚度为6mm。圆弧角度为18°,修复材料中致密层的密度为1.6g/cm3;疏松层的密度为0.25g/cm3。疏松层的孔隙率为80%。
实例4
1、将胶原溶于盐酸,配制成胶原的酸溶液,其中胶原浓度为8.0×10-4g/mL。
2、持续搅拌步骤1所得溶液,缓慢滴加含钙离子的溶液,钙离子的加入量为每克胶原对应加入钙离子0.7mol。
3、持续搅拌步骤2所得溶液,缓慢滴加含磷酸根离子的溶液,磷酸根离子的加入量与步骤1.2中钙离子加入量的摩尔比为Ca/P=5/3。
4、持续搅拌步骤3所得溶液,缓慢滴加NaOH溶液至混合体系pH=6~8,当pH=5~6时,混合体系开始出现沉淀,当pH=7时,混合 体系出现白色悬浊液。
5、将步骤4所得混合体系静置72小时,分离出沉淀并洗去杂质离子,随后进行冷冻干燥,研磨后获得仿生矿化胶原粉。
6、在步骤5所得仿生矿化胶原粉中加入磷酸八钙颗粒。其中仿生矿化胶原粉与磷酸八钙的质量比为7:3,将上述混合物混合均匀后得到用于制备致密层1的矿化胶原粉体。
7、在步骤5所得仿生矿化胶原粉中加入磷酸八钙颗粒,其中仿生矿化胶原粉与磷酸八钙的质量比为9:2,将上述混合物溶于纯化水中搅拌分散56小时,用真空泵抽真空,以排出混合溶液中的气泡,得到用于制备疏松层2的矿化胶原溶液。
8、在制造模具中加入步骤6所得矿化胶原粉体,并向制造模具施加压力,使施加在矿化胶原粉体上的压强达到450MPa,保压600秒,得到致密层。
9、在致密层内部灌注步骤7制得的矿化胶原溶液,进行充分冷冻干燥,形成疏松层,灭菌后得用于肋骨结构特征缺损的修复材料。
该实例4的修复材料长度为30mm,宽度为20mm,厚度为4mm。圆弧角度为10°,修复材料中致密层的密度为1.7g/cm3;疏松层的密度为0.2g/cm3。疏松层的孔隙率为90%。
本发明通过动物实验对前述实施例制得的用于肋骨结构特征缺损的修复材料的修复效果进行了验证。具体实验过程如下:使用新西兰大白兔作为实验动物,在术前禁食12h,脱毛剂手术区脱毛,术前30min耳缘静脉注射水合氯醛0.1mg。随后,注射水合氯醛0.1mg耳缘静脉注射全麻,麻醉起效后,动物取右侧卧位,将四肢、头颅固定于解剖台上。对手术区使用肥皂水清洗、晾干,以碘酒、酒精常规消毒,铺无菌巾。取右胸前外侧切口,长3.0cm,切开皮肤,皮下组织。逐层切开各层肌肉组织,术中严密止血。分别切开、剥离骨膜,采用电灼的方法去除骨膜,在不破坏壁层胸膜情况下剪取5~7肋骨,距离胸骨2 cm,长度为2cm,制作完成肋骨性缺损模型。在肋骨性缺损模型中植入本发明实施例1的用于肋骨结构特征缺损的修复材料,长度为2cm,制作完成仿生矿化胶原-肋骨性缺损模型。逐层缝合肌肉、皮下组织及皮肤,术毕观察动物呼吸变化,抽动脉血行血气分析。术后立即肌注庆大霉素50mg,观察伤口出血肿胀情况。术后一周每日肌注庆大霉素5mg/kg。局部创口碘伏擦拭消毒,预防感染,常规护理。术后常规给予抗生素(青霉素40万U)肌肉注射,1次/日,计1周,观察动物反常呼吸、胸壁塌陷等症状和体征、生存情况、并发症等,观察呼吸情况。术后1~3个月均无反常呼吸。全组均无手术死亡及围手术期死亡,活动情况良好,术后皮肤缝线自然脱落,伤口Ⅰ期/甲级愈合。
图9a-9c,分别为植入修复材料的术后4周、8周和12周的影像学分析结果图。图中箭头处为植入的修复材料。从图中可以观察到,12周时实验动物新骨沿移植骨边缘生长,可见肋骨断端完全愈合,成骨性连接。移植处骨密度增高,接近于周围正常肋骨。术后3月处死实验兔,大体观察见重建区胸壁均无明显畸形,周围有纤维组织包绕。清除表面软组织,对标本行脱钙、切片、HE染色后镜下观察结果如图10所示。图10中可见原始植入的修复材料大部分已经降解,并形成了骨融合。其中M为未降解的修复材料,C为成骨细胞,白色箭头处为新生成的毛细血管,T为新骨小梁。图11a和11b分别为术后12周马松染色的组织学结果图。其中,图11a中绿色部分为新骨的胶原蛋白,图11b中红色部分为成熟骨骼的胶原,白色部分为未降解的修复材料。从结果图片可以看出:骨髓细胞充填其间,成骨细胞及破骨细胞减少,骨细胞密集,可见新骨生成后出现的新生线。可见软骨岛与骨小梁形成,新形成的骨小梁边缘有大量柱状或立方状排列的成骨细胞。新骨明显增多,骨小梁排列紧密趋于规则化。因此,术后12周,植入的矿化胶原材料几乎完全降解,材料与新骨之间无纤维包裹,骨形成期间骨及周围的软组织没有炎症现象发生。从上述结果可以看出,本发明用于肋骨结构特征缺损的修复材料能成功进行成骨诱导,还有抗炎症反应作用。
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!