2‑呋喃丙烯醛类化合物在制备抗人类γ疱疹病毒药物中的应用的制作方法
本发明涉及生物制药领域,具体地,涉及2-呋喃丙烯醛类化合物在制备抗人类γ疱疹病毒药物中的应用。
背景技术:
人类γ疱疹病毒有两种亚型,包括卡波氏肉瘤相关疱疹病毒(KSHV)和EB病毒(EBV)。卡波氏肉瘤相关疱疹病毒又名人类8型疱疹病毒(HHV-8),属γ亚型疱疹病毒。EB病毒又叫人类4型疱疹病毒(HHV-4)。KSHV和EBV属于同一属型的疱疹病毒,同源性强。常称姐妹疱疹病毒。
KSHV最早是由美国哥伦比亚大学病理学家Chang等于1994年用代表性差异分析法在卡波氏肉瘤(Kaposi's sarcoma,KS)患者的肉瘤组织中发现。为双链DNA病毒,基因组全长约140kb。EB病毒是1964年Epstein和Barr最先从非洲儿童恶性淋巴瘤(Burkitt lymphoma)体外培养的淋巴瘤细胞系中,用电镜发现的一种新的疱疹病毒,并命名为EB病毒。EBV的基因组与KSHV一样为双链DNA,长度172kb,二者均编码约100个基因。
KSHV与EBV也是少数的肿瘤疱疹病毒。二者均与多种恶性肿瘤相关。KSHV能引起多种恶性肿瘤其中包括:其中包括卡波氏肉瘤(Kaposis sarcoma,KS),原发性渗出性淋巴瘤(primary effusion lymphoma,PEL),多中心卡斯特莱曼病(multicentric Castleman disease,MCD)。与EBV相关的人类疾病有传染性单核细胞增多症、慢性活动性EBV感染、EBV相关嗜血淋巴组织细胞增生症、Burkitt’s淋巴瘤、何杰金病、鼻咽癌等。
KSHV与EBV感染细胞以后均存在两种不同的生命周期,即:潜伏复制周期和裂解复制周期。两者对KHSV相关疾病的发生发展都必不可少。潜伏期是为了维持病毒基因组在细胞与子代细胞的持续存在。裂解期可以在胞内大量复制,以破碎细胞的方式释放大量的具有感染性的病毒颗粒;一方面感染新鲜的细胞维持潜伏期的进行,另一方面促进肿瘤的发生发展。
临床上应用抑制广谱的病毒复制的药物对KSHV和EBV相关疾病的治疗有明显的疗效。但目前药物种类过于单一,且活性较差,毒副作用明显。尽管现已上市新型嘌呤核苷类似物类药物如阿昔洛韦(Acyclovir)及其衍生药物对α和β亚型疱疹病毒感染均有较,但应用在肿瘤病毒EBV与KSHV疗效明显减弱,目前临床上尚无特异性针对人类γ型疱疹病毒裂解复制的药物。
技术实现要素:
本发明为了克服现有技术的上述不足,提供一类可以抑制人类γ型疱疹病毒裂解复制的化合物。
为了实现上述目的,本发明是通过以下方案予以实现的:
2-呋喃丙烯醛类化合物在制备抗人类γ疱疹病毒药物中的应用,所述2-呋喃丙烯醛类化合物具有式(Ⅰ)所示结构式:
其中,R1为氢或烷基;R2和R3独立选自氢、羟基、烷基、烷氧基、苯基、氨基、取代的氨基或糖苷;X为O或S。
作为优选实施方案,式(Ⅰ)中R1为氢或C1~C6的烷基;R2和R3独立选自氢、甲基、羟基、C1~C6的烷基、C1~C6烷氧基、苯基、氨基或糖苷。
更优选地,所述R2和R3形成环。
最优选的,所述R2和R3形成的环为环己基或取代的环己基。
以上术语“烷基”是用于表示饱和烃基,C1~C6的烷基是指含有1~6个碳原子的饱和烃基。
最优选地,所述2-呋喃丙烯醛类化合物具有以下结构式之一:
所述药学上可接受的盐类为与酸或碱形成的药学上可接受的盐。
2-呋喃丙烯醛类化合物与药学上可接受的载体和/或赋形剂所构成的组合物在制备治疗和/或预防由人类γ疱疹病毒感染引起的相关疾病的药物中的用途,所述的2-呋喃丙烯醛类化合物如式(Ⅰ)所示结构式:
其中,R1为氢或烷基;R2和R3独立选自氢、羟基、烷基、烷氧基、苯基、氨基、取代的氨基或糖苷;X为O或S。
所述的药物为抑制γ疱疹病毒的裂解复制的药物,所述γ疱疹病毒为卡波氏肉瘤相关疱疹病毒和/或EB病毒。
同时,本发明提供了抗人类γ型疱疹病毒感染的药物组合物,其中含有有效剂量的式(I)所述的化合物。
本发明通过在细胞水平进行抗KSHV及EBV裂解复制抑制的筛选实验,发现一类新型2-呋喃丙烯醛类化合物可以有效抑制KSHV及EBV的裂解复制,且细胞毒性很小。此类2-呋喃丙烯醛类化合物可用于治疗或预防KSHV、EBV感染引起的相关疾病其中包括:经典型卡波西氏肉瘤(Classic-KS)、艾滋病相关型卡波西氏肉瘤(AIDS-KS)、器官移植相关型卡波西氏肉瘤(post-transplant KS)、Burkitt’s淋巴瘤、何杰金病、鼻咽癌等。
与现有技术相比,本发明具有以下有益的效果:
本发明首次发现一类可以抑制人类γ型疱疹病毒裂解复制的化合物,本发明所述的化合物将在以下方面具有良好的应用前景:
治疗KSHV相关疾病:
1.鉴于本发明所述化合物的高效抑制KSHV裂解复制:因此所述化合物可用于治疗KSHV导致的相关恶性肿瘤,如:经典型卡波西氏肉瘤(KS)。Grundhoff等曾在研究工作中报道,KSHV的裂解复制是KS维持的重要条件,抑制KSHV的裂解复制可引起KS肉瘤的萎缩和消失(Grundhoff and Ganem,2004.J.Clin.Invest.113:124-136)。
2.鉴于本发明所述化合物可有效抑制KSHV裂解复制,因此本发明所述化合物可用于治疗艾滋病相关型卡波西氏肉瘤(AIDS-KS)。研究证实,共感染HIV和KSHV比单纯感染KSHV具有更高的KS发病几率,且病程进展迅速,致死率也明显增高。目前AIDS-KS已成为AIDS患者最主要的致死性并发症。临床上对于AIDS及AIDS-KS的治疗常采用HAART疗法,能有效降低病人体内HIV拷贝数,并可提高病人的免疫力,一定程度上降低了AIDS-KS的发病率,但HAART是通过抑制HIV从而治疗AIDS-KS并不是针对KS疾病的病原体KSHV,目前仍无报道证实HAART疗法对KSHV有直接作用。此外,部分AIDS患者在接受HAART治疗的最初阶段由于体内CD4+T细胞数增高常会引起免疫重建炎症综合征(Immune reconstitution inflammatory syndrome,IRIS),许多患者会在此阶段表现出卡波西氏肉瘤的快速发病(Connick et al.,2004.Clin Infect Dis.39:1852-5)。可见HAART对于治疗AIDS-KS还显不足。本专利中所述化合物与HAART疗法共同用药治疗AIDS-KS可作为更有效的疗法。
3.本发明所述化合物可用于治疗器官移植患者接受免疫抑制治疗后发生的KS。器官移植患者为了减少自身免疫系统对外源器官的排斥作用,常需进行免疫抑制治疗。但在使用免疫抑制剂后,部分患者出现器官移植后肿瘤,包括的器官移植后KS。对于这种情况,患者不得不停止免疫抑制治疗,承受失去移植的器官的可能性。本发明所述化合物可有效抑制KSHV的裂解复制,当与免疫抑制剂联合使用时,可减少器官移植后KS的发病或使已发病的KS消退。
治疗EBV引起的相关疾病:
EBV能感染95%以上的成人,是少数仅有的能导致肿瘤发生的病毒。它是一系列肿瘤发病与进程促进的病原体,其中包括:单核细胞坏死症、AIDS相关的淋巴瘤、移植性的淋巴细胞增殖病、霍奇金淋巴瘤、伯基利淋巴瘤、还有地方性的鼻咽癌等等。
比起KSHV只在少数病人中发病,EBV导致的鼻咽癌却严重影响了我国人民的生活质量,尤其是在广东地区高发。由于鼻咽癌发病部位的局限性,现在也只能采用传统的放疗化疗为主。此类方法不仅副作用极大,而且治标不治本容易导致疾病的复发。本专利申请的化合物能高效抑制病毒的裂解复制,阻断肿瘤发生的促进手段,结合抗肿瘤药物合用可以相当好的疗效。
附图说明
图1为C10抑制EBV裂解复制活性及细胞毒性曲线图。
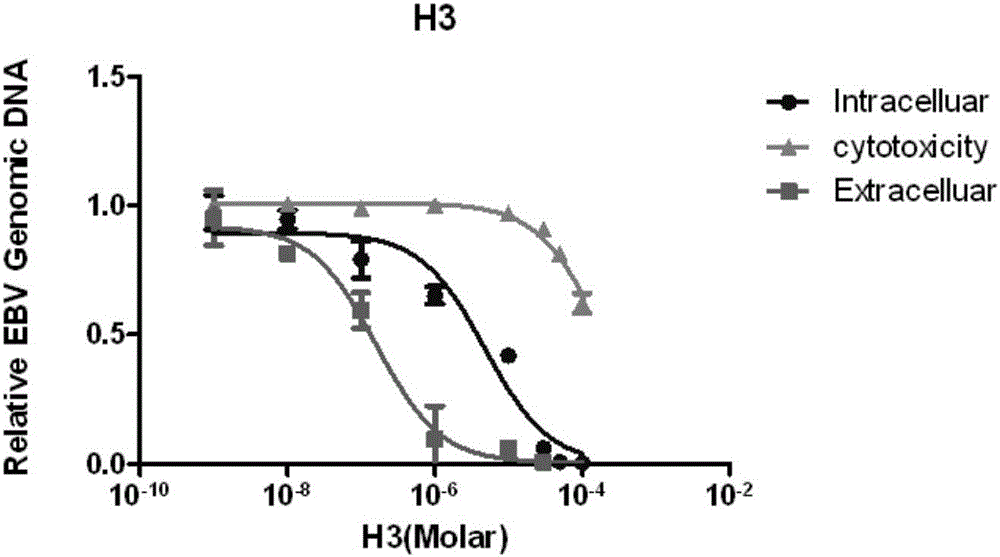
图2为H3抑制EBV裂解复制活性及细胞毒性曲线图。
图3为H5抑制EBV裂解复制活性及细胞毒性曲线图。
图4为H10抑制EBV裂解复制活性及细胞毒性曲线图。
图5为H13抑制EBV裂解复制活性及细胞毒性曲线图。
图6为H14抑制EBV裂解复制活性及细胞毒性曲线图。
图7为H17抑制EBV裂解复制活性及细胞毒性曲线图。
图8为H18抑制EBV裂解复制活性及细胞毒性曲线图。
图9为C10抑制KSHV裂解复制活性及细胞毒性曲线图
图10为26个化合物抑制KSHV、EBV细胞增殖和DNA复制活性。
图11为26个化合物的细胞毒性试验。
具体实施方式
下面结合说明书附图和具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
实施例1
化合物的筛选,步骤如下:
1、化合物库预处理:虚拟筛选化合物库为自备化合物数据库。化合物数据库作如下处理:去除离子及络合水分子、加电荷、质子化、产生三维构象。这些流程均在药物设计软件包Discovery Studio 3.0中完成。其中质子化在pH 6.5~8.5条件下进行。准备好的小分子库用于虚拟筛选。
2、以基于2-呋喃丙烯醛结构进行子结构匹配的数据库搜寻,找出含有该母核的化合物。最终筛选出26个化合物去做细胞学实验。
实施例2
KSHV、EBV裂解复制抑制活性测定,具体步骤如下:
1、细胞培养:体外培养BCBL-1(潜伏KSHV感染细胞株)、P3HR-1细胞(EBV潜伏感染细胞株)。使用含有10%胎牛血清的RPMI 1640培养基,在37℃,5%二氧化碳浓度条件下进行常规维持培养和传代。
2、药物干预:调整对数生长期使BCBL-1(KSHV阳性细胞),P3HR-1(EBV阳性细胞)的细胞密度为3×105cells/ml,使用20ng/mL的TPA+0.3mM的丁酸盐进行诱导处理,诱导细胞内的病毒进入裂解复制期。细胞经诱导剂处理3小时后,对细胞进行不同浓度的化合物(C10、H1~H25)处理,每个浓度设3个平行复孔,并设不进行TPA诱导和不经化合物处理的对照组进行比较。
3、测试方法:细胞经诱导2天后收集细胞,提取细胞总DNA。应用实时定量PCR技术,使用LightCycler FastStart DNA MasterPlus SYBR green试剂盒、应用LANA引物和GAPDH引物,分别检测上述细胞总DNA中LANA和GAPDH的拷贝数,并计算LANA/GAPDH的相对比值来评估细胞内KSHV病毒DNA的相对复制情况。应用EBNA-1引物和GAPDH引物,分别检测上述细胞总DNA中EBNA-1和GAPDH的拷贝数,并计算EBNA-1/GAPDH的相对比值来评估细胞内EBV病毒DNA的相对复制情况。
4、结果处理:按照下列公式计算各化合物在不同浓度下的KSHV裂解复制相对抑制数,和各化合物在不同浓度下的EBV裂解复制相对抑制数。
KSHV裂解复制相对抑制数=(LANA/GAPDHTPA+&compound+-LANA/GAPDHTPA-&compound+)/(LANA/GAPDHTPA+&compound--LANA/GAPDHTPA-&compound-)
EBV裂解复制相对抑制数=(EBNA-1/GAPDHTPA+&compound+-EBNA-1/GAPDHTPA-&compound+)/(EBNA-1/GAPDHTPA+&compound--EBNA-1/GAPDHTPA-&compound-)
以病毒的相对抑制数为纵坐标,药物浓度为横坐标绘制各化合物对病毒裂解复制的抑制曲线图,并计算各药物复制的半数抑制剂量(IC50)以评价各化合物对病毒裂解复制的抑制活性,结果见表1。
实施例3抑制KSHV、EBV病毒颗粒释放实验
1、细胞培养:体外培养BCBL-1细胞。使用含有10%胎牛血清,100U/ml青霉素,100μg/ml链霉素的RPMI 1640培养基,在37℃,5%二氧化碳浓度条件下进行常规维持培养和传代。
2、药物干预:调整对数生长期BCBL-1细胞密度为3×105cells/ml,使用20ng/ml TPA诱导BCBL-1细胞进入裂解复制期。使用DMSO将待测化合物配置为不同浓度溶液。BCBL-1细胞经TPA处理3小时后,对细胞进行不同浓度的化合物(C10、H1~H25)处理,每个浓度设3个平行复孔,并设不经化合物处理以及不进行TPA诱导的对照组进行比较。
3、测试方法:细胞经TPA诱导处理5天后,收集细胞培养液1,000rpm离心5min,弃除细胞沉淀。上清再次100,000g离心1h,弃除上清,使用200ul PBS重悬病毒颗粒。使用DNase I在37℃处理浓缩病毒液1小时,去除病毒颗粒外的杂质DNA分子。随后使用细胞裂解液和蛋白酶K处理病毒浓缩液,并用酚氯仿法抽提KSHV病毒DNA。提取得到的病毒DNA经冰乙醇沉淀后,最终使用50ul TE缓冲液溶解。应用实时定量PCR技术,使用LightCycler FastStart DNA MasterPlus SYBR green试剂盒、LANA或者EBNA-1引物检测细胞培养液上清液中的病毒DNA拷贝数,以评价疱疹病毒的产毒水平。
4、结果处理:按照公式:KSHV产毒相对抑制数=(LANATPA+&compound+-LANATPA+&compound-)/(LANATPA+&compound--LANATPA-&compound-)EBV产毒相对抑制数=(EBNA-1TPA+&compound+-EBNA-1TPA+&compound-)/(EBNA-1TPA+&compound--EBNA-1TPA-&compound-)计算各化合物不同浓度下的KSHV与EBV的相对产毒抑制数。以产毒相对抑制数为纵坐标,药物浓度为横坐标绘制各化合物对产毒的抑制曲线图,并计算各化合物的产毒半数抑制剂量(EC50)以评价各化合物对疱疹病毒颗粒释放的抑制活性,结果见表1、图1~10。
实施例4对宿主细胞毒性测试
1、细胞培养:体外培养BCBL-1细胞,使用含有10%胎牛血清,100U/ml青霉素,100μg/ml链霉素的RPMI 1640培养基,在37℃,5%二氧化碳浓度条件下进行常规维持培养和传代。
2、测试方法:调整BCBL-1细胞密度为3×105cells/ml,使用不同浓度各化合物处理细胞,每个浓度设3个平行复孔,2天后使用台盼蓝染色,光镜下计数活细胞数。
3、结果处理:按照公式:相对毒性=1-live cell compound+/live cell compound-计算各化合物不同浓度下的相对毒性和半数致死剂量(CC50),用于评价各化合物的细胞毒性,结果见表1和图11。另按照公式:选择抑制常数(SI)=CC50/IC50计算各化合物的选择抑制常数,以评价各化合物的用药安全性。
表1筛选的8个化合物的结构及抗EBV裂解复制活性数据
化合物C10的KSHV裂解复制半数抑制剂量(IC50)为3.4μM,KSHV产毒半数抑制剂量(EC50)为3μM,BCBL-1细胞半致死剂量(CC50)为60μM,选择抑制常数(SI)为17.6。而C10对EBV裂解复制半数抑制剂量(IC50)为1.5μM,EBV产毒半数抑制剂量(EC50)为0.76μM,P3-HR-1细胞半致死剂量(CC50)为42μM,选择抑制常数(SI)28;化合物H13对EBV裂解复制半数抑制剂量(IC50)为3.96μM,EBV产毒半数抑制剂量(EC50)为3.98μM,P3-HR-1细胞半致死剂量(CC50)为1204μM,选择抑制常数(SI)242;阳性对照阿昔洛韦的KSHV裂解复制半数抑制剂量(IC50)为1.2μM,BCBL-1细胞半致死剂量(CC50)为284μM,选择抑制常数(SI)为218。由表1可以发现:通过计算机虚拟筛选得到的新型2-呋喃丙烯醛类化合物活性比较好,且化合物H13细胞毒性明显降低,药物安全使用区间更广。
- 还没有人留言评论。精彩留言会获得点赞!