治疗卵巢癌的方法与流程
本申请要求2016年9月27日提交的美国临时申请no.62/400,495的优先权,该临时申请通过引用,整体并入本文。
背景技术:
已知卵巢肿瘤通常表达雌激素受体(er),包括erα。er可以被雌激素激活并转移到细胞核中与dna结合,从而调节各种基因的活性。参见,例如,marino等“estrogensignalingmultiplepathwaystoimpactgenetranscription,”curr.genomics7(8):497-508(2006);以及heldring等“estrogenreceptors:howdotheysignalandwhataretheirtargets”,physiol.rev.87(3):905-931(2007)。卵巢癌可以是不同类型的,包括上皮性卵巢癌、基质卵巢癌和卵巢肉瘤。上皮性卵巢癌通常分为浆液性癌、子宫内膜样癌、粘液性癌、透明细胞癌和未分化癌。卵巢癌也可能是原发性腹膜卵巢癌、基质卵巢癌和卵巢肉瘤。无论起源或类型如何,卵巢癌都是一种严重且常常致命的疾病,亟需要新的有效的治疗方法。
技术实现要素:
本发明公开的一些实施方式涉及治疗受试者的卵巢癌和/或肿瘤,包括向所述受试者给药治疗有效量的rad1901。
本发明公开的一些实施方式涉及治疗受试者的卵巢癌和/或,包括向所述受试者给药治疗有效量的rad1901和治疗有效量的一种或多种第二治疗剂。
在本发明公开的方法的一些实施方式中,所述被治疗的卵巢癌和/或肿瘤表达erα。
附图说明
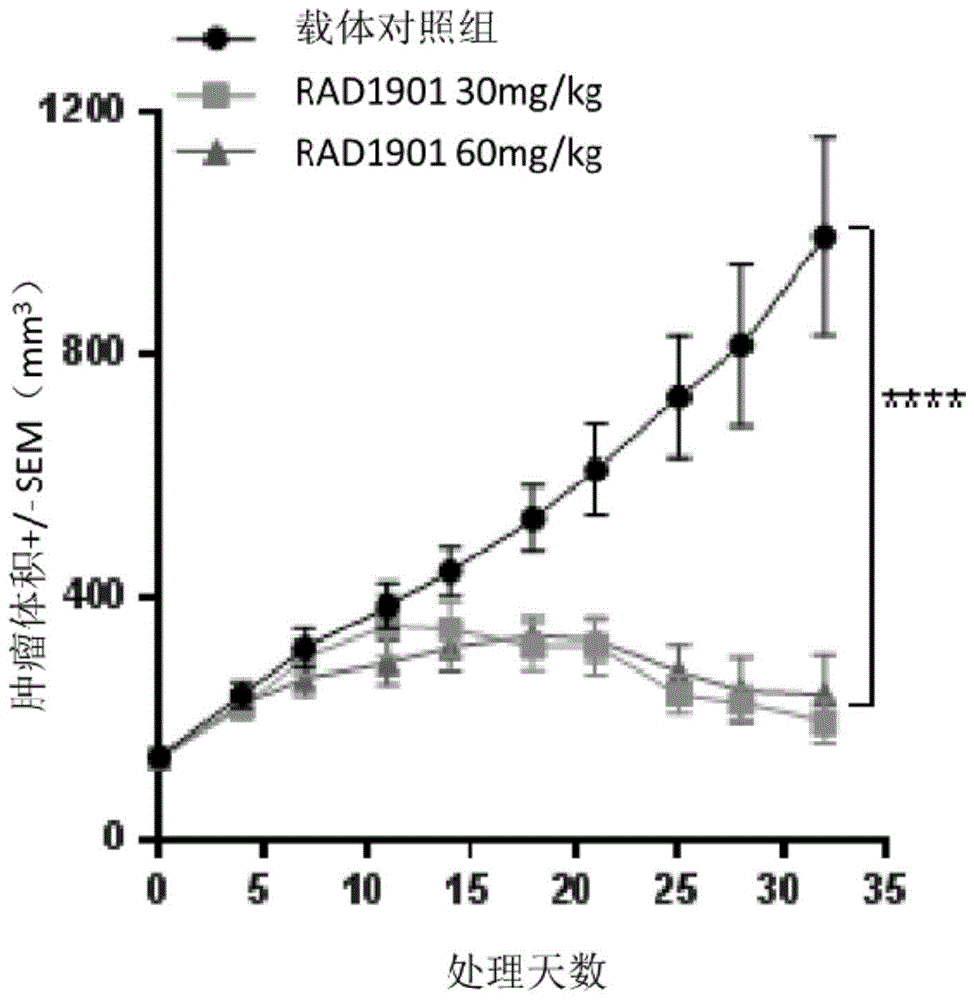
图1:rad1901(每天口服30mg/kg或60mg/kg)对肿瘤生长的抑制和消退效果的pdx肿瘤模型(携带来自既定卵巢癌患者的异种移植物的小鼠)。
图2:pdx模型中,rad1901(每天口服30mg/kg或60mg/kg)治疗第32天的个体肿瘤(individualtumor)生长抑制和消退效果。
具体实施方式
鉴于卵巢癌的长期预后通常较差,迫切需要新的且特别有效的药剂,其以迄今未经批准的治疗途径为目标。目前还没有官方指定的抗雌激素或选择性雌激素受体降解剂(selectiveestrogenreceptordegraders,serds)经fda批准用于治疗卵巢癌,因此需要一种对雌激素受体有效的、相对无毒的、耐受性良好的药物,这是一项特别令人兴奋且至关重要的突破。无论esr1突变状态和之前的内分泌治疗如何,rad1901被发现在乳腺癌异种移植模型中抑制肿瘤生长和/或驱动肿瘤消退。本发明提供的实施例显示出在某些pdx模型(携带来源于患者的卵巢癌异种移植物的小鼠)中,在30mg/kg或60mg/kg的每日口服剂量下,rad1901有效抑制肿瘤生长并且出乎预料地驱动肿瘤消退。
在本发明中,rad1901具有以下结构,
包括其盐、其异构体、其溶剂化物(例如,水合物)和其前药。
在某些实施方式中,提供了用于治疗有需要的受试者的卵巢癌或肿瘤的方法,包括向受试者给药治疗有效量的本发明公开的rad1901(例如,上述结构、或其盐或其异构体或其溶剂化物(例如,水合物)或其前药)。
在某些实施方式中,提供了抑制有需要的受试者中卵巢癌或肿瘤的生长或产生消退的方法,包括向受试者给药治疗有效量的本发明公开的rad1901(例如上述结构、或其盐或其异构体或其溶剂化物(例如,水合物)或其前药)。
在本发明公开的方法的某些实施方式中,所述卵巢癌或肿瘤是erα阳性的。
在本发明公开的方法的某些实施方式中,rad1901的盐是rad1901的双盐酸盐,具有以下结构:
根据本发明,“治疗”卵巢癌或肿瘤是指实现一种或多种治疗基准,包括但不限于减缓或停止肿瘤生长,驱动肿瘤消退,减轻或中断一种或多种症状,减少患卵巢癌或肿瘤的机会,减少再次发生卵巢癌或肿瘤等的可能性或延长时间。
根据本发明,卵巢癌或肿瘤的“抑制生长”是指减慢肿瘤生长速率或完全停止肿瘤生长。
根据本发明,卵巢癌或肿瘤的“肿瘤消退”或“消退”是指减小卵巢癌或肿瘤的最大尺寸。
在本发明的某些实施方式中,将rad1901(例如,rad1901、其盐或其异构体或其溶剂化物(例如,水合物)或其前药)给药至患有卵巢癌或肿瘤的受试者,与基线(即开始治疗前的大小)相比,可导致卵巢癌或肿瘤大小的减少,或甚至根除或部分根除卵巢癌或肿瘤。因此,本发明公开的所述方法的某些实施方式,相对于治疗前基线,导致一种或多种肿瘤的卵巢癌负荷降低或肿瘤大小减小。
根据本发明,“肿瘤”是恶性肿瘤,并且可与“癌症”互换使用。
肿瘤生长的抑制或消退可以定位于单个肿瘤或特定组织或器官内的一组肿瘤,或者可以是全身性的(即,影响所有组织或器官的肿瘤)。
已知,与雌激素受体β(erβ)相比,rad1901优先结合erα,除非另有说明,否则,本发明中雌激素受体、雌激素受体α,er-α,erα,er,野生型er-α和esr1可互换使用。“雌激素受体α”或“erα”由基因esr1编码。在本发明中,“雌激素受体α阳性”、“erα阳性”、“er+”或“erα+”的卵巢癌或肿瘤是指其中一种或多种细胞表达至少一种erα同种型的卵巢癌或肿瘤。在某些实施方式中,这些细胞过表达erα。
在本发明公开的方法的某些实施方案中,所述卵巢癌或肿瘤对选自由抗雌激素(例如他莫昔芬(tamoxifen)或氟维司群(fulvestrant))、芳香酶抑制剂(例如,阿诺新(aromasin))及他们的组合所组成的组中的药物具有抗性。
通常,本发明公开的方法适用于治疗源自卵巢的肿瘤,无论该肿瘤位于卵巢中还是位于卵巢外(包括身体的其他部位)或两者都有。例如,在一些实施方式中,已经通过外科手术除去了所述受试者的原发性卵巢癌或肿瘤(例如,通过肿瘤切除或器官切除),并且,治疗受试者以1)在她的一个或多个卵巢的外保留转移性卵巢癌或肿瘤;和/或2)减少再次发生的可能性或延长再次发生的时间。在一些实施方案中,当开始治疗时,在所述治疗的受试者的一个或多个卵巢中仍然具有原发性卵巢癌或肿瘤。
在本发明公开的方法的某些实施方式中,通过一种或多种确定风险的标志物、特性(characteristics)、病史或特征(features),预防性地向被认为具有卵巢癌或肿瘤高风险的女性给药rad1901。在这种情况下,受试者在医学上被确定为患卵巢癌或肿瘤的风险升高,并且,提供rad1901以减少女性患卵巢癌或肿瘤的机会。
在本发明公开的方法的某些实施方式中,靶向的卵巢癌或肿瘤是上皮性卵巢癌或肿瘤。在本发明公开的方法的某些实施方式中,所述卵巢癌或肿瘤是上皮性卵巢癌或肿瘤,具有高级别浆液类型、低级别浆液性类型、浆液性类型、子宫内膜样类型、粘液性类型、透明细胞类型、原发性腹膜类型、布伦纳瘤(brennertumours)类型、边缘性瘤(borderlinetumours)类型或未分化癌类型。在一些实施方案中,待治疗的卵巢癌是基质癌或肿瘤。在一些实施方案中,待治疗的卵巢癌是卵巢肉瘤。
在本发明公开的方法的某些实施方式中,所述方法还包括在给药rad1901或其盐或溶剂化物,例如双盐酸盐(1分子rad1901,2分子hcls),之前,确定患者是否患有表达erα卵巢癌或肿瘤的步骤。在某些实施方式中,待治疗的所述肿瘤在所述卵巢癌或肿瘤中>90%,>80%,>70%,>60%,>50%,>40%,>30%,>20%,>10%,>5%,或>1%的细胞表达er。
在本发明公开的方法中使用的rad1901的治疗有效量是当在特定时间间隔给药时实现一种或多种治疗基准(例如,减缓或停止肿瘤生长,驱动肿瘤消退,中断或减轻一种或多种症状,减少患卵巢癌或肿瘤的机会,减少再次发生卵巢癌或肿瘤的可能性或延长时间等)的量。
在本发明公开的方法中,使用的rad1901的治疗有效量的实例包括但不限于约150mg至约2000mg、约200mg、约400mg、约500mg或约1500mg。更优选地,rad1901可以以约100mg至约1000mg、约200mg、约400mg、约500mg、约600mg、约800mg或约1000mg的日剂量给药。在本发明公开的方法的某些实施方式中,给药的rad1901是rad1901的双盐酸盐(1分子rad1901,2个分子hcl)。
在本发明公开的方法中使用的本发明公开的rad1901(和/或其盐或其异构体或其溶剂化物或其前药)可以配制成单位剂型,其为物理离散单位(physicallydiscreteunits),适合作为接受治疗的受试者的单位剂量。每个单位剂量含有治疗有效量的rad1901,任选地与合适的药物载体结合。所述单位剂型可以是每日1次剂量(asingledailydose),也可以是每日多次剂量(oneformultipledailydoses)(例如,每日(q.d.)约1-4次或更多次)。当使用每日多次剂量时,所述单位剂型的每个剂量可以相同或不同。在某些实施方式中,本发明公开的rad1901可以配制成控释制剂。
在本发明公开的方法中使用的本发明公开的rad1901(和/或其盐或其异构体或其溶剂化物或其前药)可以作为任任意活性成分配制成药物组合物。rad1901的药物组合物可进一步含有生理学上可接受的载体(也称为药学上可接受的载体或溶液或稀释剂)。此类药物组合物根据可接受的药学方法制备,例如remington'spharmaceuticalsciences,第17版,ed.alfonsor.gennaro,mackpublishingcompany,eaton,pa.(1985)中描述的方法,其通过引用并入本文。
术语“药学上可接受的载体”是指在被给药的受试者中不引起过敏反应或其他不良反应并且与制剂中的其他成分相容的载体。药学上可接受的载体包括例如,药物稀释剂、赋形剂或载体,它们是根据意在的给药形式能够进行适当选择的,并且与常规药学实践一致。例如,固体载体/稀释剂包括但不限于树胶,淀粉(例如,玉米淀粉、预糊化淀粉)、糖(例如,乳糖、甘露醇、蔗糖、右旋糖)、纤维素材料(例如,微晶纤维素)、丙烯酸酯(例如,聚甲基丙烯酸酯)、碳酸钙、氧化镁、滑石或他们的混合物。药学上可接受的载体可以进一步包括少量辅助物质,例如润湿剂或乳化剂、防腐剂或缓冲剂,以增强治疗剂的保质期或有效性。
可以通过常规方法将游离碱形式的rad1901转化为盐。本发明使用的术语“盐”不受限制,只要该盐由游离碱形式的rad1901形成并且是药理学上可接受的即可;优选地,盐的实例包括氢卤化物盐(例如,盐酸盐、氢溴酸盐、氢碘酸盐等)、无机酸盐(例如,硫酸盐、硝酸盐、高氯酸盐、磷酸盐、碳酸盐、碳酸氢盐等)、有机羧酸盐(例如,乙酸盐、马来酸盐、酒石酸盐、富马酸盐、柠檬酸盐等)、有机磺酸盐(例如,甲磺酸盐、乙磺酸盐、苯磺酸盐、甲苯磺酸盐、樟脑磺酸盐等)、氨基酸盐(例如,天冬氨酸盐、谷氨酸盐等)、季铵盐、碱金属盐(例如,钠盐、钾盐等)、碱土金属盐(镁盐、钙盐等)。此外,本发明公开的方法中,盐酸盐、硫酸盐、甲磺酸盐、乙酸盐等是rad1901优选的“药理学上可接受的盐”。
本发明公开的rad1901的异构体(例如几何异构体,光学异构体,旋转异构体,互变异构体等)可使用通常的分离方法纯化为单一异构体,分离方法包括例如重结晶、光学拆分(opticalresolution)如非对映盐方法、酶分馏方法、各种色谱法(例如,薄层色谱法、柱色谱法、玻璃色谱法等)。本发明中的术语“单一异构体”不仅包括具有100%纯度的异构体,还包括含有除目标(target)外异构体的异构体,其通过常规的纯化操作后仍存在。rad1901或其盐有时存在的多晶型(crystalpolymorph)以及其所有多晶型都包括在本发明的范围中。rad1901的多晶型可以是rad1901的单一类型的多晶型或多种多晶型的混合物。
在某些实施方案中,rad1901是前药形式,其将被转化(例如,通过氧化或水解)成为活性形式的rad1901。
在某些实施方案中,本发明提供的方法还包括分析(profile)受试者的基因,其中所述待分析的基因为选自由下述基因所组成的组中的一种或多种基因:abl1、akt1、akt2、alk、apc、ar、arid1a、asxl1、atm、aurka、bap、bap1、bcl2l11、bcr、braf、brca1、brca2、ccnd1、ccnd2、ccnd3、ccne1、cdh1、cdk4、cdk6、cdk8、cdkn1a、cdkn1b、cdkn2a、cdkn2b、cebpa、ctnnb1、ddr2、dnmt3a、e2f3、egfr、eml4、ephb2、erbb2、erbb3、esr1、ewsr1、fbxw7、fgf4、fgfr1、fgfr2、fgfr3、flt3、frs2、hif1a、hras、idh1、idh2、igf1r、jak2、kdm6a、kdr、kif5b、kit、kras、lrp1b、map2k1、map2k4、mcl1、mdm2、mdm4、met、mgmt、mll、mpl、msh6、mtor、myc、nf1、nf2、nkx2-1、notch1、npm、nras、pdgfra、pik3ca、pik3r1、pml、pten、ptprd、rara、rb1、ret、rictor、ros1、rptor、runx1、smad4、smarca4、sox2、stk11、tet2、tp53、tsc1、tsc2和vhl。
在某些实施方案中,本发明提供的方法还包括调节本发明公开的rad1901(和/或其盐(例如盐酸盐)或其异构体或其溶剂化物(例如水合物)或其前药)的剂量,所述方法包括:
(1)给药本发明公开的rad1901(和/或其盐(例如盐酸盐)或其异构体或其溶剂化物(例如水合物)或其前药)(例如,约350至约500mg/天)的第一剂量3天、4天、5天、6天或7天;
(2)检测雌二醇-er结合活性,例如使用本发明公开的fes-pet成像;其中:
(i)如果er结合活性检测不到或低于预定阈值水平,则继续给药所述第一剂量(即维持剂量水平);或者
(ii)如果er结合活性是可检测到的或高于预定阈值水平,则按照大于第一剂量的第二剂量(例如,第一剂量加上约50至约200mg)施用3、4、5、6或7天,然后进入步骤(3);
(3)检测雌二醇-er结合活性,例如使用本发明公开的fes-pet成像;其中,
(i)如果er结合活性检测不到或低于预定阈值水平,则继续给药第二剂量(即维持剂量水平);或者
(ii)如果er结合活性是可检测到的或高于预定阈值水平,则按照大于第二剂量的第三剂量(例如,第二剂量加上约50至约200mg)施用3、4、5、6或7天,然后进入步骤(4);
(4)重复上述步骤进行第四剂量,第五剂量等的给药,直至检测不到er结合活性。
本发明公开的方法的某些实施方式还包括使用pet成像来检测和/或剂量化(dose)er敏感性或er抗性癌症。
本发明中使用的术语“和/或”包括“和”的情况和“或”的情况。
本发明公开的方法的某些实施方式还包括向受试者给药治疗有效量的一种或多种第二治疗剂,选自由cdk4和/或cdk6抑制剂(例如,瑞博西尼(ribociclib)、阿贝西尼(abemaciclib)和帕博西尼(palbociclib))、紫杉烷(例如,紫杉醇、白蛋白结合紫杉醇(例如,白蛋白结合型紫杉醇(abraxane))、多西紫杉醇(docetaxel)、卡巴他赛(cabazitaxel))、六甲蜜胺、卡培他滨、依托泊苷、吉西他滨、异环磷酰胺、伊立替康、阿霉素、脂质体阿霉素、左旋溶肉瘤素(mephalen)、培美曲塞、拓扑替康、长春瑞滨和pi3k抑制剂(例如、艾代拉利司(idelalisib)、哌立福辛、布帕瑞利司(buparlisib)、杜威利司(duvelisib)、奥派利司(alpelisib)、tgr1202、寇攀利司(copanlisib)、px-866、黛珂投利司(dactolisib)、rp6530、sf1126、ink1117、皮克提利司(pictilisib)、xl147、xl765、裴楼米得529(palomid529)、zstk474、pwt33597、cudc907、me401、ipi549、ic87114、tg100-115、cal263、rp6503、pi103、gne477、aezs136)。当给药多于一种治疗剂时,多种治疗剂可以作为一种或多种组合的或分开的药物组合物同时或基本上同时给药。或者,可以通过一种控释药物组合物或通过单独的药物组合物在不同时间给药一种以上的治疗剂。
本发明提供以下实施例以更好地说明要求保护的发明,而不应解释为限制本发明的范围。就所述的具体材料而言,仅用于说明的目的而非意图限制本发明。本领域技术人员可以在不脱离本发明的范围的情况下,不需要发明创造能力就可开发等同的方法或反应物。应当理解,可以在本发明所述的步骤中进行许多变化,这仍然属于本发明的范围。发明人的目的是将这些变化包括在本发明的范围内。
实施例
材料和方法
以下实施例中使用的rad1901是(6r)-6-(2-(n-(4-(2-(乙基氨基)乙基)苄基)-n-乙基氨基)-4-甲氧基苯基)-5,6,7,8-四氢萘-2-醇二盐酸盐,由irixpharmaceuticals,inc.(florence,sc)制造。rad1901以干粉形态储存,使用时配制成在甲基纤维素的去离子水溶液0.5%(w/v)中的均匀悬浮液,并且,对于动物模型,以口服形式给药。
体内异种移植pdx模型
将所有小鼠圈养在无病原体的实验动物独立通气笼盒中,且装有已灭菌和无尘的垫料芯。在光暗循环(人造光的12-14小时昼夜循环)和设定的室内温度和湿度的条件下,小鼠随意获得灭菌食物和水。
图1中显示的pdx是ov-10-0050卵巢癌肿瘤,其源自来自48岁女性的卵巢腺癌。该肿瘤为3级、细胞角蛋白阳性,证明所述肿瘤是上皮性卵巢癌。所述肿瘤还对er和er靶基因(孕酮受体)染色显示阳性。所述ov-10-0050pdx模型使用活的人肿瘤组织建立,所述人肿瘤组织已经在动物(雌性balb/c裸鼠)中连续传代了有限次以维持肿瘤异质性。当肿瘤达到适当的肿瘤体积起始(tumorvolumeinitiation,tvi)范围(150-250mm3)时,将动物随机分入治疗组和对照组并开始给药(第0天,每组8-10名受试小鼠);所有研究中的动物单独进行每个实验。从第0天开始初始给药,所有组中的动物按重量给药(0.01ml/g;10ml/kg)。从第0天开始,按照规定,每组用载体(对照,口服/每日一次(p.o./q.d.)至结束)或rad1901(30或60mg/kg受试小鼠,口服/每日一次至结束)进行治疗。rad1901剂量为60mg/kg的组由于虚弱和体重减轻,第32天组实验结束。剩余动物(载体和rad190130mg/kg组)的治疗期持续长达42天。
肿瘤测量
使用卡尺在两个维度上每周测量肿瘤大小两次,并且使用以下公式计算体积,单位为mm3:
v=0.5axb2
其中a和b分别是肿瘤的长径和短径。然后使用所述肿瘤大小计算肿瘤生长抑制(tgi)值。
使用下式计算每组的tgi值:tgi(%)=[1-(ti-t0)/(vi-v0)]×100;ti是给定日的治疗组的平均肿瘤体积,t0是治疗组在分组当天的平均肿瘤体积,vi是在与ti给定日相同给定日的载体对照组的平均肿瘤体积,v0是载体组分组当天的平均肿瘤体积。
统计分析
概括统计在每个时间点每组的肿瘤体积,包括平均值和平均值的标准误差(sem)。
进行单向anova分析,以比较治疗第32天载体治疗组和rad1901治疗组的肿瘤体积。使用graphpadprism分析所有数据,p<0.05被认为具有统计学意义。从图1中可看出,rad1901是有效的(导致约80%的肿瘤生长抑制,p>0.0001),并且两个剂量组具有大致相等的活性。第32天的单个动物的肿瘤大小显示在30mg/kg和60mg/kg动物组中处理的一些动物中rad1901导致肿瘤消退(图2)。
如上所述,前述内容仅旨在说明本发明的各种实施例。上面讨论的具体修改不应解释为对本发明范围的限制。对于本领域技术人员显而易见的是,在不脱离本发明的范围的情况下可以进行各种等同、改变和变型,并且应当理解,这些等同的实施例将包括在本发明中。本发明引用的所有参考文献均通过引用并入本文,就如同在本发明中完全阐述了。
- 还没有人留言评论。精彩留言会获得点赞!