用于治疗癌症、糖尿病和神经病症的新型螺环和环状双-亚苄基蛋白酶体抑制剂的制作方法
背景
泛素-蛋白酶体系统(ups)在许多疾病中改变的细胞稳态、细胞周期进程和信号传导途径中起重要作用。用直接与蛋白酶体蛋白结合的小分子调节ups功能可用于治疗多种疾病,特别是癌症、糖尿病和神经病症。靶向癌细胞的异常代谢是癌症治疗的新兴方法。事实上,尽管早期怀疑用蛋白酶体抑制剂抑制蛋白降解会为癌症治疗提供足够的治疗指数,但是在过去十年中靶向20s蛋白酶体的催化功能的三种蛋白酶体抑制剂被fda批准用于治疗多发性骨髓瘤和套细胞淋巴瘤。然而,它们对实体瘤有限的功效、毒性以及难治性多发性骨髓瘤的出现促使人们寻找具有独特和互补作用机制的替代蛋白酶体抑制剂。
概述
本文提供了螺环和环状双-亚苄基(bis-benzylidine)小分子(upi,ii和iii,以下称up化合物),一种新型的蛋白酶体抑制剂,它通过泛素受体adrm1/rpn13或蛋白酶体dub酶(usp14、uch37和rpn11)抑制蛋白酶体功能,可用于治疗癌症/糖尿病/神经病症。up化合物与蛋白酶体的19s调节颗粒结合,这触发高分子量聚泛素化蛋白聚集体的快速和有毒累积,反映去泛素化酶活性的抑制和蛋白酶体对底物的识别。
附图简述
图1:up109和up117稳定靶向蛋白酶体的萤火虫荧光素酶报道子。
图2:up109和up117累积聚泛素标记的蛋白。
图3:up109和up117抑制nfκb信号传导。
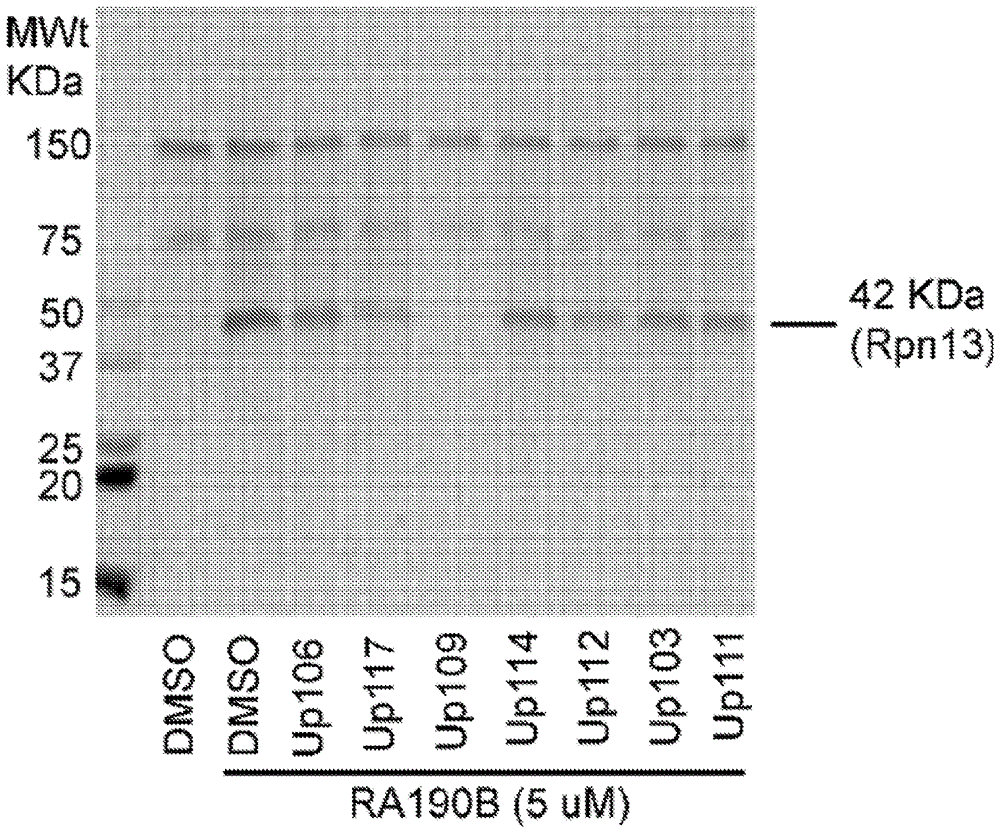
图4:up109和up117与rpn13结合。
图5:用化合物处理的polyub蛋白的累积:(a)用up化合物(1μm)处理4小时并用k48连接的抗-ub抗体进行免疫印迹的hela细胞;(b)用up化合物(1μm)处理12小时并用抗-ub抗体进行免疫印迹的ov2008细胞;(c)用up化合物处理4小时并用抗-ub抗体进行免疫印迹的lncap细胞。
图6:用up109处理的4ubfl报道蛋白的稳定化。
图7:up109与rpn13结合。
图8:(a)在用up109处理12小时的es2细胞中的chop-10定量;(b)通过facs分析用up109和硼替佐米处理12小时的es2细胞的annexin-v染色。
图9:用4ubfl基因将balb/c小鼠电穿孔并用up109处理并且ivis成像定量荧光素酶活性。
图10:up109对抗es2lu肿瘤生长的体内功效。
详细说明
本文提供具有如下所示的式i、ii、iii或iv的结构的化合物
-其中每对a是以下之一:
(i)苯基,任选被1-5个选自以下的取代基取代:r1、or1、nr1r2、s(o)qr1、so2nr1r2、nr1so2r2、c(o)r1、c(o)or1、c(o)nr1r2、nr1c(o)r2、nr1c(o)or2、cf3和ocf3;
(ii)萘基,任选被1-5个选自以下的取代基取代:r1、or1、nr1r2、s(o)qr1、so2nr1r2、nr1so2r2、c(o)r1、c(o)or1、c(o)nr1r2、nr1c(o)r2、nr1c(o)or2、cf3和ocf3;
(iii)5或6元单环杂芳基,具有1-3个选自o、n和s的杂原子,任选被1-3个选自以下的取代基取代:r1、or1、nr1r2、s(o)qr1、so2nr1r2、nr1so2r2、c(o)r1、c(o)or1、c(o)nr1r2、nr1c(o)r2、nr1c(o)or2、cf3和ocf3;和
(iv)8至10元双环杂烯丙基(heteroallylgroup),包含1-3个选自o、n和s的杂原子;并且第二个环使用3至4个碳原子与第一个环稠合,并且所述双环杂芳基任选被1-3个选自以下的取代基取代:r1、or1、nr1r2、s(o)qr1、so2nr1r2、nr1so2r2、c(o)r1、c(o)or1、c(o)nr1r2、nr1c(o)r2、nr1c(o)or2、cf3和ocf3;
(v)属于r1或r2的任何基团,
-其中n代表0-4(0,1,2,3,4)的原子数且可以是碳、氮或氧。在氮的情况下,其可以是nh、nr1或nr2;
-其中x是氢、or1或np,其中p选自r1、c(o)r1、c(o)or1、c(o)nr1r2、s-n(r1)coor1和s-n(r1),其中y选自o、s、nr1和cr1r2,并且其中r1和r2选自氢、硝基、羟基、羧基、氨基、卤素、氰基和c1-c14直链或支链烷基,其任选被1-3个选自以下的取代基取代:ci-c4直链或支链烷基、至多全卤素取代的c1-c14直链或支链烷基、ci-ci4烷氧基、氢、硝基、羟基、羧基、氨基、c1-c14烷基氨基、c-i-c-n二烷基氨基、卤素和氰基;
-其中z选自氢;c1至c14直链、支链或环状烷基;烯基、苯基;苄基、1-5取代的苄基、ci至c3烷基-苯基,其中所述烷基部分任选被卤素、至多全卤素取代;至多全卤素取代的c1至c14直链或支链烷基;-(ch2)q-k,其中k是5或6元单环杂环,含有1至4个选自氧、氮和硫的原子,其为饱和的、部分饱和的或芳族的,或具有1-4个选自o、n和s的杂原子的8至10元双环杂芳基,其中所述烷基部分任选被卤素、至多全卤素取代,并且其中所述变量q是0-4的整数;
-其中b是(i)r1、c(o)r1、c(o)or1、c(o)nr1r2、s-n(r)coor1、s-n(r1)coo(b)、s(b);
并且其中每个r1-r2,除了全卤素取代的c1-c14直链或支链烷基之外,任选被1-3个独立地选自以下的取代基取代:c-1-c14直链或支链烷基、至多全卤素取代的c1-c14直链或支链烷基、c1-c3烷氧基、羟基、羧基、氨基、c1-c3烷基氨基、c1-c6二烷基氨基、卤素、氰基;并且
-其中r3是h、c1-6-烷基、c2-6-烯基;c1-3-烷氧基-c1-6-烷基-;c1-3-烷氧基-c2-6-烯基-;芳基-c0-6-烷基-;杂芳基-c0-6-烷基-;杂环基-c0-6-烷基-;环烷基-c0-6-烷基-;---c1-6-烷基-cooc1-6-烷基;----c2-6-烷基-芳基氧基;c1-6-烷基-杂芳基;c1-6-烷基-杂环基;c1-6-烷基-环烷基;c1-6-烷基-芳基;cor4,其中r4选自:c1-6-烷基;c2-6-烯基;c1-6-烷氧基;c1-3-烷氧基-c1-6-烷基-;c1-3-烷氧基-c2-6-烯基-;芳基-c0-6-烷基-;杂芳基-c0-6-烷基-;杂环基-c0-6-烷基-;环烷基-c0-6-烷基-;---c1-6-烷基-cooc1-6-烷基;nh2;---nhc1-6-烷基;---n(c1-6烷基)2;----c0-6-烷基-芳基氧基。
本文所述的化合物作为dub抑制剂或蛋白酶体受体抑制剂与蛋白酶体蛋白结合。
本文还提供了一种通过给予哺乳动物有效量的本文公开的化合物来抑制哺乳动物中的蛋白酶体的方法。如本文所用,术语“哺乳动物”包括例如人、狗和猫。
本文还提供了一种通过给予哺乳动物治疗有效剂量的如本文所述的化合物来治疗哺乳动物中的疾病的方法。待治疗的疾病可以是例如癌症、糖尿病或神经病症。
本文公开的化合物可以单独给予或与至少一种其他治疗剂或放射联合给予,这可以由医学专业人员确定。
满足本文所述要求的示例性化合物包括以下:
实施例
实施例1:通过up治疗性化合物(up化合物)抑制癌细胞增殖和集落形成
如mtt测定所示,用up化合物处理癌细胞抑制细胞增殖。简言之,将癌细胞与up化合物温育24、48或72小时并使用mtt测定测量细胞活力。表1中列出了化合物的ic50。此外,up109和up117还显著地阻断ov2008和a2780癌细胞中的集落形成,对应于它们的ic50值。两种化合物在skov3及其抗紫杉醇系(skov3-tr)中具有相似的活性,而紫杉醇显示7倍的差异。
表1:所选up治疗性化合物的ic50值(μm)
实施例2
为了测量活细胞中的蛋白酶体功能,我们利用工程化的泛素-萤火虫(4ub-fl)报道子,其中突变体泛素(泛素g76v)基因的四个拷贝与萤火虫荧光素酶(fl)基因的n末端融合。该实验的结果如图1所示,图1揭示了4ub-fl报道蛋白被蛋白酶体快速降解。重要的是,用蛋白酶体抑制剂处理表达4ub-fl基因的293tt细胞导致其稳定化并且荧光素酶活性增加。有趣的是,up109和up117的处理以剂量依赖性方式产生比ra190更大的4ub-fl生物发光的增加。与治疗前相比,up109显示生物发光增加到13倍,而up117和ra190分别增加到11倍和5倍。
实施例3
聚泛素化蛋白的累积是蛋白酶体抑制的一般现象。我们通过抗-k48-连接的泛素免疫印迹分析考察了这些化合物对hela细胞中聚泛素化蛋白水平的影响。该实验的结果如图2所示,揭示了使用up109或up117处理hela细胞(4小时)与ra190类似地急剧地增加k48-连接的聚泛素化蛋白的水平。然而,暴露于化合物后观察到的累积的k48聚泛素化蛋白显示出比在硼替佐米处理过的细胞中观察到的更高的分子量并且发生得更快。这些结果表明,up109和up117在宫颈癌细胞中表现的毒性与高分子量聚泛素化蛋白的先前积累有关并且通过与硼替佐米不同的机制发生。
实施例4
nfκb在许多癌症包括高等级宫颈上皮内瘤变(cin)和宫颈癌中组成性激活。携带具有人tnf-α的nfκb报道构建体的293细胞的刺激导致报道子活性增加,并且在用tnf-α刺激后,up109、up117和ra190产生显著的剂量依赖性的报道子活性降低(图3)。在tnf-α存在下用up109和up117处理后在hela细胞中观察到iκb-a的稳定化。
实施例5
为了鉴定细胞靶标,使用ra190b探针进行竞争测定。早些时候我们发现生物素化的ra190(ra190b)与rpn13共价结合。我们使用ra190b作为探针来确定up化合物与rpn13的结合。用up109或up117预处理hela细胞裂解物,随后用ra190b处理。裂解物在还原条件下变性,蛋白在凝胶上分离并用hrpsreptavidin进行探测。图4显示,在up109和up117存在下42kda蛋白的ra190b标记的消失表明与ra190b竞争结合rpn13。
实施例6:在体外up化合物积累的聚泛素化蛋白
聚泛素化蛋白的累积是蛋白酶体抑制的一般现象。我们通过抗-泛素免疫印迹分析考察了这些化合物对聚泛素化蛋白癌细胞水平的影响。将用up化合物处理癌细胞系(hela,ov2008和lncap)指定的时间并细胞裂解并进行westernblot分析。用抗-泛素抗体的免疫印迹显示处理过的细胞中聚泛素化蛋白的累积(图5)。用k48-连接的抗-ub抗体探测hela细胞,该抗体通过k-48连接识别用泛素标记的蛋白。与底物蛋白连接的k48-连接的聚泛素链通常用作通过26s蛋白酶体靶向和破坏底物的识别序列。用抗-ub抗体探测ov2008和lcap细胞。
实施例7:up109稳定的蛋白酶体依赖性报道蛋白
为了测量活细胞中的蛋白酶体功能,我们利用工程化的泛素-萤火虫(4ub-fl)报道子,其中突变体泛素(泛素g76v)基因的四个拷贝与萤火虫荧光素酶(fl)基因的n末端融合。4ub-fl报道蛋白被蛋白酶体快速降解(图6)。重要的是,用up109处理表达4ub-fl基因的293tt细胞导致其稳定化并且荧光素酶活性增加。up109的处理以剂量依赖性方式在4ub-fl生物发光方面产生比更大的增加。
实施例8:up109和up117与rpn13结合
为了鉴定细胞靶标,使用ra190b探针进行竞争测定。早些时候我们显示生物素化的ra190(ra190b)与rpn13共价结合。我们使用ra190b作为探针来确定up化合物与rpn13的结合。用up化合物(25μm)预处理ov2008细胞裂解物,随后用ra190b(5μm)处理。裂解物在还原条件下变性,蛋白在凝胶上分离并用hrpstreptavidin探测。在up109和up117存在下rpn13蛋白的ra190b标记的消失表明与ra190b竞争结合rpn13(图7)。
实施例9:up109升高的er应激和凋亡
在蛋白酶体功能的抑制下未折叠蛋白的累积迅速诱导内质网(er)应激。er应激触发一系列进化上保守的信号转导事件,这构成了未折叠蛋白应答(upr)。upr试图通过消除er中积累的未折叠蛋白来恢复蛋白稳态;然而,如果不能恢复蛋白稳态,则会触发细胞凋亡。在upr-诱导的程序性细胞死亡开始时,c/ebp同源蛋白(chop)升高。es2细胞的up109处理快速上调chop-10mrna表达(图8a)。annexin-v阳性细胞指示通过up109处理的细胞凋亡的升高(图8b)。
实施例10:体内up109稳定的4ubfl:
为了测试体内up109的蛋白酶体抑制,通过电穿孔用4ubfl报道dna构建体转导活balb/c小鼠的肌细胞。在i.p.注射荧光素后,使用ivis成像仪将转染的肌肉组织中的荧光素酶的酶活性可视化为生物荧光。在4ubfldna电穿孔后两天,对小鼠进行成像并记录基线荧光。小鼠的对照组(n=5)只用溶媒进行i.p.处理,另一组(n=5)用up109(40mg/kg)i.p.处理。在处理后4小时、24小时和48小时,再次对小鼠进行成像并对荧光进行定量(图9)。该结果表明(1)up109具有良好的实体组织可及性;(2)up109可以有效地每隔一天给予一次。
实施例11:剂量限制性毒性研究
为了鉴定诱导临床效果并以可接受的毒性操作的最佳剂量,已经用up109对雌性balb/c品系小鼠进行了一组实验。各组小鼠(n=3)i.p.注射增加的单剂量的up109(3、10、20、40和100mg/kg),终点评估包括临床观察和体重。未发现与up109相关的临床上明显的不良反应迹象。另一个实验通过每隔一天重复i.p.给予up109(40mg/kg,n=5)持续两周完成。没有发现可观察到的毒性/体重减轻。
实施例12:up109对es2卵巢肿瘤生长的体内功效
为了测试up109治疗人卵巢癌es2异种移植模型的功效,将表达荧光素酶的es2细胞(es2-lu)接种到裸雌性小鼠的腹膜腔中(即原位)。接种后两天,对小鼠进行基础发光活性成像,然后随机分成两组(n=10)。第一组用溶媒治疗且第二组隔天用up109(10mg/kg)治疗持续两周。在治疗的第一周和第二周后对其荧光素酶活性进行成像。如图6所示,与溶媒相比,up109显著降低了肿瘤负荷,并且没有体重减轻和任何可观察到的副作用。溶媒组小鼠中的肿瘤负荷过量并在治疗结束时被处死(图10)。
实施例13:up化合物通用合成方案
反应条件:(a)取代的醛,naoh,乙醇;(b)4mhcl/二噁烷;(c)酰氯,dcm,三乙胺或酸,hobt,hbtu,dmf,dipea;(d)烷基溴,丙酮,k2co3;(e)磺酰氯,dcm,三乙胺。r=芳环上的不同取代基。
- 还没有人留言评论。精彩留言会获得点赞!