软骨修复用支架及其制备方法与流程
本发明涉及生物医用器材领域,具体涉及一种软骨修复用支架及其制备方法。
背景技术:
关节软骨病变是一种常见的临床疾病,其主要病因包括由创伤、炎症、关节活动压力造成的软骨退化和病变,一旦发生病变,损伤就不断累积最终引发关节疾病。严重时可导致骨关节炎,又称退化性关节炎,是一种关节软骨或关节下骨头损伤的关节炎。其主要发生在中、老年族群,也常见于体重过重、长短腿、因工作而使关节长期承受高度压力的族群;近年来,随着运动风气盛行,骨关节炎逐渐年轻化。其常见症状是关节疼痛或僵硬,严重时会导致四肢无力或麻木,非常影响日常生活和工作,已经成为世界性重要研发课题之一。
软骨具有多孔结构,且软骨内部缺少血管、神经及未分化细胞,因而自身修复能力有限,在磨损后基本不能自我修复。目前,解决关节软骨病变的传统的临床手术方法主要有骨髓刺激法、软骨镶嵌和人工关节置换术等。然而,这些手术方法普遍存在术后易复发、病情反复等问题。
近年来,软骨细胞移植、微骨折技术、人工软骨和组织工程化软骨修复技术得到了快速的发展,其对治疗关节软骨病变具有更好的效果,使用上述技术的过程中需要使用支架,现有的支架不具有同时修复软骨损伤和重建软骨润滑功能的作用。
例如,中国专利文献cn108159496a公开了一种双因子程序释放的仿生取向软骨支架,包括由胶原、壳聚糖、透明质酸、负载kgn的plga微球制成的表面层、以及由胶原、壳聚糖、负载tgf-β1的pll-hs纳米粒制成的移行层,再以丝素蛋白为粘合剂将两者粘合,制得具有上下双层结构的仿生取向软骨支架。该支架的主要作用在于修复骨关节炎软骨缺损,虽然其中的透明质酸具有润滑作用,但是透明质酸为可降解材料,在使用后会逐渐降解,损失其润滑功能,不具有长期维持软骨润滑功能的作用。
技术实现要素:
因此,本发明要解决的技术问题在于克服现有技术中的软骨修复用支架不具有同时修复软骨损伤和重建软骨润滑功能的作用,并使其润滑作用能长期维持的缺陷,从而提供一种软骨修复用支架及其制备方法。
为解决上述技术问题,一方面,本发明提供一种软骨修复用支架,包括:
润滑层,采用不可降解材料制成,所述润滑层具有润滑作用;
表面层,包括具有多孔结构的多孔层,所述表面层采用具有生物相容性的可降解材料制成;或者,所述表面层采用具有生物稳定性的不可降解材料制成;
结合层,连接在所述润滑层和多孔层之间,以使所述润滑层通过所述结合层与所述多孔层形成紧固结构。
可选地,所述表面层还包括阻隔层,所述多孔层包括第一多孔层,所述阻隔层连接在所述第一多孔层和结合层之间,用于隔离所述第一多孔层和结合层。
可选地,所述多孔层还包括第二多孔层,所述第二多孔层连接在所述阻隔层与所述结合层之间。
可选地,所述表面层的厚度、结合层的厚度以及润滑层的厚度与所述支架的总厚度的比例分别为:60%-80%、0.1%-10%以及1%-35%。
可选地,制备所述润滑层的不可降解材料的摩擦系数为0.05-1。
可选地,制备所述润滑层的不可降解材料的摩擦系数为0.05-0.3。
可选地,所述润滑层采用如下材料制成:高分子油凝胶或含有润滑液的多孔材料的一种或几种。
可选地,所述含有润滑液的多孔材料的孔径为0.1-1μm,且孔隙率为25%-95%,所述多孔材料中含有润滑液的质量分数为20%-80%。
可选地,所述润滑液的粘度为5-10000cst。
可选地,所述表面层采用可3d打印的生物医用高分子材料制成。
可选地,所述多孔层的孔隙直径为10-500μm。
可选地,采用可降解材料制成的所述多孔层的孔隙率为20%-90%,采用不可降解材料制成的所述多孔层的孔隙率不低于90%。
可选地,所述多孔结构为尺寸均匀的规则通孔;或者,
所述多孔结构为海绵结构。
可选地,所述结合层采用如下材料制成:高分子油凝胶、含有润滑液的多孔材料、可3d打印的生物医用高分子材料或生物胶黏剂中的一种或几种。
可选地,所述高分子油凝胶为聚二甲基硅氧烷油凝胶;
所述含有润滑液的多孔材料为含有全氟润滑油的聚四氟乙烯多孔膜;
所述可3d打印的生物医用高分子材料为:聚乳酸、聚己内酯、聚乙烯醇或热塑性聚氨酯中的一种或几种;
所述生物胶黏剂为α-氰基丙烯酸正丁酯。
可选地,所述支架的杨氏模量为1-100mpa,抗压强度不低于1mpa。
另一方面,本发明提供一种软骨修复用支架的制备方法,包括如下步骤:
将具有生物相容性的可降解材料通过3d打印成型成多孔层;或者,将具有生物稳定性的不可降解材料通过3d打印成型成多孔层;
将具有润滑作用的不可降解材料制成润滑层;
将结合层设置在多孔层和润滑层之间成型为支架。
再一方面,本发明提供一种软骨修复用支架的制备方法,包括如下步骤:
将具有生物相容性的可降解材料通过3d打印成型成多孔层和阻隔层;或者,将具有生物稳定性的不可降解材料通过3d打印成型成多孔层和阻隔层;
将具有润滑作用的不可降解材料制成润滑层基材;
将结合层设置在阻隔层和润滑层基材之间成型为支架初样,再对所述润滑层基材进行润滑性处理后成型为支架。
可选地,对所述润滑层基材进行润滑性处理的方法包括:
溶胀润滑液:将所述润滑层基材放置在润滑液内,将润滑层基材溶胀至溶胀平衡;或者,
灌注润滑液:将润滑液灌注至所述润滑层基材内,静置,真空脱泡,固化成型。
可选地,所述3d打印成型的方法包括:熔融沉积法、选择性激光烧结法或激光光固化法中的一种或几种。
可选地,所述结合层的制备方法包括:将所述表面层与所述润滑层或润滑层基材通过物理嵌合形成结合层;或者,所述表面层与所述润滑层或润滑层基材通过生物胶黏剂粘接固化成型为结合层。
可选地,还包括对制备所述润滑层、结合层和表面层的材料分别进行表面预处理。
本发明技术方案,具有如下优点:
1.本发明提供的支架,包括润滑层、表面层和结合层,表面层包括具有多孔结构的多孔层,结合层连接在润滑层和多孔层之间,使得表面层通过结合层可与润滑层形成紧固结构;将支架植入关节处后,表面层具有多孔结构的多孔层可临时替代自然软骨,为骨细胞、血管、神经和软骨细胞提供生长空间,以及提供氧气、营养物和代谢物的传输通道,同时能为关节处的新生组织提供支撑作用,与植入部位(关节处)的自然软骨的机械性能匹配,使新生组织能良好的生长;对于细胞增殖能力良好的患者,表面层采用生物相容性的可降解材料制成,随着细胞的增殖,可降解材料会缓慢降解,最终被软骨细胞完全替换;对于细胞增值能力有限的患者,表面层采用具有生物稳定性的不可降解材料制成,表面层的生物稳定性好,即表面层在关节处的耐生物老化性能好,为细胞提供足够的增殖时间,使软骨逐渐修复。
润滑层采用对软骨具有润滑作用的不可降解材料制成,进而使得润滑层能长时间维持关节处的润滑性,即,润滑层相当于模拟了软骨的润滑结构,使支架能长期具有润滑作用,进而保证了修复后的软骨长期具有润滑功能,减少修复后的软骨的磨损,保护关节健康。进一步地,通过结合层将表面层和润滑层结合在一起,使得支架具有修复软骨损伤的作用,同时具有重建软骨润滑功能的作用,并能使其润滑功能长期维持。
2.本发明提供的支架,表面层还包括阻隔层,当润滑层内部含有液体时,阻隔层可阻止润滑层中的液体进入第一多孔层中,确保细胞能粘附在第一多孔层的多孔结构上,利于细胞繁殖。
3.本发明提供的支架,表面层的厚度与支架的总厚度的比例为60%-80%,结合层的厚度与支架的总厚度的比例为0.1%-10%,润滑层的厚度与支架的总厚度的比例为1%-35%,这样可形成稳定的支架结构,为细胞提供稳定的成长空间。
4.本发明提供的支架,润滑层采用高分子油凝胶或含有润滑液的多孔材料制成,当润滑层采用高分子油凝胶制成时,润滑层的制备过程中不需要注入液体,表面层可以只具有多孔层,或者表面层具多孔层和阻隔层,当润滑层采用润滑液的多孔材料制成时,润滑层的制备过程需要注入液体,表面层则为多孔层和阻隔层。
5.本发明提供的支架,含有润滑液的多孔材料的孔径为0.1-1μm,孔隙率为25%-95%,这样可为润滑液提供合适的容纳空间,利于细胞繁殖;多孔材料中含有润滑液的质量分数为20%-80%,可确保润滑层的润滑作用,使润滑层的润滑效果更佳。
6.本发明提供的支架,制备润滑层的不可降解材料的摩擦系数为0.05-0.3,使润滑层对软骨具有更好的润滑作用,摩擦系数越低,润滑层对软骨的润滑作用越好。
7.本发明提供的支架,润滑液的粘度为5-10000cst,润滑液的粘度范围选择宽泛,可根据润滑层材料性质筛选适当粘度的润滑液,保证润滑液进入润滑层材料后稳定存在,摩擦系数低、且不会大幅度降低润滑层机械性能。
8.本发明提供的支架,表面层采用可3d打印的生物医用高分子材料制成,这样表面层可通过3d打印成型的方式制成,3d打印成型方法操作简便便捷,可根据病灶部位(关节处)的需求设计3d模型,打印成特定形状的支架,提高支架与关节处的匹配度,建造更适合细胞成长的空间。
9.本发明提供的支架,多孔层的孔隙直径为10-500μm,这样有利于提高多孔层的机械性能,提升细胞的繁殖环境,更有利于细胞的增值。
10.本发明提供的支架,采用可降解材料制成的多孔层的孔隙率为20%-90%,因为可降解材料最终会降解掉,使得多孔层的细胞成长空间可以比较少,采用不可降解材料制成的多孔层的孔隙率不低于90%,因为不可降解材料最终不会被降解,需要提供足够的成长空间给细胞繁殖以形成稳固的软骨结构。
11.本发明提供的支架,多孔结构为尺寸均匀的规则通孔,因为规则通孔具有更好的力学性能,其具有更好的支撑作用,使软骨细胞成长的空间结构更稳固。多孔结构为大孔与微孔并存的海绵结构,使软骨细胞在多孔结构内的吸附性能更好,能促进软骨细胞的生长。
12.本发明提供的支架,结合层采用高分子油凝胶、含有润滑液的多孔材料、可3d打印的生物医用高分子材料或生物胶黏剂中的一种或几种材料制成,这样可以提高结合层与润滑层和表面层的连接性能,使表面层、结合层和润滑层能连接更牢固。
13.本发明提供的支架,表面层采用聚乳酸、聚己内酯、聚乙烯醇或热塑性聚氨酯中的一种或几种支撑,聚乳酸和聚己内酯的降解速率和由于降解导致的机械性能下降速率与软骨组织新生速率相适应,从而使支架的表面层在使用过程(服役过程)保持有效性。
14.本发明提供的支架,支架的杨氏模量为1-100mpa,抗压强度不低于1mpa,这样可使支架具有更好的支撑作用,同时能与植入部位(关节处)的自然软骨的机械性能更匹配,更有利于细胞生长。
15.本发明提供的支架的制备方法,将具有生物相容性的可降解材料通过3d打印成型成多孔层,或者,将具有生物稳定性的不可降解材料通过3d打印成型成多孔层,提供软骨细胞生长增殖空间,使得多孔层具有修复软骨的功能,同时,3d打印成型方法操作简便便捷,可根据病灶部位(关节处)的需求设计3d模型,打印成特定形状的多孔层,提高多孔层与关节处的匹配度,建造更适合软骨细胞成长的空间。将具有润滑作用的不可降解材料制成润滑层,使得润滑层具有长期的润滑作用,能使关节处长期处于润滑状态,通过结合层将润滑层和多孔层固定,使之形成稳定的支架结构,使支架能更好地适应关节处的环境,同时,支架具有修复软骨的作用以及重建软骨润滑功能的作用,并能长期维持其润滑功能。
16.本发明提供的支架的制备方法,将具有生物相容性的可降解材料通过3d打印成型成多孔层和阻隔层,或者,将具有生物稳定性的不可降解材料通过3d打印成型成多孔层和阻隔层,使得多孔层具有修复软骨的功能,同时,3d打印成型方法操作简便便捷,可根据病灶部位(关节处)的需求设计3d模型,打印成特定形状的多孔层,提高多孔层与关节处的匹配度,建造更适合软骨细胞成长的空间。
将具有润滑作用的不可降解材料制成润滑层基材,通过结合层将表面层与润滑层固定,将结合层设置在阻隔层与润滑层之间,防止对润滑层进行润滑性处理时,润滑层的润滑液通过结合层流向多孔层,从而确保细胞能粘附在多孔结构上,利于细胞繁殖;对润滑层基材进行润滑性处理后,使得润滑层具有长期的润滑作用,能使关节处长期处于润滑状态,即,支架具有修复软骨的作用以及重建软骨润滑功能的作用,并能长期维持其润滑功能。
17.本发明提供的支架的制备方法,将表面层与润滑层或润滑层基材通过物理嵌合形成结合层,这样在制备表面层与润滑层或润滑层基材的过程中同时形成了结合层,减少了支架的制备时间,简化了支架的制备步骤。将表面层与润滑层或润滑层基材通过生物胶黏剂粘接固化成型为结合层,这样可采用现成的表面层和润滑层或润滑层基材制成支架,表面层、润滑层或润滑层基材可以外部采购或自己制备,提高了其选择性,使支架的制备更方便快捷。
18.本发明提供的支架的制备方法,对制备润滑层、结合层和表面层的材料进行表面预处理,这样可使结合层与润滑层和表面层之间形成良好的连接,形成稳定的支架。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
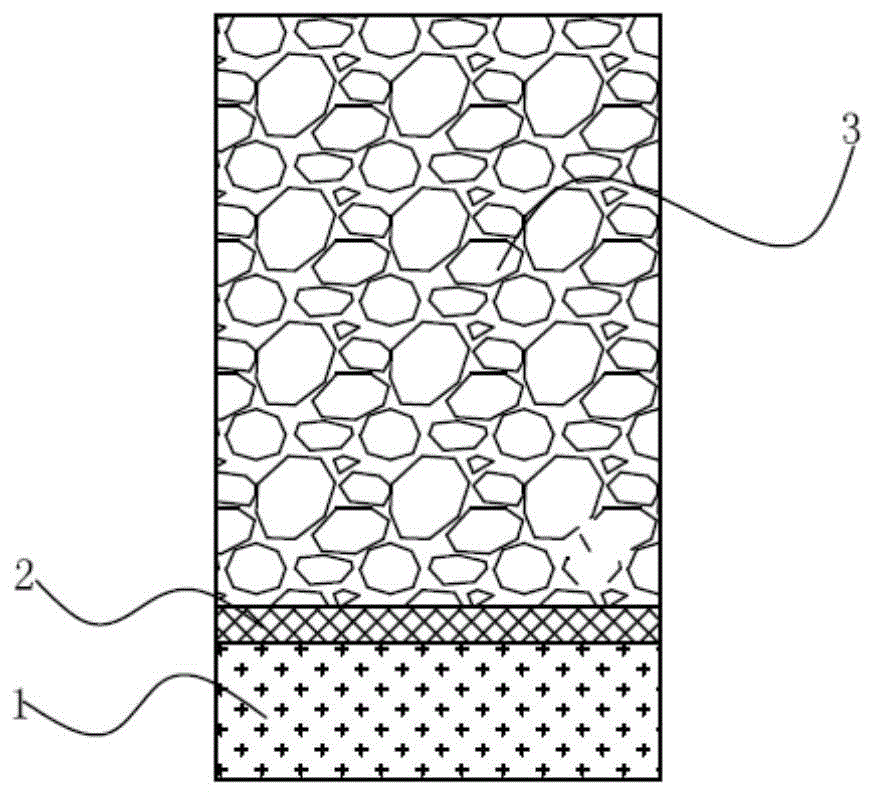
图1是本发明具体实施方式中的提供的支架的第一种实现结构;
图2是本发明具体实施方式中的提供的支架的第二种实现结构;
图3是本发明具体实施方式中的提供的支架的第三种实现结构。
附图标记:
1、润滑层;2、结合层;3、表面层;31、第一多孔层;32、第二多孔层;33、阻隔层。
具体实施方式
提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
一种软骨修复用支架,包括润滑层1、结合层2和表面层3,表面层3包括具有多孔结构的多孔层和阻隔层33,阻隔层33为实心结构,当多孔层包括第一多孔层31时,阻隔层33连接在第一多孔层31和结合层2之间,阻隔层33用于隔离第一多孔层31和结合层2,当多孔层包括第一多孔层31和第二多孔层32时,阻隔层33连接在第一多孔层31和第二多孔层32之间,第二多孔层32连接在阻隔层33与结合层2之间,阻隔层33用于隔离所述阻隔层33与所述第一多孔层31。
表面层3的厚度与支架的总厚度的比例为60%-80%,可以理解的是,当表面层3只包括多孔层时,是指多孔层的厚度与支架的总厚度的比例为60%-80%;当表面层3包括多孔层和阻隔层33时,是指多孔层和阻隔层33的总厚度与支架的总厚度的比例为60%-80%。结合层2的厚度与支架的总厚度的比例为0.1%-10%,润滑层1的厚度与支架的总厚度的比例为1%-35%。
润滑层1采用摩擦系数为0.05-1的不可降解材料制成,使得润滑层1具有很好的润滑作用,且能长期保持其润滑功能。
润滑层1采用摩擦系数为0.05-0.3的不可降解材料制成,该不可降解材料为高分子油凝胶或含有润滑液的多孔材料中的一种或多种,高分子油凝胶为聚二甲基硅氧烷(pdms)油凝胶、或者其他具有润滑作用的不可降解的高分子油凝胶。
含有润滑液的多孔材料的孔径为0.1-1μm,孔隙率为25%-95%,所述多孔材料中含有润滑液的质量分数为20%-80%。润滑液为低挥发性和低表面能的液体,这样润滑液不容易挥发同时具有很好的润滑作用,所述润滑液的粘度为5-10000cst。含有润滑液的多孔材料可以为含有全氟润滑油的聚四氟乙烯(ptfe)多孔膜、或者其他符合上述要求的含有润滑液的多孔材料。
表面层3采用可3d打印的生物医用高分子材料制成,可3d打印的生物医用高分子材料为:聚乳酸(pla)、聚己内酯(pcl)、聚乙烯醇(pva)或热塑性聚氨酯(tpu)中的一种或几种,这几种物质具有更好的生物相容性或生物稳定性,利于细胞生长。
可以理解的是,聚乙烯醇(pva)包括可降解的聚乙烯醇(pva),也包括不可降解的聚乙烯醇(pva);热塑性聚氨酯(tpu)包括可降解的热塑性聚氨酯(tpu),也包括不可降解的热塑性聚氨酯(tpu)。
多孔层的孔隙直径为10-500μm,多孔层的多孔结构为尺寸均匀的规则通孔;或者多孔层的多孔结构为同时具有大孔与微孔的海绵结构。可以理解的是,此处的大孔和微孔并不用于限定孔径的范围,只是为了说明多孔结构是由多种孔径的孔组成的海绵结构。采用可降解材料制成的多孔层的孔隙率为20%-90%,采用不可降解材料制成的多孔层的孔隙率不低于90%。
制备表面层3的材料表面加入具有生物相容性的活性官能团或者加入包含上述活性官能团的活性分子,可增加细胞的活性能力,利于细胞黏附、生长和增殖。活性官能团可以为羟基、羧基和氨基中的一种或多种。包含上述活性官能团内的活性分子为壳聚糖、氨基酸、小分子多肽或蛋白质中的一种或多种。
阻隔层33采用高分子油凝胶、含有润滑液的多孔材料、可3d打印的生物医用高分子材料或生物胶黏剂中的一种或几种材料制成。生物胶黏剂可以为α-氰基丙烯酸正丁酯等,或者其他具有生物胶黏作用的制剂。
支架的杨氏模量为1-100mpa,抗压强度不低于1mpa。
一种软骨修复用支架的制备方法,在可用于3d打印的生物医用高分子材料的表面引入活性官能团或含有上述活性官能团的活性分子,再对制备表面层3、润滑层1和结合层2的材料表面进行预处理,预处理的方法包括表面处理或化学改性等,表面处理的方法包括:表面氧等离子体处理、高强度紫外辐照或高能射线辐照等,化学改性的方法包括:表面接枝、表面氧化或表面浸涂等。
然后将生物医用高分子材料通过熔融沉积法(fdm)、选择性激光烧结法(sls)或激光光固化法(sla)中的一种方法制成表面层3,表面层3可以为只有多孔层,或者为多孔层和阻隔层33。表面层3具有阻隔层33时,多孔层包括第一多孔层31,阻隔层33连接在第一多孔层31和结合层2之间,阻隔层33用于隔离第一多孔层31和结合层2;或者,多孔层包括第一多孔层31和第二多孔层32,阻隔层33连接在第一多孔层31和第二多孔层32之间,第二多孔层32连接在阻隔层33与结合层2之间,阻隔层33用于隔离所述阻隔层33与所述第一多孔层31。
当表面层3只有多孔层时,可将高分子油凝胶制成润滑层1,然后通过高分子油凝胶、可3d打印的生物医用高分子材料或生物胶黏剂中的一种使多孔层和润滑层1固定成型为支架。
当表面层3为多孔层和阻隔层33时,可将高分子油凝胶制成润滑层1,然后通过高分子油凝胶、可3d打印的生物医用高分子材料或生物胶黏剂中的一种或多种使多孔层和润滑层1固定成型为支架。或者,将多孔材料制成润滑层1基材,然后通过高分子油凝胶、可3d打印的生物医用高分子材料或生物胶黏剂中的一种或多种使多孔层和润滑层1基材固定成型,最后将润滑层1基材放置在盛放有润滑液的烧杯中,直至润滑层1基材溶胀平衡,制成支架。
作为可替代的实施方式,可将润滑液灌注至润滑层1基材内,然后静置成型为支架。润滑层1基材进行润滑性处理对应的处理方法根据制备润滑层1基材的材料的不同而不同。例如,当润滑层1采用油凝胶型材料制成时,将润滑层1基材放置在盛放有润滑液的烧杯中,直至润滑层1基材溶胀平衡;当润滑层1采用多孔膜型材料制成时,将润滑液灌注至润滑层1基材内,然后静置。
此处的油凝胶型材料是指制备油凝胶的材料还没有吸入油之前的材料。例如,油凝胶型材料为pdms。多孔膜型材料为还没有灌注润滑液的多孔膜。例如,多孔膜型材料可以为ptfe多孔膜。
结合层2的制备方法包括:将表面层3与润滑层1或润滑层1基材通过物理嵌合形成结合层2;或者,表面层3与润滑层1或润滑层1基材通过生物胶黏剂粘接固化成型为结合层2;或者,将聚乳酸、聚己内酯、聚乙烯醇或热塑性聚氨酯中的一种或几种熔融后涂覆在表面层3与润滑层1或润滑层1基材之间固化成型为结合层2。此时,聚乳酸、聚己内酯、聚乙烯醇或热塑性聚氨酯中的一种或几种熔融后相当于具有胶黏剂的作用。
实施例1
pcl-pdms复合支架(pcl可降解)
将pcl放入3d打印机的样品台上,调整底板温度为30℃,喷头温度为200℃,打印总厚度为6.5mm的第一多孔层和阻隔层,其中阻隔层的厚度为0.2mm,第一多孔层中的孔径为10μm,孔隙率为89%;
将道康宁184a组分和道康宁184b组分按照质量比(10:1)混合,搅拌均匀成pdms前驱体,在模具中浇筑1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后,将模具和pdms前驱体一起放至50℃的烘箱中固化1h,得到接近完全固化的pdms润滑层基材。
在模具中继续浇灌1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后形成结合层,将阻隔层浸入结合层中,在50℃的烘箱中固化成型成支架初样;
在烧杯中倒入粘度为10cst的硅油,将支架初样的pdms润滑层基材浸没在硅油中,待pdms润滑层基材溶胀平衡后,取出支架初样静置30min,擦去pdms润滑层基材上多余的硅油后得到pcl-pdms复合支架。
实施例2
pla-pdms复合支架(pla可降解)
将pla放入3d打印机的样品台上,调整底板温度为60℃,喷头温度为200℃,打印总厚度为6.0mm的第一多孔层、阻隔层和第二多孔层,其中阻隔层的厚度为0.3mm,第二多孔层的厚度为1.2mm,第一多孔层中的孔径为500μm,孔隙率为75%,第二多孔层中的孔径为400μm,孔隙率为75%;
将道康宁184a组分和b组分按照质量比(10:1)混合,搅拌均匀制成pdms前驱体,在模具中浇筑1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后,将模具和pdms前驱体一起放至60℃的烘箱中固化1h,得到接近完全固化的pdms润滑层基材。
将0.03mmα-氰基丙烯酸正丁酯涂覆在第二多孔层上,将pdms润滑层基材粘附在α-氰基丙烯酸正丁酯,固化成型为支架初样;
在烧杯中倒入粘度为10000cst的硅油,将支架初样的pdms润滑层基材浸没在硅油中,待pdms润滑层基材溶胀平衡后,取出支架初样静置45min,擦去pdms润滑层基材上多余的硅油后得到pla-pdms复合支架。
实施例3
tpu-pdms复合支架(tpu不可降解)
将tpu放入3d打印机的样品台上,调整底板温度为60℃,喷头温度为200℃,打印总厚度为6.0mm的第一多孔层和阻隔层,其中阻隔层的厚度为0.1mm,第一多孔层中的孔径为100μm,孔隙率为90%;
将道康宁184a组分和道康宁184b组分按照质量比(10:1)混合,搅拌均匀制成pdms前驱体,在模具中浇筑1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后,将模具和pdms前驱体一起放至60℃的烘箱中固化1h,得到接近完全固化的pdms润滑层基材。
在模具中继续浇灌0.8mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后形成结合层,将阻隔层浸入结合层中,在60℃的烘箱中固化成型成支架初样;
在烧杯中倒入粘度为500cst的硅油,将支架初样的pdms润滑层基材浸没在硅油中,待pdms润滑层基材溶胀平衡后,取出支架初样静置1h,擦去pdms润滑层基材上多余的硅油后得到tpu-pdms复合支架。
实施例4
pla-ptfe复合支架(pla可降解)
将孔径为0.45μm,孔隙率为85%,厚度为200μm的ptfe多孔膜固定在3d打印机样品台上,将pla线材装载入3d打印机的喷头中,调整底板温度为60℃,喷头温度为200℃,调节样品台的高度和pla的打印位置,至使打印的pla第一多孔层嵌入ptfe多孔膜中,继续打印总厚度为5.5mm的pla第一多孔层后得到支架初样,pla第一多孔层中的孔径为200μm,孔隙率为52%;
在烧杯中倒入粘度为5000cst的硅油,将支架初样的ptfe润滑层基材浸没在硅油中,待ptfe润滑层基材溶胀平衡后,取出支架初样静置55min,擦去ptfe润滑层基材上多余的硅油后得到pla-ptfe复合支架。
实施例5
pva-ptfe复合支架(pva可降解)
上层孔径为0.45μm,下层孔径为0.22μm,孔隙率为80%,厚度为200μm的ptfe多孔膜固定在3d打印机样品台(即底板)上,将pva线材装载入3d打印机的喷嘴中,调整底板温度为60℃,喷头温度为200℃,调节样品台的高度和pva的打印位置,将pva打印在ptfe上,使pva第一多孔层部分嵌入ptfe多孔膜中,继续打印总厚度为5.5mm的pva第一多孔层后得到支架初样,pva第一多孔层中的孔径为300μm,孔隙率为70%。
在烧杯中倒入粘度为3000cst的硅油,将支架初样的ptfe润滑层基材浸没在硅油中,待ptfe润滑层基材溶胀平衡后,取出支架初样静置38min,擦去ptfe润滑层基材上多余的硅油后得到pva-ptfe复合支架。
实施例6
pla-pdms复合支架(pla可降解)
将pla放入3d打印机的样品台上,调整底板温度为30℃,喷头温度为200℃,打印总厚度为6.5mm的第一多孔层和阻隔层,其中阻隔层的厚度为0.2mm,第一多孔层中的孔径为80μm,孔隙率为65%;
将道康宁184a组分和道康宁184b组分按照质量比(10:1)混合,搅拌均匀制成pdms前驱体,在模具中浇筑1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后,将模具和pdms前驱体一起放至80℃的烘箱中固化1h,得到接近完全固化的pdms润滑层基材;
在模具中继续浇灌1mm厚的pdms前驱体,静置10min,抽真空脱泡至pdms前驱体中无泡沫后形成结合层,将阻隔层浸入结合层中,在50℃的烘箱中固化成型成pla-pdms复合支架。
实施例7
pla-ptfe复合支架(pla可降解)
将孔径为0.45μm,孔隙率为85%,厚度为200μm的ptfe多孔膜固定在3d打印机的样品台上,将pla线材装载到3d打印机的喷头中,调整底板温度为60℃,喷头温度为200℃,调整pla的打印位置,使pla打印在ptfe多孔膜上,以确保3d打印机打出的pla第一多孔层能部分嵌入ptfe多孔膜的孔中,形成物理嵌合,pla第一多孔层打印总厚度为5.5mm,孔径为200μm,孔隙率为52%,打印完成后得到pla-ptfe复合支架。
测试方法
采用实施例1-7中制备的支架进行杨氏模量测试、抗压强度测试、弹性压缩应变测试、摩擦系数测试,测试结果见表1。
杨氏模量测试、抗压强度测试和弹性压缩应变测试均在万能试验机的压缩模式下进行测试,选择不同的测试模式即可,具体的测试方法为:
将待测支架裁成直径为10mm的圆柱体,并放置于英斯特朗万能试验机上在压缩模式下测试,压缩最大载荷为950n,压缩速率为2mm/min。
摩擦系数测试
将待测支架的润滑层制备成76*26*1mm的长方体,并放置在安东帕摩擦磨损试验机上进行测试,对磨副为6.35mm的陶瓷球,摩擦载荷为10n,将待测支架的润滑层与对磨副直接摩擦,待测支架单次往复行程为6mm、往复频率为2hz,单次实验时间为25min。
表1
通过测试结果可知,该软骨修复用支架用具很好的结构稳定性,且其摩擦系数低,具有很好的润滑作用。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!