恩替卡韦在制备治疗感染性疾病引起炎症风暴的药物中的应用的制作方法
本发明属于医药技术领域,具体地说,涉及一种恩替卡韦在制备治疗感染性疾病引起炎症风暴的药物中的应用。
背景技术:
感染性疾病是指病人由于被病毒、衣原体、支原体、细菌或寄生虫等各种病原体感染而引起的疾病。随着感染的不断加剧,免疫系统大量产生细胞因子,这其中的促炎性细胞因子又可趋化更多免疫细胞形成正反馈循环,引起“炎症风暴”,不分敌我地进行攻击,对人体免疫系统以及肝脏、肾脏、心脏等重要脏器造成伤害。“炎症风暴”也被称作细胞因子风暴综合征(cytokinestormsyndrome,css),是指机体感染微生物后引起体液中多种细胞因子如tnfα、il-1β、il-6和mcp-1等迅速大量产生的现象,是引起急性呼吸窘迫综合症和多器官衰竭的重要原因【安纪红.感染与细胞因子风暴.中华实验和临床感染病杂志,2013,7(6):925-926.】。例如,这次在全球爆发的新型冠状病毒肺炎(“novelcoronaviruspneumonia”,简称“ncp”),是以前从未在人体中发现的冠状病毒新毒株(covid-19)感染引起的重大疫情。新冠肺炎患者体内出现“炎症风暴”现象是轻症向重症和危重症转换的一个重要节点,同时也是患者出现死亡的一个重要原因。因此,通过抑制炎症因子大量分泌是临床治疗感染性疾病的一个重要策略。
在固有免疫细胞应答中,模式识别信号受体toll样受体(tlr)识别病原体相关分子模式(pamp)。根据表达部位不同可分为表达于胞膜的tlr(如tlr4,识别细菌脂多糖)和表达于内体和吞噬体膜的tlr(tlr3、tlr7、tlr8和tlr9,识别病毒核酸),病毒和细菌虽然识别不同tlr,但是都依赖共通的信号转导途径(依赖myd88和依赖trif两种信号途径)激活nf-kb介导炎性细胞因子的表达。炎症风暴以全身和局部组织细胞因子大量释放为特征,其中tnfα主要是由单核巨噬细胞产生,可参与发热和炎症的发生。因此,以tnfα为抗炎活性指标,运用细菌内毒素成分脂多糖(lipopolysaccharides,lps)刺激小鼠腹腔巨噬细胞的模型进行药物筛选是安全快速发现有效抑制感染性疾病患者“炎症风暴”的一个策略。首先构建了抗感染老药库(包括抗病毒药物、抗菌药物等共计525个上市药物及临床研究药物),运用“老药新用,一药多用”策略开展抗炎药物筛选。
恩替卡韦(entecavir)是乙肝治疗的临床一线药物,属于鸟嘌呤核苷类似物,它能够通过磷酸化成为具有活性的三磷酸盐,与乙肝病毒多聚酶的天然底物三磷酸脱氧鸟嘌呤核苷竞争,从而发挥抗乙肝病毒的作用。目前尚没有明确报道恩替卡韦作为抑制感染性疾病所致炎症风暴的药物的临床应用。
技术实现要素:
本发明的目的是提供一种恩替卡韦在制备治疗感染性疾病引起炎症风暴的药物中的应用。
为了实现上述目的,本发明采用的技术方案如下:
本发明的第一方面提供了一种恩替卡韦在制备治疗感染性疾病引起炎症风暴的药物中的应用。
所述感染性疾病为病毒、衣原体、支原体、细菌或寄生虫等各种病原体引起的感染。
所述炎症风暴为感染性疾病引起机体内多种细胞因子迅速大量产生的现象,为感染性疾病患者轻症向重症和危重症转换时,机体内多种细胞因子如tnfα、il-1β、il-6、mcp-1、il-1α、il12、il27、gm-csf、ifnα、ifn-γ等迅速大量产生的现象。
所述恩替卡韦可以是其原料药、溶剂合物、盐的形式。
所述恩替卡韦(entecavir)的结构式[innaimo,s.f.,seifer,m.,bisacchi,g.s.,standring,d.n.,zahler,r.,&colonno,r.j..(1997).identificationofbms-200475asapotentandselectiveinhibitorofhepatitisbvirus.antimicrobialagentsandchemotherapy,41(7),1444-1448.]如式1所示:
所述恩替卡韦在细胞水平抑制tnfα的剂量为0.3125-40μmol/l。
所述恩替卡韦在动物水平抑制多种细胞因子的单次应用剂量为2mg/kg。
所述恩替卡韦可以和药剂学上的常规药用辅料制成药物制剂,所述药物制剂可以通过胃肠道或肠胃外给予。
所述药物制剂是口服剂型、注射液剂型或粉针剂。
由于采用上述技术方案,本发明具有以下优点和有益效果:
本发明的实验结果表明在lps刺激小鼠腹腔巨噬细胞模型中,恩替卡韦可以剂量依赖性地抑制细胞因子tnfα分泌,在有效剂量内没有显示细胞毒性;在lps诱发css小鼠模型中,恩替卡韦对感染性疾病引起炎症风暴的特征性细胞因子tnfα、il-1β、il-6、mcp-1、il-1α、il12、il27、gm-csf、ifnα、ifn-γ具有明显抑制作用;说明恩替卡韦可以作为治疗感染性疾病引起炎症风暴的药物。
本发明提供的恩替卡韦在细胞水平抑制tnfα的剂量为0.3125-40μmol/l,显示显著减少多种细胞因子的分泌并不产生明显的细胞毒性;本发明首次证实,恩替卡韦具有抑制感染性疾病引起炎症风暴的作用,可用于制备感染性疾病引起炎症风暴的治疗药物使用,为临床治疗提供新的抗炎方案。
附图说明
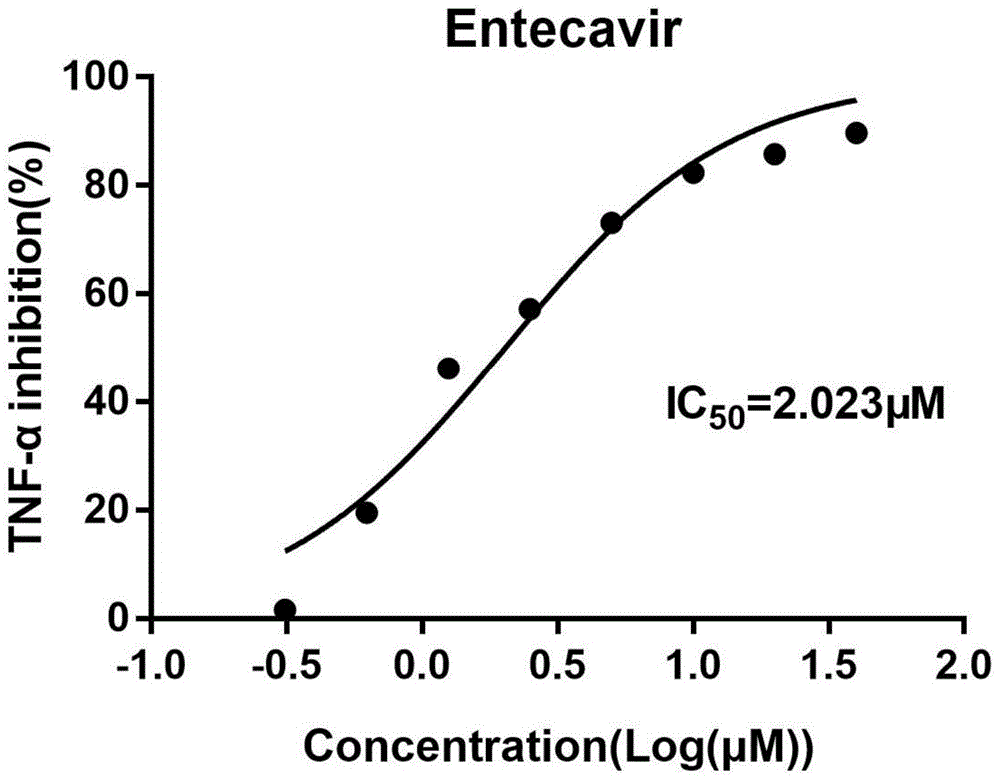
图1为lps刺激小鼠腹腔巨噬细胞模型中恩替卡韦对细胞因子tnfα分泌的抑制作用示意图。
图2为lps刺激小鼠腹腔巨噬细胞的模型中恩替卡韦在相同剂量下对细胞生存率的影响示意图。
图3为lps诱发css小鼠模型中恩替卡韦对血浆中细胞因子tnfα、il-6、il-1β、il-12、gm-csf、ifnα和ifn-γ的抑制作用示意图。
图4为lps诱发css小鼠模型中恩替卡韦对肺泡灌洗液中细胞因子tnfα、il-6、il-1α、il27、gm-csf和mcp-1的抑制作用示意图。
具体实施方式
为了更清楚地说明本发明,下面结合优选实施例对本发明做进一步的说明。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
以下实施例中使用的恩替卡韦的结构式如式1所示:
本发明实施例中所用恩替卡韦购自上海陶素生化科技有限公司。
实施例1
lps刺激小鼠腹腔巨噬细胞模型的建立:
1.1材料
c57bl/6品系小鼠,雄性,体重18-22g,购自常州卡文斯实验动物有限公司,生产许可证号scxk(苏)2016-0010;lps源于大肠杆菌0111:b4购自sigma-aldrich公司;rpmi-1640培养基、胎牛血清和双抗为gibco公司产品;cck8购自同仁化学研究所;tnfαelisa检测试剂盒购自invitrogen公司(货号:bms607-3ten);酶标仪为biotek品牌。
1.2小鼠腹腔巨噬细胞的分离培养
c57bl/6小鼠腹腔注射3ml含3%巯基硫酸盐的肉汤培养基(购自bd),3天后,颈椎脱臼处死,75%酒精浸泡2次,每次1分钟。随后将小鼠放入无菌操作台上,沿腹中线位置缓慢剪开小鼠腹部皮肤,应注意勿破坏腹膜完整性。注射器缓慢注入5mlrpmi-1640培养基,反复按摩腹部使细胞分散于培养基中,然后缓慢抽出液体,经40μm细胞筛网过滤至50ml离心管中,反复灌洗3次。过滤后的细胞1500rpm离心3分钟,细胞沉淀重悬于rpmi-1640培养基中,细胞种板于96孔板中,密度为每孔5×105个细胞。细胞贴壁4小时后,pbs冲洗细胞2次,换用含有10%血清和1%双抗的rpmi-1640培养基(全培养基)。细胞过夜培养后给予后续处理。
1.3细胞模型制备及检测
(1)配置含100ng/mllps的全培养基,恩替卡韦设置8个浓度梯度(分别为40、20、10、5、2.5、1.25、0.625、0.3125μm),共同处理细胞4小时。
(2)去细胞上清备用,细胞中加入含10%cck8的全培养基,继续孵箱30分钟,用酶标仪在450nm波长激发下测定吸光度,以lps对照组细胞的吸光度为1,将不同药物浓度对应的吸光度换算成相对细胞活力,来判定恩替卡韦的细胞毒性。
(3)细胞上清液稀释10倍,根据试剂盒的操作步骤进行elisa实验。
tnfα抑制率=(lps对照浓度值-药物组浓度值)/lps对照浓度值×100%。
结果:如图1所示,图1为lps刺激小鼠腹腔巨噬细胞模型中恩替卡韦对细胞因子tnfα分泌的抑制作用示意图。图1中横坐标为浓度的log值,纵坐标为tnfα抑制率,从图中可以看出,在lps刺激小鼠腹腔巨噬细胞的模型中,恩替卡韦在0.3125-40μmol/l剂量范围下对tnfα分泌的抑制作用成明显量效关系,半数抑制浓度ic50为2.023μmol/l。
如图2所示,图2为lps刺激小鼠腹腔巨噬细胞的模型中恩替卡韦在相同剂量下对细胞活力的影响示意图。图2中横坐标为浓度,纵坐标为细胞相对于未加药物处理的对照细胞的活力,从图中可以看出,在lps刺激小鼠腹腔巨噬细胞的模型中,恩替卡韦在0.3125-40μmol/l剂量范围下对小鼠腹腔巨噬细胞有一定的细胞毒性,在有效剂量5μmol/l以内细胞相对活力大于90%。
实施例2
lps诱发css小鼠模型的建立:
1.1材料
c57bl/6品系小鼠,雄性,体重18-22g,购自常州卡文斯实验动物有限公司,生产许可证号scxk(苏)2016-0010;lps源于大肠杆菌0111:b4购自sigma-aldrich公司;多因子检测试剂盒购自biolegend公司(mouseanti-viruspanel,catno:740622;mouseinflammationpanel,catno:740446);cytoflex流式细胞仪为美国贝克曼库尔特品牌。
1.2动物模型
lps选用15mg/kg的剂量腹腔注射小鼠诱导css。
1.3血浆分离
在lps注射后4小时,经眼眶取血至含edta的抗凝管,静置30分钟后,4000rpm转速,在4℃条件下离心15分钟,取上清即血浆至ep管中备用。
1.4收集小鼠肺泡灌洗液(bronchoalveolarlavagefluid,balf)
lps注射8小时后,颈椎脱臼处死小鼠,沿正中线缓慢剪开颈部皮肤,缓慢分离气管周围软组织,暴露组织后在甲状腺位置处切开气管,将注射器针头尖部剪断磨钝后插入气管内,并用4号手术线结扎气管固定针头,1ml注射器取0.3mlpbs溶液缓慢注入肺中,并轻柔按摩肺部,1分钟后缓慢回抽液体,回抽后的液体放于1.5mlep管中,重复灌洗3次,共0.9ml灌洗液。随后将灌洗液500g离心5分钟,上清液转移至新的ep管中备用。
1.5流式细胞仪检测多细胞因子:所用分析试剂和缓冲液均来自流式细胞仪检测多细胞因子检测试剂盒,实验操作按照试剂盒提供的步骤执行,具体如下:
(1)按样本数取相应量的1.5ml离心管并标号,另取8个1.5ml离心管分别标记为c1-c8。
(2)样本管中加入25μl的分析缓冲液,在8个标准品管中分别加入25μl基质a。
(3)涡旋混合珠瓶30秒,向每个离心管中加入25μl混合磁珠,然后在对应的离心管中分别加入样品或标准品各25μl。
(4)室温下,以500rpm的转速水平震荡2个小时。
(5)向每个离心管中加入500μl1x洗涤缓冲液后以2000rpm的转速离心10min。尽量吸去洗涤缓冲液,留下沉淀的珠子。
(6)向每个离心管中添加25μl检测抗体。
(7)涡旋后,在室温下以500rpm的转速水平震荡1个小时。
(8)将25μlsa-pe直接添加到每个1.5ml离心管中。在室温下以500rpm的转速水平震荡30分钟。
(9)重复第5步操作。
(10)向每个离心管中加入200μl1x洗涤缓冲液,并涡旋1分钟。
(11)在流式细胞仪上读取样品,生成的fcs文件应使用biolegend的legendplexv8.0数据分析软件进行分析。
1.6动物实验流程
(1)c57bl/6随机分为模型对照组(给予相同体积的生理盐水)和恩替卡韦治疗组(单次给药,剂量为2mg/kg),在造模前30分钟完成腹腔注射给药。
(2)lps选用15mg/kg的剂量腹腔注射小鼠诱导css。
(3)造模后4小时取血浆或者8小时取balf。
(4)流式细胞检测仪分别测定血浆和balf中的多细胞因子。
如图3所示,图3为lps诱发css小鼠模型中恩替卡韦对血浆中细胞因子tnfα、il-6、il-1β、il-12、gm-csf、ifnα和ifn-γ的抑制作用示意图。图3中为空白对照和恩替卡韦,纵坐标为血浆中细胞因子浓度值(单位为pg/ml)。如图4所示,图4为lps诱发css小鼠模型中恩替卡韦对肺泡灌洗液中细胞因子tnfα、il-6、il-1α、il27、gm-csf和mcp-1的抑制作用示意图。图4中为空白对照和恩替卡韦,纵坐标为肺泡灌洗液中细胞因子浓度值(单位为pg/ml)。从图3和图4可以看出,在lps诱发css小鼠模型中,恩替卡韦在2mg/kg剂量下对小鼠血浆(图3)和肺泡灌洗液中多个细胞因子有显著的抑制作用(图4)。
以上所述仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专利的技术人员在不脱离本发明技术方案范围内,当可利用上述提示的技术内容作出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明方案的范围内。
- 还没有人留言评论。精彩留言会获得点赞!