用于治疗胰岛素抵抗综合征及2型糖尿病的中药制剂的制作方法
本发明属于中药制剂领域,具体涉及用于治疗胰岛素抵抗综合征及2型糖尿病的中药制剂。
背景技术:
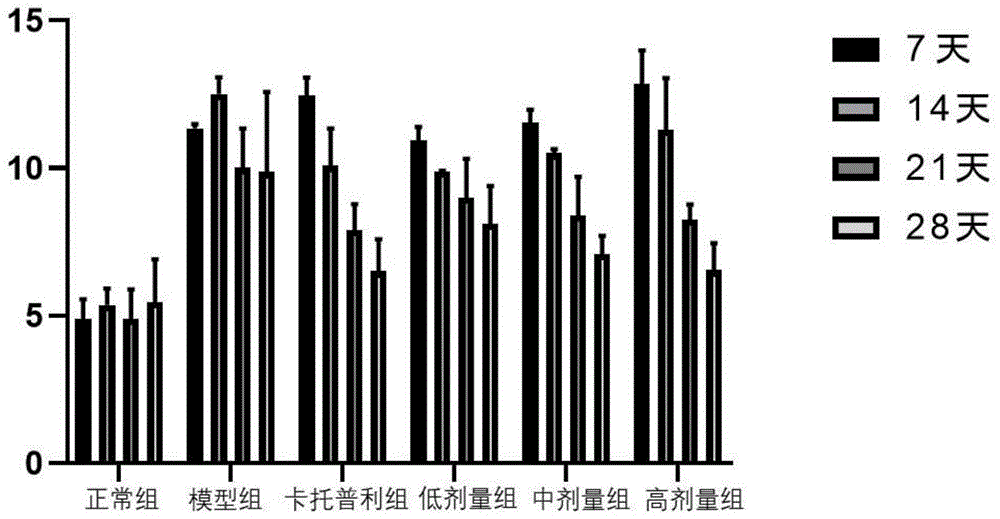
:胰岛素抵抗综合征又称“x综合征”或“代谢综合征”,主要表现为高胰岛素血症、高血糖、肥胖等。胰岛素抵抗综合征和多种心血管疾病发病相关,其形成原因比较复杂,但多数认为胰岛素抵抗是造成该疾病发展的主要原因之一。胰岛素抵抗主要指靶组织对胰岛素的敏感性下降,通常指组织对胰岛素介导葡萄糖的利用率降低。胰岛素抵抗是很多疾病的前置要素,当患有胰岛素抵抗时,机体不能够产生足够的胰岛素来满足体内葡萄糖代谢的需要时,就会发生2型糖尿病。2型糖尿病是目前发病率最高的糖尿病类型,在患者中的死亡率一直居高不下,目前2型糖尿病患者人数占据糖尿病患者总人数的90%之多。作为世界上最为常见的慢性病之一,糖尿病在各年龄群体均有高发病率。目前其发病趋势呈现年轻化,年轻群体的糖尿病的发病率明显高于老年人群体。据报道,我国的糖尿病患者达到数亿之多,而且每年都在持续增长。糖尿病的病因主要以体内糖代谢失衡为主,胰岛素抵抗与2型糖尿病及代谢疾病的发生密切相关。胰岛素抵抗被认为是2型糖尿病的发病基础,胰岛素抵抗的程度与患者葡萄糖代谢障碍水平密切相关。正常人体内胰岛素可以抑制肝脏葡萄糖输出,并促进组织对葡萄糖的吸收,所以血浆葡萄糖水平稳定在正常值。而糖尿病患者由于胰岛素抵抗,导致肝脏及外周组织对胰岛素的敏感性下降以及葡萄糖摄取减少,导致血浆葡萄糖水平升高。所以,胰岛素抵抗的治疗结果同以上疾病的治愈程度密切相关。技术实现要素:为了解决上述问题,本发明提供了用于治疗胰岛素抵抗综合征及2型糖尿病的中药制剂。本发明的目的通过下述技术方案实现:用于治疗胰岛素抵抗综合征及2型糖尿病的中药制剂,包括混合制剂,混合制剂包括柚皮苷、甘草苷、枸杞多糖、芒果苷、橄榄苦苷。进一步地,混合制剂含量为12.5~50mg/kg。进一步地,混合制剂组分为柚皮苷10份、甘草苷2份、枸杞多糖33.4份、芒果苷40份、橄榄苦苷1份。进一步地,混合制剂还包括远志皂苷元150份。进一步地,混合制剂还包括远α细辛醚20份。进一步地,混合制剂还包括银杏内酯b60份。进一步地,混合制剂还包括石杉碱甲0.15份。本发明具有如下有益效果:1.本发明组合物主要成为水果成分,无副作用,真正做到药食同源的效果。2.本发明组合物各组分相互之间起到协同作用,显著改善胰岛素抵抗综合征及2型糖尿病。附图说明图1为混合制剂对胰岛素抵抗大鼠空腹血糖(fpg(mmol/l))的影响。图2为混合制剂对胰岛素抵抗综合征大鼠空腹胰岛素(fins(mu/l))的影响。图3为混合制剂对胰岛素抵抗综合征大鼠胰岛素抵抗指数(homa-ir)的影响。图4为混合制剂对糖尿病大鼠空腹血糖(fpg(mmol/l))的影响。图5为混合制剂对糖尿病大鼠空腹胰岛素(fins(mu/l))的影响。图6为混合制剂对糖尿病大鼠胰岛素抵抗指数(homa-ir)的影响。具体实施方式下面将结合本发明实施例中的附图1~6,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。远志皂苷元是中药远志中的一种活性成分,具有保护神经、抗氧化等作用。在大鼠海马神经元中,可以减轻急性脑出血带来的损伤在新生大鼠海马神经干细胞中,远志皂苷元对氧剥夺/再复氧诱导的细胞损伤有良好的治愈效果。石杉碱甲是中药蛇足杉中提取的生物碱,是一种具有可逆性的高效、高选择性ache抑制剂,易透过血脑屏障,可以改善阿兹海默症导致的认知损伤。在国外,石杉碱甲已经被制成营养品来预防认知障碍相关疾病。银杏内酯是银杏中的一种活性成分,是常用的血小板活化因子受体拮抗剂,对中枢神经系统、心血管系统均有一定的保护作用。α细辛醚是中药石菖蒲的提取物,石菖蒲是我国传统中药,有治疗精神和心脑血管疾病的作用。α-细辛醚被报道可以抑制hmg-coa还原酶并治疗高脂血症。基于以上几种药物被报道的药理作用,我们同之前选择的五种水果苷一起组成配伍配方,并发现了其中最佳治疗胰岛素抵抗综合征及2型糖尿病的比例。1.药物配伍设计按照l12(211)正交设计表设计的组别随机组合12个组别,分别配制不同比例的远志皂苷元、α细辛醚、银杏内酯b、石杉碱甲、甘草苷、柚皮苷、枸杞多糖、芒果苷和橄榄苦苷的混合物溶液。确定9种有效组分的剂量水平。以实际误差进行全面分析的正交实验,确定9者防治胰岛素抵抗综合征及糖尿病小鼠记忆力减退的最佳疗效比例。根据实验结果,组别7为最佳药物配伍组。给药4周后进行指标检测。9种有效组分剂量水平见表1,9种有效组分剂量分组见表2。表1.药物配伍:浓度水平(mg/kg/d)药物低剂量高剂量远志皂苷元60150α细辛醚2080银杏内酯b1560石杉碱甲0.10.15柚皮苷1040甘草苷28枸杞多糖8.333.4芒果苷1040橄榄苦苷14表29种有效组分剂量分组(mg/kg/d)组别远志皂苷元α细辛醚银杏内酯b石杉碱甲柚皮苷甘草苷枸杞多糖芒果苷橄榄苦苷16020150.11028.310126020150.110833.440436020600.154028.310446080150.1540233.440156080600.14088.340166080600.1510833.4104715020600.1510233.4401815020600.140833.4101915020150.154088.34041015080600.11028.34041115080150.151088.31011215080150.140233.41042.造模与分组2.1胰岛素抵抗综合征模型48只spf级8周龄雄性wistar大鼠(来自温州医科大学实验动物中心),体质量(180-200)g,所有的实验中照料和使用老鼠程序是与温州医科大学附属第一医院道德伦理委员会主张的一致。基础饲料喂养一周后,按随机区组设计分为正常组,模型组,阳性对照组(二甲双胍),低中高剂量治疗组(混合制剂),每组各8只。正常组喂养基础饲料,其余组用高糖高脂高盐饲料喂养6周建立胰岛素抵抗综合征模型。模型建立后进行灌胃给药,阳性对照组给予卡托普利(0.1g/kg),低剂量治疗组给予给予混合制剂12.5mg/kg,中剂量治疗组给予混合制剂20mg/kg,高剂量治疗组混合制剂50mg/kg,每日一次,连续4周。正常组及模型组分别以等体积生理盐水,4周后进行实验相关指标检测。2.22型糖尿病大鼠模型48只spf级8周龄雄性wistar大鼠(来自温州医科大学实验动物中心),体质量(180-200)g,所有的实验中照料和使用老鼠程序是与温州医科大学附属第一医院道德伦理委员会主张的一致。基础饲料喂养一周后,按随机区组设计分为正常组,模型组,阳性对照组(二甲双胍),低中高剂量治疗组(混合制剂),每组各8只。高脂高糖饲料喂饲4周后,禁食12h,腹腔注射stz30mg/kg,空白组注射等体积柠檬酸缓冲液。以空腹血糖≥11.1mmol/l、随机血糖≥16.7mmol/l为2型糖尿病成模标准。1周后开始进行给药,阳性对照组给予二甲双胍(85mg/kg),低剂量治疗组给予给予混合制剂12.5mg/kg,中剂量治疗组给予混合制剂20mg/kg,高剂量治疗组混合制剂50mg/kg,正常组及模型组分别以等体积生理盐水,每日一次。一共给药28天,每隔7天进行空腹血浆胰岛素、空腹血糖检测,并计算胰岛素抵抗指数(homa-ir)。2.3检测指标记录大鼠给药前后体重变化;采用尾套法测定大鼠清醒状态下尾动脉收缩压(sbp)。均取连续3次读数的平均值。最后一次灌胃结束后,大鼠均禁食12h,称取体重,用苯巴比妥那(50mg/kg)经腹腔麻醉后,分别由颈总动脉插管取血检测各项指标;甘油三酯(tg)采用磷酸甘油氧化酶法测定;总胆固醇(tc)、高密度脂蛋白(hdl-c)采用胆固醇氧化酶法测定;空腹血浆胰岛素(fins)采用放射免疫法;空腹血糖(fpg)采用氧化酶法;胰岛素抵抗指数(homa-ir)=空腹血浆葡萄糖(mmol/l)*空腹血浆胰岛素(mu/l)/22.5。采用spss.22软件进行分析,数据以±s表示,组间比较采用t检验进行分析,以p<0.05位差异学有统计意义。3.结果3.1胰岛素抵抗综合征与2型糖尿病大鼠各组治疗前后收缩压、血脂变化比较。与治疗后正常组相比,模型组大鼠尾动脉收缩压升高,两组间比较差异具有显著性(p<0.05);与治疗后模型组相比,治疗后,混合制剂各剂量组、卡托普利组大鼠动脉收缩压均降低,各组间比较具有显著性差异(p<0.05)。与正常组相比,模型组大鼠tc、tg、hdl-c均明显升高,且两组间比较具有显著性差异(p<0.05);混合制剂各剂量组tc、tg、hdl-c均有所降低,与模型组比较具有显著性差异(p<0.05),见表3。表3混合制剂对胰岛素抵抗综合征大鼠治疗前后动脉收缩压、血脂的影响(n=8,±s)与治疗后正常组相比,模型组大鼠尾动脉收缩压升高,两组间比较差异具有显著性(p<0.05);与治疗后模型组相比,治疗后,混合制剂各剂量组、二甲双胍组大鼠动脉收缩压均降低,各组间比较具有显著性差异(p<0.05)。与正常组相比,模型组大鼠tc、tg升高,hdl-c下降,且两组间比较具有显著性差异(p<0.05);混合制剂各剂量组tc、tg均有所降低,hdl-c升高,与模型组比较具有显著性差异(p<0.05),见表4。表4混合制剂对2型糖尿病大鼠治疗前后动脉收缩压、血脂的影响(n=8,±s)3.2胰岛素抵抗综合征与2型糖尿病大鼠各组体重、摄食量、饮水量变化。给药前,各组大鼠体重均无明显差异;喂养4周后,与正常组相比,模型组体重下降,两组间比较具有显著性差异(p<0.05);喂养8周后,模型组体重显著下降,两组间比较具有显著性差异(p<0.05)。与模型组相比,卡托普利组及低中高剂量组具有明显改善糖尿病大鼠症状的效果,各组间比较具有显著性差异(p<0.05),见表5。表5混合制剂对胰岛素抵抗综合征体重的影响(n=8,±s)给药前,各组大鼠体重均无明显差异;喂养4周后,与正常组相比,模型组体重下降,两组间比较具有显著性差异(p<0.05);喂养8周后,模型组体重显著下降,两组间比较具有显著性差异(p<0.05)。与模型组相比,二甲双胍组及低中高剂量组具有明显改善糖尿病大鼠症状的效果,各组间比较具有显著性差异(p<0.05),见表6。表6混合制剂对2型糖尿病大鼠体重的影响(n=8,±s)3.3胰岛素抵抗综合征与2型糖尿病大鼠各组空腹血糖、胰岛素、胰岛素抵抗指数结果比较。在胰岛素抵抗综合征大鼠中,治疗4周后,与正常组相比,模型组大鼠空腹血糖、空腹胰岛素水平、homa-ir指数均升高,两组间比较具有显著性差异(p<0.05);与模型组相比,各治疗组大鼠空腹血糖、空腹胰岛素水平、homa-ir指数均下降,卡托普利组空腹胰岛素水平、homa-ir指数均下降,各组间比较具有显著性差异(p<0.05),见表7。表7混合制剂对胰岛素抵抗综合征大鼠空腹血糖、空腹胰岛素、胰岛素抵抗指数的影响(n=8,±s)组别fpg(mmol/l)fins(mu/l)homa-ir正常组5.45±1.4615.35±4.213.05±.0.56模型组9.87±2.7130.17±3.1814.53±1.22卡托普利组6.51±1.0920.58±6.096.33±1.06低剂量组8.12±1.2724.77±5.268.62±0.92中剂量组7.09±0.6121.19±6.017.02±1.33高剂量组6.54±0.9219.54±5.316.22±0.98共给药28天,每隔7天进行空腹血浆胰岛素、空腹血糖检测,并计算胰岛素抵抗指数(homa-ir),空腹血糖检测结果见表8,空腹胰岛素检测结果见表9,胰岛素抵抗指数计算结果见表10,统计结果见图1-3。表8混合制剂对胰岛素抵抗大鼠空腹血糖(fpg(mmol/l))的影响(n=8,±s)组别7天14天21天28天正常组4.89±0.675.37±0.554.89±1.015.45±1.46模型组11.34±0.1512.52±0.5610.02±1.339.87±2.71卡托普利12.47±0.610.08±1.267.91±0.876.51±1.09低剂量组10.94±0.459.88±0.029±1.328.12±1.27中剂量组11.53±0.4510.5±0.148.39±1.317.09±0.61高剂量组12.84±1.1511.3±1.768.25±0.526.54±0.92表9混合制剂对胰岛素抵抗综合征大鼠空腹胰岛素(fins(mu/l))的影响(n=8,±s)组别7天14天21天28天正常组13.93±0.9514.36±1.1812.97±1.8315.35±4.21模型组30.89±0.129.03±0.5228.94±1.5730.17±3.18卡托普利31.33±0.5127.71±0.2322.94±1.1220.58±6.09低剂量组30.45±1.2427.39±0.9524.68±0.4524.77±5.26中剂量组29.72±0.6926.83±0.823.62±0.9321.19±6.01高剂量组31.03±0.3527.73±0.7322.54±1.3219.54±5.31表10混合制剂对胰岛素抵抗综合征大鼠胰岛素抵抗指数(homa-ir)的影响(n=8,±s)组别7天14天21天28天正常组3.25±0.033.24±0.053.01±0.123.05±0.56模型组15.97±0.0216.13±0.0913.11±0.2914.53±1.22卡托普利16.89±0.0312.37±0.227.93±0.086.33±1.06低剂量组15.03±0.0511.99±0.1210.03±0.138.62±0.92中剂量组15.09±0.1111.83±0.039.09±0.257.02±1.33高剂量组17.81±0.0812.91±0.078.82±0.336.22±0.98表11混合制剂对糖尿病大鼠空腹血糖、空腹胰岛素、胰岛素抵抗指数的影响(n=8,±s)组别fpg(mmol/l)fins(mu/l)homa-ir正常组5.01±0.2615.52±0.113.88±1.23模型组19.08±2.4828.78±1.7825.41±0.99二甲双胍8.17±1.2719.56±3.347.68±1.33低剂量组12.11±2.4521.15±0.7112.97±2.44中剂量组10.25±1.1920.63±3.659.40±0.88高剂量组8.58±1.6219.67±2.887.32±1.09共给药28天,每隔7天进行空腹血浆胰岛素、空腹血糖检测,并计算胰岛素抵抗指数(homa-ir),空腹血糖检测结果见表12,空腹胰岛素检测结果见表13,胰岛素抵抗指数计算结果见表14,统计结果见图4-6。表12混合制剂对糖尿病大鼠空腹血糖(fpg(mmol/l))的影响(n=8,±s)组别7天14天21天28天正常组5.21±0.555.13±0.644.99±0.995.01±0.26模型组23.44±0.1220.53±1.5418.97±2.5619.08±2.48二甲双胍20.33±1.5918.45±2.0112.77±1.948.17±1.27低剂量组22.45±0.3320.54±0.7818.36±1.6612.11±2.45中剂量组25.67±1.2319.49±0.0313.11±3.110.25±1.19高剂量组24.13±2.120.12±0.1311.24±2.528.58±1.62表13混合制剂对糖尿病大鼠空腹胰岛素(fins(mu/l))的影响(n=8,±s)组别7天14天21天28天正常组14.23±1.2215.56±0.1813.24±2.2315.52±0.11模型组30.3±2.128.79±1.0227.34±0.5728.78±1.78二甲双胍31.22±0.2326.56±1.3323.78±0.5719.56±3.34低剂量组28.44±0.5725.34±2.223.46±1.721.15±0.71中剂量组29.56±0.5926.24±0.1124.78±1.3220.63±3.65高剂量组33.1±1.2924.29±1.0221.33±0.2719.67±2.88表14混合制剂对糖尿病大鼠胰岛素抵抗指数(homa-ir)的影响(n=8,±s)组别7天14天21天28天正常组3.52±0.153.55±0.053.10±0.183.88±1.23模型组33.73±0.0725.94±0.1222.95±1.0225.41±0.99二甲双胍29.94±0.2221.59±0.3413.70±0.097.68±1.33低剂量组28.38±0.3323.98±0.1318.87±0.6512.97±2.44中剂量组32.44±0.0323.01±0.0714.89±0.189.40±0.88高剂量组36.70±0.8421.22±0.0211.12±0.137.32±1.09对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明,因此无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1