血管外科用纳米止血抗菌复合材料及其制备方法与流程
本发明涉及血管外科止血抗菌材料技术领域,特别是涉及血管外科用纳米止血抗菌复合材料及其制备方法。
背景技术:
血管外科是外科学的一个分支学科,主要针对除脑血管、心脏血管以外的外周血管疾病的预防、诊断和治疗,其治疗手段主要包括药物治疗、物理治疗、手术治疗和介入治疗。在血管外科的治疗过程中,通常需要使用止血抗菌材料对患者创面进行止血及防护作用,以促进创面的修复,保证患者健康。由于使用的止血抗菌材料的止血性能及抗菌性能将直接影响患者创面的恢复情况,进而影响患者的身体健康,因此,对血管外科用止血抗菌材料的研究具有重要意义。
传统的血管外科用止血抗菌材料主要由纱布及抗菌药物复合而成,其制备简单、使用方便,但功能较为单一,止血效果较差,与创面相容性不佳,已逐渐难以满足实际应用的需求。近年来,为改善止血抗菌材料的止血效果及抗菌作用,针对天然高分子类、合成高分子类及无机纳米类止血抗菌材料的研究均取得了一定进展,但单一类型的止血抗菌材料性能仍存在不足,如何寻求更适合的方法对各类止血抗菌材料进行有效复合,是当前的研究重点。
公开号为cn109453418a的专利提供了一种血管外科用止血抗菌敷料,该止血抗菌敷料包括纤维层和凝胶层,该凝胶层由丙烯酸、n-羟甲基丙烯酰胺、聚乙烯醇和聚乙烯吡咯烷酮交联聚合而成,并添加了甘羟铝、滑石粉、纳米银及中药抗菌液,从而达到止血和抗菌的效果。但该止血抗菌敷料仅将各类止血、抗菌物质简单复合,作用机制不明确,不仅对止血、抗菌作用的改善效果不明显,还容易引起过敏及感染;且该止血抗菌敷料中使用的丙烯酸、n-羟甲基丙烯酰胺等物质刺激性相对较大,不利于创面的快速修复,生物相容性不佳。
有鉴于此,当前仍有必要对血管外科用纳米止血抗菌复合材料及其制备方法进行研究,以获得止血速度快、抗菌效率高、生物相容性好的止血抗菌材料,促进患者创面的恢复,保障患者的健康。
技术实现要素:
本发明的目的在于针对上述问题,提供血管外科用纳米止血抗菌复合材料及其制备方法,通过对壳聚糖进行氨基化及邻苯三酚接枝处理,有效提高壳聚糖碳链上的氨基数量,改善壳聚糖对组织的黏附作用,使制得的纳米纤维薄膜具有丰富的活性位点和优异的生物相容性;并通过将纳米纤维薄膜浸入含有氧化纤维素与纳米氧化锌的后处理液中,使纳米氧化锌被包覆于壳聚糖与氧化纤维素形成的三维网络中,从而使制得的纳米止血抗菌复合材料同时具有较优的机械性能、止血性能和抗菌性能。
为实现上述目的,本发明提供了血管外科用纳米止血抗菌复合材料的制备方法,包括如下步骤:
s1、将壳聚糖溶于盐酸溶液中,并调节溶液ph至5.0~5.5,得到壳聚糖溶液;向所述壳聚糖溶液中加入预定量的乙二胺和碳二亚胺,在35~40℃下反应5~7h后,对产物依次进行透析和冷冻干燥处理,得到氨基化壳聚糖;
s2、将步骤s1得到的所述氨基化壳聚糖溶液盐酸溶液中,并调节溶液ph至5.0~5.5,得到氨基化壳聚糖溶液;将3,4,5-三羟基苯甲酸溶于乙醇中得到3,4,5-三羟基苯甲酸溶液;再将所述3,4,5-三羟基苯甲酸溶液加入所述氨基化壳聚糖溶液中得到混合溶液,并向所述混合溶液中加入预定量的碳二亚胺和n-羟基丁二酰亚胺,在惰性气氛下充分反应后,经透析、冷冻干燥处理,得到邻苯三酚接枝壳聚糖;
s3、将聚氧化乙烯与步骤s2得到的所述邻苯三酚接枝壳聚糖按预设质量比混合均匀后溶于有机溶剂中,配制成纺丝液;对所述纺丝液进行静电纺丝,得到纳米纤维薄膜;所述纳米纤维薄膜的厚度为50~100μm,所述纳米纤维薄膜中纳米纤维的平均直径为400~600nm;
s4、将四氧化二氮溶于四氯化碳中,配制成氧化剂;将纤维素与所述氧化剂按预设质量比混合,在室温下充分反应后对产物进行洗涤,得到氧化纤维素;
s5、将步骤s4得到的所述氧化纤维素与纳米氧化锌按预设质量比混合后分散于去离子水中,配制成悬浮液;向所述悬浮液中加入预定量的碳二亚胺,得到后处理液;将步骤s3得到的所述纳米纤维薄膜置于所述后处理液中浸渍8~12h,取出后经洗涤、烘干,得到纳米止血抗菌复合材料。
进一步地,在步骤s1中,加入的乙二胺与所述壳聚糖碳链上羧基的物质的量之比为(20~30):1;加入的碳二亚胺与所述壳聚糖碳链上羧基的物质的量之比为2:1。
进一步地,在步骤s2中,加入的3,4,5-三羟基苯甲酸中羧基与所述氨基化壳聚糖中氨基的物质的量之比为(0.3~0.7):1;加入的碳二亚胺、n-羟基丁二酰亚胺与3,4,5-三羟基苯甲酸中羧基的物质的量之比为2:1:1。
进一步地,在步骤s2中,所述惰性气氛为n2气氛,在所述n2气氛下的反应温度为20℃,反应时间为12h。
进一步地,在步骤s3中,所述聚氧化乙烯与所述邻苯三酚接枝壳聚糖的预设质量比为(0.2~0.4):1。
进一步地,在步骤s3中,所述有机溶剂由三氟乙酸和二氯甲烷按质量比7:3混合而成;所述纺丝液中聚氧化乙烯与邻苯三酚接枝壳聚糖总量的质量分数为6%~10%。
进一步地,在步骤s4中,所述纤维素与所述氧化剂的预设质量比为1:(40~50)。
进一步地,在步骤s5中,所述氧化纤维素与纳米氧化锌的预设质量比为(20~40):1;加入的碳二亚胺与所述氧化纤维素中羧基的物质的量之比为2:1。
进一步地,在步骤s5中,所述悬浮液中氧化纤维素与纳米氧化锌总量的质量分数为8%~12%。
为实现上述目的,本发明还提供了血管外科用纳米止血抗菌复合材料,该纳米止血抗菌复合材料根据上述技术方案中任一技术方案制备得到。
与现有技术相比,本发明的有益效果是:
1、本发明提供的血管外科用纳米止血抗菌复合材料的制备方法通过对壳聚糖进行氨基化及邻苯三酚接枝处理,有效提高了壳聚糖碳链上的氨基数量,并改善壳聚糖对组织的黏附作用,使制得的纳米纤维薄膜具有丰富的活性位点和优异的生物相容性;同时,本发明通过将纳米纤维薄膜浸入含有氧化纤维素与纳米氧化锌的后处理液中,使纳米氧化锌被包覆于壳聚糖与氧化纤维素形成的三维网络中,从而使制得的纳米止血抗菌复合材料同时具有较优的机械性能、止血性能和抗菌性能。
2、本发明通过向壳聚糖溶液中加入乙二胺和碳二亚胺,能够利用碳二亚胺与壳聚糖碳链上的羧基先反应生成中间产物,该中间产物再与乙二胺反应,从而将乙二胺接枝于壳聚糖的羧基上,使壳聚糖碳链上的羧基转化为氨基,有效提高了壳聚糖碳链上的氨基数量。基于本发明制备的氨基化壳聚糖,其丰富的氨基不仅能够为邻苯三酚接枝反应提供丰富的活性位点,有效提高邻苯三酚的接枝率,还能够促进制得的纳米纤维薄膜与氧化纤维素间的交联反应,为制备性能优异的纳米止血抗菌复合材料奠定了基础。
3、本发明通过引入3,4,5-三羟基苯甲酸与氨基化壳聚糖进行反应,能够利用3,4,5-三羟基苯甲酸的羧基与氨基化壳聚糖上丰富的氨基进行酰胺化反应,从而使3,4,5-三羟基苯甲酸的邻苯三酚基团接枝于壳聚糖的氨基上,制备邻苯三酚接枝壳聚糖。基于本发明制备的邻苯三酚接枝壳聚糖,其引入的邻苯三酚基团能够在生理条件下部分去质子化,转化为活性醌基团,进而与存在于生物组织中的生物大分子的硫醇和末端胺反应,从而有效解决壳聚糖对生物组织黏附力不足的问题,使最终制得的纳米止血抗菌复合材料具有优异的生物相容性。
4、本发明通过将聚氧化乙烯与邻苯三酚接枝壳聚糖共混后进行静电纺丝,不仅能够利用聚氧化乙烯优异的可纺性有效提高壳聚糖的纺丝性能,还能够利用聚氧化乙烯良好的水溶性使其在后处理液中被脱除,从而使后处理后的纳米纤维薄膜具有多孔结构。基于该多孔结构,不仅能够促进氧化纤维素与壳聚糖之间交联反应的进行,还有利于纳米氧化锌的释放,并且能够有效提高制得的纳米止血抗菌复合材料对血液的吸附作用,从而使本发明制得的纳米止血抗菌复合材料具有优异的止血性能和抗菌效果。
5、本发明通过配制含有四氧化二氮的氧化剂对纤维素进行氧化,能够使制得的氧化纤维素具有较高的羧基含量,从而使其能够与具有丰富氨基的壳聚糖发生交联反应,并利用脱除聚氧化乙烯形成的多孔结构形成三维结构,使后处理液中的纳米氧化锌被包覆与形成的三维结构中。该方式不仅能够使止血效果优异的氧化纤维素与纳米纤维薄膜紧密结合,有效提高所得纳米止血抗菌复合材料的止血性能;还能够使兼具止血和抗菌作用的纳米氧化锌被均匀包覆于所得的复合材料中,并基于多孔结构进行释放,进一步提高纳米止血抗菌复合材料的止血性能和抗菌性能,同时改善其机械性能。
6、本发明提供的血管外科用纳米止血抗菌复合材料同时具有较优的机械性能、止血性能和抗菌性能,且生物相容性好,能够起到快速止血和高效抗菌的作用,从而促进患者创面修复,具有较高的应用价值。
附图说明
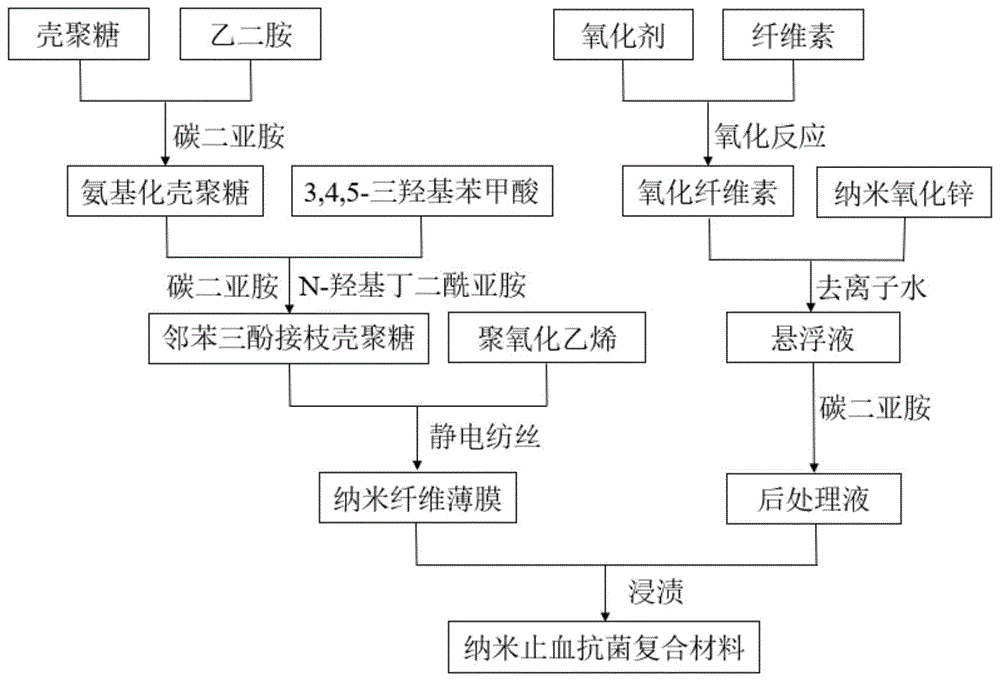
图1是本发明提供的血管外科用纳米止血抗菌复合材料制备方法的流程示意图。
具体实施方式
下面结合附图对本发明的较佳实施例进行详细阐述,以使本发明的优点和特征能更易于被本领域技术人员理解,从而对本发明的保护范围做出更为清楚明确的界定。显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施例,都属于本发明所保护的范围。
本发明提供了血管外科用纳米止血抗菌复合材料的制备方法,包括如下步骤:
s1、将壳聚糖溶于盐酸溶液中,并调节溶液ph至5.0~5.5,得到壳聚糖溶液;向所述壳聚糖溶液中加入预定量的乙二胺和碳二亚胺,在35~40℃下反应5~7h后,对产物依次进行透析和冷冻干燥处理,得到氨基化壳聚糖;
s2、将步骤s1得到的所述氨基化壳聚糖溶液盐酸溶液中,并调节溶液ph至5.0~5.5,得到氨基化壳聚糖溶液;将3,4,5-三羟基苯甲酸溶于乙醇中得到3,4,5-三羟基苯甲酸溶液;再将所述3,4,5-三羟基苯甲酸溶液加入所述氨基化壳聚糖溶液中得到混合溶液,并向所述混合溶液中加入预定量的碳二亚胺和n-羟基丁二酰亚胺,在惰性气氛下充分反应后,经透析、冷冻干燥处理,得到邻苯三酚接枝壳聚糖;
s3、将聚氧化乙烯与步骤s2得到的所述邻苯三酚接枝壳聚糖按预设质量比混合均匀后溶于有机溶剂中,配制成纺丝液;对所述纺丝液进行静电纺丝,得到纳米纤维薄膜;所述纳米纤维薄膜的厚度为50~100μm,所述纳米纤维薄膜中纳米纤维的平均直径为400~600nm;
s4、将四氧化二氮溶于四氯化碳中,配制成氧化剂;将纤维素与所述氧化剂按预设质量比混合,在室温下充分反应后对产物进行洗涤,得到氧化纤维素;
s5、将步骤s4得到的所述氧化纤维素与纳米氧化锌按预设质量比混合后分散于去离子水中,配制成悬浮液;向所述悬浮液中加入预定量的碳二亚胺,得到后处理液;将步骤s3得到的所述纳米纤维薄膜置于所述后处理液中浸渍8~12h,取出后经洗涤、烘干,得到纳米止血抗菌复合材料。
在步骤s1中,加入的乙二胺与所述壳聚糖碳链上羧基的物质的量之比为(20~30):1;加入的碳二亚胺与所述壳聚糖碳链上羧基的物质的量之比为2:1。
在步骤s2中,加入的3,4,5-三羟基苯甲酸中羧基与所述氨基化壳聚糖中氨基的物质的量之比为(0.3~0.7):1;加入的碳二亚胺、n-羟基丁二酰亚胺与3,4,5-三羟基苯甲酸中羧基的物质的量之比为2:1:1。
在步骤s2中,所述惰性气氛为n2气氛,在所述n2气氛下的反应温度为20℃,反应时间为12h。
在步骤s3中,所述聚氧化乙烯与所述邻苯三酚接枝壳聚糖的预设质量比为(0.2~0.4):1。
在步骤s3中,所述有机溶剂由三氟乙酸和二氯甲烷按质量比7:3混合而成;所述纺丝液中聚氧化乙烯与邻苯三酚接枝壳聚糖总量的质量分数为6%~10%。
在步骤s4中,所述纤维素与所述氧化剂的预设质量比为1:(40~50)。
在步骤s5中,所述氧化纤维素与纳米氧化锌的预设质量比为(20~40):1;加入的碳二亚胺与所述氧化纤维素中羧基的物质的量之比为2:1。
在步骤s5中,所述悬浮液中氧化纤维素与纳米氧化锌总量的质量分数为8%~12%。
本发明还提供了血管外科用纳米止血抗菌复合材料,该纳米止血抗菌复合材料根据上述技术方案中任一技术方案制备得到。
下面结合实施例及附图对本发明提供的血管外科用纳米止血抗菌复合材料及其制备方法进行说明。
实施例1
本实施例提供了血管外科用纳米止血抗菌复合材料的制备方法,包括如下步骤:
s1、将2g壳聚糖溶于100ml浓度为0.1mol/l的盐酸溶液中,并调节ph至5.0,再依次加入乙二胺和碳二亚胺,用磁力搅拌器在37℃下搅拌反应6h后,将反应产物装入截留分子量为3500的透析袋中,置于ph=5的酸性去离子水中透析48h,除去未反应完全的乙二胺和碳二亚胺;再置于-60℃下冷冻干燥48h,得到氨基化壳聚糖;
其中,乙二胺与壳聚糖碳链上羧基的物质的量之比为25:1;碳二亚胺与壳聚糖碳链上羧基的物质的量之比为2:1。
s2、将步骤s1得到的所述氨基化壳聚糖继续溶于100ml浓度为0.1mol/l的盐酸溶液中,并调节ph至5.0,得到氨基化壳聚糖溶液;将3,4,5-三羟基苯甲酸溶于乙醇中得到3,4,5-三羟基苯甲酸溶液;再将所述3,4,5-三羟基苯甲酸溶液滴加入所述氨基化壳聚糖溶液中得到混合溶液,并向所述混合溶液中加入碳二亚胺和n-羟基丁二酰亚胺,置于n2气氛中,在20℃下充分搅拌12h后,将反应产物装入截留分子量为3500的透析袋中,先置于ph=5的酸性去离子水中透析36h,再置于ph=7的去离子水中透析12h;再将得到的产物置于-60℃下冷冻干燥48h,得到邻苯三酚接枝壳聚糖;
其中,3,4,5-三羟基苯甲酸中羧基与所述氨基化壳聚糖中氨基的物质的量之比为0.5:1;碳二亚胺和n-羟基丁二酰亚胺与3,4,5-三羟基苯甲酸中羧基的物质的量之比为2:1:1。
s3、将三氟乙酸和二氯甲烷按质量比7:3混合均匀,配制成溶剂;将聚氧化乙烯与步骤s2得到的所述邻苯三酚接枝壳聚糖按质量比0.3:1混合后溶于所述溶剂中,配制质量分数为8%的纺丝液;将所述纺丝液置于注射器中,用注射泵将纺丝液流速控制为0.5ml/h,采用静电纺丝法进行纺丝,由针尖喷出的聚合物被距针尖10cm的铝箔收集,形成纳米纤维薄膜;所述纳米纤维薄膜的厚度为70μm,所述纳米纤维薄膜中纳米纤维的平均直径为500nm。
s4、将四氧化二氮按质量体积比20g:100ml溶于四氯化碳中,配制成氧化剂;将纤维素与所述氧化剂按质量比1:45混合后,在室温下反应48h,将得到的反应产物先用异丙醇洗涤两次,再用去离子水洗涤两次,得到氧化纤维素。
s5、将步骤s4得到的所述氧化纤维素与纳米氧化锌按质量比30:1混合后分散于去离子水中,得到质量分数为10%的悬浮液,并向所述悬浮液中加入碳二亚胺,使碳二亚胺与所述氧化纤维素中羧基的物质的量之比为2:1,得到后处理液;再将步骤s3得到的所述纳米纤维薄膜置于所述后处理液中浸渍10h,取出后用去离子水洗涤三次并烘干,得到纳米止血抗菌复合材料。
采用万能试验机对本实施例制备的纳米止血抗菌复合材料的力学性能进行测试:将纳米止血抗菌复合材料裁剪成40mm×10mm的大小,设置拉伸速率为10mm/min,拉伸夹具间距离为20mm,对纳米止血抗菌复合材料的断裂强度和断裂伸长率进行测试。
采用体外凝血测定法对本实施例制备的纳米止血抗菌复合材料的止血性能进行测试:将新鲜兔血与抗凝剂柠檬酸钠按照9:1的比例混合均匀,配制成抗凝兔血;将20mg本实施例制备的纳米止血抗菌复合材料置于试管中,在37℃下预热5min后向试管中加入1ml所述抗凝兔血,再加入500μl浓度为0.025mol/l的氯化钙溶液,并开始计时;每隔10s将试管取出并倾斜,观察血液是否流动,当血液不再流动时,记录时间,即为体外凝血时间;并设置不含本实施例制备的纳米止血抗菌复合材料的对照组,按同样的方式测试体外凝血时间。
采用振荡法对本实施例制备的纳米止血抗菌复合材料的抗菌性能进行测试:以金黄色葡萄球菌为例,通过测定振荡前后的活菌浓度,计算纳米止血抗菌复合材料的抑菌率。
通过上述方式,测得本实施例制备的纳米止血抗菌复合材料的断裂强度、断裂伸长率、体外凝血时间和抑菌率,结果如图1所示。
表1实施例1制备的纳米止血抗菌复合材料的性能数据
由表1可以看出,本实施例制备的纳米止血抗菌复合材料的断裂强度、断裂伸长率和抑菌率均较高,表明本实施例制备的纳米止血抗菌复合材料具有较优的机械性能和抗菌性能;此外,测试得未添加本实施例制备的纳米止血抗菌复合材料的对照组的体外凝血时间为230s,与本实施例测得的体外凝血时间相比可以看出,本实施例制备的纳米止血抗菌复合材料能够明显提高凝血时间,具有优异的止血效果。
实施例2~5与对比例1~2
实施例2~5与对比例1~2分别提供了一种血管外科用纳米止血抗菌复合材料的制备方法,与实施例1相比,不同之处在于改变了步骤s1中乙二胺与壳聚糖碳链上羧基的物质的量之比或步骤s2中3,4,5-三羟基苯甲酸中羧基与氨基化壳聚糖中氨基的物质的量之比,其他步骤均与实施例1一致,在此不再赘述。各实施例及对比例中步骤s1~s2对应的具体物质的量之比如表2所示。
表2实施例2~5及对比例1~2的步骤s1~s2对应的物质的量之比
其中,对比例1中未添加乙二胺,其与壳聚糖中羧基的物质的量之比用0:1进行表示,其他步骤均与实施例1一致;对比例2中未添加3,4,5-三羟基苯甲酸,其与氨基化壳聚糖中氨基的物质的量之比用0:1进行表示,其他步骤均与实施例1一致。
对实施例2~5与对比例1~2制备的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能进行测试,结果如表3所示。
表3实施例2~5与对比例1~2制备的产品性能参数
由表3可以看出,随着乙二胺添加量的增加,制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能都逐渐提高。对比例1中未添加乙二胺制得的纳米止血抗菌复合材料的各项性能均明显低于本发明实施例,主要是因为本发明通过将乙二胺接枝于壳聚糖的羧基上,使壳聚糖碳链上的羧基转化为氨基,从而有效提高壳聚糖碳链上的氨基数量;该氨基数量的增加不仅有利于提高邻苯三酚的接枝率,还能够促进制得的纳米纤维薄膜与氧化纤维素间的交联反应,从而明显提高本发明制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能。
同时,随着3,4,5-三羟基苯甲酸添加量的增加,制得的血管外科用纳米止血抗菌复合材料的止血性能和抗菌性能都逐渐提高,对机械性能的改善不够明显。对比例2中未添加3,4,5-三羟基苯甲酸制得的纳米止血抗菌复合材料的止血性能和抗菌性能均明显低于本发明实施例,主要是因为本发明通过将3,4,5-三羟基苯甲酸的邻苯三酚基团接枝于氨基化壳聚糖的氨基上,利用引入的邻苯三酚基团提高血管外科用纳米止血抗菌复合材料与组织间的黏附力,提高其生物相容性,促进止血及抗菌过程的进行,从而提高本发明制得的血管外科用纳米止血抗菌复合材料的止血性能和抗菌性能。
实施例6~9与对比例3
实施例6~9与对比例3分别提供了一种血管外科用纳米止血抗菌复合材料的制备方法,与实施例1相比,不同之处在于改变了步骤s3中聚氧化乙烯与邻苯三酚接枝壳聚糖的质量比或纺丝液的质量分数,其他步骤均与实施例1一致,在此不再赘述。各实施例及对比例中步骤s3对应的相关参数如表4所示。
表4实施例6~9及对比例3的步骤s3对应的相关参数
其中,对比例3中未添加聚氧化乙烯,其与邻苯三酚接枝壳聚糖的质量比用0:1进行表示,其他步骤均与实施例1一致。
对实施例6~9与对比例3制备的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能进行测试,结果如表5所示。
表5实施例6~9与对比例3制备的产品性能参数
由表5可以看出,随着聚氧化乙烯添加量及纺丝液质量分数的增加,制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能都逐渐提高。对比例3中未添加聚氧化乙烯制得的纳米止血抗菌复合材料的各项性能均明显低于本发明实施例,主要是因为本发明通过将将聚氧化乙烯与邻苯三酚接枝壳聚糖共混后进行静电纺丝,并经后处理脱除聚氧化乙烯,使后处理后的纳米纤维薄膜具有多孔结构,该多孔结构不仅能够促进氧化纤维素与壳聚糖之间交联反应的进行,还有利于纳米氧化锌的释放,并且能够有效提高制得的纳米止血抗菌复合材料对血液的吸附作用,从而提高本发明制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能。
实施例10~15与对比例4~5
实施例10~15与对比例4~5分别提供了一种血管外科用纳米止血抗菌复合材料的制备方法,与实施例1相比,不同之处在于改变了步骤s4中纤维素与氧化剂的质量比或步骤s5中氧化纤维素与纳米氧化锌的质量比、悬浮液的质量分数、浸渍时间,其他步骤均与实施例1一致,在此不再赘述。各实施例及对比例中步骤s4~s5对应的具体参数如表6所示。
表6实施例10~15及对比例4~5的步骤s4~s5对应的具体参数
其中,对比例4中未添加纤维素,则未进行步骤s4,且步骤s5中氧化纤维素与纳米氧化锌的质量比用0:1进行表示,其他步骤均与实施例1一致;对比例5中未添加纳米氧化锌,则步骤s5中氧化纤维素与纳米氧化锌的质量比用30:0进行表示,其他步骤均与实施例1一致。
对实施例10~15与对比例4~5制备的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能进行测试,结果如表7所示。
表7实施例10~15与对比例4~5制备的产品性能参数
由表7可以看出,随着氧化剂添加量的增加,制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能都逐渐提高,主要是因为本发明通过氧化剂对纤维素进行氧化,从而使得到的氧化纤维素具有较高的羧基含量,进而能够与具有丰富氨基的壳聚糖发生交联反应,并利用脱除聚氧化乙烯形成的多孔结构形成三维结构,使后处理液中的纳米氧化锌被包覆与形成的三维结构中。而对比例4中未添加纤维素,不仅失去了氧化纤维素的止血效果,还会因为缺乏氧化纤维素与纳米纤维薄膜间的交联作用,削弱了纳米止血抗菌复合材料的机械性能,并降低了纳米氧化锌的包覆量,从而导致对比例4制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能均明显低于本发明实施例。
同时,随着纳米氧化锌添加量及悬浮液质量分数和浸渍时间的增加,制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能也逐渐提高。对比例5中未添加纳米氧化锌制得的纳米止血抗菌复合材料的各项性能均低于本发明实施例,主要是因为本发明通过利用氧化纤维素与纳米纤维薄膜的交联反应使纳米氧化锌颗粒被均匀、充分地包覆,不仅能够利用纳米氧化锌的复合改善纳米止血抗菌复合材料的机械性能,还能够将其通过多孔结构进行释放,起到止血和抗菌的作用,从而提高本发明制得的血管外科用纳米止血抗菌复合材料的机械性能、止血性能和抗菌性能。
综上所述,本发明通过对壳聚糖依次进行氨基化及邻苯三酚接枝处理,再将其与聚氧化乙烯共混纺丝,得到了纳米纤维薄膜;再将所述纳米纤维薄膜浸入含有氧化纤维素与纳米氧化锌的后处理液中,制备了纳米止血抗菌复合材料。通过上述方式,本发明不仅能够有效提高壳聚糖碳链上的氨基数量,改善壳聚糖对组织的黏附作用,使制得的纳米纤维薄膜具有丰富的活性位点和优异的生物相容性;还能够使氧化纤维素与所述纳米纤维薄膜交联形成三维结构,并将纳米氧化锌均匀包覆其中,进一步提高纳米止血抗菌复合材料的止血性能和抗菌性能,同时改善其机械性能,具有较高的应用价值。
需要说明的是,本领域技术人员应当理解,本发明提供的血管外科用纳米止血抗菌复合材料的制备方法中,步骤s1中调节后的溶液ph值可以在5.0~5.5的范围内波动,且氨基化反应的反应温度可以在35~40℃间进行调整,反应时间可以在5~7h间进行调整;步骤s2中调节后的溶液ph值同样可以在5.0~5.5的范围内波动;步骤s3中得到的纳米纤维薄膜的厚度可以是50~100μm,该纳米纤维薄膜中纳米纤维的平均直径可以是400~600nm间的任意值,均属于本发明的保护范围。
以上所述仅用以说明本发明的技术方案,而非对其进行限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;凡是利用本发明说明书及附图内容所作的等效结构或等效流程变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!