将硫氢化物转化为单质硫的工艺的制作方法
本发明涉及在包含硫化物氧化细菌的水溶液中将硫氢化物(bisulphide)转化为单质硫的工艺的控制方法。
ep0958251b描述了一种生物处理含有硫化物的苛性碱水溶液的工艺。在硫化物氧化细菌存在下,硫化物部分转化为单质硫,并且部分转化为硫酸盐。根据该公开物,在氧气受限的情况下(即在do(溶解氧)值至少低于0.1mg·l-1)或在高硫化物加载速率下,硫化物微生物氧化为单质硫。在后一种情形中,生物质过度加载,并且作为中间产物形成硫。在低于250mg硫化物l-1·h-1的加载速率下,在增加的do值下,硫化物氧化细菌倾向于生成不希望的硫酸盐而不是生成硫,因为硫酸盐的形成为微生物生长提供了更多的能量。出于工艺稳定性,工艺优选地不在“过度加载条件”下运行。因此,需要化学计量的氧气供应以便将所有硫化物氧化成单质硫。由于当前可用的氧气传感器的检测极限为约0.1mg·l-1,因此它们不适合作为测量装置,因此在ep0958251b中描述了另一个参数。所述的控制氧气供应的方法是通过测量溶液的氧化还原(还原-氧化)电位。氧化还原电位是溶液接受或给予电子的倾向性的量度。该公开物描述了在硫化物氧化生物反应器中,实测的氧化还原电位主要由硫化物浓度决定。当氧化还原电位表明较高的硫化物含量时,通过添加较多的氧气来控制该工艺,反之亦然。
如ep0958251中所述的使用氧化还原电位的控制方法已证明是非常有用的控制所述工艺的工具,例如在小时尺度上。该方法的缺点是它不提供关于硫化物氧化细菌本身的生物活性的任何信息。可能的是,看起来恰当地将工艺控制在了氧化还原设定点之内,同时硫化物氧化细菌的生物活性在数天内逐渐下降到h2s去除效率降低的水平,过度消耗化学物质或甚至工艺停止。当前用于测量硫化物氧化细菌的生物学活性的方法是所谓的呼吸测试。在该测试中,从有氧反应器或其流出物中取出水溶液的样品并用氧气饱和。接下来,添加已知量的硫氢化物,并及时测量溶解氧的减少。该实验适当地重复进行三次。溶解氧的减少速率是硫化物氧化细菌将硫氢化物转化为单质硫和硫酸盐的能力的量度。该量度用于调整特别是有氧反应器中的工艺条件。
该呼吸测试是耗时的并且不适合于简单的在线测量和工艺控制。例如,只能在一天或几天之后获得结果,这对于控制工艺而言不是最佳的。此外,该测试不能代表wo2015/114069中所述的工艺。该公开物描述了一种工艺,其中在第一生物反应器中在厌氧条件下使硫氢化物和硫化物氧化细菌接触。在这些厌氧条件下,硫化物氧化细菌能够将硫氢化物转化为单质硫。在随后的有氧步骤中使硫化物氧化细菌再生。再生的硫化物氧化细菌被再循环到厌氧的第一生物反应器中。在该工艺中,在没有氧气的情况下,硫化物氧化细菌将硫氢化物转化为单质硫。由于呼吸测试是通过用氧气饱和水溶液进行的,因此结果是不能通过该测试获得该工艺的硫化物氧化细菌转化硫氢化物的能力的代表性测量。
本发明的目的是提供一种用于在包含硫化物氧化细菌的水溶液中将硫氢化物转化为单质硫的工艺的简单控制方法。
这通过以下控制方法来实现。一种用于在包含硫化物氧化细菌的水溶液中将硫氢化物转化为单质硫的工艺的控制方法,其中该控制方法包括:
提供包含阴极电极、阳极电极和参比电极的电化学电池,
其中所述电极与水溶液接触,
其中在阳极电极和阴极电极之间或者在阳极电极和参比电极之间施加电位,从而在阴极电极和阳极电极之间产生电流,
其中在保持阳极电极和阴极电极之间的恒定电位或在保持阳极电极和参比电极之间的恒定电位的同时,测量在阴极电极和阳极电极之间流动的电流,以及
响应于所测电流调整工艺。
申请人发现,对于早先描述的有氧工艺和厌氧工艺两者,在电化学电池中在设定的施加电位下测得的电流是硫化物氧化细菌将硫氢化物转化为单质硫的能力和/或硫化物氧化细菌将硫氢化物转化为不期望的硫酸盐的能力的可靠量度。测量可以在线或离线进行。可以实时测量电流,并提供有关硫化物氧化细菌将硫氢化物转化为单质硫的能力的实时信息。与使用现有技术呼吸测试和/或氧化还原电位的控制方法相比,这导致更直接和有效的工艺控制。
申请人已发现,在没有氧气的情况下,硫化物氧化细菌能够将硫氢化物氧化成单质硫。硫化物的氧化可以用下式描述:
hs-+bac+→1/8s8+h++bac-(1)
这里,bac+是氧化的硫化物氧化细菌。当硫氢化物被氧化时,该细菌被还原(bac-)。为了使细菌再生,使它们与例如提供给例如再生器反应器的氧气接触。氧气的还原由下式给出:
bac-+1/2o2+2h+→bac++h2o(2)
我们现在已发现还原的硫化物氧化细菌(bac-)能够将电子转移到电化学电池中的阳极。该发现使人们能够使用该电池并在施加电位时测量电流,该电流是生物活性(即硫化物氧化细菌将硫氢化物转化为单质硫的能力)的量度。
在根据本发明的工艺中由电化学电池测量的电流可以例如用于:
(i)提供有关细菌再生速率的信息,并且其中可以响应于所测电流通过例如添加或多或少的氧化剂(例如氧气)来调整该再生过程,
(ii)提供有关细菌总活性和/或生物质浓度的信息,其中可以通过添加或多或少的营养物来调整该工艺,
(iii)提供有关加载的水溶液中溶解的硫氢化物浓度的信息,并且其中可以通过向所述加载的水溶液中添加或多或少的氧化的硫化物氧化细菌来调整该工艺,和/或
(iv)提供有关细菌形成不希望的副产物硫酸盐的电位的信息,其中可以通过减少提供给该工艺的电子受体(例如氧气和硝酸盐)来调整该工艺。
所述电化学电池包括阴极电极、阳极电极和参比电极。可以存在更多的电极,例如以便在不同条件下同时测量电流。电极与水溶液接触。在保持阳极电极和阴极电极之间的恒定电位或者在保持阳极电极和参比电极之间的恒定电位的同时,测量在阴极电极和阳极电极之间流动的电流。在施加的电位下测得的电流将提供电子从细菌到阳极的转移速率的量度,并因此将反映细菌的活性。测得的电流将提供以下的量度:细菌吸收硫化物的程度以及硫化物氧化细菌存储电荷的程度。如果电流减小,则测量到硫化物氧化细菌活性的降低,反之亦然。
施加的电位适宜在-1.0v和1v之间,优选在-0.6v和0.4v之间,以相对于ag/agcl参比的阳极电位表示。所测的电流从而不为零,适宜为大于1μa,并且优选为大于0.001a/m2阳极电极面积。
优选地,在改变在阳极电极和阴极电极之间或者在阳极电极和参比电极之间施加的电位的同时,测量在阴极电极和阳极电极之间流动的电流。因此,对于施加的电位而言在多于一个不同值处测量电流。优选地,对于施加的电位的至少一个值测得的电流大于0.001a/m2阳极电极面积。可以按线性扫描伏安法、循环伏安法或极化曲线进行的该测量是有利的,因为其提供了根据电极电位和电流快速测量生物活性。这提供了关于细菌吸收硫化物的程度的算子(operator)或工艺控制算法输入,其可用于在使硫化物氧化细菌再生时调节氧气供应。
可通过恒电位仪、电阻和/或外部电源以本领域技术人员已知的方式控制电化学电池。
阴极电极可以由任何导电材料制成,例如碳基电极或钛基电极,具有或不具有催化剂涂层以提高反应速率。阴极的优选金属是铂,因为其作为产氢催化剂的良好性能。阳极可以由任何导电材料制成,例如具有涂层的钛、碳、石墨。阳极的优选材料为石墨。参比电极可以是任何类型,例如ag/agcl电极,更适宜为饱和甘汞电极(sce)。
优选在不存在溶解氧的情况下进行测量,并且优选在厌氧条件下进行测量,以使与电极上的电子受体邻近的其它电子受体对测量电位的影响最小化。可以在线或离线进行测量。
在包含硫化物氧化细菌的水溶液中将硫氢化物转化为单质硫的工艺优选地至少包括以下步骤:
(a)在水溶液中使硫氢化物与氧化的硫化物氧化细菌接触,以获得还原的硫化物氧化细菌和单质硫,
(b)氧化该还原的硫化物氧化细菌,以获得氧化的硫化物氧化细菌,
(c)在步骤(a)中使用步骤(b)中获得的氧化的硫化物氧化细菌,以及
(d)从步骤(a)和/或步骤(b)中获得的水溶液中分离出单质硫。
如上所述的工艺可以是诸如例如在先前提及的ep0958251b、wo2015/114069或us5976868中所述的工艺。如这些公开物中所述,可以获得步骤(a)的包含硫氢化物和氧化的硫化物氧化细菌的水溶液。所述溶液可以通过如下方式获得:将氧化的硫化物氧化细菌的水溶液与包含硫氢化物的废苛性碱溶液或与用于从酸性气流中吸收硫化氢或其它还原的硫化合物的碱性吸收溶液合并。作为替代,所述水溶液可以通过如下方式来获得:用注射器从高浓度或基本上纯的硫化氢气体将硫化氢溶解到包含氧化的硫化物氧化细菌的水溶液中。
优选地,通过使包含氧化的硫化物氧化细菌的水溶液与包含硫化氢的气体接触来进行步骤(a)。优选在气体吸收器中进行该接触,其中使包含氧化的硫化物氧化细菌的水溶液与包含硫化氢的气体接触以获得加载的水溶液。在这样的气体吸收器中,气体和水溶液彼此逆流接触。发现通过在氧化的硫化物氧化细菌存在下进行该接触,实现了更有效的硫化氢吸收。在该气体吸收器中将发生硫氢化物到单质硫的部分转化。为了实现更高的转化,优选将加载的水溶液提供给生物反应器。通过将气体吸收器与该生物反应器组合,总停留时间能够实现可接受的单质硫转化。其它优点是可以向该生物反应器提供新鲜的氧化的硫化物氧化细菌,以进一步增强这种向单质硫的转化。涉及上述气体吸收器和任选的生物反应器的步骤(a)优选在厌氧条件下进行。
在(a)中,水溶液中的硫氢化物浓度并不关键。可以使用硫氢化物浓度(以硫表示)高达20克/升或更高的溶液。在该计算中,还包括已被硫化物氧化细菌吸收的硫。优选地,水溶液中的硫氢化物浓度在100mg/l至15g/l的范围内,更优选150mg/l至10g/l。
包含硫氢化物的水溶液与氧化的硫化物氧化细菌的接触(a)适宜在厌氧条件下进行。厌氧条件是指不存在分子氧。在这样的接触期间不供应分子氧和/或不存在分子氧。优选地,这样的接触在不存在其它氧化剂例如硝酸盐的情况下进行。厌氧条件在这里是指“不存在分子氧”,其中水溶液中的分子氧的浓度为至多1μm,更优选为至多0.1μm。
硫化物氧化细菌可以是任何硫化物氧化细菌,优选地,所述硫化物氧化细菌是以下菌株之一:卤硫杆菌属(halothiobacillus)、硫碱微菌属(thioalkalimicrobium)、硫碱螺旋菌属(thioalkalispira)、硫碱杆菌属(thioalkalibacter)、硫碱弧菌属(thioalkalivibrio)、碱湖生菌属(alkalilimnicola)、碱螺菌属(alkalispirillum)和相关细菌。这些嗜盐嗜碱的硫化物氧化细菌适用于该工艺。细菌可以原样使用,即可以作为水溶液中的浮游细胞形式存在,或者可以承载在分散的载体上。
包含硫氢化物的水溶液与氧化的硫化物氧化细菌的接触(a)可以在适合于将硫氢化物生物氧化成单质硫的关于温度、压力和水力停留时间的任何合适的条件下进行。优选地,温度在10-60℃的范围内,更优选地在20-40℃的范围内。压力适宜地在0-100巴的范围内,更优选在大气压至80巴的范围内。水溶液的ph适宜地在7-10的范围内,更优选在7.5-9.5的范围内。以阳离子的摩尔浓度表示的(优选以钠和/或钾的总阳离子摩尔浓度表示的)水溶液的盐度优选为0.3-4m,更优选为0.5-1.5m。该水溶液可包含几种不同化合物的痕量化合物,例如铁、铜或锌,作为硫化物氧化细菌的营养物。
在连续工艺情形中的步骤(a)中的停留时间或者在分批工艺中的接触时间优选为至少3分钟,更优选为至少5分钟,更优选为至少10分钟。最大停留时间并不关键,但是出于实际原因,停留时间优选为至多2小时,更优选为至多1小时。优选地,作为全部硫化物氧化细菌的一部分的氮与硫氢化物总量的重量比为至少0.1mgn/mg硫氢化物,优选为至少0.5mgn/mg硫氢化物,更优选为至少0.7mgn/mg硫氢化物。
在步骤(a)中,气体吸收器中的接触可以通过吸收硫氢化物的公知方法进行。气体温度可以在0-100℃的范围内,优选在20-80℃的范围内,更优选在25-50℃的范围内,并且压力在0-100巴的范围内,优选为大气压至80巴。液体碱性吸收剂可以是已知适用于吸收硫化氢(即已知会溶解硫化物)的任何液体碱性吸收剂。合适的液体碱性吸收剂的实例为碳酸盐、碳酸氢盐和/或磷酸盐的溶液,更优选为包含碳酸盐和碳酸氢盐的缓冲溶液。特别优选为包含碳酸钠或碳酸钾和碳酸氢钠或碳酸氢钾的缓冲溶液,更特别为包含碳酸钠和碳酸氢钠的缓冲溶液。供至吸收塔上部的液体碱性吸收剂的ph优选在7-10的范围内,更优选在7.5-9.5的范围内。
优选地,该吸收在吸收塔中进行,其中使含硫化氢的气流在吸收塔中与步骤(b)中获得的全部或优选部分液体流出物接触。将步骤(b)中获得的部分液体流出物直接再循环到步骤(a)的生物反应器中。步骤(b)的液体流出物可以在被再循环到步骤(a)的气体吸收器和/或生物反应器之前进行步骤(d)。可以清除步骤(d)中获得的部分贫含单质硫的流出物。步骤(d)可以通过公知的工艺步骤进行,例如在us5976868中所述的硫分离器中。
本发明的工艺特别适合于控制上述工艺的步骤(b)。对于有效的工艺,重要的是硫化物氧化细菌将硫氢化物转化为单质硫的能力高于某些最小值,并且更优选在恒定值附近。现在可以通过使用电化学电池测量电流来快速且准确地测量该能力。因此,优选通过使电化学电池的电极与步骤(b)中获得的包含氧化的硫化物氧化细菌的水溶液接触来测量由电化学电池所测的电流。如果电流太低,则可以增加步骤(b)中的氧化速率以提高该能力。以这种方式,可以确保在例如气体吸收器中吸收硫化氢的能力足够,并且所得气体中的硫化氢水平低于所需水平。
还可以通过使电化学电池与在上述气体吸收器中获得的加载水溶液接触而进行该工艺。特别是在将加载的水溶液提供给在厌氧条件下运行的生物反应器的工艺中。以这种方式,能够控制从步骤(b)直接再循环到该厌氧运行的生物反应器中的氧化的硫化物氧化细菌的量。加载的水溶液可以包含与已经被细菌本身吸收的硫氢化物邻近的溶解的硫氢化物。如果加载的水溶液含有高水平的溶解的硫氢化物,则将更多的氧化硫化物氧化细菌直接再循环到在厌氧条件下运行的生物反应器中可能是有利的。以这种方式,在厌氧条件下运行的生物反应器中,加载的水溶液中的溶解硫氢化物的转化可得以增强。可以使用基于分析方法的传感器(如化学传感器)对加载的水溶液测量溶解的硫氢化物的含量。
除了测量电流之外,还可以测量细菌的浓度。可以用hachlange比色皿测试lck138,根据370nm处硝基酚的吸光度,以有机氮(n-organic)的总量来测量细菌的浓度。通过测量细菌浓度以及电流,可发现该工艺需要或多或少的营养物。因此,响应于所测电流和所测细菌浓度,通过调整添加到工艺中的营养物的量来适当地调整该工艺。
适宜地,通过使还原的硫化物氧化细菌与氧化剂接触来进行步骤(b)。该氧化剂可以是氧气或硝酸盐。在该工艺中,优选通过使电池的电极与步骤(b)中获得的水溶液接触,通过电化学电池来测量电流,并且其中响应于所测电流通过调节步骤(b)中的氧化速率来调整该工艺。
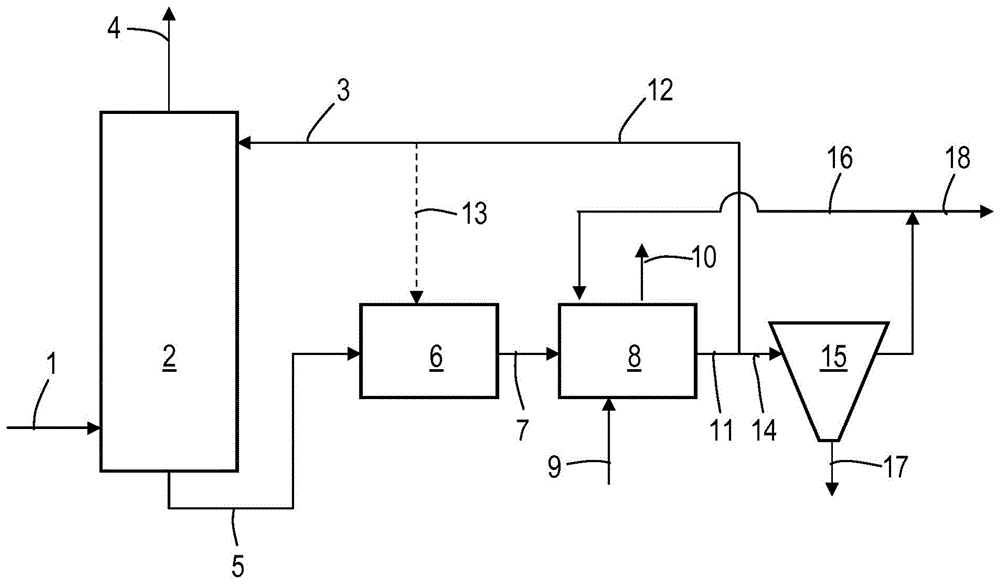
将通过图1来说明本发明,图1示出了可以由根据本发明的方法控制的工艺。经由管线1向气体吸收器2中供应包含硫化氢和二氧化碳的气体。还经由管线3向所述气体吸收器2中供应进一步包含氧化的硫化物氧化细菌的碱性水溶液。经由管线5从所述气体吸收器2中排出包含硫氢化物化合物、硫化物氧化细菌和单质硫的加载水溶液,并经由管线4从所述气体吸收器中排出具有较低硫化氢含量的气体。在生物反应器6中,将经由管线5供应的加载水溶液保持在厌氧条件下持续至少足以将溶解的硫氢化物的浓度降低至5mm以下的时间。经由管线13向所述第一生物反应器6供应进一步包含氧化的硫化物氧化细菌的碱性水溶液。在再生器8中,经由管线7将从生物反应器6排出的加载水溶液与经由管线9供应的作为氧化剂的空气接触,以氧化所述还原的硫化物氧化细菌。经由管线11,包含氧化的硫化物氧化细菌的液体流出物经由管线12排放到气体吸收器2中,经由管线13直接排放到生物反应器6中,以及排放到分离器15中。在分离器15中,将沉淀的固体单质硫从流出物中分离,从而得到贫硫的流出物(其经由管线16再循环到再生器8)和固体单质硫(其经由管线17从工艺中排出)。一部分贫硫的流出物经由管线18从工艺中清除。可以使用本发明工艺的3电极电池测量的优选水性组合物是管线11、12、3、13、5和7中的水溶液。最优选为管线11或12和5中的水溶液。
实施例1
在该实施例中,使用由恒电位仪控制的电化学电池,如图2所示。该电池包含石墨棒作为阳极(a),铂箔作为阴极(c),以及ag/agcl电极作为参比电极(r)。在测量期间,对于已知的阳极电位(相比于参比)测量阳极与阴极之间的电流(电子流)。对于在图1的管线12中采样的典型水溶液,在改变阳极和参比电极之间的电位时使用该3-电极电池测量电流。实验以所谓的线性扫描进行。结果示于图3,其中所测电流在y轴上,阳极和参比电极之间的电位在x轴上。在该测量中,初始阳极电位为-0.6v,并以1mv/s增加直至0.4v。如果所测电流为负(<0ma),其表示电子从阴极流向阳极;如果电流为正(>0),则电子从阳极流向阴极,表明电子从细菌中提取出来。从下图可以得出,阳极电位为-0.45v和更高时,还原的细菌将它们的电子转移到阳极。阳极电位越高,细菌和电极之间的电子转移的驱动力就越高,电流也就越大。在一定的阳极电位下,由于最大的电荷转移速率或扩散限制而达到最大电流。当电位比-0.45v更负时,电流为负并且电子从阴极向阳极移动。在这种情况下,电子转移到细菌。如此测得的细菌吸收电子的能力也是适于调整该工艺的重要工艺性能。
实施例2
使用与实施例1相同的3电极电池,在图1的管线11中采样的典型加载水溶液的样品的时间测量电流。在0.1v的固定阳极电位下进行测量。从新样品中,从加载的水溶液分离出细菌,并进行相同的测量。结果示于图4中,其中上面的两条线表示对于原始加载溶液测得的电流,下面的两条线是对于没有细菌的加载溶液测得的电流。这表明与没有细菌的溶液相比,可以从有细菌的溶液提取更多的电荷,表明细菌已经存储了可以在阳极处释放的电荷。
实施例3
在该实施例中,使用含有嗜盐嗜碱硫化物氧化细菌(ha-sob)的污泥a(其得自包括吸收塔和曝气生物反应器的商业运行的生物脱硫工艺)和含有嗜盐嗜碱硫化物氧化细菌(ha-sob)的污泥b(其得自根据wo2015114069的包括吸收塔、厌氧和曝气生物反应器的中试规模工艺(中试设备))。两种污泥的样品均取自曝气的生物反应器。两种样品均具有ph8.5的碳酸氢盐和碳酸盐组成的培养基。污泥a的以总n计的生物质浓度为72.4mgn/l,而污泥b为29.2mgn/l。
实验分三个步骤进行。将生物质主动地曝气持续>12小时的时段。当氧气水平保持饱和时,通过用n2冲洗从溶液中除去氧气。然后,用na2s.~3h2o形式的0.2mm硫化物(analarnormapur,vwr,分析级)供应生物质。使用0.45um过滤器过滤溶液,并在5分钟后测量硫化物浓度。
在电化学电池中测试生物质产生电流的能力。单室电池的总液体体积为50ml(图2)。阳极(20)由碳制成,与液体接触的外部面积为3cm2。阴极(21)由pt箔(2.82cm2)制成;用铂丝建立到电池(22)外部的连接。使用ag/agcl,3mkcl参比电极(+0.205v,相对于she),并经由毛细管(24)离子连接到溶液。所有电位都相对该参比电极报告。使用磁力搅拌器(23)以确保良好的质量传递,并且在室温下运行该电池。通过如下方式用不含sob的溶液进行对照实验:以10000rpm将溶液离心10分钟,并测试电化学电池中的上清液。
使用计时电流法通过恒电位仪(iviumstat,eindhoven,荷兰)相对于参比电极控制阳极电位,阳极电位控制在+0.1v,相对于参比电极。在-0.6至+0.4v的阳极电位范围内以1mv/s的扫描速率得到线性扫描。
在该实施例中,以na2s.~3h2o的形式添加硫化物(analarnormapur,vwr,分析级)。将1ml厌氧原液添加到80ml4%(w/v)naoh和1ml30%(w/v)nh4oh中,以稳定所有存在的溶解硫化物。
以回收的总电荷除以硫化物形式添加的总电荷来计算阳极库仑效率。为了评价ha-sob对溶解的硫化物的去除能力以及在没有外部电子受体(氧气)的情况下它们的电子穿梭能力,使污泥经受上述三步制备过程。在添加0.2mm硫化物之后,对于污泥a的硫化物浓度从最初的0.2mm降低到5分钟后的0.056mm,而对于污泥b的硫化物浓度降低到检测限以下。如果没有sob,还观察到硫化物浓度从1.2mm略微降低到0.9mm,表明如果没有微生物活性,也有一些硫化物被转化。按生物质的量表示,对于污泥b的硫化物吸收是5.2mms/gn,而对于污泥a的硫化物吸收是0.6mms/gn。
测试了ha-sob的使用电极作为硫化物氧化或储存电子释放的电子受体的能力。在相对于ag/agcl为+0.1v的阳极电位下在电化学电池中测量电流。图5示出了污泥b(左侧的两个柱形体)和污泥a(右侧的柱形体)的以mc为单位的测量电荷。较小的白色柱形体分别表示仅测量污泥b和a的培养基。在没有硫化物和氧气的情况下,从污泥b(测量数:n=4)和污泥a(测量数:n=2)中回收电荷,包括标准误差。污泥b的总电荷也较高,尽管其生物质浓度低于污泥a。对于没有细菌的培养基,最初600秒的电荷回收率最小,这表明ha-sob在电子转移中起主要作用。最初600秒的平均电流密度,对于污泥b为481ma/m2,对于污泥a为239ma/m2。
在相对于ag/agcl为0v和+0.1v下,随阳极电位的变化测量电流。表1示出了所测电荷,标准化至两种污泥的生物质的量(mc/mgn)。大多数电荷在+0.1v时回收,并且总电荷随着阳极电位的降低而降低。污泥b再次显示出比污泥a更高的电流密度。
表1
实施例4
按实施例3中所述对两种类型的ha-sob(污泥a和污泥b)以及它们的两种培养基进行线性扫描,阳极电位范围在-0.6v和+0.4v之间(相对于ag/agcl)。对于污泥b在阳极电位>-0.45v时,以及对于污泥a在阳极电位>-0.48时,电流从负值变为正值。在正电流下,从ha-sob中回收电。电流随着阳极电位的增加而增加,并且在更正的阳极电位下,污泥b产生的电流大于污泥a。在-0.48至-0.3v(相对于ag/agcl)之间的更负的阳极电位下,污泥b产生的电流大于污泥a。在没有ha-sob的情况下,电流显著低于使用ha-sob时的电流。图6示出结果,其中线a为污泥b,线b为添加0.2mm硫化物的污泥b的培养基,线c为污泥a,线d为污泥a的培养基,以及线e为污泥b的培养基。
如实施例3和4中所述的测量结果可用于(全规模)生物脱硫工艺的控制。生物活性(即如实施例3中所述的电流产生的测量)可以例如用于确定系统能够处理的硫化物的量。基于此,能够调节向系统的总硫化物加载量(与酸性气体中的气流和h2s浓度成正比)。当发现细菌活性受限时,可以增加对细菌生长至关重要的含微量元素的营养物投放量,以刺激细菌生长。
此外,在不同阳极电位下的活性测量(实施例4)揭示了系统朝向硫和硫酸盐形成的选择性如何。该信息可用于优化空气供应量,例如通过调节orp设定点(氧化还原电位设定点),该设定点用于向生物反应器供应氧气。当活性测试表明硫酸盐形成的可能性增加时,可以降低orp设定点。
- 还没有人留言评论。精彩留言会获得点赞!