含胆甾醇的香豆素类衍生物及其合成和应用的制作方法
本发明涉及含胆甾醇的香豆素类衍生物及其合成和应用,属于生物有机合成领域。
背景技术:
香豆素类化合物是指以苯并a-吡喃酮结构为母环的化合物,生物活性广泛,如抗hiv,抗氧化性,抗细菌,抗病毒,抗凝血,抗结核,抗肿瘤等。华法林钠,是最早涉及抗癌领域的香豆素药物,能显著的抗v2癌细胞。香豆素具有强的分子内电子转移能力,且分子中存在c=c、c=o双键增加了分子的共轭程度使其具有较大的共轭体系,内酯结构增强了分子刚性,使得香豆素类衍生物具有荧光,而且光量子稳定性及光致发光量子效率都比较高,使其在食品、燃料、香料、医药、农药、光电材料、超分子识别等众多领域具有广泛的潜在应用。胆甾醇与细胞膜、胆酸、维生素d的形成息息相关,对动物体作用重大,并且有些胆甾醇衍生物具有抗肿瘤、抗癌活性。胆甾醇上具有一个羟基官能团,酯化修饰得到了许多衍生物。羟基固醇类的水溶性衍生物对小鼠krebsii具有强的抗癌作用。mohamedramadanelsayedaly等人合成了胆甾醇三唑衍生物表现出明显的抗真菌活性及细胞毒性。
技术实现要素:
本发明提供一类含胆甾醇的香豆素类衍生物的合成及应用。将修饰后的胆甾醇引入香豆素,研发具有抗癌效果的新药。
本发明所述的含胆甾醇的香豆素类衍生物,(1)用不同水杨醛合成不同的香豆素衍生物,研究药物分子的构效关系。(2)将香豆素与胆甾醇通过酰化反应或dcc法酯化反应生成具有抗癌活性的新型含胆甾醇的萘酰亚胺类衍生物的目标化合物。
本发明解决上述技术问题所采用的技术方案是:含胆甾醇的香豆素类衍生物,其化学分子结构通式c如下:
通式c中:
r选自h原子、n,n-二乙胺基、甲基、甲氧基。
本发明提供上述含胆甾醇的香豆素类衍生物的制备方法,以5位取代的水杨醛为起始原料,与丙二酸二乙酯经knoevenagel反应得到7-r-香豆素-3-甲酸乙酯,碱性水解、酸化得到7-r-香豆素-3-羧酸,最后生成目标产物有两种途径,途径一:7-r-香豆素-3-羧酸继续与氯化亚砜反应生成7-r-香豆素-3-甲酰氯,再与胆甾醇通过酰化反应得到含胆甾醇的香豆素类衍生物的目标化合物;途径二:7-r-香豆素-3-羧酸直接与胆甾醇通过dcc法发生酯化反应生成含胆甾醇的香豆素类衍生物的目标化合物。
所述r选自h原子、n,n-二乙胺基、甲基、甲氧基。
上述的含胆甾醇的香豆素类衍生物的合成路线如下:
本发明提供上述含胆甾醇的萘酰亚胺类衍生物在抑制癌细胞药物中的应用。所述的癌细胞株为hepg2(人肝癌细胞)、hela(人宫颈癌细胞)、mcf-7(人乳腺癌细胞)、a549(人肺癌细胞)。
用上述合成的含胆甾醇的萘酰亚胺类衍生物用mtt比色法对hepg2(人肝癌细胞)、hela(人宫颈癌细胞)、mcf-7(乳腺癌细胞)、a549(肺癌细胞)进行体外抑制肿瘤细胞生长活性的测定,结果表明,该类化合物对肝癌、宫颈癌、乳腺癌、肺癌等癌细胞具有抑制生长的效果。
用mtt比色法将hepg2(人肝癌细胞)、hela(人宫颈癌细胞)、mcf-7(乳腺癌细胞)、a549(肺癌细胞)以5×103个细胞/孔接种于96孔板内,培养24h后加入梯度浓度药液200μl/孔,对每个肿瘤细胞株,设置5个复孔,另设无细胞调零孔;肿瘤细胞在37℃、5%co2条件下培养24h后,加20μl的mtt液继续培养4h后,用移液枪小心地吸出上清液,加入dmso溶解结晶,然后用酶标仪测od490值,利用寇式改良法计算被测物对癌细胞生长的ic50值。
本发明所述的含胆甾醇的香豆素类衍生物具有液晶相,可用于液晶显示屏。
附图说明
图1为化合物c1的液晶相图;
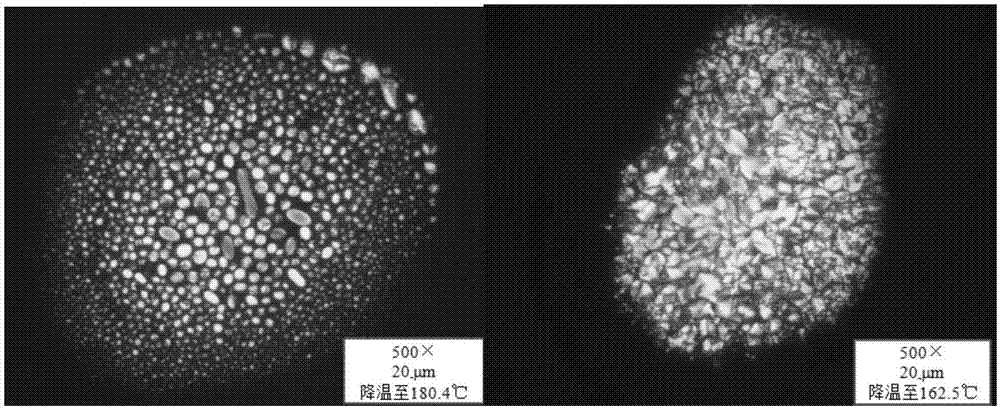
图2为化合物c2的液晶相图。
具体实施方式
通过实施例对本发明作进一步的说明。
实施例1(途径一)
香豆素-3-甲酸胆甾醇酯(c1)的合成
(1)中间体7-r-香豆素-3-甲酸乙酯的合成:
香豆素-3-甲酸乙酯(中间体1)的合成:
干净的三口烧瓶,45ml无水乙醇作溶剂,依次加入7.86ml水杨醛、13.50ml丙二酸乙二酯、0.9ml哌啶、1-3ml冰醋酸,装上带有无水氯化钙干燥管的球形冷凝管,加热回流2-5h,停止加热,冷却至室温后转移至烧杯,冰水浴中冷却,使产物充分结晶析出,然后减压抽滤,并用冷却过的50%的乙醇溶液洗涤晶体2~3次,得到白色晶体12.4g,产率75.6%。熔点:124.0-125.0℃。
(2)中间体7-r-香豆素-3-羧酸的合成:
香豆素-3-羧酸(中间体2)的合成:
在干燥的圆底烧瓶中依次加入上述所得的4.0g中间体55.0g氢氧化钠、25ml95%的无水乙醇和10ml水,油浴回流,待酯全部溶解后继续回流20min。
停止加热,冷却至室温,将反应液转移到锥形瓶中,滴加稀盐酸,边滴边震荡,可看到有白色晶体析出,冰水浴冷却使结晶完全。抽滤、洗涤、干燥,得产物约2.87g,产率82.5%。熔点:190.0-191.0℃。
(3)中间体7-r-香豆素-3-甲酰氯的合成:
香豆素-3-甲酰氯(中间体3)的合成:
在干燥的50ml圆底烧瓶中加入2.87g中间体6,20ml新蒸的socl2,油浴加热回流2h,tlc跟踪至反应结束,减压蒸出残余的socl2,得到淡黄色固体3.05g,产率96.8%。熔点:146.0-147.0℃。
(4)终产物7-r-香豆素-3-甲酸胆甾醇酯的合成:
终产物香豆素-3-甲酸胆甾醇酯(c1)的合成:
在25ml两口瓶中,20ml二氯甲烷作溶剂,加入0.50g中间体7,置于冰水浴中搅拌使溶解;再加入0.84g(2.17mmol)胆甾醇,搅拌1h,再缓慢加入0.3ml三乙胺,室温下搅拌反应12h,tlc跟踪。减压蒸发除去溶剂,柱层析法提纯(洗脱液ch2cl2),得白色固体d30.80g。产率:66.5%。
+esims(m+na):c37h50o4,计算值:558.3709,实测值:558.3599。
1hnmr(400mhz,cdcl3)δ8.44(s,1h),7.63–7.56(m,2h),δ7.29(t,j=7.9hz,2h).,5.37(d,j=3.6hz,1h),4.88–4.78(m,1h),2.44(d,j=7.8hz,2h),2.01–1.70(m,7h),1.60–1.39(m,7h),1.35–1.27(m,3h),1.22–1.05(m,8h),1.02(s,4h),0.88(d,j=6.4hz,3h),0.83(d,j=6.5hz,6h),0.64(s,3h).
13cnmr(126mhz,cdcl3)δ162.34(s),156.65(s),155.14(s),148.08(s),139.43(s),134.18(s),129.44(s),124.78(s),123.00(s),118.74(s),117.93(s),116.77(s),75.77(s),56.69(s),56.15(s),50.03(s),42.33(s),39.63(d,j=26.6hz),38.04(s),37.00(s),36.64(s),36.20(s),35.80(s),31.90(d,j=8.7hz),28.24(s),28.02(s),27.75(s),24.30(s),23.85(s),22.71(d,j=32.0hz),21.06(s),19.37(s),18.74(s),11.87(s).
化合物c1属于液晶分子,在225.1-108.4℃时出现液晶相如图1所示。
实施例2(途径二)
7-(二乙氨基)香豆素-3-甲酸胆甾醇酯(c2)的合成
(1)7-(二乙氨基)香豆素-3-甲酸乙酯(中间体4)的合成:
除用4-(二乙氨基)-水杨醛代替水杨醛外,其它操作同实施例1中间体1的合成,得中间体4,黄色固体,产率90.8%。熔点:220.4-222.3℃。
(2)7-(二乙氨基)香豆素-3-甲酸(中间体5)的合成:
除用中间体4代替中间体1,其它操作同实施例1中间体2的合成,得黄色固体,产率80.8%。熔点:224.0-224.5℃。
(3)终产物7-r-香豆素-3-甲酸胆甾醇酯的合成:
7-(二乙氨基)香豆素-3-甲酸胆甾醇酯(c2)的合成:
将0.71g(1.84mmol)胆甾醇和0.40g(1.53mmol)7-(二乙氨基)香豆素-3-甲酸(中间体9)的溶解在20ml干燥的二氯甲烷中,常温搅拌5min,然后加入0.02g(0.18mmol)dmap和0.38g(1.84mmol)dcc继续在室温下搅拌反应,tlc跟踪,16h后停止。减压蒸发除去溶剂,柱层析提纯(洗脱液ch2cl2:ch3cooc2h5=20:1)。得橘黄色固体d40.44g,收率:45.8%。
+esims(m+h):c41h59no4,计算值:629.4444,实测值:629.4498。
1hnmr(400mhz,cdcl3)δ8.34(s,1h),7.31(d,j=9.0hz,1h),6.55(d,j=9.0hz,1h),6.40(s,1h),5.33(t,j=11.0hz,1h),4.85–4.72(m,1h),3.40(q,j=6.9hz,4h),2.42(d,j=7.7hz,2h),1.93(dt,j=28.8,20.1hz,6h),1.70(dd,j=23.5,11.4hz,2h),1.56–1.39(m,8h),1.30(dd,j=23.5,16.1hz,6h),1.18(t,j=7.1hz,9h),1.01(s,4h),0.87(d,j=6.3hz,3h),0.82(d,j=6.6hz,6h),0.63(s,3h).13cnmr(126mhz,cdcl3)δ163.40(s),158.32(d,j=19.7hz),152.78(s),148.79(s),139.79(s),130.97(s),122.65(s),109.39(d,j=16.8hz),107.65(s),96.72(s),74.74(s),56.42(d,j=70.4hz),50.04(s),45.07(s),42.32(s),39.64(d,j=28.8hz),38.21(s),37.08(s),36.65(s),36.19(s),35.80(s),31.91(d,j=7.6hz),28.24(s),28.01(s),27.87(s),24.29(s),23.84(s),22.70(d,j=32.1hz),21.05(s),19.39(s),18.73(s),12.45(s),11.86(s).
化合物c2属于液晶分子,在180.4-162.5℃时出现液晶相如图2所示,可用于液晶显示屏和电子书显示器。
应用例1:体外抗肿瘤活性抑制实验
本章实验选用hepg2(人肝癌细胞)、hela(人宫颈癌细胞)、mcf-7(乳腺癌细胞)、a549(肺癌细胞)四种癌细胞对目标化合物c1-c2进行测试.采用mtt法计算相应的ic50值。
表2化合物c1-2对hepg2,hela,mcf-7,a549细胞株的ic50值
tab.2thevaluesofic50ofcompoundsc1-2againsthepg2,hela,mcf-7,a549
如上表所示,化合物c1、c2对hepg2,hela,mcf-7,a549四种癌细胞均在微摩尔级别表现出良好的抗肿瘤效果。化合物c1、c2对a549细胞株的抑制效果最好,ic50分别是26.42μm、23.74μm。化合物c1对mcf-7和a549的抑制作用低于化合物c2,而对hepg2和hela的抑制作用却高于化合物c2。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种1‑(4‑氯苯基)‑2‑吡啶‑1‑基‑1‑基乙酮溴化物的制备方法与制造工艺
- 一种1‑(4‑溴苯基)‑2‑吡啶‑1‑基‑1‑基乙酮溴化物的制备方法与制造工艺
- 一类噁唑并香豆素衍生物在农药方面的应用
- 一种香豆素衍生物、其制备方法以及由其制得的水凝胶的制作方法
- 3-(2-芳基-1h-吲哚-3-基)-4-羟基香豆素衍生物及其合成方法
- 一种羟甲香豆素的药物组合物及其医药用图
- 含卤素或苯并咪唑类功能基团的香豆素类衍生物及其制备方法和应用
- 一种有机叠氮与香豆素合成3-氨基苯并吡喃-2-酮类衍生物的新方法
- 香豆素-3-羧酸/1-辛烷磺酸/LGdH复合体及其合成方法
- 香豆素-3-羧酸/1-辛烷磺酸/LGdH复合体及其合成方法