一种净化养殖水体中氨的玫瑰红红球菌菌株XHRR1及其应用的制作方法
本发明属于玫瑰红红球菌技术领域,具体涉及一种净化养殖水体中氨的玫瑰红红球菌菌株xhrr1及其应用。
背景技术:
在高密度集约化的水产养殖模式中,水体环境的高效控制是整个生产过程的关键技术环节之一。氨氮对水产动物有严重毒害作用,在高密度养殖水体中容易大量积累(周平2013),因此有效调控水体中有害氮素的含量极其重要(刘兴国2011)。目前国内外常见的处理方法主要有物理、化学和生物等三种方法。物理法利用固体的吸附能力净化氨氮,常用物料主要有沸石粉、白云石粉、珊瑚沙等,但由于其吸附净化能力有限(饶力2016),在养殖生产过程中多通过排换水的方式缓解氨氮等有害氮素对养殖生物的胁迫。化学法通过应用化学氧化剂的强氧化效应净化水体中的有害物质,但在生产应用时无法彻底根除潜在污染源的积累问题,往往需要多次使用才能达到良好效果,其使用的成本相对较高,若操作不当还容易造成水体生态环境的潜在安全风险(林虹2006)。生物法利用特定的微生物吸收转化水体中的氨氮、亚硝酸盐等有害物质,相较而言具有环境友好,不易产生二次污染、可持续性强等优点(王战蔚等2013)。李长玲等(2008)在培育奥尼罗非鱼苗的水体中引入不同浓度的硝化菌,结果显示,当初始硝化菌的浓度在100cfu/l时,氨氮含量较对照组降低25.05%,鱼苗成活率较对照组提高7.58%,体重增加46.15%;梁拥军等(2005)以澳洲银鲈为研究对象,结果显示,通过提前投放硝化菌和以7-10天的时间间隔定期向水体中补充硝化菌可缓解氨态氮和亚硝酸盐的积累,改善养殖环境。可见,在水产养殖过程中科学应用硝化菌有利于解决有害氮素的积累问题,起到净化水质,促进养殖生物健康生长的良好效果。已报道的自养硝化菌主要包括硝化杆菌属(nitrobacter)(郑金来等2003)、硝化刺菌属(nitrospina)(李君文等2004)、硝化球菌属(nitrococcus)(bartosch,etal1999)、硝化螺旋菌属(nitrospira)(koops,etal.1990)、亚硝化单胞菌属(nitrosomonas)(grunditz2001)、亚硝化螺旋菌属(nitrosospira)(shaw,etal.2006)、亚硝化叶菌属(nitrosolobus)(webster1996)、亚硝化球菌属(nitrosococcus)(klotz,etal.2006)、亚硝化弧菌属(nitrosovibrio)(ida,etal.2004)。其中,自养氨氧化菌均属变形菌纲(proteobacteria)β亚纲与γ亚纲;异养硝化菌包括细菌、真菌、放线菌等(spiller,etal.1976),如:球形节杆菌(arthrobacterglobiformis)(王小娟等2009)、绿脓假单胞菌(pseudomonasaeruginosa)(李强等2015),寄生曲霉(aspergillusparasiticus)(何霞等2006)。然而,由于硝化菌难以分离纯化,国内外大多数研究者都是采用活性污泥来富集培养硝化菌,极少采用纯菌扩大培养方式(杨宁2003;王娟2006)。金志刚等(1998)利用活性污泥富集硝化菌表明当温度为30℃、ph6.5-8.0、溶氧量高于2.0mg/l时,经过1-13周的富集培养,是未经富集污泥中硝化菌浓度的12.5-20倍。shan和obbard(2001)用固定化的硝化菌处理龙虾养殖废水获得了理想的效果。刘伶俐(2012)以固定化方式研究淡水型硝化菌、海水型硝化菌,结果淡水型硝化菌对氨氮的去除率为0.12mg/g·h,海水型菌对氨氮的去除率为0.13mg/g·h。
在自然条件下红球菌可在污染环境中存活,可用作生物去污的接种介体,红球菌属的细菌对许多化合物有转化及降解作用,可将之用作生物表面活性剂及生物絮凝剂。红球菌的细胞表面活性物如枝菌酸可降低交界面的表面张力,使亲水性化合物更易进入菌体细胞,增加了菌体的侵入面;此外,红球菌产生还能产生由多肽、脂类聚集而成的糖脂絮凝物质,对许多悬浮物产生絮凝作用,有助于废水或废物处理中悬浮物的清除(华苟根2003)。红球菌菌体中具有大型基因组和线性质粒,这有益于容纳大量的氧化酶和其他酶系物质,使得红球菌能充分利用来自有机化合物的能源和碳源,并且还能产出类胡萝卜素(邱孜博2016)。
虽然微生物固定化技术备受关注也进行了不少的有益探索和尝试,但目前大多还只停留在小规模、小范围的应用实验阶段,还未达到大规模产业化的高效应用效果。为有效推进相关技术在水产养殖产业的安全高效应用,有必要以养殖水体环境为基础,从中筛选获得具有有害氮素净化功能的土著菌株,并分析菌株的环境适应性、生态功能效率、应用安全性等特点,进而研发适宜水产养殖生产实际应用的菌剂产品和应用技术。而非简单套用污水处理工程技术中的相关细节,忽视养殖生物与生产对安全、高效、可持续发展的具体实际需求。目前未见关于以玫瑰红红球菌(rhodococcusrhodochrous)净化养殖水体氨的相关菌株的研究报道。
技术实现要素:
本发明的目的在于提供一种净化养殖水体中氨的玫瑰红红球菌菌株xhrr1,该菌株xhrr1对养殖水体中的氨具有较强的净化能力,且环境适应性良好,对养殖对虾无不良影响。
本发明的目的还在于提供上述玫瑰红红球菌菌株xhrr1在净化养殖水体中氨的应用。
本发明的第一个目的是通过如下技术方案实现的:一种净化养殖水体中氨的玫瑰红红球菌菌株xhrr1,该菌株xhrr1的保藏名称为:玫瑰红红球菌xhrr1,分类命名为:rhodococcusrhodochrousxhrr1,保藏单位为:中国典型培养物保藏中心,保藏地址为:中国武汉,保藏日期为:2017年8月3日,保藏编号为:cctccno:m2017437。
本发明中的玫瑰红红球菌xhrr1的筛选分离鉴定过程为:选取对虾集约化高密度养殖池塘的后期养殖水体(养殖50~75天),以0.22μm的混合纤维素酯滤膜过滤水样,再将聚集了微生物样品的滤膜置于光合细菌液体培养基中密闭震荡培养3~5天,温度25~30℃,光照强度2500~4000lx;将培养好的菌液在光合细菌固体平板培养基上进行划线培养,培养3~5天,挑选不同形态的单菌落,分离纯化获得生长性能好的菌株。然后把菌株接种至光合细菌液体培养基,28~30℃,光照强度2500~4000lx,150~200rpm进行摇床扩大培养3~5天。把不同的菌液分别添加到调整了nh4cl浓度的灭菌养殖水中(以nh4cl调节水体中氨的浓度至10~30mg/l),28~30℃,光照强度2500~4000lx,150~200rpm进行摇床扩大培养3~5天。选取可有效降低水体氨浓度的菌株进行菌种鉴定和保种备用。
从集约化养殖池塘的养殖中后期水体中分离获得菌株并进行纯培养,在将菌液放入以nh4cl调配的含高浓度氨(以nh4cl调节水体中氨的浓度至10~30mg/l)的养殖水体中,分析菌株对水体中氨的净化效果影响,获得能高效净化养殖水体氨的菌株,并确定该菌株的培养条件。
该玫瑰红红球菌xhrr1在温度15~35℃、盐度5~45、ph6~9均可正常生长,最佳条件为温度15~35℃,盐度25~45,ph7.0~8.5。在最佳条件下与养殖水体营养环境中生长2天左右可达到峰值,2~5天期间维持在108cfu/ml的数量水平。该菌株适宜在大部分池塘应用。
本发明的第二个目的是通过以下技术方案来实现的:上述玫瑰红红球菌菌株xhrr1在净化养殖水体中氨的应用。
该玫瑰红红球菌xhrr1在养殖水体营养环境下生长2天左右可达到峰值,2~5天期间维持在108cfu/ml的数量水平。该菌株适宜在大部分池塘应用。将该菌株置于含高氨氮的养殖水体中,当水体盐度为5~45时,温度30℃,加菌组水体中氨的去除率3天可达到79%~99%;当盐度达到25~45时水体氨的去除率大于90%。当水温为15~35℃,盐度25时,加菌组水体中氨的去除率3天可达到90%以上;水温低于15℃或高于40℃时,玫瑰红红球菌xhrr1的除氨效果受到明显影响。
而且,在实验养殖水体中以107cfu/ml浓度施用该菌时,测试凡纳滨对虾的7天成活率可达到90%以上,表明其对养殖生物无明显不良影响。
本发明中养殖池塘环境与背景技术中的水体环境存在巨大差异,有必要以养殖水体环境为基础,从中筛选获得具有硝化功能的土著菌株,并分析评估菌株的环境适应性、生态功能效率、应用安全性等特点进而研发适宜水产养殖生产实际应用的菌剂产品和应用技术。而非简单套用污水处理工程技术中的相关细节,忽视养殖生物与生产对安全、高效、可持续发展的具体实际需求。因此,本发明通过分离、筛选的玫瑰红红球菌xhrr1对养殖水体中的氨具有明显的去除作用,凡纳滨对虾没有明显不良影响。为进一步研发适用于水产养殖实际应用需求的硝化菌菌剂与配套技术提供了理论和技术支持。
与现有技术相比,本发明具有如下优点:
(1)本发明中的玫瑰红红球菌xhrr1对集约化养殖水体中氨的去除效果显著,且对养殖生物无不良影响;
(2)本发明中的玫瑰红红球菌xhrr1筛选自集约化养殖中期的水体,具有良好的环境适应性,适宜大部分的养殖池塘水体应用;
(3)本发明中的玫瑰红红球菌xhrr1应用于集约化养殖的水质净化调控可达到良好的应用效果,有利于大幅减少养殖生产过程中的水体更换,还可不必配置价格昂贵的水质净化设备,能为进一步研发或实施养殖水环境定向调控技术,推动实现生态环保的水产高效健康养殖产业发展提供技术储备与支持。
附图说明
图1是实施例3中菌株玫瑰红红球菌xhrr1的生长曲线;
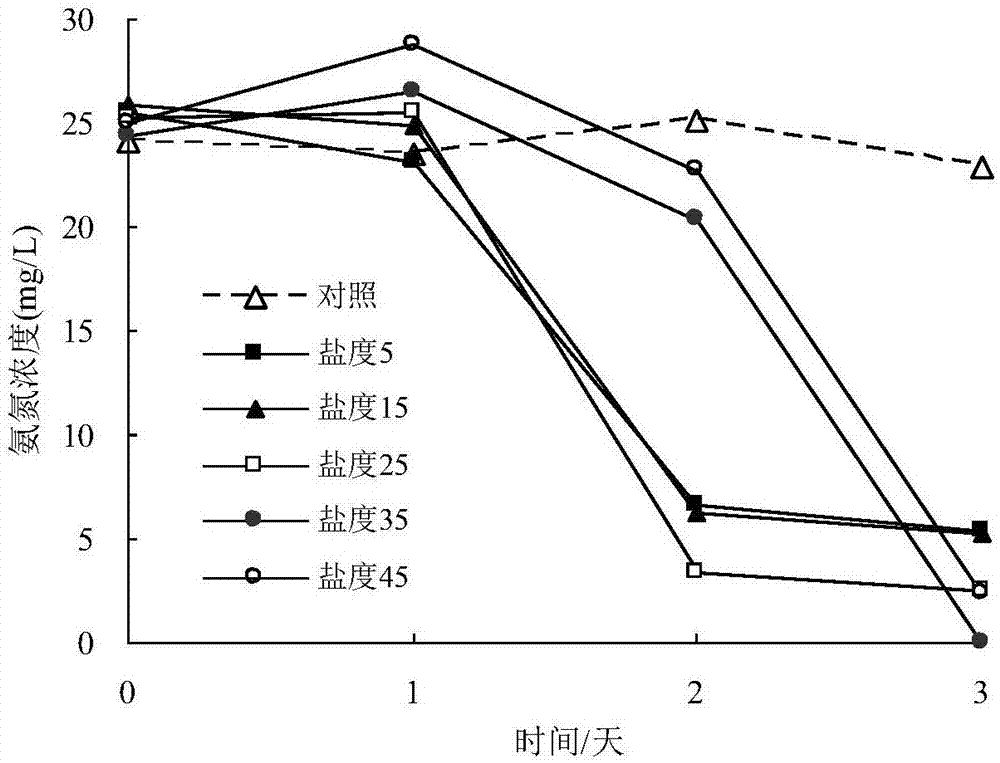
图2是实施例3中菌株玫瑰红红球菌xhrr1在不同盐度下净化水体氨的变化曲线;
图3是实施例3中菌株玫瑰红红球菌xhrr1的不同温度下净化水体氨的变化曲线;
图4是实施例4中菌株玫瑰红红球菌xhrr1对凡纳滨对虾的影响。
具体实施方式
下面结合附图和实施例对本发明做进一步说明,但不以任何形式限制本发明。
实施例1净化养殖水体氨的玫瑰红红球菌xhrr1的筛选与培养
1、材料准备
1.1、菌源
在集约化对虾养殖池塘采集养殖50~75天的水样,用光合细菌培养基平板进行分离培养。
1.2、培养基
(1)光合细菌液体培养基:ch3coona:1g、酵母膏:1g、mgso4·7h2o:0.4g、nacl:0.1g、cacl2·2h2o:0.05g、nahco3:0.3g、kh2po4:1g、微量元素溶液1ml,以上药品分别溶于蒸馏水中,并定溶至1000ml,ph7.0。
微量元素溶液:edta:2.5g、znso4·7h2o:10.95g、mnso4·h2o:1.54g、cus04·5h2o:0.39g、cocl2·6h2o:0.2g、feso4·7h2o:7g,以上药品分别溶于蒸馏水中,并定溶至1000m1,ph7.0。
(2)光合细菌固体平板培养基:在光合细菌液体培养基的基础上加入琼脂粉20g/l,制备成固体平板培养基。
2、菌株的筛选培养
选取对虾集约化高密度养殖池塘的后期养殖水体(养殖50~75天),以0.22μm的混合纤维素酯滤膜过滤水样,再将聚集了微生物样品的滤膜置于光合细菌液体培养基中密闭震荡培养3~5天,温度25~30℃,光照强度2500~4000lx;将培养好的菌液在光合细菌固体平板培养基上进行划线培养,培养3~5天,挑选不同形态的单菌落,分离纯化获得生长性能好的菌株。然后把菌株接种至光合细菌液体培养基,28~30℃,光照强度2500~4000lx,150~200rpm进行摇床扩大培养3~5天。把不同的菌液分别添加到调整了nh4cl浓度的灭菌养殖水中(以nh4cl调节水体中氨的浓度至10~30mg/l),28~30℃,光照强度2500~4000lx,150~200rpm进行摇床扩大培养3~5天。选取可有效降低水体氨浓度的菌株进行菌种鉴定。
从集约化养殖池塘的养殖中后期水体中分离获得菌株并进行纯培养,在将菌液放入以nh4cl调配的含高浓度氨的养殖水体中,分析菌株对水体中氨的净化效果影响,获得能高效净化养殖水体氨的菌株,并确定该菌株的培养条件。
实施例2净化养殖水体氨的玫瑰红红球菌xhrr1的鉴定
本发明对净化养殖水体氨的玫瑰红红球菌xhrr1进行了16srdna分子的鉴定,从分子水平,并结合细菌形态学特征及生理生化特性分析确定菌株的种属。16srdna序列分析主要按照以下步骤:
1、细菌基因组dna的提取:
(1)用无菌牙签挑单菌落接种于扩大培养基内培养;
(2)取细菌培养液1.5ml,10000rpm(11,500g)离心1分钟,尽量吸净上清;
(3)向菌体沉淀中加入200μl缓冲液ga,振荡至菌体彻底悬浮,加入180μl终浓度为20mg/ml的溶菌酶,37℃处理30分钟以上;
(4)向管中加入20μl蛋白酶k溶液,混匀;
(5)加入220μl缓冲液gb,振荡15秒,70℃放置10分钟,溶液变清亮,简短离心以去除管盖内壁的水珠;
(6)加220μl无水乙醇,充分振荡混匀15秒,简短离心以去除管盖内壁的水珠;
(7)将上一步所得溶液和絮状沉淀都加入一个吸附柱cb3中(吸附柱放入收集管中),12000rpm(13,400×g)离心30秒,倒掉废液,将吸附柱cb3放入收集管中;
(8)向吸附柱cb3中加入500μl缓冲液gd,12000rpm(13,400g)离心30秒,倒掉废液,将吸附柱cb3放入收集管中;
(9)向吸附柱cb3中加入700μl漂洗液pw,12000rpm(13,400g)离心30秒,倒掉废液,吸附柱cb3放入收集管中;
(10)向吸附柱cb3中加入500μl漂洗液pw,12000rpm(13,400g)离心30秒,倒掉废液,将吸附柱cb3放入收集管中;
(11)将吸附柱cb3放回收集管中,12000rpm(13,400g)离心2分钟,倒掉废液。将吸附柱cb3置于室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液;
(12)将吸附柱cb3转入一个干净的离心管中,向吸附膜的中间部位悬空滴加50~200μl洗脱缓冲液te,室温放置2~5分钟,12000rpm(13,400g)离心2分钟,将溶液收集到离心管中;
(13)dna浓度及纯度检测
回收得到的dna片段用琼脂糖凝胶电泳和紫外分光光度计检测浓度与纯度。
2、16srdna基因的pcr扩增
16srdna的扩增所采用的细菌通用引物由英潍捷基(上海)贸易有限公司公司合成,正向引物(8f)为:5’-agagtttgatcctggctcag-3’;反向引物(1492r)为:5’-ggttaccttgttacgactt-3’。50μlpcr反应体系包括:灭菌双蒸水37μl,引物各1μl,dntps(2.5mmol/l),tap酶1μl,10×pcrbuffer5μl,dna模板1μl。pcr反应条件:95℃3分钟,95℃1分钟,48℃1分钟,72℃2分钟,共30个循环;72℃10分钟。
3、16srdna序列测定
扩增结束,pcr产物用1.0%琼脂糖凝胶电泳检测,送英潍捷基(上海)贸易有限公司公司测序。测得其序列:
4、净化养殖水体氨的玫瑰红红球菌xhrr1菌落形态、生理特征
玫瑰红红球菌xhrr1菌落形态、生理特征见下表1。
表1玫瑰红红球菌xhrr1菌落形态、生理特征
5、玫瑰红红球菌xhrr1的鉴定
将该菌16srdna基因序列与genbank中已登录的基因序列进行比对分析,利用biologmicrostationtmsystem细菌鉴定系统分别进行菌株生化特性鉴定,结果显示该菌株玫瑰红红球菌(rhodococcusrhodochrous)。综合16srdna基因序列分析、生化鉴定,以及形态特质等各项结果。认定菌株xhrr1为玫瑰红红球菌(rhodococcusrhodochrous)。查阅有关资料,尚无以玫瑰红红球菌(rhodococcusrhodochrous)净化对虾池水体氨的研究报道。
该菌株xhrr1的保藏名称为:玫瑰红红球菌xhrr1,分类命名为:rhodococcusrhodochrousxhrr1,保藏单位为:中国典型培养物保藏中心,保藏地址为:中国武汉,保藏日期为:2017年8月3日,保藏编号为:cctccno:m2017437。
实施例3净化养殖水体氨的玫瑰红红球菌xhrr1的小规模应用
1、菌株的生长
将实施例1获得的菌株玫瑰红红球菌xhrr1按106cfu/ml接种至灭菌养殖池塘水中,2~5天期间的菌浓度稳定在108cfu/ml数量水平,菌株xhrr1的生长曲线如图1中所示。
2、菌株在不同盐度养殖水体中氨的去除效果
将灭菌养殖池塘水(水体盐度为25)为基础测试水体,以nh4cl调节水体中氨的浓度至于24mg/l左右,以蒸馏水和海盐调节水体盐度为5、15、25、35、45。将实施例1获得的菌株玫瑰红红球菌xhrr1按106cfu/ml接种至实验水体中,于30℃,光照强度2500~4000lx,150~200rpm进行摇床培养3天。每天监测水体中氨浓度的变化状况。结果如图2所示,当水体盐度为5~45时,加菌组水体中氨的去除率3天可达到79%~99%;当盐度达到25~45时水体氨的去除率大于90%,在整个监测过程中对照组(以盐度为25的测试培养体系为参照,其中未添加红球菌xhrr1)的氨浓度变化不大。可见,xhrr1菌具有良好的盐度适应性,可适用于不同盐度养殖水体氨的净化,相较而言,盐度大于25的水体其效果更佳。
3、菌株在不同温度养殖水体中氨的去除效果
将灭菌养殖池塘水(水体盐度为25)为基础测试水体,以nh4cl调节水体中氨的浓度至于24mg/l左右。将实施例1获得的菌株玫瑰红红球菌xhrr1按106cfu/ml接种至实验水体中,培养温度分别设置为5℃、15℃、25℃、30℃、35℃、45℃,于光照强度2500~4000lx,150~200rpm条件下进行摇床培养3天。每天监测水体中氨浓度的变化状况。结果如图3所示,当水温为15~35℃时加菌组水体中氨的去除率3天可达到90%以上;当水温低于15℃或高于40℃时,玫瑰红红球菌xhrr1的除氨效果受到明显影响,在整个监测过程中对照组(以温度为30℃的测试培养体系为参照,其中未添加红球菌xhrr1)的氨浓度变化不大。总体而言,在养殖生产期间xhrr1菌株可适应养殖水体温度条件,具备良好的温度适应性,将其科学应用于水体调控技术环节中能有效降低水体中氨的浓度,达到优化养殖水质的效果。
实施例4菌株xhrr1对凡纳滨对虾的影响
在汕尾和深圳养殖基地测试菌株对凡纳滨对虾的影响。养殖水体盐度为25~28,ph7.5~8.1,溶氧6.0~6.7mg/l,温度28~32℃,水体容积为200l。实验组以107cfu/ml浓度施用该菌,对照组不加菌,每组均设3个平行。测试凡纳滨对虾初始体长为6.7±0.5cm,体重为2.8±0.2g。测试周期7天。结果如图4所示,测试结束时加菌组和对照组的对虾成活率分别为92.7%和93.3%。可见,在养殖水体中以107cfu/ml浓度施用该菌时,菌株对养殖生物无明显不良影响。
本发明不局限于上述特定的实施方案范围内,上述实施方案仅仅是为了能够对本发明的使用过程进行详细地说明,而且有相等功能的生产方法和技术细节也属于本发明内容的一部分。事实上,本领域技术人员根据前文的描述,就能够根据各自需要找到不同的调整方案,这些调整都应在本文所附的权利要求书的范围内。
序列表
<110>中国水产科学研究院南海水产研究所
潮州市正诚农业科技有限公司
<120>一种净化养殖水体中氨的玫瑰红红球菌菌株xhrr1及其应用
<160>1
<170>siposequencelisting1.0
<210>1
<211>1390
<212>dna
<213>玫瑰红红球菌菌株xhrr1(rhodococcusrhodochrousxhrr1)
<400>1
acggctccctcccacaaggggttaggccaccggcttcgggtgttaccgactttcatgacg60
tgacgggcggtgtgtacaaggcccgggaacgtattcaccgcagcgttgctgatctgcgat120
tactagcgactccgacttcacggggtcgagttgcagaccccgatccgaactgagaccggc180
tttaagggattcgctccacctcacggtatcgcagccctctgtaccgaccattgtagcatg240
tgtgaagccctggacataaggggcatgatgacttgacgtcgtccccaccttcctccgagt300
tgaccccggcagtctcctgcgagtccccaccatcacgtgctggcaacacaggacaagggt360
tgcgctcgttgcgggacttaacccaacatctcacgacacgagctgacgacagccatgcac420
cacctgtctaccggccacaagggaaaccacatctctgcagtcgtccggtacatgtcaaac480
ccaggtaaggttcttcgcgttgcatcgaattaatccacatgctccgccgcttgtgcgggc540
ccccgtcaattcctttgagttttagccttgcggccgtactccccaggcggggcgcttaat600
gcgttggctacggcacggatcccgtggaaggaaacccacacctagcgcccaccgtttacg660
gcgtggactaccagggtatctaatcctgttcgctacccacgctttcgctcctcagcgtca720
gttactgcccagagacccgccttcgccaccggtgttcctcctgatatctgcgcatttcac780
cgctacaccaggaattccagtctcccctgcagtactcgagtctgcccgtatcgcctgcaa840
gcccgcagttgagctgcgggatttcacagacgacgcgacaaaccgcctacgagctcttta900
cgcccagtaattccggacaacgctcgcaccctacgtattaccgcggctgctggcacgtag960
ttggccggtgcttcttctcccactaccgtcacttgcgcttcgtcatgggtgaaagaggtt1020
tacaacccgaaggccgtcatccctcacgcggcgtcgctgcatcaggcttgcgcccattgt1080
gcaatattccccactgctgcctcccgtaggagtctgggccgtgtctcagtcccagtgtgg1140
ccggtcgccctctcaggccggctacccgtcgtcgccttggtaggccattaccccaccaac1200
aagctgataggccgcgggctcatcctgcaccgaaaaactttccaccccagaacatgcatc1260
ccgaggtcatatccggtattagacccagtttcccaggcttatcccagagtgcagggcaga1320
tcacccacgtgttactcacccgttcgccactaatccacccagcaagctgggcttcatcgt1380
tcgactgcat1390
- 还没有人留言评论。精彩留言会获得点赞!