与肝癌诊疗相关的血清外泌体hsa-miR-17-5p及其应用的制作方法
本发明属于生物技术和诊断领域,具体涉及与肝癌诊疗相关的血清外泌体hsa-mir-17-5p及其应用。
背景技术:
肝癌是发生率居全球第四,死亡率第二的恶性肿瘤。因为饮食、酒精性肝病尤其是肝硬化、乙肝的关系,肝癌在中国具有高发性及高危性。很多肝癌通常被发现时已经是在临床上呈现晚期,使得我国肝癌的5年生存率低于10%。因此,早期的肝硬化和肝癌的诊断至关重要。目前用于肝癌诊断的血液标志物主要是甲胎蛋白(afp),但是其准确度欠佳,灵敏度和特异性不足以满足肝癌的早期检测。
外泌体是指包含了复杂rna和蛋白质的、直径在40-100nm的盘状囊泡。多种细胞在正常及病理状态下均可分泌外泌体,其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。所有培养的细胞类型均可分泌外泌体,且外泌体天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中。
随着液态活检领域的发展,外泌体来源的生物标志物越来越被大家所重视。外泌体在血液循环中的稳定性及便利性,是一类非常好的循环肿瘤标志物,是无创且有效的诊断标志物。mirna是一种内源性的、长度在22nt左右的非编码rna,它可以通过结合靶基因的3’utr区来调控基因的表达和功能。大量研究表明,mirna可以作为肿瘤及其他疾病的诊断标志物。
技术实现要素:
本发明的目的是提供与肝癌诊疗相关的血清外泌体hsa-mir-17-5p及其应用。
本发明首先保护用于检测hsa-mir-17-5p的物质在制备产品中的应用;所述产品的功能为如下(c1)或(c2):
(c1)鉴定或辅助鉴定肝癌细胞;
(c2)诊断或辅助诊断肝癌。
所述用于检测hsa-mir-17-5p的物质为由逆转录引物、上游引物和下游引物组成的引物组;
所述逆转录引物为如下(d1)或(d2):
(d1)序列表的序列2所示的单链dna分子;
(d2)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的dna分子;
所述上游引物为如下(e1)或(e2):
(e1)序列表的序列3所示的单链dna分子;
(e2)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的dna分子;
所述下游引物为如下(f1)或(f2):
(f1)序列表的序列4所示的单链dna分子;
(f2)将序列4经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列4具有相同功能的dna分子。
本发明还保护一种引物组,由逆转录引物、上游引物和下游引物组成;
所述逆转录引物为如下(d1)或(d2):
(d1)序列表的序列2所示的单链dna分子;
(d2)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的dna分子;
所述上游引物为如下(e1)或(e2):
(e1)序列表的序列3所示的单链dna分子;
(e2)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的dna分子;
所述下游引物为如下(f1)或(f2):
(f1)序列表的序列4所示的单链dna分子;
(f2)将序列4经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列4具有相同功能的dna分子。
所述引物组的功能为如下(c1)或(c2):
(c1)鉴定或辅助鉴定肝癌细胞;
(c2)诊断或辅助诊断肝癌。
本发明还保护所述引物组在制备产品中的应用;所述产品的功能为如下(c1)或(c2):
(c1)鉴定或辅助鉴定肝癌细胞;
(c2)诊断或辅助诊断肝癌。
以上任一所述hsa-mir-17-5p如序列表的序列1所示。
以上任一所述检测hsa-mir-17-5p的物质为检测外泌体中hsa-mir-17-5p的物质。
以上任一所述检测hsa-mir-17-5p的物质为检测血清外泌体中hsa-mir-17-5p的物质。
以上任一所述产品具体可为试剂盒。
本发明首次发现了血清外泌体中的hsa-mir-17-5p可作为肝癌的生物标志物,具有较高诊断价值,为临床提供快速准确的诊断方式,使肝癌的诊断更加方便易行。
附图说明
图1为采用投射电子显微镜观察外泌体的示例性照片。
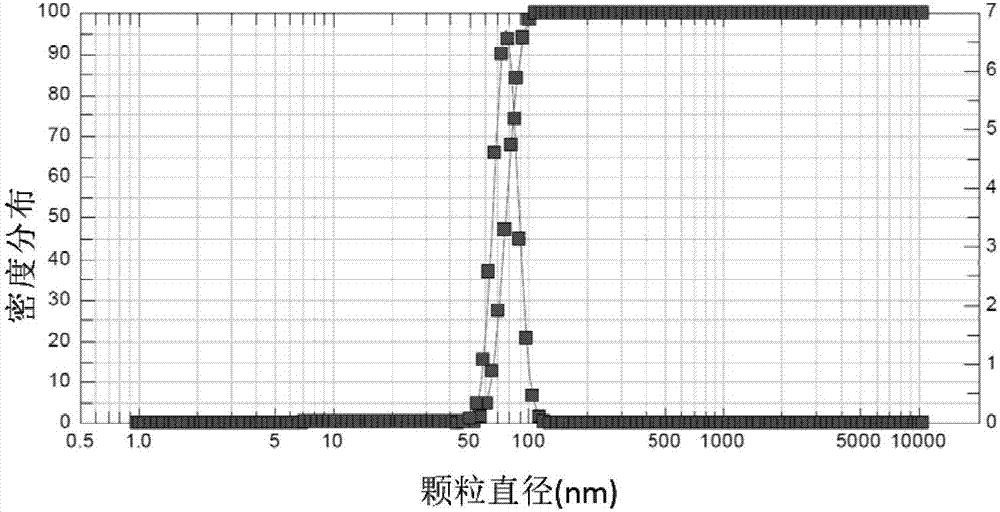
图2为采用纳米激光粒度仪检测外泌体的直径的示例性结果。
图3为采用westernblot检测外泌体的标志性抗原的示例性结果。
图4为肝癌患者组和健康人组血清外泌体中hsa-mir-17-5p的相对表达水平。
图5为roc曲线分析。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
以下的实施例便于更好地理解本发明,但并不限定本发明。任何熟悉本领域的技术人员在本发明的纰漏范围内,根据本发明的技术方案及构思进行替换或改变均属于本发明的保护范畴。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。使用t检验方法统计实验所得数据,p值小于0.05且变化倍数大于2倍被认为具有统计学意义。
pbs缓冲液(ph7.4):含140mmnacl、2.7mmkcl、10mmna2hpo4、1.8mmkh2po4,余量为水。
抗cd63的兔多抗:proteintech,25682-1-ap。
抗cd9的兔多抗:proteintech,20597-1-ap。
实施例1、hsa-mir-17-5p作为肝癌标志物的发现和验证
血清样本为108份,其中85份来自2015年12月至2017年1月在苏州大学附属第一医院确诊的85例肝癌患者(知情同意的志愿者,经病理组织学确诊为i-iv期肝癌患者,于入院后未经手术及放化疗前采血),剩余的23份来自同期进行疾病筛查的健康人(知情同意的志愿者)。各个血清样本分别进行检测。
一、血清外泌体的提取及鉴定
1、取血清样本,采用peg-base沉淀法提取外泌体。
2、取步骤1得到的外泌体,采用投射电子显微镜进行观察。各个血清样本均得到了外泌体,示例性照片见图1。外泌体见图1中的箭头标示。
3、取步骤1得到的外泌体,采用纳米激光粒度仪(德国新帕泰克公司)检测外泌体的直径。各个血清样本得到的外泌体的直径情况一致,均集中于40nm-100nm,示例性结果见图2。
4、取步骤1得到的外泌体,用细胞裂解液裂解后提取总蛋白。取总蛋白,进行sds-page和westernblot。采用的一抗为抗cd63的兔多抗或抗cd9的兔多抗,采用的二抗为辣根过氧化物酶标记的山羊抗兔lgg。将血清样本作为外泌体的对照。各个血清样本得到的外泌体均为cd63和cd9双阳性,示例性结果见图3。
二、外泌体总rna的抽提
取步骤一的1得到的外泌体,提取总rna。
三、逆转录以及qpcr检测
1、取步骤二得到的总rna,进行逆转录,得到cdna。
2、以步骤三得到的cdna为模板,进行荧光定量pcr,检测hsa-mir-17-5p。
反应体系(20μl):由10μl2×sybrgreenqpcrmix、上游引物溶液(20μm)、下游引物溶液(20μm)、模板、rtaqdna聚合酶溶液(5u/μl)和ddh2o组成。反应体系中,上游引物和下游引物的浓度均为0.10μm,rtaqdna聚合酶的浓度为0.05u/μl,模板加入量为50ng。
反应条件:94℃3min;94℃12s、62℃30s、72℃30s,40个循环。
hsa-mir-17-5p的序列(序列表的序列1):5’-caaagugcuuacagugcagguag-3’。
用于hsa-mir-17-5p的逆转录引物如下(序列表的序列2):
5’-gtcgggtccagagcagggtccgaggtacacgttcgctctggacccgacctacct-3’。
用于检测hsa-mir-17-5p的引物如下:
上游引物(序列表的序列3):5’-gccgccaaagtgcttaca-3’;
下游引物(序列表的序列4):5’-cagagcagggtccgaggta-3’。
将hsa-mir-16作为hsa-mir-17-5p的内参。hsa-mir-16为已知在血清外泌体中含量稳定的mirna。
hsa-mir-16的序列(序列表的序列5):5’-uagcagcacguaaauauuggcg-3’。
用于hsa-mir-16的逆转录引物如下(序列表的序列6):
5’-gtcgtatccagagcagggtccgaggtacacgttcgctctggatacgaccgccaatatt-3’。
用于检测hsa-mir-16的引物如下:
上游引物(序列表的序列7):5’-cgcctgtagcagcacgtaa-3’;
下游引物(序列表的序列8):5’-cagagcagggtccgaggta-3’。
将血清外泌体中hsa-mir-16的含量作为1,计算hsa-mir-17-5p相对表达水平。
比较肝癌患者组和健康人组血清外泌体中hsa-mir-17-5p的相对表达水平,结果见图4。在肝癌患者组中血清外泌体中hsa-mir-17-5p的相对表达水平显著高于健康人组(p=0.003)。进行roc曲线分析,结果见图5。auc面积为0.836,p<0.001,95%的置信区间为0.754-0.918。结果表明,血清外泌体中hsa-mir-17-5p的相对表达水平与肝癌发生相关。
肝癌患者组,hsa-mir-17-5p的相对表达水平的中位值为0.00078。健康人组,hsa-mir-17-5p的相对表达水平的中位值为0.00033。将hsa-mir-17-5p的相对表达水平大于0.00078作为判断为肝癌患者的阈值,准确率为83.6%。
sequencelisting
<110>苏州吉玛基因股份有限公司
上海吉玛制药技术有限公司
<120>与肝癌诊疗相关的血清外泌体hsa-mir-17-5p及其应用
<130>gncyx180341
<160>8
<170>patentinversion3.5
<210>1
<211>23
<212>rna
<213>artificialsequence
<400>1
caaagugcuuacagugcagguag23
<210>2
<211>54
<212>dna
<213>artificialsequence
<400>2
gtcgggtccagagcagggtccgaggtacacgttcgctctggacccgacctacct54
<210>3
<211>18
<212>dna
<213>artificialsequence
<400>3
gccgccaaagtgcttaca18
<210>4
<211>19
<212>dna
<213>artificialsequence
<400>4
cagagcagggtccgaggta19
<210>5
<211>22
<212>rna
<213>artificialsequence
<400>5
uagcagcacguaaauauuggcg22
<210>6
<211>58
<212>dna
<213>artificialsequence
<400>6
gtcgtatccagagcagggtccgaggtacacgttcgctctggatacgaccgccaatatt58
<210>7
<211>19
<212>dna
<213>artificialsequence
<400>7
cgcctgtagcagcacgtaa19
<210>8
<211>19
<212>dna
<213>artificialsequence
<400>8
cagagcagggtccgaggta19
- 还没有人留言评论。精彩留言会获得点赞!