一种探针法数字定量PCR试剂盒及其应用和使用方法与流程
本发明涉及试剂盒及其应用,尤其涉及一种探针法数字定量pcr试剂盒及其应用和使用方法。
背景技术
肺腺癌和结核性胸膜炎是临床常见的呼吸系统疾病,两种疾病的一些临床表现较为相似,但是其治疗方案和预后却有明显的不同,因此准确地诊断这两种疾病对于患者的预后极为重要。
胸腔积液即胸水,是指机体受到某些疾病影响胸膜后导致的胸腔液体异常增多。肺腺癌和结核性胸膜炎是引发胸水的常见病因,可通过检测胸水中的结核杆菌或者肿瘤细胞来确诊,但是在实际临床工作中阳性检测率较低,因此临床上还将通过病史、血液检测、胸水生化检测、血沉检测、结核抗体检测、细胞染色体检测、肿瘤抗原检测等等对两者进行鉴别诊断,鉴别过程较为繁琐,耗时,也增加了患者的经济负担。
技术实现要素:
本发明旨在解决现有技术中肺腺癌和结核性胸膜炎难以鉴别的问题,提出了探针法数字定量pcr试剂盒及其应用,该试剂盒能够快速地对肺腺癌和结核性胸膜进行鉴别,同时检测准确率高。
为了实现上述发明目的,本发明的技术方案如下:
环状rnahsa_circ_051778作为检测指标在探针法数字定量pcr试剂盒中的应用。
一种如上所述的探针法数字定量pcr试剂盒,所述试剂盒通过检测胸水外泌体样本中环状rnahsa_circ_051778的拷贝数作为检测指标。
进一步地,本发明所述试剂盒包括环状rnahsa_circ_051778特异性引物、环状rnahsa_circ_051778特异性探针、肺腺癌患者胸水外泌体rna逆转录后所得到的cdna、探针法数字pcr专用pcr扩增预混液和无菌去离子水。所述探针法数字pcr专用pcr扩增预混液为2xddpcrsupermixforprobes。
进一步地,本发明所述环状rnahsa_circ_051778特异性引物包括前引物和后引物;所述前引物序列为:5’-gaaataaaatgccaaagaacacaca-3’;所述后引物序列为5’-tgggcagagaatgacgaacag-3’。
进一步地,本发明所述环状rnahsa_circ_051778特异性mgb探针的序列为:5’-tgtcagccagcccac-3’。
进一步地,本发明所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记fam荧光报告基团、vic荧光报告基团或hex荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记minorgroovebinder和quencher荧光淬灭基团。
进一步地,本发明所述的探针法数字定量pcr试剂盒的使用方法,包括以下步骤:
a.取样
取患者1µg的胸水外泌体rna逆转录得到cdna;
b.pcr扩增体系配制
将步骤a中的cdna加入以下物质形成扩增体系:2xddpcrsupermixforprobes10µl;环状rnahsa_circ_051778特异性引物的前引物和后引物,其终浓度各为900nm;环状rnahsa_circ_051778特异性mgb探针,其终浓度为250nm;
c.扩增反应
将步骤b的扩增体系在以下条件下进行扩增反应得到环状rnahsa_circ_051778:
95℃10分钟激活酶活性;94℃变性30秒,60℃退火/延伸1分钟,共40个循环;98℃10分钟灭活酶活性;
d.拷贝数测定
采用探针法对步骤c所得扩增产物进行定量检测,得环状rnahsa_circ_0051778拷贝数;
e.鉴别
将步骤d中的环状rna拷贝数与参考值(3.4拷贝/孔)进行比较;
若前者大于后者,则判断该患者为结核性胸膜炎患者;反之该患者为肺腺癌患者。
进一步地,本发明所述的探针法数字定量pcr试剂盒的使用方法,所述步骤a中的rna的纯度为:a260/a280=1.4~2.1。
进一步地,本发明所述的探针法数字定量pcr试剂盒的使用方法,所述步骤a中rna逆转录采用随机六聚体引物。
本发明的有益效果:
(一)本发明为快速鉴别肺腺癌和结核性胸膜炎提供了一种新检测指标的新型检测工具。
(二)使用本发明所述检测工具对肺腺癌和结核性胸膜炎进行鉴别,检测结果表明:该检测工具的灵敏度可达90%以上左右,远远高于目前临床使用的单一方法。
(三)本发明提供的检测工具检测效率较高,仅需6小时即可判断96个待测样本的来源,大大提高了诊疗效率。
(四)本发明提供的检测试剂盒成本较低,每个样本仅需100元左右,极大的降低了患者的费用。
(五)本发明提供的检测工具通过拷贝数即可直接判断待测样本的来源,结果判断较容易,不需要专业培训。
附图说明
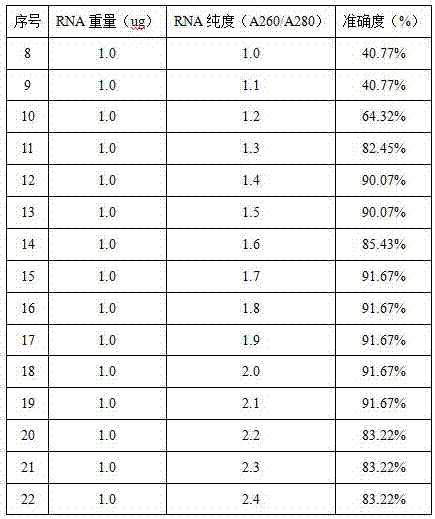
图1为rna纯度与准确度关系示意图。
图2为采用本发明所述试剂盒诊断10个病例的结果与最终诊断结果对比。
具体实施方式
下面结合实施例对本发明作进一步地详细说明,但本发明的实施方式不限于此。
实施例1
以环状rnahsa_circ_051778作为检测指标在探针法数字定量pcr试剂盒中的应用,所述试剂盒通过检测胸水外泌体样本中环状rnahsa_circ_051778拷贝数作为指标。
上述的以环状rnahsa_circ_051778作为检测指标在探针法数字定量pcr试剂盒,包括环状rnahsa_circ_051778特异性引物、环状rnahsa_circ_051778特异性探针、肺腺癌患者胸水外泌体rna逆转录后所得到的cdna和无菌去离子水。
本实施例中,所述环状rnahsa_circ_051778特异性引物包括前引物和后引物;所述前引物序列为:5’-gaaataaaatgccaaagaacacaca-3’;所述后引物序列为5’-tgggcagagaatgacgaacag-3’。
本实施例中,所述环状rnahsa_circ_051778特异性mgb探针的序列为:5’-tgtcagccagcccac-3’。
本实施例中,所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记fam荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记minorgroovebinder荧光淬灭基团。
实施例2
本实施例与实施例1的区别在于:所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记fam荧光报告基团quencher荧光淬灭基团。
实施例3
本实施例与实施例2的区别在于:所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记vic荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记minorgroovebinder荧光淬灭基团。
实施例4
本实施例与实施例2的区别在于:所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记vic荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记quencher荧光淬灭基团。
实施例5
本实施例与实施例2的区别在于:所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记hex荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记minorgroovebinder荧光淬灭基团。
实施例6
本实施例与实施例2的区别在于:所述环状rnahsa_circ_051778特异性mgb探针序列5’端标记hex荧光报告基团;所述环状rnahsa_circ_051778特异性mgb探针序列3’端标记quencher荧光淬灭基团。
实施例7
本实施例提供了一种以环状rnahsa_circ_051778作为检测指标的探针法数字定量pcr试剂盒的使用方法,包括以下步骤:
a.取患者1µg的胸水外泌体rna逆转录得到cdna;
b.将步骤a中的cdna加入以下物质形成扩增体系:2xddpcrsupermixforprobes10µl;环状rnahsa_circ_051778特异性引物的前引物和后引物,其终浓度各为900nm;环状rnahsa_circ_051778特异性mgb探针,其终浓度为250nm;
c.将步骤b的扩增体系在以下条件下进行扩增反应得到环状rnahsa_circ_051778:
95℃保持10分钟;94℃变性30秒,60℃退火/延伸1分钟;变性、退火和延伸进行40个循环;然后98℃保持10分钟;
d.将步骤c中的环状rna与参考值(3.4拷贝/孔)进行比较,若前者大于后者,则判断该患者为结核性胸膜炎患者;反之该患者为肺腺癌患者。
探针参考值计算方法如下:先通过探针法数字定量pcr检测了用50例胸水样本(其中25例为肺癌,25例为结核性胸膜炎)进行外泌体环状rnahsa_circ_0051778的检测,结果显示胸水中外泌体rna的拷贝数均值为12.35,标准差为14.03。之后使用medscisamplesizetools软件中诊断性研究工具计算所需样本数量,设置相对允许误差为0.1,绝对允许误差为0.1,计算结果显示总共需要469例样本。最终,我们检测了240例肺癌和240例结核性胸膜炎胸水中外泌体环状rnahsa_circ_0051778的拷贝数,并用受试者工作特征曲线评价了其诊断价值,结果显示在拷贝数为3.4时,环状rna51778对肺癌和结核性胸膜炎的鉴别能力最强,灵敏度达到90%以上。
本实施例中,步骤a中rna的纯度为a260/a280=1.9~2.1。
本实施例中,步骤z中rna逆转录采用随机六聚体引物。
将上述实施例1~7用于鉴别临床肺腺癌和结核性胸膜炎的鉴别中,并将检测的灵敏度统计在下表1中:
表1
实施例8~实施例22
实施例8~实施例22为采用不同的rna纯度对准确度的影响,rna重量为胸水外泌体中的rna重量。如图1所示。
rna纯度在1.7~2.1之间的时候,准确度能够稳定在91.67%左右,本发明选取了rna的纯度为1.9~2.1。
(1)选取10例有胸腔积液的患者,每个患者抽取5ml胸水分别装入15ml离心管内,置于4℃冷冻离心机(eppendorf,德国)3000g离心15分钟;
(2)用5ml无菌注射器吸取离心管内的上清液,然后用0.22µm针式滤器(millipore,美国)过滤,过滤后的液体装入5ml无酶无菌ep管内;
(3)按照外泌体rna提取试剂盒(qiagen,德国)的操作步骤,提取2ml胸水中的外泌体rna,用nanophotometern60(implen,德国)检测rna的浓度及纯度;
(4)用iscript逆转录超混合液(bio-rad,美国)将1µgrna逆转录为cdna;
(5)配制pcr扩增体系:2xddpcrsupermixforprobes(bio-rad,美国)10µl;前引物0.1µl(终浓度900nm)(成都擎科生物科技有限公司,中国);后引物0.1µl(终浓度900nm)(成都擎科生物科技有限公司,中国);环状rnahsa_circ_051778特异性mgb探针,其终浓度为250nm;无菌去离子水8.8µl;cdna1µl;
(6)将pcr扩增体系和70µl微滴发生油(bio-rad,美国)放入微滴发生卡内的相应位置,放入微滴发生仪(bio-rad,美国)内生成微滴;
(7)将生成的微滴分别加入96孔pcr扩增板内,放入pcr仪扩增(bio-rad,美国),扩增条件:95℃10分钟激活酶活性;94℃变性30秒,60℃退火/延伸1分钟,共40个循环;98℃10分钟灭活酶活性;
(8)将pcr扩增板取出,放入微滴读取仪(bio-rad,美国),读取数据。
结果显示如图2所示。
以上所述,仅是本发明的较佳实施例,并非对本发明做任何形式上的限制,凡是依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化,均落入本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!