一种布瓦西坦中间体的制备方法与流程
本发明涉及布瓦西坦及其中间体制备方法,属于医药
技术领域:
。
背景技术:
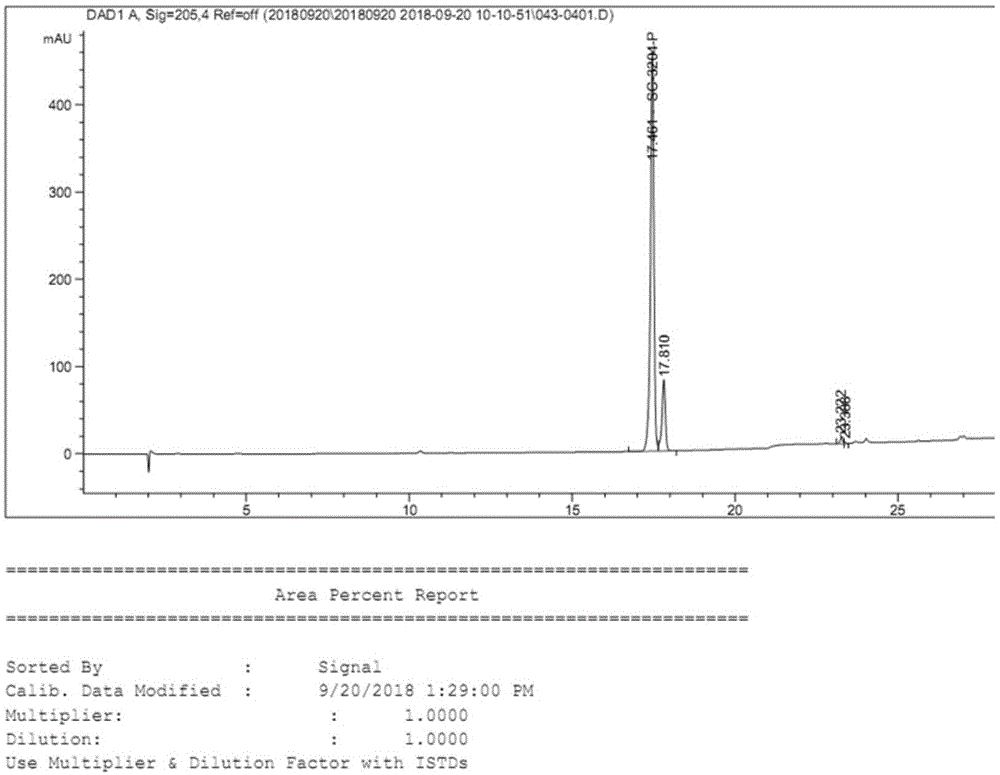
:布瓦西坦(brivaracetam),化学名称为(s)-2-(r)-3-丙基吡咯烷-1-基丁酰胺,由比利时优时比制药公司(ucbpharma)研制,是抗癫药左乙拉西坦(levetiracetam)吡咯烷烃的4位碳原子连接正丙基的类似物。布瓦西坦也是大脑突触囊泡蛋白2a(sv2a)选择性和高亲和力的配体,sv2a是抑制癫部分性发作的重要位点。欧洲医药管理局(ema)和美国食品药品管理局(fda)分别于2016年1月14日和2016年2月18日批准用于治疗16岁及以上部分性发作型的癫痫患者,伴或不伴随继发全身性发作的辅助治疗药,商品名为布瓦西坦是左乙拉西坦的衍生物,属于第3代抗癫痫药物。布瓦西坦具有高度亲和力,可选择性的结合突触囊泡蛋白2a(sv2a),是aed左乙拉西坦的作用位点。sv2a位于突触前膜,参与调解神经递质的释放和囊泡循环进而维持着突触囊泡的正常功能。aed与sv2a结合可减少兴奋性神经递质的释放,并通过调节脑内兴奋性递质和抑制性递质的平衡达到控制癫痫发作的效果。布瓦西坦的亲和力是左乙拉西坦的15-30倍,使其使用剂量降低约10倍。一项小型(n=29)、开放标签、前瞻性研究表明,在那些因行为不良事件从左乙拉西坦转变为布瓦西坦的患者中,生活质量得到改善,且癫痫控制效果未减。由于布瓦西坦是一种新型aed,其长期疗效和安全性尚不得而知。目前,现有的布瓦西坦的制备工艺几乎都不可避免的要用手性色谱柱分离其非对应异构体(s)-2-(s)-3-丙基吡咯烷-1-基丁酰胺。如原研专利wo2005028435就提到了在25±2℃温度下,采用手性固相、正己烷/乙醇(45/55,v/v)为洗脱剂,以色谱法分离得到的两个非对映异构体。wo2007065634使用了另外一条路线,使用了价格昂贵的金属催化剂rucl3,且该制备方法同样不可避免的通过柱色谱分离得到布瓦西坦(26%,e.e.=94%)和非对映异构体。它们结构如下式所示:cn106748950a报道了一种制备中间体(s)-2-3-丙基吡咯烷-1-基丁酸的方法。并提到了用r-苯乙胺/异丙醇体系拆分中间体(s)-2-3-丙基吡咯烷-1-基丁酸后,再氨化得到高纯度布瓦西坦,但在实验人员重复实施例后发现,r-苯乙胺/异丙醇体系并无拆分纯化效果,专利重现性有待考察。同时,cn106748950a同样也报道了一种能将高纯度(s)-2-3-丙基吡咯烷-1-基丁酸进一步氨化转化为布瓦西坦的方法。鉴于现有的制备方法生产成本高,工业可行性差,因此迫切的需要提供一种更简单且能重复的工业化生产的制备高纯度布瓦西坦的方法。技术实现要素:本发明提供了一种b-r所示布瓦西坦中间体的制备方法,包括如下步骤:a.将b-p与1s,2s-二苯基乙二胺溶于溶剂中,升温溶清,降温析晶,过滤得到固体b-q粗品;b.将上述固体重结晶,得b-q;c.将b-q加酸转化为b-r。;其中,步骤a所述的拆分溶剂选自甲基叔丁基醚、异丙醚、四氢呋喃、乙腈、乙酸乙酯、乙酸异丙酯和乙二醇二甲醚的中的一种或几种,优选为乙酸异丙酯、乙酸乙酯、乙腈和乙二醇二甲醚;所述的溶剂与底物b-p的体积质量比为(1-30):1,优选体积质量比为(1-10):1,更优选体积质量比为3~6:1;所述的拆分温度为1℃~100℃,优选为50℃~75℃。所述的b-p与1s,2s-二苯基乙二胺的摩尔比为1:(0.5-1.5),优选为1:1;所述b步骤中的重结晶溶剂为甲基叔丁基醚、乙腈、乙酸乙酯、乙酸异丙酯和乙二醇二甲醚,优选为乙酸异丙酯、乙腈、乙酸乙酯和乙二醇二甲醚;所述的重结晶溶剂与底物b-p的体积质量比为(1-30):1,优选体积质量比为(1-10):1,更优选体积质量比为3:1;步骤c中用到的酸为不同比例的稀盐酸、三氟乙酸的一种或它们的组合;步骤c用到的溶剂选自异丙醇、乙酸乙酯、乙酸异丙酯和水中的一种或几种,酸的当量即以酸调ph至1~2左右即可,因此不做进一步说明。本发明还提供一种布瓦西坦的制备方法,其特征在于:将按上述制备方法得到的b-r氨化为布瓦西坦。在不违背本领域常识的基础上,上述各优选条件可任意组合,即得本发明各较佳实施例。本发明所用试剂和原料均市售可得。与现有技术相比,本发明体系的技术优点体现在:(1)能够避免在合成过程中使用手性色谱柱分离非对映异构体,大大缩短工艺时间,简化操作及降低工艺成本,有了工业化生产的基础;(2)与现有的r-苯乙胺拆分方法对比有着较为明显的拆分优势。附图说明附图1:实施例1得到化合物b-p的液相谱图附图2:实施例2得到化合物b-p的液相谱图附图3:实施例3得到化合物b-q的液相谱图具体实施方式下面通过实施例的方式进一步说明本发明,它们专用于说明目的,不在任何方面限制本发明的范围。原料(s)-2(4-丙基-1,5-二氢吡咯-2-酮)丁酸的制备可参考专利cn107513031,b-p化合物((s)-2-3-丙基吡咯烷-1-基丁酸)可按常规钯碳加氢方法制备得到,也可参考专利cn106748950a,布瓦西坦(s)-2-3-丙基吡咯烷-1-基丁酰胺的制备方法可参考专利cn106748950a。其他原料和试剂均为市售得到。实施例1:化合物b-p的制备将150g(s)-2(4-丙基-1,5-二氢吡咯-2-酮)丁酸(0.71mol),加入到2l氢气高压釜中,加入1.5l甲醇,加入1.5gpd(oh)2/c(1%),在15~20mpa压力下反应20小时,过滤,浓缩蒸去甲醇,得140g化合物b-p固体,rs:ss=85:15。hplc图谱见附图1。实施例2:化合物b-p的制备将150g(s)-2(4-丙基-1,5-二氢吡咯-2-酮)丁酸(0.71mol)加入到2l氢气高压釜中,加入1.5l异丙醇,加入45g钯碳(30%),在15~20mpa压力下反应20小时,过滤,浓缩蒸去甲醇,得145g化合物b-p固体,rs:ss=54:45。hplc图谱见附图2。实施例3:化合物b-q的制备向500ml三口瓶中加入180ml醋酸异丙酯(3v)和60g化合物b-p(0.28mol,1.0eq,含异构体15%)和59.4g1s,2s-二苯基乙二胺(1.0eq,0.28mol),升温至72℃左右,溶清,自然降温至20℃±5℃,搅拌1小时后抽滤,得60g湿品,再将湿品直接加入180ml的乙酸异丙酯,升温至72℃下溶解,经1.5小时缓慢降温至20℃,抽滤,得35.7g化合物b-q。收率:30%,纯度:99.8%,非对映异构体0.2%。hplc图见附图3。实施例4:化合物b-r的制备在500ml三口瓶中加入上述化合物b-q30g,加入120ml水,240ml乙酸乙酯,用6n盐酸调ph至1~2,搅拌0.5小时后分层,水相用30ml乙酸乙酯萃取后,合并有机相,减压浓缩,得到化合物b-r白色固体15g,收率100%,纯度99.8%。实施例5:溶剂对拆分收率和手性纯度的影响向反应瓶加入化合物b-p和溶剂,升温至50℃,再加入等当量的1s,2s-二苯基乙二胺,继续升温至70℃左右,冷却至20℃析晶3~5小时,过滤得化合物b-q。溶剂及不同体积比的拆分数据如表2:表2:溶剂及不同体积比的拆分数据实验结果:乙酸乙酯、乙酸异丙酯、乙腈和乙二醇二甲醚对化合物b-p有拆分效果。溶剂体积比高于6或者低于3时,都会导致b-q的收率或含量显著降低。实施例6:重结晶溶剂对产物纯度及收率的影响:将拆分得到的化合物b-q固体和溶剂混合,加热至50℃,冷却至20℃析晶3~5小时,过滤得精制化合物b-q固体。溶剂对结晶效率的影响如表3:表3:溶剂对结晶效率的影响实验结果:用乙二醇二甲醚、乙酸乙酯、乙腈、乙酸异丙酯四种溶剂重结晶时,纯化效果最好,均能达到99%以上的纯度,其中,乙酸乙酯的收率最高,为49%。实施例7:布瓦西坦的制备参考专利cn10106748950a实施例1-(7),向250ml四口瓶加入80ml四氢呋喃,6.4g化合物b-r(0.03mol),28.5ghatu(0.075mol),4.9g氯化铵(0.09mol)和11.7g二异丙基乙胺(0.09mol),室温搅拌2小时,向体系加入80ml水和160ml乙酸乙酯搅拌,静置分层。有机相用40ml饱和碳酸氢钠,40ml饱和氯化铵溶液和40ml饱和食盐水各洗涤一次。有机相用5g无水硫酸钠干燥,过滤,浓缩,得7g布瓦西坦固体,hplc纯度99.5%,手性纯度99.85%。我们对专利cn106748950a中提到r-苯乙胺拆分化合物b-p的实施实例进行重复,无拆分效果。进一步考察溶剂对r/s-苯乙胺拆分化合物b-p(rs:ss=55:45)的影响,如表4:表4:考察r/s-苯乙胺拆分溶剂拆分剂溶剂析晶温度rs/ss收率r-苯乙胺异丙醇0~5℃55/4513%r-苯乙胺乙醇(-20)~(-15)℃——无固体析出r-苯乙胺异丙醚(-20)~(-15)℃——无固体析出r-苯乙胺四氢呋喃(-20)~(-15)℃——无固体析出r-苯乙胺甲苯(-20)~(-15)℃——无固体析出r-苯乙胺丙酮(-20)~(-15)℃——无固体析出r-苯乙胺乙二醇二甲醚(-20)~(-15)℃——无固体析出r-苯乙胺甲基叔丁基醚(-20)~(-15)℃——无固体析出r-苯乙胺乙腈(-20)~(-15)℃——无固体析出r-苯乙胺乙酸乙酯0~5℃55/4525%r-苯乙胺乙酸异丙酯(-20)~(-15)℃——无固体析出s-苯乙胺异丙醇0~5℃55/4513%s-苯乙胺乙醇(-20)~(-15)℃——无固体析出s-苯乙胺异丙醚(-20)~(-15)℃——无固体析出s-苯乙胺四氢呋喃(-20)~(-15)℃——无固体析出s-苯乙胺甲苯0~5℃55/4525%s-苯乙胺丙酮(-20)~(-15)℃——无固体析出s-苯乙胺乙二醇二甲醚(-20)~(-15)℃——无固体析出s-苯乙胺甲基叔丁基醚0~5℃55/4536%s-苯乙胺乙腈0~5℃55/4510%s-苯乙胺乙酸乙酯0~5℃55/4520%s-苯乙胺乙酸异丙酯0~5℃57/4335%由上表可知,r/s苯乙胺对化合物b-p无拆分效果。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1