锦绣杜鹃EST-SSR标记开发及应用的制作方法
本发明属于生物技术领域,具体涉及基于锦绣杜鹃转录组数据的ssr分子标记开发和跨物种扩增应用。
背景技术:
锦绣杜鹃(rhododendronpulchrumsweet)属杜鹃花科(ericaceae)杜鹃花属(rhododendron)常绿灌木,花期主要在2~4月,颜色艳丽,适应性强且生长迅速,适合丛植或盆栽,广泛用于园林绿化和屋前舍后的绿化美观中。锦绣杜鹃干燥叶片可以祛痰、止咳等,具有重要的药用价值。锦绣杜鹃含有大量的天然色素、黄酮类、萜类、芳香类和醛类等植物挥发性有机化合物。长期以来,育种学者对锦绣杜鹃的花期调控研究做了大量工作,为杜鹃花育种研究提供了大量优良性状材料,选育出了多种符合生产需求的杜鹃花品种。分子标记作为品种鉴定、遗传结构解析、遗传图谱构建、目标性状基因定位的重要工具,已经成为花卉研究和应用的重要技术手段,但是目前锦绣杜鹃育种中可以应用的分子标记十分有限,限制了其在优质品种资源快速、有效的选育和应用开发。
微卫星(microsatellite),又称为简单重复序列(simplesequencerepeats,ssr)或者短串联重复序列,是1-6碱基作为重复单元的,广泛分布在真核生物基因组上,且两侧序列非常保守。微卫星序列重复类型和基序的重复次数存在大量变异,故ssr标记具有多态性。与其他分子标记相比,ssr标记具有分布广泛、多态信息含量高、重复性好、操作简单、共显性遗传、特异性强等优点,是较为可靠的分子标记类型。微卫星标记是基于pcr技术的分子标记,对dna的质量要求低、检测方法简单、实验周期短。由于其稳定性从而实验的重现性较好。微卫星是共显性标记,可以区分杂合子和纯合子,同时ssr两端的侧翼序列非常保守,因而微卫星标记在近缘物种间可以通用。因此,ssr标记在遗传多样性分析、遗传图谱的构建、比较基因组研究、系统学研究、基因定位等研究将中广泛运用。然而,锦绣杜鹃公布的可用于遗传学研究的微卫星标记非常有限,限制了分子标记辅助选育锦绣杜鹃新品种的应用。
随着第二代高通量测序技术的发展,使得通过转录组测序数据获取大量微卫星标记成为了可能。目前尚未有利用锦绣杜鹃转录组数据开发ssr的相关报道。
技术实现要素:
本发明针对现有技术的不足,提供基于转录组测序开发的锦绣杜鹃ssr引物对及筛选方法与应用。本发明利用rna-seq技术对锦绣杜鹃盛花期花材料进行转录组测序,将数据组装拼接后挖掘含有ssr标记的序列,并将符合ssr引物设计要求的unigenes进行ssr标记的开发,并随机合成部分ssr引物,进行适用性验证。该引物的开发为锦绣杜鹃的遗传多样性和遗传结构研究、遗传图谱构建、分子标记辅助育种、重要性状基因定位和克隆等研究奠定基础,同时也用于多个锦绣杜鹃近缘种的遗传多样性和遗传变异的研究。
第一方面,提供一种基于转录组测序开发的锦绣杜鹃est-ssr引物对,在检测过程中使用15对引物,所述引物分别为:
表1锦绣杜鹃开发的多态性est-ssr引物信息
第二方面,提供上述锦绣杜鹃est-ssr引物对的下述a1-a6中的任一种用途:
a1、所述est-ssr引物对在构建锦绣杜鹃遗传图谱中的应用;
a2、所述est-ssr引物对在锦绣杜鹃种质鉴定中的应用;
a3、所述est-ssr引物对在锦绣杜鹃育种中的应用;
a4、所述est-ssr引物对在锦绣杜鹃遗传多样性分析中的应用;
a5、所述est-ssr引物对在锦绣杜鹃亲缘关系分析中的应用;
a6、所述est-ssr引物对在锦绣杜鹃分子标记辅助育种中的应用。
第三方面,提供一种鉴定锦绣杜鹃亲缘关系和遗传特性的试剂盒,包括表1中的15对est-ssr引物。
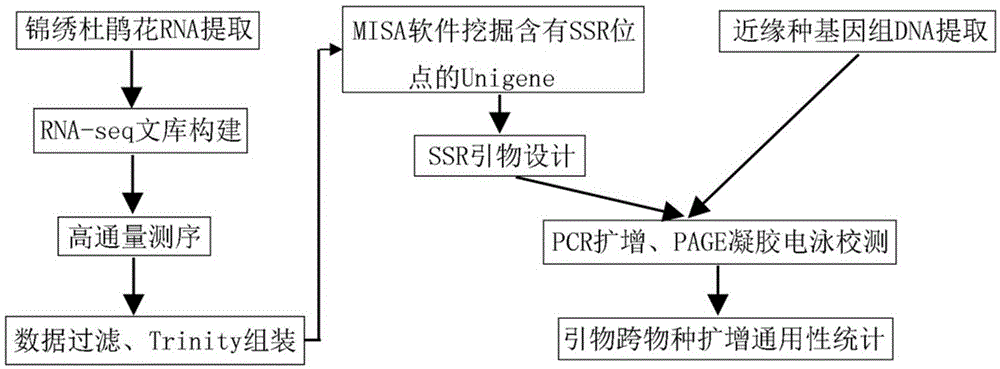
第四方面,提供基于转录组测序开发锦绣杜鹃est-ssr引物的方法,包括
(1)选取锦绣杜鹃盛花期新鲜花材料,获取后用锡箔纸包裹置于液氮中速冻并迅速转移至-70度冰箱保存;采用高盐trizol试剂和rna结合柱的方法提取总rna;
(2)利用链特异性转录组文库构建试剂盒对总rna先进行mrna磁珠富集;将富集到的mrna进行双链cdna合成、末端修复和接头连接;再用user酶降解cdna第二链,保留真实转录的mrna第一链信息;经pcr扩增和2%的琼脂糖凝胶电泳,回收300-500bp范围的片段,即得到测序文库;再利用illuminahiseq2500pe125进行高通量rna-seq测序;
(3)采用fastx和cutadapt软件过滤数据,并采用cufflinks软件进行数据组装得到unigene,将其作为后续ssr引物开发的背景数据;
(4)使用misa软件对unigene进行ssr位点搜索,搜索标准为:二核苷酸、三核苷酸、四核苷酸、五核苷酸、六核苷酸最少重复次数分别为10次、8次、6次、5次、4次,筛选出符合ssr引物设计的序列;
(5)利用primer3.0软件对含有est-ssr位点且侧翼序列大于50bp的unigene序列进行引物设计,引物退火温度50-65℃之间,pcr产物大小100-300bp,引物长度18-24nt之间,cg含量40%-60%,避免引物产生二聚体结构、发夹结构和引物错配;
(6)挑选合成步骤(5)设计的est-ssr引物对,对锦绣杜鹃种群进行pcr扩增和6%page凝胶电泳检测,验证est-ssr引物对的有效性;将多态性引物用于黄杜鹃等3个近缘种的跨物种扩增研究中,验证其通用性。
第五方面,提供鉴定植物样品基因型的方法,包括:
(1)提取所述植物样品的dna;
(2)用选自表1的至少一个引物对扩增至少一种est-ssr标记;
(3)鉴定所述植物样品中的至少一种多态等位基因;
所述植物选自锦绣杜鹃、黄杜鹃、云锦杜鹃、映山红。
优选地,上述步骤(2)包括用对应引物对扩增2种或更多est-ssr标记。
进一步地,上述步骤(2)包括用对应引物对扩增15种est-ssr标记。
优选地,上述步骤(2)中,用所述引物对扩增至少一种est-ssr标记时,所述pcr扩增采用的引物退火条件为50-65℃,30s。
进一步地,上述步骤(2)中,所述pcr扩增中采用的pcr反应温度程序可为:94℃预变性5min;然后进入35个循环:94℃变性40s,55-60℃下退火30s,72℃延伸40s,最后72℃延伸7min。
第六方面,提供由表1所述的引物对以锦绣杜鹃、黄杜鹃、云锦杜鹃、映山红的基因组为模板扩增得到的分离的est-ssr标记。
与现有技术相比,本发明的有益效果在于:
1、本发明通过转录组数据获取锦绣杜鹃多态性ssr引物开发的背景数据,相比较于基因组上开发的ssr具有更高的通用性。
2、本发明的15个est-ssr分子标记引物在3个锦绣杜鹃种内均有较强的跨物种转移能力,可将本发明提供的标记应用于锦绣杜鹃及其他杜鹃花科植物的遗传多样性分析研究、系统进化研究、遗传连锁图谱构、目标性状关键基因定位、分子标记辅助育种等研究中。
附图说明
图1是基于rna-seq数据开发ssr引物和应用的流程示意图。
图2是实施示例中rpe-1引物对在3个近缘种杜鹃内的跨物种检测结果。
具体实施方式
通过以下详细说明结合附图可以进一步理解本发明的特点和优点。所提供的实施例仅是对本发明方法的说明,而不以任何方式限制本发明揭示的其余内容。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
【实施例1】多态性高的锦绣杜鹃的est-ssr引物的开发
本发明提供的基于转录组高通量测序,并结合生物信息学方法进行ssr序列查找和ssr标记引物设计和验证,其具体实施方式如下:
(1)富含ssr位点的unigene序列筛选:选取锦绣杜鹃花材料提取总rna,构建转录组测序文库,采用illumina二代测序仪进行高通量测序。测序数据进过严格的过滤后进行组装,得到unigene,将其作为后续ssr引物开发的背景数据。采用misa软件对unigene进行ssr位点搜索,搜索标准为:二核苷酸、三核苷酸、四核苷酸、五核苷酸、六核苷酸最少重复次数分别为10、8、6、5、4次。
其中,拼接得到的60,125个unigene,含ssr序列的unigene有10,219个,从中统计出12,313个ssr,见表2。
表2锦绣杜鹃unigene中ssr重复序列和次数统计
(2)采用primer3.0软件批量设计含有ssr位点的unigene序列引物,并且ssr位点离侧翼序列长度大于50bp,引物退火温度50-65℃之间,pcr产物大小100-300bp,引物长度18-24nt之间,cg含量40%-60%,避免引物产生二聚体结构、发夹结构和错配情况,筛选出符合ssr引物设计要求的序列。
(3)采用8个锦绣杜鹃个体,pcr扩增后3%琼脂糖凝胶电泳筛选多态性的ssr引物对。ssr引物序列见表1。引物由南京金斯瑞生物科技有限公司合成,并采用rpc的方式进行纯化。
【实施例2】15对est-ssr引物在锦绣杜鹃种群遗传多样性研究中的应用
(1)dna提取:在湖北大别山区采集锦绣杜鹃居群,共35个个体(采集地分布于东经114.56°-115.043°e、北纬31.03°-31.68°n、海拔220-650m),编号为编号为jxdj1-jxdj30。利用3×ctab法提取叶片组织的基因组dna,并经1%琼脂糖凝胶电泳检测质量和紫外分光光度测定浓度,稀释至100ng/μl后置于-20℃冰箱保存备用。
(2)pcr扩增:20μl反应体系包含:ddh2o15.7μl,10×buffer(含mg2+)1.5μl,dntps(10mm)0.2μl,10μm正反引物各0.2μl,taqdna聚合酶0.2μl,dna模板(50ng/μl)1μl。反应程序为:94℃5min;94℃40sec,退火温度(见表1)30sec,72℃30sec,30cycles;72℃7min。所选引物序列见表1。
(3)6%的page胶检测。将pcr扩增产物取3μl,加0.5μl6×dnaloadingbuffer,进行6%page胶电泳,page胶经硝酸银染色和氢氧化钠溶液进行染色和显色。
(4)根据引物扩增条带的有无和大小,统计基因型,采用popgene32.0软件计算锦绣杜鹃种群的遗传结构,结果表明开发的ssr引物能够较好地解析锦绣杜鹃种群遗传结构。结果见表3。
表3基于est-ssr标记的锦绣种群的遗传结构解析
na:等位基因;i:shannon信息指数;nei's:nei's遗传距离;ho:观察杂合度;he:期望杂合度;fis:种群内近交系数;fit:总近交系数;fst:遗传分化系数
【实施例3】15对est-ssr引物在3个锦绣杜鹃近缘种中跨物种扩增检测
est-ssr引物在3个锦绣杜鹃近缘种中通用性检测步骤:
(1)基因组dna的提取:均采用3×ctab法提取3个锦绣杜鹃近缘种新鲜叶片组织的基因组dna:液氮研磨、酚/氯仿(体积比1:1)抽提、异丙醇沉淀、70%乙醇洗涤、rna酶处理后,将提取的dna溶于50μlte溶液。
(2)pcr扩增。采用15μl的反应体系,包含ddh2o11.6μl,10×buffer(含mg2+)1.5μl、dntps(10mm)0.2μl、正反向引物(10μm)各0.2μl、taqdna聚合酶(2.5u/μl)0.3μl、dna模板(50ng/μl)1μl。反应程序设置如下:94℃预变性5min,35个扩增循环(94℃变性40sec,最适合退火温度下扩增30sec,72℃延伸40sec),72℃延伸7min。所选引物序列见表1。
(3)page凝胶检测。将上述pcr扩增产物加入6×dnaloadingbuffer,进行6%page凝胶电泳检测,page胶分别用硝酸银溶液和氢氧化钠溶液进行染色和显色。结果见图2。
(4)根据个体扩增的条带有无和page凝胶上的位置确定其基因型,统计能够跨物种转移的ssr标记,统计结果见表4。
表4锦绣杜鹃开发的est-ssr标记跨物种扩增结果
申请人开发的est-ssr引物跨物种检测结果表明本发明利用转录组数据开发了大量的多态性ssr引物,并对这些引物进行跨物种通用性应用。据此,本发明适用于锦绣杜鹃est-ssr引物的开发,可将本发明提供的est-ssr分子标记应用于更多的杜鹃花科植物中,为锦绣杜鹃及其他杜鹃花科植物的遗传多样性分析研究、遗传连锁图谱构、花性状关键基因定位、分子标记辅助育种等研究奠定了基础。
序列表
<110>黄冈师范学院
<120>锦绣杜鹃est-ssr标记开发及应用
<160>30
<170>siposequencelisting1.0
<210>1
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>1
ggagaagaggtacagagtc19
<210>2
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>2
aattcacatttccccgatca20
<210>3
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>3
tattgtacagctcccctttg20
<210>4
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>4
cctcaatgttctatcgacgt20
<210>5
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>5
caagccgaagaaacaagaa19
<210>6
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>6
aatcaaacgtccacacaaac20
<210>7
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>7
gatcagccaaaacacacac19
<210>8
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>8
agacctgaccctccttatac20
<210>9
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>9
cgacgagtttcccaaattg19
<210>10
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>10
ctccttcaccttgtcattga20
<210>11
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>11
tccttctctttcgcgcgt18
<210>12
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>12
accagtgtgttgatcttg18
<210>13
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>13
ccaccaaggtatctcgaaaa20
<210>14
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>14
aaaaccctaaaacccgttct20
<210>15
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>15
atagtcttccacaactctgc20
<210>16
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>16
cgatttgcttacctagagct20
<210>17
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>17
ctctctctcatctcgaaacc20
<210>18
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>18
atgtttgtgagttcgtggat20
<210>19
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>19
aaaagtcgaatcgtacccat20
<210>20
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>20
ggaatgataaggcgaggatt20
<210>21
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>21
aacagagagagcaaaaca18
<210>22
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>22
ccgttgagcttgagagtag19
<210>23
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>23
tgaagctgttttagactccc20
<210>24
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>24
catgatgggaaagcaaagt19
<210>25
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>25
ccatgacgaaccctattga19
<210>26
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>26
tcctgatattcctttgcaca20
<210>27
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>27
ctctttcccctttcatgtga20
<210>28
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>28
aagtgttgagtcctcgtatg20
<210>29
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>29
tacctacagtcctaatgcca20
<210>30
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>30
acacataagaaaccctgcat20
- 还没有人留言评论。精彩留言会获得点赞!