一种高韧性丝素蛋白凝胶的制备方法与流程
本发明涉及一种高韧性凝胶及其制备方法,特别涉及一种以丝素蛋白为原料,不需要有机溶剂或其他添加物,制备具有可弯曲、高韧性性能的丝素水凝胶的制备技术。
背景技术:
丝素蛋白是一种天然蛋白质材料,再生丝素材料具有良好的生物相容性、生物可降解速度及可调控的理化性质,这使得这种材料作为一种组织修复支架材料获得研究者的广泛关注。
丝素蛋白水凝胶具有类似细胞外基质的结构,是一种生物相容性良好的组织修复材料。但是,水凝胶的机械性能通常较弱、抗弯强度差,脆而易折。主要原因是其内部聚合物链密度较低,大分子链之间纠缠少,摩擦小。提高丝素蛋白浓度可以提高丝素水凝胶的强度,却无法改变其脆性。而许多人体组织如软骨等则表现出较强的韧性、机械强度。因此,当前的丝素水凝胶性能与软骨等组织的机械性能并不匹配,具有高韧性的水凝胶的制备仍需进一步探索。
当前,丝素蛋白高韧性凝胶的制备已有报道:
(1)公开号为CN106492279A的中国发明专利“一种丝素蛋白-透明质酸复合凝胶的快速制备方法”中,需要将丝素蛋白溶液与透明质酸混合,在交联剂的作用下制成快速复合凝胶。该凝胶克服了普通丝素蛋白水凝胶的柔韧性差,易脆等缺点。但交联剂的使用有损凝胶的生物相容性。
(2)公开号为CN106866996A的中国发明专利“一种蚕丝丝素蛋白质凝胶的快速制备方法”中,需要向一定浓度的丝素溶液加入pH调节剂,调节溶液pH值,最终在弱电场条件下快速形成具有良好机械性能的丝素蛋白凝胶。该法制备丝素凝胶不需要添加交联剂,但是调节pH值,引入大量H+离子,仍会有损凝胶的生物相容性。
制备条件温和,生物相容性良好的丝素蛋白高韧性凝胶的制备仍需进一步探索。
技术实现要素:
本发明鉴于现有技术存在的不足,本发明提供一种无需交联剂、酸等有损凝胶的生物相容性的处理,操作简单,且制备效率高的丝素蛋白高韧性凝胶的制备方法。
为达到上述目的,本发明的技术方案步骤如下:
步骤(1)制备普通丝素蛋白水溶液,将得到的溶液进行浓缩或稀释,溶液的质量分数为0.1~30%;然后将调整浓度后的丝素蛋白溶液进行结晶化处理,得到丝素蛋白纳米纤维溶液;
步骤(2)对普通丝素蛋白溶液进行浓缩或稀释,调节其浓度,令丝素蛋白质量分数不低于2%;
步骤(3)将结晶型丝素蛋白纳米纤维溶液与步骤(2)调整浓度后的丝素蛋白溶液共混,共混时普通丝素蛋白占总蛋白的含量低于99%;在0-100℃的条件下,静置0~96小时,得到高韧性丝素蛋白凝胶。
作为优选,步骤(1)中制备丝素蛋白水溶液的具体方法为:将剪碎的蚕丝在浓度为0.001~0.05M的碳酸钠溶液中微沸蒸煮5~60min,其中蚕丝与碳酸钠溶液的浴比为1:100~1:1000,用去离子水洗净蚕丝表面的丝胶,将脱胶后的蚕丝于20~90℃条件下烘干,并于10~80℃温度下溶解于溴化锂溶液中,浴比1:100~30:100,溶解后采用去离子水透析3d以上,得到的丝素蛋白溶液。
作为优选,步骤(1)中,丝素蛋白纳米纤维溶液中的蛋白结构为结晶型蛋白。
作为优选,步骤(3)中将丝素蛋白纳米纤维溶液与稀释后的普通丝素蛋白溶液共混,共混时结晶型丝素蛋白占总蛋白的含量低于90%。
作为优选,所述步骤(3)中静置温度为25-80℃。
本发明具有以下明显优点:
(1)可在短时间内形成丝素蛋白高韧性凝胶,时间可以短至几分钟,大大增加了制备丝素蛋白高韧性凝胶的工作效率。
(2)由于本发明在制备过程是利用丝蛋白的自组装行为,改变丝素蛋白的构象,形成水凝胶网络,整个制备过程不需添加任何化学交联剂或其他有毒试剂,不会引起丝素蛋白水凝胶生物相容性降低。
(3)由于本发明所制备的丝素蛋白高韧性水凝胶只包含可降解的丝素蛋白,降解产物为氨基酸,可被人体吸收,炎症反应小,显著提高了材料的生物安全性。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
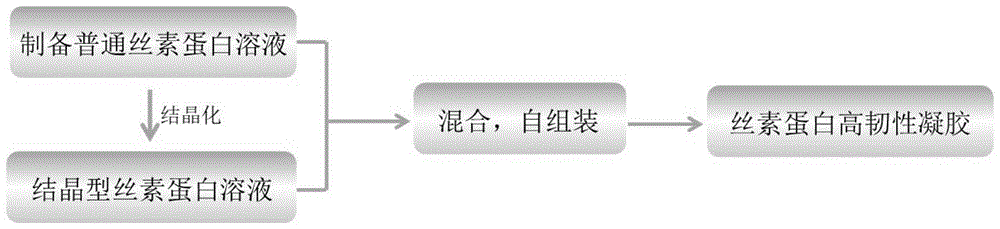
图1是本实施例一所述发明所提供的一种丝素蛋白高韧性凝胶制备方法的流程图。
图2是实施例二所述的丝素蛋白高韧性凝胶的抗弯曲情况图像。
图3是实施例三所述的丝素蛋白高韧性凝胶与普通丝素凝胶的透光性对比图。
图4是实施例四所述的丝素蛋白高韧性凝胶与普通丝素凝胶压缩后的形状保持能力对比图。
具体实施方式
下面结合附图及实施例对本发明做进一步描述:
实施例一:
制备丝素蛋白溶液。具体为:将10g蚕丝在0.02M的Na2CO3溶液中100℃煮30min,以去除蚕丝外部的丝胶蛋白,使用去离子水冲洗,重复以上操作3次后将蚕丝60℃下烘干。称取上述处理后的脱胶蚕丝27g溶解于100mL浓度为9.3mol/L LiBr溶液中,60℃下溶解处理6小时。然后用截留分子量3500的透析袋浸在去离子水中透析3天,期间每两小时换一次水,去除溶液中的LiBr,从而得到纯净的丝素蛋白溶液。
将丝素溶液在60℃条件下浓缩到30%后,用去离子水稀释到1%,在烘箱中放置24h,然后用超声细胞粉碎仪超声30s,得到丝素蛋白纳米纤维溶液。
将普通丝素蛋白溶液浓度调整到2%,然后将其与1%的结晶型丝素蛋白溶液以40:1的体积比混合,在100℃条件下静置后得到丝素蛋白凝胶。
请参见图1,图1是本发明中丝素蛋白高韧性凝胶制备方法的流程图。
实施例二:
采用与实施例一相同的方法制备纯净丝素蛋白溶液与丝素蛋白纳米纤维溶液。
将普通丝素蛋白溶液浓度调整到9%,然后将其与1%的结晶型丝素蛋白溶液在室温下以1:1的体积比混合,后吸取到圆柱形模具中,静置后得到丝素蛋白凝胶棒。将凝胶棒取出,两端对弯,凝胶棒可被弯曲,未发生断裂。
请参见图2,图2是丝素蛋白高韧性凝胶的抗弯曲情况图像。从图2可见,该凝胶具有较强的韧性。
实施例三:
采用与实施例一相同的方法制备纯净丝素蛋白溶液与结晶型丝素蛋白溶液。
将普通丝素蛋白溶液稀释到3%,然后将其与1%的结晶型丝素蛋白溶液在60℃条件下以1:1的体积比混合,得到丝素蛋白高韧性水凝胶。
将2%的普通丝素溶液超声处理,静止后得到普通丝素水凝胶。
请参见图3,图3是实施例三所述的相同蛋白浓度的丝素蛋白高韧性凝胶与普通丝素凝胶的对比图,高韧性凝胶具有较高的透明度。
实施例四:
采用与实施例三相同的方法制备丝素蛋白高韧性凝胶与丝素蛋白普通凝胶。以2mm/min的速度进行压缩测试,产生40%的应变后,停止压缩,取出载荷。
请参见图4,图4是实施例四所述的丝素蛋白高韧性凝胶压缩后的形状完整性图像。产生40%的应变后,普通丝素凝胶因其脆性产生碎裂,而丝素蛋白高韧性凝胶压缩后的形状保持完整。
实施例五:
采用与实施例一相同的方法制备纯净丝素蛋白溶液。
将普通丝素蛋白溶液稀释到0.1%,然后放置在60℃条件下进行结晶化诱导直至普通丝素蛋白转变为结晶型丝素,用超声细胞粉碎仪超声30s,得到丝素蛋白纳米纤维溶液。然后将其与5%的丝素蛋白溶液以1:1的体积比混合,在0℃条件下静置96小时,得到丝素蛋白高强度、高韧性水凝胶。
综上所述,本发明利用丝蛋白的自组装行为,改变丝素蛋白的二级结构及蛋白形态,得到高韧性的丝素蛋白水凝胶。本发明在制备过程不需要交联剂等有毒试剂,不会引起丝素蛋白支架生物相容性降低。并且所制备的水凝胶具有较高的抗弯曲、抗压缩能力,能够在较大程度上维持支架的形态,满足软骨等承重组织修复的需要。
- 还没有人留言评论。精彩留言会获得点赞!