用于LINE-1的检测引物组及其应用的制作方法
本发明涉及基因领域,特别涉及用于line-1的检测引物组及其应用。
背景技术:
癌症是困扰人类的一大疾病,根据统计数据,2018年全球新增约1810万癌症病例,另有970癌症患者死亡。在中国2018年新发癌症病例约380万,死亡人数约229万,总体癌症发病率上升3.2%左右。癌症已成为我国四大慢性病之一,严重影响人民健康。癌症的早期筛查、诊断能有效的降低癌症死亡率。治疗效果、复发的有效监测能为癌症病人的精准治疗提供可靠参考。目前癌症诊断的金标准是影像学检测。但是影像学检测存在一些局限性:很难在早期发现肿瘤发生,且部分影像学检测存在适应性差〔如肠镜〕、成本较高等缺点。
cell-freedna(cfdna)即游离dna,是存在于血清、血浆和其它体液(即尿、腹水等)且高度降解的细胞外dna。主要来源于细胞的凋亡和死亡。当细胞发生癌变时,会释放特异的dna进入血液,通过检测肿瘤特也cfdna,可以监测癌症的发生与发展。随着技术的发展循环肿瘤dna(ctdna)在肿瘤检测中便捷、快速、无创等优点,表现出很强的优势。
然而目前以ctdna为标志物的检测方法大多需要检测多个基因,且只能监测一种癌症,导致检测成本居高不下,很难广泛推广,且检测特异性和灵敏度较低。
长散布元件(line-1,longinterspersednucleotidelement1,l1)属于中度重复序列,是人类基因组中最丰富的能自主转座的非末端重复序列反转录转座子,约有850000个拷贝,占基因组的17%。典型的l1元件全长为6500kb,包括5’utr,两个读码框(orf1和orf2),和3’utr。两个读码框分别编码两种蛋白,具有分子伴侣活性的非特异rna结合蛋白(40kda)及具有反转录酶(rt)和核酸内切酶(en)的活性150kda的蛋白质,是反转座作用所必须的。line-1过表达可以促进细胞增殖,对肿瘤的预后及转移产生影响。line-1反转录转座和甲基化状态在临床诊断、预后、疾病监测以及治疗等方面有着潜在的应用价值。
line-1与多种肿瘤相关,通过检测line-1的表达情况下,可以对多种肿瘤进行筛查。然而line-1在人类基因组中虽然存在很多份拷贝,但是由于95%以上的line-15′端存在缺失,其中有10%line-1还存在重排,因此具有序列全长及转座活性的line-1非常少见,具体line-1上哪些片段可作为肿瘤筛查的检测靶点,需要对line-1相关研究做广泛调研,并需要较为大量样品的验证。且单一引物检测效果可能并不具备足够的特异性和灵敏度,两对甚至多对引物结合可能有更好的效果,如何筛选出合适的引物组合是一个难点所在。
技术实现要素:
本发明的目的在于克服现有技术的至少一个不足,提供一种用于line-1的检测引物组及其应用。
本发明所采取的技术方案是:
本发明的第一个方面,提供:
一种用于游离line-1检测的引物组,包括以下至少一对引物:
line1-s-a引物对,其正向序列为:tggcacatatacaccatggaa,反向序列为:tgagaatgatggtttccaatttc;
line1-l-a引物对,其正向序列为:acacctattccaaaattgaccac,反向序列为:ttccctctacacactgctttga。
在一些实例中,所述引物组同时包括line1-s-a引物对和line1-l-a引物对。
本发明的第二个方面,提供:
一种用于游离line-1检测的试剂盒,其包括本发明第一个方面的用于游离line-1检测的引物组。
在一些实例中,所述试剂盒的引物组同时包括line1-s-a引物对和line1-l-a引物对。
在一些实例中,所述试剂盒还包括游离dna提取试剂。
在一些实例中,所述试剂盒为定量pcr试剂盒。
本发明的第三个方面,提供:
本发明第一个方面的用于游离line-1检测的引物组在制备肿瘤筛查、诊断或监测试剂中的应用。
在一些实例中,所述引物组同时包括line1-s-a引物对和line1-l-a引物对。
在一些实例中,所述肿瘤选自结直肠癌、淋巴癌、肺癌、肝癌、宫颈癌、胃癌。
在一些实例中,基于line1-s-a引物对和line1-l-a引物对对样品的绝对定量pcr结果,计算负荷指数,确定肿瘤的情况。
在一些实例中,所述负荷指数的计算方法为:
y=22.457+8.507*x1+1.59*x2-0.314*x1*x2
式中,x1为通过引物line1-s-act值计算出的浓度取log2,x2为通过引物line1-l-act值计算出的浓度取log2,y为负荷指数,浓度单位为ng/μl。
肿瘤的情况包括但不限于肿瘤发生的风险、预后、复发风险、治疗进展或响应、转移风险、特别是淋巴转移风险。
本发明的第四个方面,提供:
本发明第二个方面的用于游离line-1检测的试剂盒在制备肿瘤筛查、诊断或监测试剂中的应用。
在一些实例中,所述试剂盒的引物组同时包括line1-s-a引物对和line1-l-a引物对。
在一些实例中,所述肿瘤选自结直肠癌、淋巴癌、肺癌、肝癌、宫颈癌、胃癌。
在一些实例中,基于line1-s-a引物对和line1-l-a引物对对样品的绝对定量pcr结果,计算负荷指数,确定肿瘤的情况。
在一些实例中,所述负荷指数的计算方法为:
y=22.457+8.507*x1+1.59*x2-0.314*x1*x2
式中,x1为通过引物line1-s-act值计算出的浓度取log2,x2为通过引物line1-l-act值计算出的浓度取log2,y为负荷指数,浓度单位为ng/μl。
本发明的第五个方面,提供:
一种用于肿瘤筛查、诊断或监测的系统,包括:
游离line-1基因提取装置;
游离line-1基因定量装置,其使用的引物组如本发明第一个方面所述;
数据处理装置,基于游离line-1基因定量的结果,计算负荷指数,确定肿瘤的情况。
在一些实例中,所述引物组同时包括line1-s-a引物对和line1-l-a引物对。
在一些实例中,所述肿瘤选自结直肠癌、淋巴癌、肺癌、肝癌、宫颈癌、胃癌。
在一些实例中,基于line1-s-a引物对和line1-l-a引物对对样品的绝对定量pcr结果,计算负荷指数,确定肿瘤的情况。
在一些实例中,所述负荷指数的计算方法为:
y=22.457+8.507*x1+1.59*x2-0.314*x1*x2
式中,x1为通过引物line1-s-act值计算出的浓度取log2,x2为通过引物line1-l-act值计算出的浓度取log2,y为负荷指数,浓度单位为ng/μl。
实例中负荷指数越高,肿瘤发生风险越高,或进展越严重。在同一肿瘤患者对比中,肿瘤负荷指数升高,说明肿瘤发展出现恶化。
本发明的有益效果是:
本发明一些实例的引物组,可以有效扩增出能有效反应肿瘤情况的游离line-1基因片段,同时具有很好反应的特异性及极佳的扩增效率。特别的,结合于line1-s-a引物对和line1-l-a引物对的绝对定量pcr结果,可以通过计算负荷指数反应肿瘤情况,可以用于多种肿瘤的早期筛查、复发诊断、治疗监测,具有简便、快捷、准确的优势。
本发明一些实例的试剂盒,具有很好的特异性及极佳的扩增效率。可以用于多种肿瘤的早期筛查、复发诊断、治疗监测,具有简便、快捷、准确的优势。
附图说明
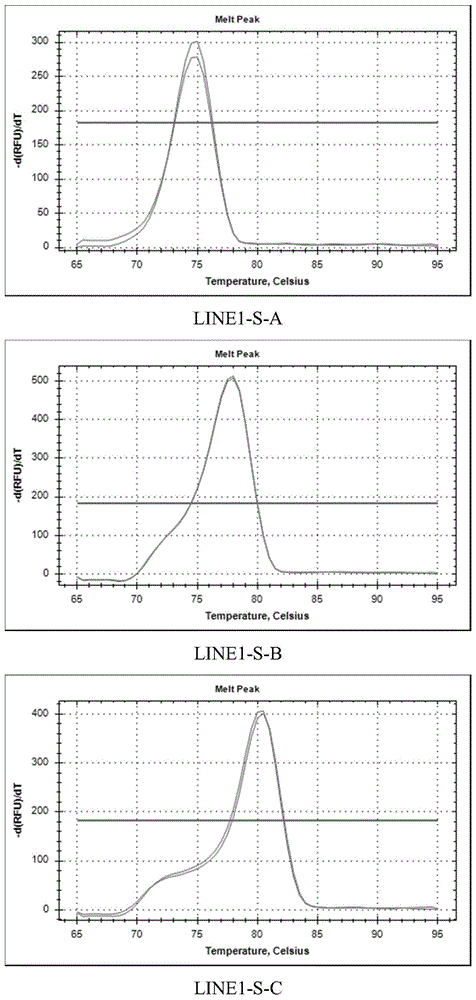
图1、三对短片段引物line1-s-a、line1-s-b、line1-s-c溶解曲线;
图2、三对长片段引物line1-l-a、line1-l-b、line1-l-c溶解曲线;
图3、三对短片段引物line1-s-a、line1-s-b、line1-s-c在相同模板浓度下扩增曲线;
图4、三对长片段引物line1-l-a、line1-l-b、line1-l-c在相同模板浓度下扩增曲线;
图5、line1-s-a灵敏度检测结果;
图6、line1-l-a灵敏度检测结果;
图7、肿瘤患者与健康人line1负荷指数;
图8、健康人、肿瘤患者line-a检测浓度的roc曲线;
图9、健康人、肿瘤患者line-b检测浓度的roc曲线;
图10、健康人、肿瘤患者肿瘤负荷指数的roc曲线;
图11、肿瘤患者手术前和手术后一个月肿瘤负荷指数比对。
具体实施方式
下面结合实验,进一步说明本发明的技术方案。
特异性比较:
基于公开的line1序列,设计了2对长片段扩增引物、2对短片段扩增引物,并选则以往文献中报道过的一长一短2对引物(表1)作为比较,发现line1-s-a、line1-l-a两对引物具有最好的扩增效率和特异性,因此后续检测实验均用line1-s-a、line1-l-a。
表1:设计引物与文献中引物序列
注:“*”处所注文献为:宋现让.以line1基因为测定对象的ctdna含量和完整性测定方法。引物序列的seqidno.编号由上到下依次为1~12。
用标准品对表2中引物灵敏度和特异性进行qpcr检测。利用实时荧光定量pcr中溶解曲线的原理,通过分别测试line1-s-a和line1-l-a两对引物的特异性,发现line1-s-a和line1-l-a的溶解曲线具有单一的峰(图1和图2),表明该方法中的line1-s-a和line1-l-a两对引物具有较高的特异性,能够特异地检测到line基因。并且从pcr扩增曲线看出line1-s-a和line1-l-a具有比其他引物更好的扩增能力(图3和图4)。因此挑选line1-s-a和line1-l-a作为检测引物。
扩增灵敏度实验:
利用梯度稀释,将标准品dna稀释到10-2、10-3、10-4、10-5、10-6ng/μl5个浓度梯度,分别对line1-s-a和line1-l-a两对引物灵敏度进行检测。发现line1-s-a和line1-l-a引物灵敏度均可达到10-6ng/μl(图5和图6)。
实际样品的检测:
血液采集:用edta采血管或游离dna采血管采集血液样品,在4℃条件下1600×g离心10min,离心后取上清(血浆),再4℃条件下以12000×g离心10min去除残余细胞,上清所需的血浆,标记后-20℃保存。
cfdna提取:取分离得到的上清200μl,用qiagenqiaampbloodminikitdna提取试剂盒提取cfdna,测定dna浓度。
qpcr检测:采用绝对定量pcr的方法。其中标准品为themo公司的taqmancontrolgenomicdna(human),货号为4312660。将标准品稀释至以下浓度:10-3、10-2、10-1、0.5、1、2ng/μl。标准品各浓度和样品用line1-s-a、line1-l-a两对引物进行qpcr检测。每个样品做3个重复。两对引
结果分析:根据标准品浓度与ct值拟合标准曲线,得出计算浓度公式,将样品ct值带入公式,计算得到样品中目的基因浓度。将浓度带入以下公式,得到负荷指数。
y=22.457+8.507*x1+1.59*x2-0.314*x1*x2
其中x1为通过引物line1-s-act值计算出的浓度取log2,log2dna97,x2为通过引物line1-l-act值计算出的浓度取log2,y为负荷指数。
肿瘤患者line1负荷指数均比健康人高
首先我们收集了健康人样品,肠癌、淋巴瘤、肺癌、肝癌、宫颈癌、胃癌患者样品。检测结果如图7所示,肿瘤患者line1负荷指数均比健康对照组高。
肿瘤负荷指数更能区分肿瘤患者和健康人
我们分别以line-a检测浓度,line-b检测浓度、肿瘤负荷指数作为区分指标,做roc曲线,roc曲线下的面积(auc)分别为0.934、0.916、0.976(图8~10)。说明用肿瘤负荷指数作为区分指标,更能分辨出肿瘤患者和健康人。
line1负荷指数检测结果在手术前后对比结果
其次我们收集了癌症患者手术前,或者手术过程中的血液样品,以及手术1个月后的血液样品进行检测。所有患者在手术1个月后临床表现比术前好转。手术前与手术后一个月对比,通过配对t检验,p值为1.206×10-6。结果如图11。可以清楚地看出,手术前后的line1负荷指数具有显著区别。
sequencelisting
<110>邹畅
<120>用于line-1的检测引物组及其应用
<130>line-1
<160>12
<170>patentinversion3.5
<210>1
<211>21
<212>dna
<213>人工序列
<400>1
tggcacatatacaccatggaa21
<210>2
<211>23
<212>dna
<213>人工序列
<400>2
tgagaatgatggtttccaatttc23
<210>3
<211>20
<212>dna
<213>人工序列
<400>3
aacaacaggtgctggagagg20
<210>4
<211>20
<212>dna
<213>人工序列
<400>4
tgaggaatcgccacactgac20
<210>5
<211>22
<212>dna
<213>人工序列
<400>5
aggagatgtgctggagaaagag22
<210>6
<211>24
<212>dna
<213>人工序列
<400>6
ctccactgataggaagaaaagaat24
<210>7
<211>23
<212>dna
<213>人工序列
<400>7
acacctattccaaaattgaccac23
<210>8
<211>22
<212>dna
<213>人工序列
<400>8
ttccctctacacactgctttga22
<210>9
<211>20
<212>dna
<213>人工序列
<400>9
cccaatacaggagcacccag20
<210>10
<211>20
<212>dna
<213>人工序列
<400>10
ataggtgtggtgtggtgctg20
<210>11
<211>22
<212>dna
<213>人工序列
<400>11
aggagatgtgctggagaaagag22
<210>12
<211>22
<212>dna
<213>人工序列
<400>12
caagttgctagtggtgagcttc22
- 还没有人留言评论。精彩留言会获得点赞!