树脂组合物、固化物、紫外线吸收剂、紫外线截止滤波器、透镜、保护材料、化合物及化合物的合成方法与流程
1.本发明涉及一种树脂组合物。更详细而言,涉及一种包含苯并二硫醇化合物的树脂组合物。并且,本发明涉及一种固化物、紫外线吸收剂、紫外线截止滤波器、透镜、保护材料、化合物及化合物的合成方法。
背景技术:
2.苯并二硫醇化合物的紫外线的吸收性优异,用于紫外线吸收剂等。例如,专利文献1中记载有将特定的苯并二硫醇化合物用作紫外线吸收剂的内容。
3.以往技术文献
4.专利文献
5.专利文献1:国际公开第2019/159570号
技术实现要素:
6.发明要解决的技术课题
7.作为对紫外线吸收剂要求的特性之一,要求着色少。并且,近年来,要求对波长400nm附近的更长波长的紫外线也具有高吸收能力。
8.因此,本发明的目的在于提供一种能够制造对波长400nm附近的紫外线的吸收能力优异的固化物等的树脂组合物、固化物、紫外线吸收剂、紫外线截止滤波器、透镜、保护材料、化合物及化合物的合成方法。
9.用于解决技术课题的手段
10.本发明人对具有由式(1)表示的骨架的化合物进行深入研究的结果,发现由后述式(1)表示的化合物是对波长400nm附近的紫外线的吸收能力优异且着色少的化合物,并且为可用作紫外线吸收剂的化合物,直至完成本发明。因此,本发明提供以下内容。
11.<1>一种树脂组合物,其包含由式(1)表示的化合物和树脂;
12.[化学式1]
[0013][0014]
在式(1)中,r1及r2分别独立地表示烷基、芳基或杂环基,
[0015]
r3及r6分别独立地表示烷氧基、酰氧基、氨基甲酰氧基或烷氧基羰氧基,
[0016]
r4表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0017]
r5表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0018]
r1与r2可以相互键合而形成环;
[0019]
r3与r4可以相互键合而形成环;
[0020]
r4与r5可以相互键合而形成环;
[0021]
r5与r6可以相互键合而形成环;
[0022]
其中,r3及r6分别独立地为酰氧基或氨基甲酰氧基时,r4及r5中的至少一个为芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基。
[0023]
<2>根据<1>所述的树脂组合物,其中,
[0024]
在式(1)中,r4是烷基、芳基、烷氧基或芳氧基,r5是氢原子、烷基、芳基、烷氧基或芳氧基。
[0025]
<3>根据<1>或<2>所述的树脂组合物,其中,
[0026]
在式(1)中,r3及r6中的至少一个为烷氧基。
[0027]
<4>根据<1>所述的树脂组合物,其中,
[0028]
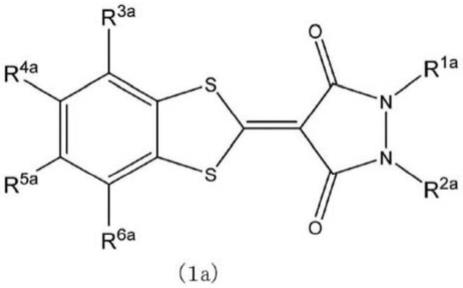
由上述式(1)表示的化合物是由下述式(1a)表示的化合物;
[0029]
[化学式2]
[0030][0031]
在式(1a)中,r
1a
及r
2a
分别独立地表示烷基,
[0032]r3a
及r
6a
分别独立地表示烷氧基或酰氧基,
[0033]r4a
表示烷基或烷氧基,
[0034]r5a
表示氢原子、烷基或烷氧基;
[0035]r1a
与r
2a
可以相互键合而形成环;
[0036]r3a
与r
4a
可以相互键合而形成环;
[0037]r4a
与r
5a
可以相互键合而形成环;
[0038]r5a
与r
6a
可以相互键合而形成环;
[0039]
其中,r
3a
及r
6a
为酰氧基时,r
4a
及r
5a
中的至少一个为烷氧基。
[0040]
<5>根据<1>至<4>中任一项所述的树脂组合物,其进一步包含由式(2)表示的化合物;
[0041]
[化学式3]
[0042][0043]
在式(2)中,r
11
及r
12
分别独立地表示烷基、芳基或杂环基,
[0044]r13
及r
16
分别独立地表示羟基、烷氧基、芳氧基、酰氧基、氨基甲酰氧基、烷氧基羰氧基、芳氧基羰氧基、亚磺酰基氧基或磺酰氧基,
[0045]r14
表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0046]r15
表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0047]r11
与r
12
可以相互键合而形成环;
[0048]r13
与r
14
可以相互键合而形成环;
[0049]r14
与r
15
可以相互键合而形成环;
[0050]r15
与r
16
可以相互键合而形成环;
[0051]
其中,r
13
及r
16
中的至少一个为羟基。
[0052]
<6>根据<1>至<5>中任一项所述的树脂组合物,其进一步包含除由上述式(1)表示的化合物以外的其他紫外线吸收剂。
[0053]
<7>根据<1>至<6>中任一项所述的树脂组合物,其中,
[0054]
上述树脂为选自(甲基)丙烯酸树脂、聚苯乙烯树脂、聚酯树脂、聚氨酯树脂、聚硫氨基甲酸酯树脂、聚酰亚胺树脂、环氧树脂、聚碳酸酯树脂及酰化纤维素树脂中的至少一种。
[0055]
<8>一种固化物,其通过使用<1>至<7>中任一项所述的树脂组合物而得到。
[0056]
<9>一种紫外线吸收剂,其包含由式(1)表示的化合物;
[0057]
[化学式4]
[0058][0059]
在式(1)中,r1及r2分别独立地表示烷基、芳基或杂环基,
[0060]
r3及r6分别独立地表示烷氧基、酰氧基、氨基甲酰氧基或烷氧基羰氧基,
[0061]
r4表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0062]
r5表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0063]
r1与r2可以相互键合而形成环;
[0064]
r3与r4可以相互键合而形成环;
[0065]
r4与r5可以相互键合而形成环;
[0066]
r5与r6可以相互键合而形成环;
[0067]
其中,r3及r6分别独立地为酰氧基或氨基甲酰氧基时,r4及r5中的至少一个为芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基。
[0068]
<10>根据<9>所述的紫外线吸收剂,其进一步包含由式(2)表示的化合物;
[0069]
[化学式5]
[0070][0071]
在式(2)中,r
11
及r
12
分别独立地表示烷基、芳基或杂环基,
[0072]r13
及r
16
分别独立地表示羟基、烷氧基、芳氧基、酰氧基、氨基甲酰氧基、烷氧基羰氧基、芳氧基羰氧基、亚磺酰基氧基或磺酰氧基,
[0073]r14
表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0074]r15
表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0075]r11
与r
12
可以相互键合而形成环;
[0076]r13
与r
14
可以相互键合而形成环;
[0077]r14
与r
15
可以相互键合而形成环;
[0078]r15
与r
16
可以相互键合而形成环;
[0079]
其中,r
13
及r
16
中的至少一个为羟基。
[0080]
<11>一种紫外线截止滤波器,其包含<9>或<10>所述的紫外线吸收剂。
[0081]
<12>一种透镜,其包含<9>或<10>所述的紫外线吸收剂。
[0082]
<13>一种保护材料,其包含<9>或<10>所述的紫外线吸收剂。
[0083]
<14>一种由式(1a)表示的化合物,其中,
[0084]
[化学式6]
[0085][0086]
在式(1a)中,r
1a
及r
2a
分别独立地表示烷基,
[0087]r3a
及r
6a
分别独立地表示烷氧基或酰氧基,
[0088]r4a
表示烷基或烷氧基,
[0089]r5a
表示氢原子、烷基或烷氧基;
[0090]r1a
与r
2a
可以相互键合而形成环;
[0091]r3a
与r
4a
可以相互键合而形成环;
[0092]r4a
与r
5a
可以相互键合而形成环;
[0093]r5a
与r
6a
可以相互键合而形成环;
[0094]
其中,r
3a
及r
6a
为酰氧基时,r
4a
及r
5a
中的至少一个为烷氧基。
[0095]
<15>一种由式(1a)表示的化合物的合成方法,其包括使由式(2a)表示的化合物与卤代烷基化合物或羧酸卤化物进行反应的工序;
[0096]
[化学式7]
[0097][0098]
在式(1a)中,r
1a
及r
2a
分别独立地表示烷基,
[0099]r3a
及r
6a
分别独立地表示烷氧基或酰氧基,
[0100]r4a
表示烷基或烷氧基,
[0101]r5a
表示氢原子、烷基或烷氧基;
[0102]r1a
与r
2a
可以相互键合而形成环;
[0103]r3a
与r
4a
可以相互键合而形成环;
[0104]r4a
与r
5a
可以相互键合而形成环;
[0105]r5a
与r
6a
可以相互键合而形成环;
[0106]
其中,r
3a
及r
6a
为酰氧基时,r
4a
及r
5a
中的至少一个为烷氧基;
[0107]
[化学式8]
[0108][0109]
在式(2a)中,r
11a
及r
12a
分别独立地表示烷基,
[0110]r14a
表示烷基或烷氧基,
[0111]r15a
表示氢原子、烷基或烷氧基;
[0112]r14a
与r
15a
可以相互键合而形成环。
[0113]
发明效果
[0114]
根据本发明,能够提供一种能够制造波长400nm附近的紫外线的吸收能力优异的固化物等的树脂组合物、固化物、紫外线吸收剂、紫外线截止滤波器、透镜、保护材料、化合物及化合物的合成方法。
附图说明
[0115]
图1是液晶显示装置的一实施方式,是表示在前侧的偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图。
[0116]
图2是液晶显示装置的一实施方式,是表示在背光侧的偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图。
[0117]
图3是液晶显示装置的一实施方式,是表示在前侧的内保护膜上添加有本发明的紫外线吸收剂的结构的概略图。
[0118]
图4是液晶显示装置的一实施方式,是表示在背光侧的内保护膜上添加有本发明的紫外线吸收剂的结构的概略图。
[0119]
图5是液晶显示装置的一实施方式,是表示通过粘合剂或粘结剂而在前侧的相位差膜上贴合有包含本发明的紫外线吸收剂的光学膜的结构的概略图。
[0120]
图6是液晶显示装置的一实施方式,是表示通过粘合剂或粘结剂而在背光侧的相位差膜上贴合有包含本发明的紫外线吸收剂的光学膜的结构的概略图。
[0121]
图7是液晶显示装置的一实施方式,是表示在前侧的粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图。
[0122]
图8是液晶显示装置的一实施方式,是表示在背光侧的粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图。
[0123]
图9是液晶显示装置的一实施方式,是表示在前侧的功能层中添加有本发明的紫外线吸收剂的结构的概略图。
[0124]
图10是液晶显示装置的一实施方式,是表示在背光侧的功能层中添加有本发明的紫外线吸收剂的结构的概略图。
[0125]
图11是有机电致发光显示装置的一实施方式,是表示在偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图。
[0126]
图12是有机电致发光显示装置的一实施方式,是表示在粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图。
[0127]
图13是有机电致发光显示装置的一实施方式,是表示通过粘合剂或粘结剂而在触控面板上贴合有包含本发明的紫外线吸收剂的光学膜的结构的概略图。
具体实施方式
[0128]
以下,对本发明的内容进行详细说明。
[0129]
在本说明书中的基团(原子团)的标记中,未标有经取代及未经取代的标记包含不具有取代基的基团和具有取代基的基团。例如,“烷基”不仅包括不具有取代基的烷基(未经取代的烷基),也包括具有取代基的烷基(取代烷基)。
[0130]
在本说明书中,使用“~”表示的数值范围是指将“~”前后记载的数值作为下限值及上限值而包括的范围。
[0131]
在本说明书中,总固体成分表示从树脂组合物的总成分去除溶剂的成分的合计量。
[0132]
在本说明书中,“(甲基)丙烯酸酯”表示丙烯酸酯及甲基丙烯酸酯两者或任一者,“(甲基)丙烯酸”表示丙烯酸及甲基丙烯酸两者或任一者,“(甲基)烯丙基”表示烯丙基及甲基烯丙基两者或任一者,“(甲基)丙烯酰基”表示丙烯酰基及甲基丙烯酰基两者或任一者。
[0133]
在本说明书中,“工序”这一术语不仅包括独立的工序,在无法与其他工序明确区分的情况下,只要可实现该工序所期待的作用,则也包括在本术语中。
[0134]
在本说明书中,重均分子量(mw)及数均分子量(mn)定义为通过凝胶渗透色谱法(gpc)测定的聚苯乙烯换算值。
[0135]
<树脂组合物>
[0136]
本发明的树脂组合物的特征为包含由式(1)表示的化合物和树脂。
[0137]
由式(1)表示的化合物是波长400nm附近的紫外线的吸收能力优异且着色少的化合物。因此,本发明的树脂组合物能够制造波长400nm附近的紫外线的吸收能力优异的固化物等。
[0138]
并且,由式(1)表示的化合物与树脂等的相溶性良好,也能够抑制固化物表面的面状不均匀等。可获得这种效果的详细原因尚不明确,但推测由式(1)表示的化合物因空间排斥等影响而容易在r3与r4之间产生扭曲。推测通过这种扭曲的产生,化合物的结晶性下降而与树脂等的相溶性得到了提高。
[0139]
以下,对本发明的树脂组合物进行详细说明。
[0140]
<<由式(1)表示的化合物(化合物(1))>>
[0141]
本发明的树脂组合物包含由式(1)表示的化合物(以下,也称为化合物(1))。
[0142]
[化学式9]
[0143][0144]
在式(1)中,r1及r2分别独立地表示烷基、芳基或杂环基,
[0145]
r3及r6分别独立地表示烷氧基、酰氧基、氨基甲酰氧基或烷氧基羰氧基,
[0146]
r4表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0147]
r5表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0148]
r1与r2可以相互键合而形成环;
[0149]
r3与r4可以相互键合而形成环;
[0150]
r4与r5可以相互键合而形成环;
[0151]
r5与r6可以相互键合而形成环;
[0152]
其中,r3及r6分别独立地为酰氧基或氨基甲酰氧基时,r4及r5中的至少一个为芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基。
[0153]
在式(1)中,r1及r2分别独立地表示烷基、芳基或杂环基,优选为烷基或芳基。从耐光性的观点考虑,优选r1及r2分别独立地为烷基。并且,从波长400nm附近的紫外线的吸收性的观点考虑,优选r1及r2分别独立地为芳基。
[0154]
r1及r2所表示的烷基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷基可以为直链、支链及环状中的任一种,优选为直链或支链。烷基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0155]
r1及r2所表示的芳基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。作为芳基,优选为苯基及萘基,更优选为苯基。芳基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0156]
r1及r2所表示的杂环基中的杂环优选包括5元或6元的饱和或不饱和杂环。可以在杂环中缩合有脂肪族环、芳香族环或其他杂环。作为构成杂环的环的杂原子,可举出b、n、o、s、se及te,优选为n、o及s。杂环的碳原子优选具有游离的原子价(一价)(杂环基在碳原子上键合)。优选的杂环基的碳原子数为1~40,更优选为1~30,进一步优选为1~20。作为杂环基中的饱和杂环的例子,可举出吡咯烷环、吗啉环、2-硼-1,3-二氧戊环及1,3-噻唑烷环。作为杂环基中的不饱和杂环的例子,可举出咪唑环、噻唑环、苯并噻唑环、苯并噁唑环、苯并三唑环、苯并硒唑环、吡啶环、嘧啶环及喹啉环。杂环基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0157]
r1与r2可以相互键合而形成环。r1与r2键合而形成的环优选为5元环或6元环。r1与
r2键合而形成的环可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0158]
在式(1)中,r3及r6分别独立地表示烷氧基、酰氧基、氨基甲酰氧基或烷氧基羰氧基,优选为烷氧基或酰氧基,从抑制着色且更容易提高波长400nm附近的紫外线的吸收性的理由考虑,进一步优选r3及r6中的至少一个为烷氧基。根据本发明人的研究,发现关于苯并二硫醇的苯环上的取代基,电子供给能力越高的基团,越容易使化合物的极大吸收波长转向长波长侧。由于烷氧基是电子供给能力更高的取代基,因此推测更能够使化合物的极大吸收波长转向长波长侧。尤其优选r3及r6两者均为烷氧基。
[0159]
r3及r6所表示的烷氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷氧基可以为直链及支链中的任一种。烷氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0160]
r3及r6所表示的酰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10。酰氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0161]
r3及r6所表示的氨基甲酰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10,最优选为2~8。氨基甲酰氧基可以为直链及支链中的任一种。氨基甲酰氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0162]
r3及r6所表示的烷氧基羰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10,最优选为2~8。烷氧基羰氧基可以为直链及支链中的任一种。烷氧基羰氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0163]
在式(1)中,r4表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,r5表示氢原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基。
[0164]
r4及r5所表示的烷基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷基可以为直链、支链及环状中的任一种,优选为直链或支链。烷基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0165]
r4及r5所表示的芳基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。作为芳基,优选为苯基及萘基,更优选为苯基。芳基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0166]
r4及r5所表示的烷氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷氧基可以为直链及支链中的任一种。烷氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0167]
r4及r5所表示的芳氧基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。芳氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0168]
r4及r5所表示的苯胺基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。苯胺基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0169]
r4及r5所表示的酰氨基的碳原子数优选为2~30,更优选为2~20,进一步优选为2
~15,尤其优选为2~10。酰氨基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0170]
r4及r5所表示的烷基磺酰基氨基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10。烷基磺酰基氨基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0171]
r4及r5所表示的芳基磺酰基氨基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。芳基磺酰基氨基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0172]
r4及r5所表示的烷硫基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷硫基可以为直链及支链中的任一种。烷硫基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0173]
r4及r5所表示的芳硫基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。芳硫基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0174]
在式(1)中,r3与r4可以相互键合而形成环,r4与r5可以相互键合而形成环,r5与r6可以相互键合而形成环。这些基团彼此键合而形成的环优选为5元环或6元环。这些基团彼此键合而形成的环可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0175]
从抑制着色且更容易提高波长400nm附近的紫外线的吸收性的理由考虑,优选r4为烷基、芳基、烷氧基或芳氧基,r5为氢原子、烷基、芳基、烷氧基或芳氧基,更优选r4为烷基或烷氧基,r5为氢原子、烷基或烷氧基。
[0176]
并且,从容易合成的观点考虑,优选r4为烷基、芳基、烷氧基或芳氧基,r5为氢原子,更优选r4为烷基或烷氧基,r5为氢原子。
[0177]
并且,从吸收光谱的长波长化的观点考虑,优选r4及r5分别独立地为烷基、芳基、烷氧基或芳氧基,更优选为烷基或烷氧基,进一步优选r4及r5两者均为烷基或者r4及r5两者均为烷氧基。
[0178]
并且,也优选r4与r5相互键合而形成环。
[0179]
然而,在式(1)中,r3及r6为酰氧基时,r4及r5中的至少一个为芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,优选为芳基、烷氧基、芳氧基或酰氧基,进一步优选为烷氧基。
[0180]
由式(1)表示的化合物(化合物(1))优选为由下述式(1a)表示的化合物。
[0181]
[化学式10]
[0182]
[0183]
在式(1a)中,r
1a
及r
2a
分别独立地表示烷基,
[0184]r3a
及r
6a
分别独立地表示烷氧基或酰氧基,
[0185]r4a
表示烷基或烷氧基,
[0186]r5a
表示氢原子、烷基或烷氧基;
[0187]r1a
与r
2a
可以相互键合而形成环;
[0188]r3a
与r
4a
可以相互键合而形成环;
[0189]r4a
与r
5a
可以相互键合而形成环;
[0190]r5a
与r
6a
可以相互键合而形成环;
[0191]
其中,r
3a
及r
6a
为酰氧基时,r
4a
及r
5a
中的至少一个为烷氧基。
[0192]r1a
及r
2a
所表示的烷基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷基可以为直链、支链及环状中的任一种,优选为直链或支链。烷基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0193]r1a
与r
2a
可以相互键合而形成环。r
1a
与r
2a
键合而形成的环优选为5元环或6元环。r
1a
与r
2a
键合而形成的环可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0194]
在式(1a)中,r
3a
及r
6a
分别独立地表示烷氧基或酰氧基,从抑制着色且更容易提高波长400nm附近的紫外线的吸收性的理由考虑,优选r
3a
及r
6a
中的至少一个为烷氧基,更优选r
3a
及r
6a
两者均为烷氧基。
[0195]r3a
及r
6a
所表示的烷氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷氧基可以为直链及支链中的任一种。烷氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0196]r3a
及r
6a
所表示的酰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10。酰氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0197]
在式(1a)中,r
4a
表示烷基或烷氧基,r
5a
表示氢原子、烷基或烷氧基。
[0198]r4a
及r
5a
所表示的烷基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷基可以为直链、支链及环状中的任一种,优选为直链或支链。烷基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0199]r4a
及r
5a
所表示的烷氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷氧基可以为直链及支链中的任一种。烷氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0200]
在式(1a)中,r
3a
与r
4a
可以相互键合而形成环,r
4a
与r
5a
可以相互键合而形成环,r
5a
与r
6a
可以相互键合而形成环。这些基团彼此键合而形成的环优选为5元环或6元环。这些基团彼此键合而形成的环可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0201]
(取代基t)
[0202]
作为取代基t,可举出以下基团。
[0203]
卤素原子(例如,氯原子、溴原子、碘原子);
[0204]
烷基[直链、支链、环状的烷基。具体而言,直链或支链的烷基(优选为碳原子数1~
30的直链或支链的烷基,例如甲基、乙基、正丙基、异丙基、叔丁基、正辛基、二十烷基、2-氯乙基、2-氰基乙基、2-乙基己基)、环烷基(优选为碳原子数3~30的环烷基,例如,环己基、环戊基、4-正十二烷基环己基)、双环烷基(优选为碳原子数5~30的双环烷基,即从碳原子数5~30的双环烷烃去除一个氢原子的一价基团。例如,双环[1,2,2]庚烷-2-基、双环[2,2,2]辛烷-3-基),而且也包括环结构多的三环结构等。以下说明的取代基中的烷基(例如烷硫基的烷基)也表示这种概念的烷基。];
[0205]
烯基[直链、支链、环状的烯基。具体而言,直链或支链的烯基(优选为碳原子数2~30的直链或支链的烯基,例如,乙烯基、烯丙基、异戊二烯基、香叶基、油烯基)、环烯基(优选为碳原子数3~30的环烯基。即为将碳原子数3~30的环烯烃的氢原子去除一个的一价基团。例如,2-环戊烯-1-基、2-环己烯-1-基)、双环烯基(优选为碳原子数5~30的双环烯基,即为将具有一个双键的双环烯烃的氢原子去除一个的一价基团。例如,包括双环[2,2,1]庚-2-烯-1-基、双环[2,2,2]辛-2-烯-4-基)。];
[0206]
炔基(优选为碳原子数2~30的直链或支链的炔基。例如,乙炔基、炔丙基);
[0207]
芳基(优选为碳原子数6~30的芳基。例如苯基、对甲苯基、萘基、间氯苯基、邻十六酰基氨基苯基);
[0208]
杂环基(优选为从5元或6元的芳香族或非芳香族杂环化合物去除一个氢原子的一价基团,进一步优选为碳原子数3~30的5元或6元的芳香族杂环基。例如,2-呋喃基、2-噻吩基、2-嘧啶基、2-苯并噻唑基);
[0209]
氰基;
[0210]
羟基;
[0211]
硝基;
[0212]
羧基;
[0213]
烷氧基(优选为碳原子数1~30的直链或支链的烷氧基。例如,甲氧基、乙氧基、异丙氧基、叔丁氧基、正辛氧基、2-甲氧基乙氧基);
[0214]
芳氧基(优选为碳原子数6~30的芳氧基。例如,苯氧基、2-甲基苯氧基、4-叔丁基苯氧基、3-硝基苯氧基、2-十四烷酰氨基苯氧基);
[0215]
杂环氧基(优选为碳原子数2~30的杂环氧基。例如,1-苯基四唑-5-氧基、2-四氢吡喃氧基);
[0216]
酰氧基(优选为甲酰氧基、碳原子数2~30的烷基羰氧基、碳原子数6~30的芳基羰氧基。例如,甲酰氧基、乙酰氧基、三甲基乙酰氧基、硬脂酰氧基、苯甲酰氧基、对甲氧基苯基羰氧基);
[0217]
氨基甲酰氧基(优选为碳原子数1~30的氨基甲酰氧基。例如,n,n-二甲基氨基甲酰氧基、n,n-二乙基氨基甲酰氧基、吗啉基羰氧基、n,n-二-正辛氨基羰氧基、n-正辛基氨基甲酰氧基);
[0218]
烷氧基羰氧基(优选为碳原子数2~30的烷氧基羰氧基。例如甲氧基羰氧基、乙氧基羰氧基、叔丁氧基羰氧基、正辛基羰氧基);
[0219]
芳氧基羰氧基(优选为碳原子数7~30的芳氧基羰氧基。例如,苯氧基羰氧基、对甲氧基苯氧基羰氧基、对正十六烷氧基苯氧基羰氧基);
[0220]
氨基(优选为氨基、碳原子数1~30的烷基氨基、碳原子数6~30的苯胺基。例如,氨
基、甲基氨基、二甲基氨基、苯胺基、n-甲基-苯胺基、二苯基氨基);
[0221]
酰氨基(优选为甲酰氨基、碳原子数2~30的烷基羰氨基、碳原子数6~30的芳基羰基氨基。例如,甲酰氨基、乙酰氨基、三甲基乙酰氨基、月桂酰氨基、苯甲酰氨基、3,4,5-三-正辛氧基苯基羰基氨基);
[0222]
氨基羰基氨基(优选为碳原子数1~30的氨基羰基氨基。例如,氨基甲酰氨基、n,n-二甲基氨基羰基氨基、n,n-二乙基氨基羰基氨基、吗啉基羰基氨基);
[0223]
烷氧基羰基氨基(优选为碳原子数2~30的烷氧基羰基氨基。例如,甲氧基羰基氨基、乙氧基羰基氨基、叔丁氧基羰基氨基、正十八烷氧基羰基氨基、n-甲基-甲氧基羰基氨基);
[0224]
芳氧基羰基氨基(优选为碳原子数7~30的芳氧基羰基氨基。例如,苯氧基羰基氨基、对氯苯氧基羰基氨基、间正辛氧基苯氧基羰基氨基);
[0225]
氨磺酰基氨基(优选为碳原子数0~30的氨磺酰基氨基。例如,氨磺酰基氨基、n,n-二甲基氨基磺酰基氨基、n-正辛氨基磺酰基氨基);
[0226]
烷基或芳基磺酰基氨基(优选为碳原子数1~30的烷基磺酰基氨基、碳原子数6~30的芳基磺酰基氨基。例如,甲基磺酰基氨基、丁基磺酰基氨基、苯基磺酰基氨基、2,3,5-三氯苯基磺酰基氨基、对甲基苯基磺酰基氨基);
[0227]
巯基;
[0228]
烷硫基(优选为碳原子数1~30的烷硫基。例如甲硫基、乙硫基、正十六烷硫基);
[0229]
芳硫基(优选为碳原子数6~30的芳硫基。例如,苯硫基、对氯苯硫基、间甲氧基苯硫基);
[0230]
杂环硫基(优选为碳原子数2~30的杂环硫基。例如,2-苯并噻唑硫基、1-苯基四唑-5-基硫基);
[0231]
氨磺酰基(优选为碳原子数0~30的氨磺酰基。例如,n-乙基氨磺酰基、n-(3-十二烷氧基丙基)氨磺酰基、n,n-二甲基氨磺酰基、n-乙酰基氨磺酰基、n-苯甲酰基氨磺酰基、n-(n
’‑
苯基氨基甲酰基)氨磺酰基);
[0232]
磺基;
[0233]
烷基或芳基亚磺酰基(优选为碳原子数1~30的烷基亚磺酰基、6~30的芳基亚磺酰基。例如,甲基亚磺酰基、乙基亚磺酰基、苯基亚磺酰基、对甲基苯基亚磺酰基);
[0234]
烷基或芳基磺酰基(优选为碳原子数1~30的烷基磺酰基、6~30的芳基磺酰基。例如,甲基磺酰基、乙基磺酰基、苯基磺酰基、对甲基苯基磺酰基);
[0235]
酰基(优选为甲酰基、碳原子数2~30的烷基羰基、碳原子数7~30的芳基羰基、通过碳原子数4~30的碳原子与羰基键合的杂环羰基。例如,乙酰基、三甲基乙酰基、2-氯乙酰基、硬脂酰基、苯甲酰基、对正辛氧基苯基羰基、2-吡啶基羰基、2-呋喃基羰基);
[0236]
芳氧基羰基(优选为碳原子数7~30的芳氧基羰基。例如,苯氧基羰基、邻氯苯氧基羰基、间硝基苯氧基羰基、对叔丁基苯氧基羰基);
[0237]
烷氧基羰基(优选为碳原子数2~30的烷氧基羰基。例如,甲氧基羰基、乙氧基羰基、叔丁氧基羰基、正十八烷氧基羰基);
[0238]
氨基甲酰基(优选为碳原子数1~30的氨基甲酰基。例如,氨基甲酰基、n-甲基氨基甲酰基、n,n-二甲基氨基甲酰基、n,n-二-正辛基氨基甲酰基、n-(甲基磺酰基)氨基甲酰
基);
[0239]
芳基或杂环偶氮基(优选为碳原子数6~30的芳基偶氮基、碳原子数3~30的杂环偶氮基。例如,苯基偶氮基、对氯苯基偶氮基、5-乙硫基-1,3,4-噻二唑-2-基偶氮基);
[0240]
酰亚胺基(优选为n-琥珀酰亚胺基、n-邻苯二甲酰亚胺基);
[0241]
膦基(优选为碳原子数2~30的膦基。例如,二甲基膦基、二苯基膦基、甲基苯氧基膦基)
[0242]
膦酰基(优选为碳原子数2~30的膦酰基。例如,膦酰基、二辛氧基膦酰基、二乙氧基膦酰基);
[0243]
膦酰基氧基(优选为碳原子数2~30的膦酰基氧基。例如,二苯氧基膦酰基氧基、二辛氧基膦酰基氧基);
[0244]
膦酰基氨基(优选为碳原子数2~30的膦酰基氨基。例如,二甲氧基膦酰基氨基、二甲基氨基膦酰基氨基);
[0245]
在以上举出的基团中,关于具有氢原子的基团,1个以上的氢原子可以被上述取代基t取代。作为这种取代基的例子,可举出烷基羰基氨基磺酰基、芳基羰基氨基磺酰基、烷基磺酰基氨基羰基、芳基磺酰基氨基羰基。作为具体例,可举出甲基磺酰基氨基羰基、对甲基苯基磺酰基氨基羰基、乙酰氨基磺酰基、苯甲酰氨基磺酰基等。
[0246]
作为化合物(1)的具体例,可举出以下结构的化合物。在以下所示的结构式中,me是甲基,et是乙基,bu是丁基,tbu是叔丁基,pr是丙基,ph是苯基。
[0247]
[化学式11]
[0248][0249]
[化学式12]
[0250][0251]
[化学式13]
[0252][0253]
化合物(1)可优选地用作紫外线吸收剂。化合物(1)的极大吸收波长优选存在于381~420nm的波长范围内,更优选存在于381~400nm的波长范围内。
[0254]
根据下述式算出的化合物(1)在波长405nm处的摩尔吸光系数ε
405
优选为500以上,更优选为1000以上,进一步优选为2000以上,尤其优选为3000以上。
[0255]
ε
405
=ε
max
×
(a
405
/a
max
)
[0256]
ε
405
是化合物(1)在波长405nm处的摩尔吸光系数,ε
max
是化合物(1)在极大吸收波长处的摩尔吸光系数,a
405
是化合物(1)在波长405nm处的吸光度,a
max
是化合物(1)在极大吸收波长处的吸光度。
[0257]
在乙酸乙酯中测定的化合物(1)的分光吸收光谱中,在波长405nm处的吸光度a
405
与在波长430nm处的吸光度a
430
之比(a
430
/a
405
)优选小于0.13,更优选为0.1以下。上述比的下限并没有特别限定,能够设为0以上。具有这种吸光度比的化合物与在波长405nm附近的吸收高无关而在紫外区域附近的可见区域的透光性优异,因此在更长波长侧的紫外线的吸收性优异且可见透明性优异。另外,欲将化合物中的紫外线的吸收区域转向更长波长侧时,可见区域的透光性(尤其,紫外区域附近的可见区域的透光性)也存在下降的趋势,但根据本发明的化合物(1),具有以高水准维持可见区域的透光性且更长波长侧的紫外线的吸收性优异等技术上优异的效果。
[0258]
化合物(1)能够参考日本特开2016-081035号公报、日本专利第5376885号公报等中记载的合成法来合成。
[0259]
树脂组合物的总固体成分中的化合物(1)的含量优选为0.01~50质量%。下限优选为0.05质量%以上,更优选为0.1质量%以上。上限优选为40质量%以下,更优选为30质量%以下,更优选为20质量%以下。
[0260]
化合物(1)的含量相对于树脂的100质量份,优选为0.01~50质量份。下限优选为0.05质量份以上,更优选为0.1质量份以上。上限优选为40质量份以下,更优选为30质量份
以下,更优选为20质量份以下。
[0261]
树脂组合物可以仅包含1种化合物(1),也可以包含2种以上。包含2种以上化合物(1)时,优选这些的合计量在上述范围内。
[0262]
<<由式(2)表示的化合物(化合物(2))>>
[0263]
本发明的树脂组合物进一步优选包含由式(2)表示的化合物(以下,也称为化合物(2))。根据该方式,能够进一步提高树脂组合物的保存稳定性。
[0264]
[化学式14]
[0265][0266]
在式(2)中,r
11
及r
12
分别独立地表示烷基、芳基或杂环基,
[0267]r13
及r
16
分别独立地表示羟基、烷氧基、芳氧基、酰氧基、氨基甲酰氧基、烷氧基羰氧基、芳氧基羰氧基、亚磺酰基氧基或磺酰氧基,
[0268]r14
表示卤素原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,
[0269]r15
表示氢原子、卤素原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基;
[0270]r11
与r
12
可以相互键合而形成环;
[0271]r13
与r
14
可以相互键合而形成环;
[0272]r14
与r
15
可以相互键合而形成环;
[0273]r15
与r
16
可以相互键合而形成环;
[0274]
其中,r
13
及r
16
中的至少一个为羟基。
[0275]
式(2)的r
11
及r
12
所表示的烷基、芳基及杂环基的含义与式(1)的r1及r2所表示的烷基、芳基及杂环基相同,优选范围也相同。式(2)的r
11
及r
12
优选为烷基或芳基。
[0276]
式(2)的r
13
及r
16
分别独立地表示羟基、烷氧基、芳氧基、酰氧基、氨基甲酰氧基、烷氧基羰氧基、芳氧基羰氧基、亚磺酰基氧基或磺酰氧基,优选为羟基、烷氧基或酰氧基,更优选为羟基或烷氧基,进一步优选为羟基。其中,r
13
及r
16
中的至少一个为羟基。
[0277]r13
及r
16
所表示的烷氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷氧基可以为直链及支链中的任一种。烷氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0278]r13
及r
16
所表示的芳氧基的碳原子数优选为6~40,更优选为6~30,进一步优选为6~20,尤其优选为6~15,最优选为6~12。芳氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0279]r13
及r
16
所表示的酰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为
2~15,尤其优选为2~10。酰氧基可以具有取代基。作为取代基,可举出在后述取代基t中说明的基团。
[0280]r13
及r
16
所表示的氨基甲酰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10,最优选为2~8。氨基甲酰氧基可以为直链及支链中的任一种。氨基甲酰氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0281]r13
及r
16
所表示的烷氧基羰氧基的碳原子数优选为2~30,更优选为2~20,进一步优选为2~15,尤其优选为2~10,最优选为2~8。烷氧基羰氧基可以为直链及支链中的任一种。烷氧基羰氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0282]r13
及r
16
所表示的芳氧基羰氧基的碳原子数优选为7~40,更优选为7~30,进一步优选为7~20,尤其优选为7~15,最优选为7~12。芳氧基羰氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0283]r13
及r
16
所表示的亚磺酰基氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15。亚磺酰基氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0284]r13
及r
16
所表示的磺酰氧基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15。磺酰氧基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。
[0285]
式(2)的r
14
表示烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基,r
15
表示氢原子、卤素原子、烷基、芳基、烷氧基、芳氧基、酰氧基、烷基氨基、苯胺基、酰氨基、烷基磺酰基氨基、芳基磺酰基氨基、烷硫基或芳硫基。关于式(2)的r
14
及r
15
所表示的这些基团的详细含义与式(1)的r4及r5相同,优选范围也相同。
[0286]
优选r
14
为烷基、芳基、烷氧基或芳氧基,r
15
为氢原子、烷基、芳基、烷氧基或芳氧基,更优选r
14
为烷基或烷氧基,r
15
为氢原子、烷基或烷氧基。
[0287]
作为优选的方式之一,可举出r
14
是烷基、芳基、烷氧基或芳氧基且r
15
是氢原子的方式。在该方式中,优选r
14
为烷基或烷氧基,r
15
为氢原子。
[0288]
并且,作为其他优选方式之一,可举出r
14
及r
15
分别独立地为烷基、芳基、烷氧基或芳氧基的方式。在该方式中,优选r
14
及r
15
分别独立地为烷基或烷氧基,更优选r
14
及r
15
两者均为烷基或者r
14
及r
15
两者均为烷氧基。
[0289]
并且,作为其他优选方式之一,可举出r
14
与r
15
可以相互键合而形成环的方式。
[0290]
作为化合物(2)的具体例,可举出以下结构的化合物。在以下所示的结构式中,me是甲基,et是乙基,tbu是叔丁基,pr是丙基,bu是丁基,ph是苯基。
[0291]
[化学式15]
[0292][0293]
[化学式16]
[0294][0295]
[化学式17]
[0296][0297]
[化学式18]
[0298][0299]
化合物(2)能够按照日本专利第5376885号公报、国际公开第2019/142539号中记载的方法合成。
[0300]
化合物(2)优选地用作紫外线吸收剂。化合物(2)的极大吸收波长优选存在于381~420nm的波长范围内,更优选存在于381~400nm的波长范围内。
[0301]
树脂组合物含有化合物(2)时,化合物(2)的含量相对于化合物(1)的100质量份,优选为5质量份以下,更优选为3质量份以下,进一步优选为1质量份以下。下限优选为0.1质量份以上。
[0302]
并且,树脂组合物的总固体成分中的化合物(1)和化合物(2)的合计含量优选为0.01~50质量%。下限优选为0.05质量%以上,更优选为0.1质量%以上。上限优选为40质量%以下,更优选为30质量%以下,更优选为20质量%以下。
[0303]
化合物(1)和化合物(2)的合计含量相对于树脂的100质量份优选为0.01~50质量份。下限优选为0.05质量份以上,更优选为0.1质量份以上。上限优选为40质量份以下,更优选为30质量份以下,更优选为20质量份以下。
[0304]
树脂组合物可以包含1种化合物(2),也可以包含2种以上。包含2种以上化合物(2)时,优选这些的合计量在上述范围内。
[0305]
并且,也优选树脂组合物实质上不包含化合物(2)。根据该方式,容易获得更优异的耐光性。另外,在本说明书中,树脂组合物实质上不包含化合物(2)是指树脂组合物的总固体成分中的化合物(2)的含量为0.001质量%以下,优选为0.0001质量%以下,更优选不含有。
[0306]
<<其他紫外线吸收剂>>
[0307]
本发明的树脂组合物能够包含除上述化合物(1)以外的其他紫外线吸收剂(以下,也称为其他紫外线吸收剂)。根据该方式,能够形成在广范围内遮住紫外区域的波长的光的固化物。
[0308]
其他紫外线吸收剂的极大吸收波长优选存在于390nm以下的波长范围内,更优选存在于380nm以下的波长范围内。
[0309]
作为其他紫外线吸收剂,可举出苯并三唑系紫外线吸收剂、二苯甲酮系紫外线吸收剂、水杨酸系紫外线吸收剂、丙烯酸酯系紫外线吸收剂、苯并二硫醇系紫外线吸收剂及三嗪系紫外线吸收剂等,优选为苯并三唑系紫外线吸收剂、二苯甲酮系紫外线吸收剂及三嗪系紫外线吸收剂,更优选为苯并三唑系紫外线吸收剂及三嗪系紫外线吸收剂。关于苯并三唑系紫外线吸收剂、二苯甲酮系紫外线吸收剂、水杨酸系紫外线吸收剂、丙烯酸酯系紫外线吸收剂及三嗪系紫外线吸收剂的具体例,可举出日本特开2009-263616号公报的0065~0070段中记载的化合物、国际公开第2017/122503号的0065段中记载的化合物等,这些内容编入本说明书中。并且,下述结构的化合物也能够优选地用作其他紫外线吸收剂。
[0310]
[化学式19]
[0311][0312]
树脂组合物含有其他紫外线吸收剂时,树脂组合物的总固体成分中的其他紫外线吸收剂的含量优选为0.01~50质量%。下限优选为0.05质量%以上,更优选为0.1质量%以上。上限优选为40质量%以下,更优选为30质量%以下,更优选为20质量%以下。
[0313]
并且,树脂组合物的总固体成分中的化合物(1)、化合物(2)及其他紫外线吸收剂的合计含量优选为0.01~50质量%。下限优选为0.05质量%以上,更优选为0.1质量%以上。上限优选为40质量%以下,更优选为30质量%以下,更优选为20质量%以下。
[0314]
树脂组合物可以仅包含1种其他紫外线吸收剂,也可以包含2种以上。包含2种以上其他紫外线吸收剂时,优选这些的合计量在上述范围内。
[0315]
<<树脂>>
[0316]
本发明的树脂组合物包含树脂。作为树脂的种类,可举出(甲基)丙烯酸树脂、聚酯树脂、聚碳酸酯树脂、乙烯基聚合物[例如,聚二烯树脂、聚烯烃树脂、聚苯乙烯树脂、聚乙烯醚树脂、聚乙烯醇树脂、聚乙烯酮树脂、聚氟乙烯树脂及聚溴化乙烯树脂等]、聚硫醚树脂、聚苯树脂、聚氨酯树脂、聚硫氨基甲酸酯树脂、聚磺酸盐树脂、亚硝基聚合物树脂、聚硅氧烷树脂、聚硫化物树脂、聚硫酯树脂、聚砜树脂、聚砜酰胺树脂、聚酰胺树脂、聚亚胺树脂、聚脲
树脂、聚膦氮烯树脂、聚硅烷树脂、聚硅氮烷树脂、聚呋喃树脂、聚苯并噁唑树脂、聚噁二唑树脂、聚苯并噻嗪吩噻嗪树脂、聚苯并噻唑树脂、聚吡嗪并喹噁啉树脂、聚均苯四甲酰亚胺树脂、聚喹噁啉树脂、聚苯并咪唑树脂、聚氧代异吲哚啉树脂、聚二氧代异吲哚啉树脂、聚三嗪树脂、聚哒嗪树脂、聚哌嗪树脂、聚吡啶树脂、聚哌啶树脂、聚三唑树脂、聚吡唑树脂、聚吡咯烷树脂、聚碳硼烷树脂、聚氧杂双环壬烷树脂、聚二苯并呋喃树脂、聚酞内酯树脂、聚缩醛树脂、聚酰亚胺树脂、烯烃树脂、环状烯烃树脂、环氧树脂、酰化纤维素树脂等。能够根据用途和目的适当选择。关于这些的详细内容,能够参考日本特开2009-263616号公报的0075~0097段中的记载,该内容编入本说明书中。
[0317]
并且,作为树脂,也能够使用具有聚合性基团的树脂。作为具有聚合性基团的树脂的市售品,可举出dianal br系列(聚甲基丙烯酸甲酯(pmma),例如dianal br-80、br-83、br-87;mitsubishi chemical corporation);photomer6173(含有cooh的聚氨酯丙烯酸低聚物,diamond shamrock co.,ltd.);viscoat r-264、ks resist 106(均为osaka organic chemical industry ltd.);cyclomer p系列(例如aca230aa)、placcel cf200系列(均为daicel corporation);ebecryl 3800(daicel ucb co.,ltd.);acrycure-rd-f8(nippon shokubai co.,ltd.)等。
[0318]
作为树脂,从容易获得与化合物(1)的相溶性良好且面状不均匀得到抑制的固化物的理由考虑,优选为选自(甲基)丙烯酸树脂、聚苯乙烯树脂、聚酯树脂、聚氨酯树脂、聚硫氨基甲酸酯树脂、聚酰亚胺树脂、环氧树脂、聚碳酸酯树脂及酰化纤维素树脂中的至少一种,更优选为选自(甲基)丙烯酸树脂、聚苯乙烯树脂、聚酯树脂、聚氨酯树脂、聚硫氨基甲酸酯树脂、聚碳酸酯树脂及酰化纤维素树脂中的至少一种。
[0319]
作为酰化纤维素树脂,可优选地使用日本特开2012-215689号公报的0016~0021段中记载的酰化纤维素。作为聚酯树脂,也能够使用toyobo co.,ltd.制的byron系列(例如,byron 500)等市售品。作为(甲基)丙烯酸树脂的市售品,也能够使用soken chemical&engineering co.,ltd.的sk dyne系列(例如,sk dyne-sf2147等)。
[0320]
作为聚苯乙烯树脂,优选使用以下记载的聚苯乙烯系树脂。在此,苯乙烯系树脂是指如下树脂:构成树脂的单体单元中比率最高的单体单元是源自苯乙烯单体的单体单元。例如,由2种成分组成的树脂的情况下,是指包含50质量%以上源自苯乙烯系单体的单体单元的树脂。在此,苯乙烯系单体是指在其结构中具有苯乙烯骨架的单体。苯乙烯系树脂优选包含70质量%以上源自苯乙烯系单体的单体单元,更优选包含85质量%以上。
[0321]
作为苯乙烯系单体的具体例,可以为苯乙烯或其衍生物的均聚物,也可以为苯乙烯或其衍生物与其他共聚性单体的二元共聚物或二元以上的共聚物。在此,苯乙烯衍生物是苯乙烯上键合有其他基团的化合物,例如,可举出邻甲基苯乙烯、间甲基苯乙烯、对甲基苯乙烯、2,4-二甲基苯乙烯、邻乙基苯乙烯、对乙基苯乙烯之类的烷基苯乙烯、以及羟基苯乙烯、叔丁氧基苯乙烯、乙烯基苯甲酸、邻氯苯乙烯、对氯苯乙烯之类的在苯乙烯的苯核上导入有羟基、烷氧基、羧基、卤素等的取代苯乙烯等。
[0322]
并且,苯乙烯系树脂包括在苯乙烯系单体成分中共聚了其他单体成分者。作为能够共聚的单体,可举出甲基丙烯酸甲酯、甲基丙烯酸环己酯、甲基丙烯酸甲基苯酯、甲基丙烯酸异丙酯等甲基丙烯酸烷基酯;丙烯酸甲酯、丙烯酸乙酯、丙烯酸丁酯、丙烯酸2-乙基己酯、丙烯酸环己酯等丙烯酸烷基酯等不饱和羧酸烷基酯单体;甲基丙烯酸、丙烯酸、衣康酸、
马来酸、富马酸、桂皮酸等不饱和羧酸单体;作为马来酸酐、衣康酸、乙基马来酸、甲基衣康酸、氯马来酸等酸酐的不饱和二羧酸酐单体;丙烯腈、甲基丙烯腈等不饱和腈单体;1,3-丁二烯、2-甲基-1,3-丁二烯(异戊二烯)、2,3-二甲基-1,3-丁二烯、1,3-戊二烯、1,3-己二烯等共轭二烯等,也能够使这些的2种以上共聚。苯乙烯系树脂也能够使用市售品。作为市售品,可举出as-70(丙烯腈/苯乙烯共聚树脂,nippon steel chemical&material co.,ltd.制)、sma2000p(苯乙烯/马来酸共聚物,kawahara petrochemical co.,ltd)等。
[0323]
作为苯乙烯系树脂,能够同时使用组成、分子量等不同的多种。
[0324]
苯乙烯系树脂能够通过公知的阴离子、块状、悬浮、乳化或溶液聚合方法获得。并且,在聚苯乙烯系树脂中,共轭二烯、苯乙烯系单体的苯环的不饱和双键可以被氢化。氢化率能够通过核磁共振装置(nmr)测定。
[0325]
树脂的重均分子量(mw)优选为3000~2000000。上限优选为1000000以下,更优选为500000以下。下限优选为4000以上,更优选为5000以上。
[0326]
树脂的总透光率优选为80%以上,更优选为85%以上,进一步优选为90%以上。另外,在本说明书中,树脂的总透光率是根据日本化学会编“第4版实验化学讲座29高分子材料介质”(丸善、1992年)225~232页中记载的内容测定的值。
[0327]
树脂组合物的总固体成分中的树脂的含量优选为1~99.9质量%。下限优选为70质量%以上。上限优选为95质量%以下,更优选为90质量%以下。树脂组合物可以包含1种树脂,也可以包含2种以上。包含2种以上树脂时,优选这些的合计量在上述范围内。
[0328]
<<固化性化合物>>
[0329]
树脂组合物能够含有固化性化合物。作为固化性化合物,可举出聚合性化合物、具有-o-si-o-结构的化合物等。
[0330]
作为聚合性化合物,能够没有限制地使用通过赋予能量而能够聚合固化的化合物。作为聚合性化合物,可举出具有含有烯属不饱和键的基团的化合物、具有环氧基的化合物、具有羟甲基的化合物等,优选为具有含有烯属不饱和键的基团的化合物,更优选为具有2个以上含有烯属不饱和键的基团的化合物。作为含有烯属不饱和键的基团,可举出乙烯基、烯丙基、(甲基)丙烯酰基等。
[0331]
关于聚合性化合物,例如,可以为单体、预聚物(即二聚体、三聚体或低聚物)及这些的混合物、以及选自单体及预聚物的化合物的(共)聚合物等中的任一种。
[0332]
作为用作聚合性化合物的具有含有烯属不饱和键的基团的化合物,可举出不饱和羧酸(例如,丙烯酸、甲基丙烯酸、衣康酸、巴豆酸、异巴豆酸、马来酸等)、不饱和羧酸的酯及不饱和羧酸的酰胺、以及不饱和羧酸或其酯或酰胺的(共)聚合物。其中,优选为不饱和羧酸和脂肪族多元醇的酯及不饱和羧酸和脂肪族多元胺的酰胺、以及这些的均聚物或共聚物。
[0333]
并且,作为用作聚合性化合物的具有含有烯属不饱和键的基团的化合物,可举出具有亲核性取代基(例如,羟基、氨基、巯基等)的不饱和羧酸酯或不饱和羧酸酰胺与单官能或多官能异氰酸酯化合物或环氧化合物的加成反应物;具有亲核性取代基的不饱和羧酸酯或不饱和羧酸酰胺与单官能或多官能羧酸的脱水缩合反应物;具有亲电子性取代基(例如,异氰酸酯基、环氧基等)的不饱和羧酸酯或不饱和羧酸酰胺与单官能或多官能醇、胺或硫醇的加成反应物;具有脱离性取代基(例如,卤素基、甲苯磺酰氧基等)的不饱和羧酸酯或不饱和羧酸酰胺与单官能或多官能醇、胺或硫醇的取代反应物;等。此外,也可举出将上述不饱
和羧酸取代为不饱和膦酸、苯乙烯或乙烯醚等而获得的化合物。
[0334]
并且,可以在用作聚合性化合物的具有含有烯属不饱和键的基团的化合物中,同时使用官能数不同的多种化合物或聚合性基团的种类不同的多种化合物(例如,丙烯酸酯、甲基丙烯酸酯、苯乙烯系化合物、乙烯醚系化合物等)。
[0335]
作为具有含有烯属不饱和键的基团的化合物的市售品,可举出nippon kayaku co.,ltd.的kyarad(注册商标)系列(例如,pet-30、tpa-330等)、evonik公司的polyvest(注册商标)110m等、shin-nakamura chemical co.,ltd.的nk ester系列(例如nk estera-9300等)的多官能(甲基)丙烯酸酯化合物。
[0336]
作为用作聚合性化合物的具有环氧基的化合物(以下,也称为环氧化合物),可举出单官能或多官能环氧丙基醚化合物、多官能脂肪族环氧丙基醚化合物等。并且,作为环氧化合物,也能够使用具有脂环式环氧基的化合物。作为环氧化合物,可举出在1分子中具有1个环氧基的化合物。环氧化合物优选为在1分子中具有1~100个环氧基的化合物。环氧基数的上限例如能够设为10个以下,也能够设为5个以下。环氧基的下限优选为2个以上。作为单官能环氧化合物的具体例,可举出2-乙基己基环氧丙基醚等。作为多官能环氧化合物的具体例,可举出1,4-环己烷二甲醇二环氧丙基醚、3’,4
’‑
环氧环己基甲基3,4-环氧环己烷羧酸酯等。
[0337]
环氧化合物可以为低分子化合物(例如,分子量小于1000),也可以为高分子化合物(macromolecule)(例如,分子量为1000以上,在聚合物的情况下,重均分子量为1000以上)中的任一种。环氧化合物的重均分子量优选为2000~100000。重均分子量的上限优选为10000以下,更优选为5000以下,进一步优选为3000以下。作为环氧化合物的市售品,可举出daicel corporation制的celloxide 2021p(商品名,3’,4
’‑
环氧环己基甲基3,4-环氧环己烷羧酸酯)、new japan chemical co.,ltd.的rikaresin dme-100(商品名,含有1,4-环己烷二甲醇二环氧丙基醚作为主成分)等多官能环氧化合物等。
[0338]
作为具有羟甲基的化合物(以下,也称为羟甲基化合物),可举出羟甲基与氮原子或形成芳香族环的碳原子键合的化合物。作为羟甲基与氮原子键合的化合物,可举出烷氧基甲基化三聚氰胺、羟甲基化三聚氰胺、烷氧基甲基化苯并胍胺、羟甲基化苯并胍胺、烷氧基甲基化甘脲、羟甲基化甘脲、烷氧基甲基化脲、羟甲基化脲及二异氰酸甲苯酯的三羟甲丙烷赋予物等。
[0339]
作为聚合性化合物,也能够使用高分子化合物。作为高分子的聚合性化合物,可举出(甲基)丙烯酸树脂、酯树脂、氨基甲酸酯树脂、氟系树脂等。作为市场上销售的市售品的例子,可举出dianal br系列(聚甲基丙烯酸甲酯(pmma),例如dianal br-80、br-83、br-87;mitsubishi chemical corporation);photomer 6173(含有cooh的聚氨酯丙烯酸低聚物,diamond shamrock co.,ltd.);viscoat r-264、ks resist 106(均为osaka organic chemical industry ltd);cyclomer p系列(例如aca230aa)、placcel cf200系列(均为daicel corporation);ebecryl 3800(daicel ucb co.,ltd.);acrycure-rd-f8(nippon shokubai co.,ltd.)等。另外,高分子的聚合性化合物是也符合树脂的成分。
[0340]
从提高固化后的强度的观点考虑,高分子的聚合性化合物优选为能够形成交联结构的化合物。交联结构的形成并没有特别限制,例如,可举出同时使用高分子的聚合性化合物和多官能(甲基)丙烯酸酯单体的方法;同时使用导入了反应性基团的高分子的聚合性化
合物和具有能够与上述反应性基团反应的交联性基团的交联剂的方法等。
[0341]
作为反应性基团,可举出包含活性氢的基团,具体而言,例如可举出选自羟基、伯氨基及仲氨基中的基团。作为导入了反应性基团的高分子的聚合性化合物,例如,可举出包含源自(甲基)丙烯酸酯单体的结构单元且具有2个以上包含活性氢的基团的(甲基)丙烯酸树脂等。
[0342]
作为交联剂,可举出具有2个以上异氰酸酯基作为交联性基团的聚异氰酸酯,作为市场上销售的市售品的例子,可举出shin-nakamura chemical co.,ltd.的ad-tmp、a-9550(均为商品名)等。其中,优选同时使用具有2个以上(优选为3个以上)包含活性氢的基团的(甲基)丙烯酸树脂和具有2个以上异氰酸酯基的交联剂(优选具有2个以上异氰酸酯基的聚异氰酸酯,更优选具有3个以上异氰酸酯基的聚异氰酸酯)。由此,通过使包含活性氢的基团与异氰酸酯基进行反应,能够形成交联结构。
[0343]
作为具有-o-si-o-结构的化合物,优选为水解性硅化合物,更优选为水解性烷氧基硅烷,进一步优选为3官能或4官能烷氧基硅烷。作为具有-o-si-o-结构的化合物的具体例,能够举出四甲氧基硅烷、四乙氧基硅烷、四-正丙氧基硅烷、四-异丙氧基硅烷、四-正丁氧基硅烷、甲基三甲氧基硅烷、甲基三乙氧基硅烷、乙基三甲氧基硅烷、乙基三乙氧基硅烷、正丙基三甲氧基硅烷、正丙基三乙氧基硅烷、苯基三甲氧基硅烷、苯基三乙氧基硅烷、γ-环氧丙氧基丙基三甲氧基硅烷、γ-环氧丙氧基丙基三乙氧基硅烷、γ-环氧丙氧基丙基甲基二甲氧基硅烷、γ-环氧丙氧基丙基甲基二乙氧基硅烷、γ-甲基丙烯酰氧基丙基三甲氧基硅烷、γ-甲基丙烯酰氧基丙基三乙氧基硅烷、γ-甲基丙烯酰氧基丙基甲基二甲氧基硅烷、乙烯基三甲氧基硅烷、乙烯基三乙氧基硅烷、3,4-环氧环己基乙基三甲氧基硅烷、3,4-环氧环己基乙基三乙氧基硅烷、三-(三甲氧基甲硅烷基丙基)异氰脲酸酯、4-三甲氧基甲硅烷基苯乙烯、3,3,3-三氟丙基三甲氧基硅烷、二甲基二甲氧基硅烷、二甲基二乙氧基硅烷、二乙基二甲氧基硅烷、二乙基二乙氧基硅烷、二-正丙基二甲氧基硅烷、二-正丙基二乙氧基硅烷、二苯基二甲氧基硅烷、二乙烯基二乙氧基硅烷、双(三乙氧基甲硅烷基丙基)四硫化物、3-(三甲氧基甲硅烷基)丙基异氰酸酯、3-(三乙氧基甲硅烷基)丙基异氰酸酯等。
[0344]
树脂组合物含有固化性化合物时,树脂组合物的总固体成分中的固化性化合物的含量优选为0.1~90质量%。下限优选为1质量%以上,更优选为5质量%以上。上限优选为80质量%以下,更优选为70质量%以下。树脂组合物可以仅包含1种固化性化合物,也可以包含2种以上。包含2种以上固化性化合物时,优选这些的合计量在上述范围内。
[0345]
<<聚合引发剂>>
[0346]
树脂组合物能够含有聚合引发剂。尤其,使用聚合性化合物作为固化性化合物时,优选含有聚合引发剂。通过树脂组合物包含聚合引发剂,能够良好地开始聚合性化合物的聚合反应。聚合引发剂能够使用通过赋予能量而能够产生聚合反应所需的起始物质的化合物。作为聚合引发剂,例如,能够适当从光聚合引发剂及热聚合引发剂中选择,优选为光聚合引发剂。
[0347]
作为光聚合引发剂,例如,优选为从紫外区域至可见区域(例如280nm~400nm)内具有光吸收的化合物,可举出生成活性自由基而使光自由基聚合开始的光自由基引发剂、使光阳离子聚合开始的阳离子引发剂。
[0348]
作为光聚合引发剂,可举出卤化烃衍生物(例如,具有三嗪骨架的化合物、具有噁
二唑骨架的化合物等)、酰基膦化合物、六芳基双咪唑、肟化合物、有机过氧化物、硫化合物、酮化合物、芳香族鎓盐、氨基苯乙酮化合物、羟基苯乙酮化合物等。作为氨基苯乙酮化合物,可举出日本特开2009-191179号公报、日本特开平10-291969号公报中记载的胺基苯乙酮系引发剂。作为酰基膦化合物,可举出日本专利第4225898号公报中记载的酰基膦系引发剂。光聚合引发剂可以使用合成品,也可以使用市场上销售的市售品。
[0349]
作为羟基苯乙酮化合物的市售品,可举出omnirad 184、omnirad 1173、omnirad 2959、omnirad 127(以上为igm resins b.v.公司制)等。作为氨基苯乙酮化合物的市售品,可举出omnirad 907、omnirad 369、omnirad 369e、omnirad 379eg(以上为igm resins b.v.公司制)等。作为酰基膦化合物的市售品,可举出omnirad 819、omnirad tpo(以上为igm resins b.v.公司制)等。
[0350]
作为光聚合引发剂,优选为肟化合物。作为肟化合物的具体例,可举出日本特开2001-233842号公报中记载的化合物、日本特开2000-080068号公报中记载的化合物、日本特开2006-342166号公报中记载的化合物、日本特开2016-006475号公报的0073~0075段中记载的化合物等。肟化合物中,优选为肟酯化合物。作为肟化合物的市售品,可举出irgacure oxe01、irgacure oxe02(basf公司制)、irgacure oxe03(basf公司制)。
[0351]
作为阳离子聚合引发剂,可举出用于使光阳离子聚合开始的引发剂、色素化合物的光消色剂、光变色剂、微抗蚀剂等的公知的产酸剂等及这些的混合物。具体而言,作为阳离子聚合引发剂,例如,可举出鎓化合物、有机卤素化合物、二砜化合物。
[0352]
作为鎓化合物,例如,可举出重氮盐、铵盐、亚胺盐、鏻盐、錪盐、锍盐、鉮盐、硒盐等。关于鎓化合物的详细内容,可举出日本特开2002-029162号公报的0058~0059段中记载的化合物等。
[0353]
树脂组合物含有聚合引发剂时,树脂组合物的总固体成分中的聚合引发剂的含量优选为0.1~20质量%。下限优选为0.3质量%以上,更优选为0.4质量%以上。上限优选为15质量%以下,更优选为10质量%以下。树脂组合物可以仅包含1种聚合引发剂,也可以包含2种以上。包含2种以上聚合引发剂时,优选这些的合计量在上述范围内。
[0354]
<<产酸剂>>
[0355]
本发明的树脂组合物能够含有产酸剂。尤其,作为聚合性化合物,使用具有环氧基的化合物等阳离子聚合性化合物时,优选含有产酸剂。产酸剂可以为光产酸剂,也可以为热产酸剂。另外,在本说明书中,产酸剂是指通过施加热、光等能量而产生酸的化合物。并且,热产酸剂是指通过热分解而产生酸的化合物。并且,光产酸剂是指通过光照射而产生酸的化合物。作为产酸剂的种类、具体的化合物及优选例,能够举出日本特开2008-013646号公报的0066~0122段中记载的化合物等,能够将这些应用于本发明。
[0356]
关于热产酸剂,可举出热分解温度优选为在130℃~250℃的范围内、更优选为在150℃~220℃的范围内的化合物。作为热产酸剂,例如,可举出通过加热而产生磺酸、羧酸、二磺酰基酰亚胺等低亲核性的酸的化合物。作为从热产酸剂产生的酸,pka优选为4以下的酸,pka更优选为3以下的酸,pka进一步优选为2以下的酸。例如,优选为磺酸、被吸电子基团取代的烷基羧酸、芳基羧酸、二磺酰基酰亚胺等。作为吸电子基团,能够举出氟原子等卤素原子、三氟甲基等卤代烷基、硝基、氰基。
[0357]
作为光产酸剂,可举出通过光照射分解而产生酸的重氮盐、鏻盐、锍盐、錪盐等鎓
盐化合物、酰亚胺磺酸盐、肟磺酸盐、重氮二砜、二砜、邻硝基苄基磺酸酯等磺酸盐化合物。作为光产酸剂的市售品,可举出wpag-469(fujifilm wako pure chemical corporation.制)、cpi-100p(san-apro ltd.制)、irgacure290(basf japan ltd.)等。并且,在光产酸剂中也能够使用2-异丙基噻吨酮等。
[0358]
树脂组合物含有产酸剂时,产酸剂的含量相对于固化性化合物的100质量份,优选为0.1~100质量份,更优选为0.1~50质量份,进一步优选为0.1~20质量份。树脂组合物可以仅包含1种产酸剂,也可以包含2种以上。包含2种以上产酸剂介质时,优选这些的合计量在上述范围内。
[0359]
<<催化剂>>
[0360]
树脂组合物能够含有催化剂。尤其,作为固化性化合物,使用了具有-o-si-o-结构的化合物时,优选含有催化剂。根据该方式,溶胶凝胶反应得到促,并且容易获得更牢固的膜。作为催化剂,可举出盐酸、硫酸、乙酸、丙酸等酸催化剂、氢氧化钠、氢氧化钾、三乙胺等碱催化剂等。树脂组合物含有催化剂时,催化剂的含量相对于固化性化合物的100质量份,优选为0.1~100质量份,更优选为0.1~50质量份,进一步优选为0.1~20质量份。树脂组合物可以仅包含1种催化剂,也可以包含2种以上。包含2种以上催化剂时,优选这些的合计量在上述范围内。
[0361]
<<硅烷偶联剂>>
[0362]
本发明的树脂组合物能够含有硅烷偶联剂。根据该方式,能够进一步提高所获得的膜与支承体的密接性。在本发明中,硅烷偶联剂是指具有水解性基团及其以外的官能团的硅烷化合物。并且,水解性基团是指直接与硅原子键合且能够通过水解反应及缩合反应中的至少一种而生成硅氧烷键的取代基。作为水解性基团,例如可举出卤素原子、烷氧基、酰氧基等,优选为烷氧基。即,硅烷偶联剂优选为具有烷氧基甲硅烷基的化合物。并且,作为除了水解性基团以外的官能团,例如可举出乙烯基、(甲基)烯丙基、(甲基)丙烯酰基、巯基、环氧基、氧杂环丁基、氨基、脲基、硫醚基、异氰酸酯基、苯基等,优选为氨基、(甲基)丙烯酰基及环氧基。作为硅烷偶联剂的具体例,可举出日本特开2009-288703号公报的0018~0036段中记载的化合物、日本特开2009-242604号公报的0056~0066段中记载的化合物,这些内容编入本说明书中。作为硅烷偶联剂的市售品,可举出soken chemical&engineering co.,ltd.的a-50(有机硅烷)等。树脂组合物的总固体成分中硅烷偶联剂的含量优选为0.1~5质量%。上限优选为3质量%以下,更优选为2质量%以下。下限优选为0.5质量%以上,更优选为1质量%以上。硅烷偶联剂可以仅为1种,也可以为2种以上。2种以上的情况下,优选合计量在上述范围内。
[0363]
<<表面活性剂>>
[0364]
本发明的树脂组合物能够含有表面活性剂。作为表面活性剂,能够使用氟系表面活性剂、非离子系表面活性剂、阳离子系表面活性剂、阴离子系表面活性剂、硅酮系表面活性剂等各种表面活性剂。表面活性剂优选为氟系表面活性剂。通过在树脂组合物中含有氟系表面活性剂,液体特性(尤其流动性)进一步得到提高,也能够形成厚度不均匀较少的膜。氟系表面活性剂中的含氟率优选为3~40质量%,更优选为5~30质量%,尤其优选为7~25质量%。含氟率在该范围内的氟系表面活性剂在涂布膜的厚度的均匀性和省液性方面有效,在树脂组合物中的溶解性也良好。
[0365]
作为氟系表面活性剂的市售品,例如,可举出megafac f-171、f-172、f-173、f-176、f-177、f-141、f-142、f-143、f-144、f-437、f-475、f-477、f-479、f-482、f-554、f-555-a、f-556、f-557、f-558、f-559、f-560、f-561、f-565、f-563、f-568、f-575、f-780、exp、mfs-330、r-01、r-40、r-40-lm、r-41、r-41-lm、rs-43、tf-1956、rs-90、r-94、rs-72-k、ds-21(以上为dic corporation制)、fluorad fc430、fc431、fc171(以上为sumitomo 3m limited制)、surflon s-382、sc-101、sc-103、sc-104、sc-105、sc-1068、sc-381、sc-383、s-393、kh-40(以上为agc inc.制)、polyfox pf636、pf656、pf6320、pf6520、pf7002(以上为omnova solutions inc.制)、footgent 208g、215m、245f、601ad、601adh2、602a、610fm、710fl、710fm、710fs、ftx-218、(以上为neos company limited制)等。并且,下述化合物也例示为本发明中使用的氟系表面活性剂。
[0366]
[化学式20]
[0367][0368]
作为非离子系表面活性剂,可举出丙三醇、三羟甲基丙烷、三羟甲基乙烷以及这些的乙氧基化物及丙氧基化物(例如,丙三醇丙氧基化物、丙三醇乙氧基化物等)、聚氧乙烯月桂基醚、聚氧乙烯硬酯醚、聚氧乙烯油烯醚、聚氧乙烯辛基苯基醚、聚氧乙烯壬基苯基醚、聚乙二醇二月桂酸、聚乙二醇二硬脂酸酯、山梨糖醇酐脂肪酸酯、pluronic l10、l31、l61、l62、10r5、17r2、25r2(basf公司制)、tetronic 304、701、704、901、904、150r1(basf公司制)、solsperse 20000(日本lubrizol corporation制)、ncw-101、ncw-1001、ncw-1002(fujifilm wako pure chemical corporation.制)、pionin d-6112、d-6112-w、d-6315(takemoto oil&fat co.,ltd制)、olfin e1010、surfynol 104、400、440(nissin chemical industry co.,ltd.制)等。
[0369]
作为硅酮系表面活性剂,例如可举出toray silicone dc3pa、toray silicone sh7pa、toray silicone dc11pa、toray silicone sh21pa、toray silicone sh28pa、toray silicone sh29pa、toray silicone sh30pa、toray silicone sh8400(以上为dow corning toray co.,ltd.制)、tsf-4440、tsf-4300、tsf-4445、tsf-4460、tsf-4452(以上为momentive performance materials inc.制)、kp-341、kf-6001、kf-6002(以上为shin-etsu chemical co.,ltd.制)、byk-307、byk-323、byk-330、byk-3760、byk-uv3510(以上为byk chemie公司制)等。
[0370]
近年来,具有碳原子数7以上的直链状全氟烷基的化合物的毒性和生物蓄积性高的情况已经变得很明确,因此全氟辛烷酸、全氟辛烷磺酸的使用逐渐受到了限制。因此,优选利用使用了全氟辛烷酸、全氟辛烷磺酸的替代材料的表面活性剂。并且,作为氟系表面活性剂,从提高环境适性的观点考虑,优选使用源自全氟辛烷酸(pfoa)及全氟辛烷磺酸(pfos)等具有碳原子数7以上的直链状全氟烷基的化合物的替代材料的表面活性剂。
[0371]
树脂组合物的总固体成分中表面活性剂的含量优选为0.001质量%~5.0质量%,
更优选为0.005~3.0质量%。表面活性剂可以仅为1种,也可以为2种以上。2种以上的情况下,优选合计量在上述范围内。
[0372]
<<溶剂>>
[0373]
树脂组合物优选进一步包含溶剂。作为溶剂,并没有特别限定,可举出水及有机溶剂。作为有机溶剂,可举出醇系溶剂、酯系溶剂、酮系溶剂、酰胺系溶剂、醚系溶剂、烃系溶剂、卤素系溶剂等。作为有机溶剂的具体例,可举出甲醇、乙醇、1-丙醇、2-丙醇、1-丁醇、2-丁醇、2-甲基-1-丙醇、1-甲氧基-2-丙醇、2-乙氧基乙醇、2-丁氧基乙醇、聚乙二醇单烷基醚、聚丙二醇单烷基醚、乙二醇、丙二醇、聚乙二醇、聚丙二醇、丙三醇、碳酸乙烯酯、n-甲基吡咯烷酮、二噁烷、四氢呋喃、乙二醇二烷基醚、丙二醇二烷基醚、聚乙二醇二烷基醚、聚丙二醇二烷基醚、乙腈、丙腈、苄腈、羧酸酯、磷酸酯、膦酸酯、二甲基亚砜、环丁砜、二甲基甲酰胺、二甲基乙酰胺、乙酸乙酯、氯仿、二氯甲烷、乙酸甲酯等。溶剂可以仅为1种,也可以同时使用2种以上。溶剂的含量相对于树脂组合物的总量,优选为10~90质量%。
[0374]
<<其他添加剂>>
[0375]
树脂组合物可以根据需要适当含有抗氧化剂、光稳定剂、加工稳定剂、抗老化剂、相溶剂等任意添加剂。通过适当含有这些成分,能够适当调整所获得的固化物的各种特性。
[0376]
<<用途>>
[0377]
本发明的树脂组合物能够优选地用于有可能暴露于包括日光或紫外线的光的用途。作为具体例,可举出房屋、设施、运输设备等的窗玻璃用的涂层材料或膜;房屋、设施、运输设备等的内外装饰材料及内外装饰用涂料;荧光灯、汞灯等发射紫外线的光源用部件;太阳能电池、精密机械、电子电气设备、显示装置用部件;食品、化学品、药品等的容器或包装材料;农工业用片材;运动服、长袜、帽子等的衣料用纤维制品及纤维;塑料透镜、隐形眼镜、眼镜、义眼等透镜或其涂层材料;滤光器、棱镜、镜子、照片材料等光学用品;胶带、油墨等文具;标示板、标示器等及其表面涂层材料等。关于这些的详细内容,能够参考日本特开2009-263617号公报的0158~0218段中的记载,该内容编入本说明书中。
[0378]
本发明的树脂组合物优选地用于紫外线截止滤波器、透镜或保护材料。作为保护材料的形态,并没有特别限定,可举出涂膜状、膜状、片材状等。并且,本发明的树脂组合物也能够用作粘结剂、粘合剂。
[0379]
并且,本发明的树脂组合物也能够用于显示装置的各种部件。例如,液晶显示装置的情况下,能够用于防反射膜、偏振片保护膜、光学膜、相位差膜、粘结剂、粘合剂等构成液晶显示装置的各部件。并且,有机电致发光显示装置的情况下,能够用于光学膜、圆偏振片中的偏振片保护膜、1/4波片等相位差膜、粘合剂或粘结剂等构成有机电致发光显示装置的各部件。
[0380]
<固化物及其应用>
[0381]
本发明的固化物可使用上述本发明的树脂组合物来获得。本说明书中的“固化物”中包括使树脂组合物干燥来固化的干燥物,树脂组合物进行固化反应时则包括使树脂组合物进行固化反应来固化的固化物。
[0382]
本发明的固化物可以为将树脂组合物成型为所需形状而得的成型体。关于成型体的形状,能够根据用途、目的而适当选择。例如,可举出涂膜状、膜状、片状、板状、透镜状、管状、纤维状等。
[0383]
本发明的固化物可优选地用作光学部件。作为光学部件,可举出紫外线截止滤波器、透镜、保护材料等。并且,也能够用于偏振片等。
[0384]
关于紫外线截止滤波器,例如,能够用于滤光器、显示装置、太阳能电池、窗玻璃等物品。关于显示装置的种类,并没有特别限定,可举出液晶显示装置、有机电致发光显示装置等。
[0385]
将本发明的固化物用于透镜时,可以将本发明的固化物本身形成为透镜状来使用。并且,可以将本发明的固化物用于透镜表面的涂膜、接合透镜的中间层(粘合层)等。关于接合透镜,可举出国际公开第2019/131572号的0094~0102段中记载的内容等,该内容编入本说明书中。
[0386]
作为保护材料的种类,并没有特别限定,可举出显示装置用保护材料、太阳能电池用保护材料、窗玻璃用保护材料、有机电致发光显示装置等。关于保护材料的形状,并没有特别限定,可举出涂膜状、膜状、片状等。
[0387]
<紫外线吸收剂>
[0388]
本发明的紫外线吸收剂包含由上述式(1)表示的化合物(化合物(1))。关于化合物(1),与在上述树脂组合物一项中说明的内容相同,优选范围也相同。用于紫外线吸收剂的化合物(1)优选为由上述式(1a)表示的化合物。
[0389]
本发明的紫外线吸收剂也可以添加至粘结剂或粘合剂中使用。作为粘结剂,例如,可举出丙烯酸系粘结剂、橡胶系粘结剂、硅酮系粘结剂等。丙烯酸系粘结剂是指包含(甲基)丙烯酸单体的聚合物((甲基)丙烯酸聚合物)的粘结剂。作为粘合剂,例如,可举出氨基甲酸酯树脂粘合剂、聚酯粘合剂、丙烯酸树脂粘合剂、乙烯乙酸乙烯基树脂粘合剂、聚乙烯醇粘合剂、聚酰胺粘合剂及硅酮粘合剂等。其中,从粘合强度高这一方面考虑,作为粘合剂,优选为氨基甲酸酯树脂粘合剂或硅酮粘合剂。粘合剂可以使用市场上销售的市售品,作为市售品的例子,可举出toyo ink co.,ltd.的氨基甲酸酯树脂粘合剂(lis-073-50u:商品名)、soken chemical&engineering co.,ltd.的丙烯酸系粘结剂(sk dyne-sf2147:商品名)等。粘合剂可以进一步与固化剂同时使用。作为固化剂的市售品,可举出toyo ink co.,ltd.的cr-001(商品名)等。
[0390]
紫外线吸收剂中的化合物(1)的含量优选为1~100质量%,更优选为10~100质量%,进一步优选为20~100质量%。紫外线吸收剂可以仅包含1种化合物(1),也可以包含2种以上。包含2种以上化合物(1)时,优选这些的合计量在上述范围内。
[0391]
本发明的紫外线吸收剂优选进一步包含由上述式(2)表示的化合物(化合物(2))。关于化合物(2),与在上述树脂组合物一项中说明的内容相同,优选范围也相同。
[0392]
紫外线吸收剂含有化合物(2)时,化合物(2)的含量相对于化合物(1)的100质量份,优选为5质量份以下,更优选为3质量份以下,进一步优选为1质量份以下。下限优选为0.1质量份以上。紫外线吸收剂可以仅包含1种化合物(2),也可以包含2种以上。包含2种以上化合物(2)时,优选这些的合计量在上述范围内。
[0393]
<光学部件>
[0394]
本发明的光学部件包含上述本发明的紫外线吸收剂。本发明的光学部件也优选包含使用上述本发明的树脂组合物来获得的固化物。本发明的固化物可以为将上述本发明的树脂组合物成型为所需形状而得的成型物。关于成型体的形状,能够根据用途、目的而适当
选择。例如,可举出涂膜状、膜状、片状、板状、透镜状、管状、纤维状等。
[0395]
并且,本发明的光学部件可以使用包含本发明的紫外线吸收剂的粘结剂或粘合剂来获得。例如,可以为使用包含紫外线吸收剂的粘结剂或粘合剂来贴附偏振片与偏振片保护膜的部件。
[0396]
作为光学部件,可举出紫外线截止滤波器、透镜、保护材料等。
[0397]
关于紫外线截止滤波器,例如,能够用于滤光器、显示装置、太阳能电池、窗玻璃等物品。关于显示装置的种类,并没有特别限定,可举出液晶显示装置、有机电致发光显示装置等。
[0398]
作为透镜,可举出将本发明的固化物本身形成为透镜状的透镜;使透镜表面的涂膜、接合透镜的中间层(粘合层、粘结层)等中含有本发明的紫外线吸收剂的透镜等。
[0399]
作为保护材料的种类,并没有特别限定,可举出显示装置用保护材料、太阳能电池用保护材料、窗玻璃用保护材料等。关于保护材料的形状,并没有特别限定,可举出涂膜状、膜状、片状等。
[0400]
并且,作为光学部件的一方式,可举出树脂膜。树脂膜能够使用上述本发明的树脂组合物来形成。作为用于树脂膜形成用的树脂组合物的树脂,可举出上述树脂,优选为(甲基)丙烯酸树脂、聚酯纤维、环状烯烃树脂及酰化纤维素树脂,更优选为酰化纤维素树脂。在包含酰化纤维素树脂的树脂组合物中能够包含日本特开2012-215689号公报的0022~0067段中记载的添加剂。作为这种添加剂,例如,可举出糖酯等。通过将糖酯化合物添加至包含酰化纤维素树脂的树脂组合物中,在不损害光学特性的显现性且在拉伸工序前不进行热处理的情况下,也能够降低总雾度及内部雾度。作为糖酯,例如,可举出后述实施例中记载的糖酯1、糖酯2等。并且,使用包含酰化纤维素树脂的树脂组合物的树脂膜(酰化纤维素膜)能够通过日本特开2012-215689号公报的0068~0096段中记载的方法来制造。并且,树脂膜上可以进一步层叠有日本特开2012-215689号公报的0097~0113段中记载的硬涂层。
[0401]
并且,作为光学部件的其他方式,可举出具有透明性支承基材与树脂层的层叠体的光学部件。此时,支承基材及树脂层中的至少一个使用上述本发明的树脂组合物来获得或包含上述本发明的紫外线吸收剂。这种光学部件可优选地用作膜或片状的紫外线截止滤波器或保护材料。
[0402]
作为支承基材,优选在不损害光学性能的范围内具有透明性。支承基材为透明性是指光学透明,具体而言,是指支承基材的总透光率为85%以上。支承基材的总透光率优选为90%以上,更优选为95%以上。支承基材的总透光率能够通过以下方法测定。支承基材的总透光率是利用uv/vis光谱仪(例如,shimadzu corporation制的uv/vis光谱仪uv3400)测定支承基材的分光光谱并根据测定值求得的值。
[0403]
作为支承基材,可举出树脂膜作为优选例。作为形成支承基材的树脂,可举出酯树脂(例如,聚对苯二甲酸乙二酯(pet)、聚萘二甲酸乙二酯(pen)、聚对苯二甲酸丁二酯(pbt)、聚对苯二甲酸环己烷二甲酯(pct)等)、烯烃树脂(例如,聚丙烯(pp)、聚乙烯(pe)等)、聚氯乙烯(pva)、三乙酸纤维素(tac)等。其中,从通用性方面考虑,优选为pet。
[0404]
关于支承基材,可通过常规方法将上述树脂成型为板状来获得。并且,支承基材也可以使用市场上销售的市售树脂膜等。并且,也可以用上述本发明的树脂组合物来获得。
[0405]
支承基材的厚度能够根据用途或目的等而适当选择。通常,厚度优选为5μm~2500
μm,更优选为20μm~500μm。
[0406]
树脂层是用树脂组合物而形成的层。树脂组合物中能够使用上述本发明的树脂组合物。树脂层可以为经干燥固化的层,也可以为通过固化反应来获得的固化层。
[0407]
树脂层的厚度并没有特别限制,能够从所需可见光透过率的观点考虑而任意选择。作为树脂层的厚度,例如,能够设为5μm~2500μm。关于树脂层的厚度,尤其从容易确保阻断甚至抑制紫外线及蓝光的功能及可见光透过率且操作容易的观点考虑,优选为5μm~500μm,更优选为5μm~100μm。
[0408]
并且,作为上述透明性支承基材,能够使用剥离性的支承基材(剥离性层叠膜)。使用了这种支承基材的光学部件可优选地用于偏振片等。
[0409]
作为剥离性层叠膜,可举出包含聚对苯二甲酸乙二酯的支承体与含有本发明的紫外线吸收剂的树脂层直接接触的结构的剥离性层叠膜。
[0410]
上述剥离性层叠膜的支承体是能够从树脂层剥离的材料。从树脂层剥离支承体时的应力优选为0.05n/25mm以上且2.00n/25mm以下,更优选为0.08n/25mm以上且0.50n/25mm以下,进一步优选为0.11n/25mm以上且0.20n/25mm以下。上述应力若为0.05n/25mm以上,则由于偏振片加工过程中不易产生剥离而优选,上述应力若为2.00n/25mm以下,则由于剥离支承体时,偏振片不易发生折弯而优选。通过丙烯酸系粘结剂片而在玻璃基材上贴合并固定裁切成宽度25mm、长度80mm的剥离性层叠膜的光学膜的表面之后,利用拉伸试验机(a&dcompany,limited制rtf-1210)夹持试验片的长度方向一端(宽25mm的一边)的基材膜,在温度23℃、相对湿度60%的气氛下,以200mm/分钟的十字头速度(夹持移动速度),实施90
°
剥离试验(遵照日本工业标准(jis)k 6854-1:1999“粘合剂-剥离粘合强度试验方法-第1部:90度剥离”),由此评价了从树脂层剥离剥离性层叠膜的支承体时的应力。
[0411]
对剥离性层叠膜所具有的支承体进行说明。剥离性层叠膜所具有的支承体可使用包含聚对苯二甲酸乙二酯(pet)的支承体。支承体的主成分(构成支承体的成分中,质量基准的含有率最大的成分)优选为聚对苯二甲酸乙二酯(pet)。从力学强度的观点考虑,pet的重均分子量优选为20000以上,更优选为30000以上,进一步优选为40000以上。能够将支承体溶解于六氟异丙醇(hfip)并通过前述gpc法来确定pet的重均分子量。支承体的厚度并没有特别限定,优选为0.1~100μm,更优选为0.1~75μm,进一步优选为0.1~55μm,尤其优选为0.1~10μm。并且,可以对支承体进行作为公知的表面处理的电晕处理、辉光放电处理、底涂等。
[0412]
剥离性层叠膜能够通过在上述支承体上涂布包含本发明的紫外线吸收剂、树脂及溶剂的溶液并使其干燥而形成树脂层来制造。溶剂能够从能够溶解或分散树脂、在涂布工序、干燥工序中容易成为均匀的面状、能够确保液体保存性、具有适当的饱和蒸气压等观点考虑而适当选择。
[0413]
并且,作为光学部件的其他方式,可举出依次层叠有硬涂层、透明性支承基材及粘结层或粘合层的层叠体。这种层叠体可优选地用作紫外线截止滤波器、保护材料(保护膜、保护片)。
[0414]
在该方式的光学部件中,只要在支承基材、硬涂层及粘结层或粘合层中的任一个包含上述本发明的紫外线吸收剂即可。作为透明性支承基材,可举出在第1方式中说明的透明性支承基材。
[0415]
该方式的光学部件在支承基材上具有硬涂层。通过在光学部件的最表层具有硬涂层,能够提高光学部件的耐擦伤性。可以通过湿式涂布法或干式涂布法(真空成膜)中的任一种来形成硬涂层。从生产性优异的方面考虑,优选为湿式涂布法。用本发明的树脂组合物形成硬涂层时,优选利用湿式涂布法形成。
[0416]
硬涂层不是本发明的树脂组合物的固化物时,作为硬涂层,例如,能够使用日本特开2013-045045号公报、日本特开2013-043352号公报、日本特开2012-232459号公报、日本特开2012-128157号公报、日本特开2011-131409号公报、日本特开2011-131404号公报、日本特开2011-126162号公报、日本特开2011-075705号公报、日本特开2009-286981号公报、日本特开2009-263567号公报、日本特开2009-075248号公报、日本特开2007-164206号公报、日本特开2006-096811号公报、日本特开2004-075970号公报、日本特开2002-156505号公报、日本特开2001-272503号公报、国际公开第2012/018087号、国际公开第2012/098967号、国际公开第2012/086659号及国际公开第2011/105594号中记载的硬涂层。
[0417]
从进一步提高耐擦伤性的观点考虑,硬涂层的厚度优选为5μm~100μm。
[0418]
该方式的光学部件在支承基材的与具有硬涂层的一侧相反的一侧具有粘结层或粘合层。用于粘结层或粘合层的粘结剂或粘合剂的种类并没有特别限制。可举出上述粘结剂或粘合剂。并且,粘结剂或粘合剂中也能够使用添加了上述本发明的紫外线吸收剂的粘结剂或粘合剂。并且,粘结剂或粘合剂中能够使用上述本发明的树脂组合物。关于粘结剂或粘合剂,也优选使用包含日本特开2017-142412号公报的0056~0076段中记载的丙烯酸树脂及日本特开2017-142412号公报的0077~0082段中记载的交联剂的粘结剂或粘合剂。并且,粘结剂或粘合剂中,粘结剂或粘合剂可以包含日本特开2017-142412号公报的0088~0097段中记载的密接性改善剂(硅烷系化合物)及日本特开2017-142412号公报的0098段中记载的添加剂。并且,粘结层或粘合层能够通过日本特开2017-142412号公报的0099~0100段中记载的方法来形成。
[0419]
从兼顾粘结力及操作性的观点考虑,粘结层或粘合层的厚度优选为5μm~100μm。
[0420]
<显示用途中的光学部件的配置>
[0421]
本发明的光学部件能够优选地用作液晶显示装置(lcd)、有机电致发光显示装置(oled)等显示器的构成部件。
[0422]
<<液晶显示装置>>
[0423]
作为液晶显示装置,可举出在防反射膜、偏振片保护膜、光学膜、相位差膜、粘结剂、粘合剂等部件中含有本发明的紫外线吸收剂的液晶显示装置。包含本发明的紫外线吸收剂的光学部件在液晶单元中可以配置于观察者侧(前侧)、背光侧中的任一侧,并且,在起偏器中能够配置于远离液晶单元的一侧(外)、靠近液晶单元的一侧(内)中的任一侧。在图1~图10中示出具有包含本发明的紫外线吸收剂的光学部件的液晶显示装置的优选结构。另外,图1~图10是示意图,各层的厚度的关系、位置关系等并不一定与实际情况一致。图1是表示在前侧的偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图,图2是表示在背光侧的偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图。图3是表示在前侧的内保护膜上添加有本发明的紫外线吸收剂的结构的概略图,图4是表示在背光侧的内保护膜上添加有本发明的紫外线吸收剂的结构的概略图。另外,上述内保护膜也能够兼作相位差膜。图5是表示通过粘合剂或粘结剂而在前侧的相位差膜上贴合有包含本发明的
紫外线吸收剂的光学膜的结构的概略图,图6是表示通过粘合剂或粘结剂而在背光侧的相位差膜上贴合有包含本发明的紫外线吸收剂的光学膜的结构的概略图。图7是表示在前侧的粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图,图8是表示在背光侧的粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图。图9是表示在前侧的功能层中添加有本发明的紫外线吸收剂的结构的概略图,图10是表示在背光侧的功能层中添加有本发明的紫外线吸收剂的结构的概略图。作为功能层,可举出反射防止层、硬涂层等。
[0424]
包含本发明的紫外线吸收剂的光学部件配置于观察者侧(前侧)时,能够防止因外光导致的液晶单元中的材料劣化。
[0425]
将本发明的紫外线吸收剂添加到偏振片保护膜中时,优选将上述酰化纤维素膜、上述剥离性层叠膜中的树脂层用作偏振片保护膜。将本发明的紫外线吸收剂添加到偏振片保护膜中时,在靠近液晶单元侧的一侧或远离液晶单元的一侧中的任一侧、或者两者中含有本发明的紫外线吸收剂即可。
[0426]
用于液晶显示装置的偏振片中使用酰化纤维素膜。包含酰化纤维素膜的偏振片能够通过日本特开2012-215689号公报的0114~0117段中记载的方法来制造。
[0427]
并且,将上述剥离性层叠膜中的树脂层用作偏振片保护膜时,通过粘合剂而在起偏器上贴合剥离性层叠膜的与树脂层的支承体侧界面相反的一侧的表面之后剥离支承体,由此能够获得具有起偏器及包含本发明的紫外线吸收剂的树脂层的偏振片。对包含上述紫外线吸收剂的树脂层的渗透深度除了根据粘合剂与包含紫外线吸收剂的树脂层之间的(溶解度参数)sp值差发生变化以外,也根据粘合剂与包含紫外线吸收剂的树脂层接触后的经时条件(温度、时间)发生变化,例如,低温/短时间的条件适于抑制渗透。并且,关于渗透深度,由于能够一旦通过照射活性能量射线来降低渗透速度,因此在通过临时照射来抑制渗透深度之后,以促进用于确保偏振片的耐久性的固化为目的,进行追加照射也有效。
[0428]
可以根据需要,通过辉光放电处理、电晕处理、碱皂化处理等对剥离性层叠膜的与包含紫外线吸收剂的树脂层的支承体侧界面相反的一侧的表面进行亲水化处理。
[0429]
关于支承体的剥离,能够通过与在通常的带粘结剂的偏振片中进行的隔膜(剥离膜)的剥离工序相同的方法来进行剥离。关于支承体的剥离,可以在通过粘合剂将包含紫外线吸收剂的树脂层与起偏器层叠并干燥的工序之后立即直接剥离,也可以在干燥工序之后暂时卷取成卷状,并在其后的工序中另行剥离。
[0430]
<<有机电致发光显示装置>>
[0431]
作为有机电致发光显示装置,可举出在光学膜、圆偏振片中的偏振片保护膜、1/4波片等的相位差膜、粘合剂、粘结剂等部件中含有本发明的紫外线吸收剂的有机电致发光显示装置。并且,通过粘合剂或粘结剂而将上述剥离性层叠膜贴合在圆偏振片的方式也作为本发明的紫外线吸收剂的导入方法而优选。通过在上述结构中添加本发明的紫外线吸收剂,能够抑制因外光导致的有机电致发光显示装置的劣化。
[0432]
图11~图13示出具有包含本发明的紫外线吸收剂的光学部件的有机电致发光显示装置的优选结构。另外,图11~图13是示意图,各层的厚度的关系、位置关系等并不一定与实际情况一致。图11是表示在偏振片保护膜上添加有本发明的紫外线吸收剂的结构的概略图。图12是表示在粘合剂或粘结剂中添加有本发明的紫外线吸收剂的结构的概略图。图
13是表示通过粘合剂或粘结剂而在触控面板上贴合有包含本发明的紫外线吸收剂的光学膜的结构的概略图。
[0433]
<化合物及化合物的合成方法>
[0434]
本发明的化合物是由上述式(1a)表示的化合物。关于由式(1a)表示的化合物,与在上述树脂组合物一项中说明的内容相同,优选范围也相同。由式(1a)表示的化合物可优选地用作紫外线吸收剂。
[0435]
由式(1a)表示的化合物的极大吸收波长优选存在于381~420nm的波长范围内,更优选存在于381~400nm的波长范围内。
[0436]
根据下述式算出的由式(1a)表示的化合物在波长405nm处的摩尔吸光系数ε
405
优选为500以上,更优选为1000以上,进一步优选为2000以上,尤其优选为3000以上。
[0437]
ε
405
=ε
max
×
(a
405
/a
max
)
[0438]
ε
405
是由式(1a)表示的化合物在波长405nm处的摩尔吸光系数,ε
max
是由式(1a)表示的化合物在极大吸收波长处的摩尔吸光系数,a
405
是由式(1a)表示的化合物在波长405nm处的吸光度,a
max
是由式(1a)表示的化合物在极大吸收波长处的吸光度。
[0439]
在乙酸乙酯中测定的由式(1a)表示的化合物的分光吸收光谱中,在波长405nm处的吸光度a
405
与在波长430nm处的吸光度a
430
之比(a
430
/a
405
)优选小于0.13,更优选为0.10以下。上述比的下限并没有特别限定,能够设为0以上。
[0440]
由上述式(1a)表示的化合物能够经过使由式(2a)表示的化合物与卤代烷基化合物或羧酸卤化物进行反应的工序来合成。
[0441]
[化学式21]
[0442][0443]
在式(2a)中,r
11a
及r
12a
分别独立地表示烷基,
[0444]r14a
表示烷基或烷氧基,
[0445]r15a
表示氢原子、烷基或烷氧基;
[0446]r14a
与r
15a
可以相互键合而形成环。
[0447]
式(2a)的r
11a
、r
12a
、r
14a
及r
15a
所表示的各基团的含义与作为式(2)的r
11
、r
12
、r
14
及r
15
说明的基团相同,优选范围也相同。
[0448]
作为与由式(2a)表示的化合物进行反应的卤代烷基化合物,可举出由r
30-x
30
表示的化合物。作为与由式(2a)表示的化合物进行反应的羧酸卤化物,可举出由r
30-c(=o)-x
30
表示的化合物。r
30
是烷基,x
30
是卤素原子。r
30
所表示的烷基的碳原子数优选为1~30,更优选为1~20,进一步优选为1~15,尤其优选为1~10,最优选为1~8。烷基可以为直链及支链中的任一种。烷基可以具有取代基。作为取代基,可举出在上述取代基t中说明的基团。作为x
30
所表示的卤素原子,可举出氯原子、溴原子及碘原子。
[0449]
实施例
[0450]
以下,举出实施例对本发明进行进一步详细的说明。以下实施例中示出的材料、使用量、比例、处理内容、处理步骤等只要不脱离本发明的主旨,则能够适当进行变更。因此,本发明的范围并不限定于以下所示的具体例。并且,在以下所示的结构式中,me是甲基,et是乙基,bu是丁基,tbu是叔丁基,pr是丙基,ph是苯基,ac是乙酰基。
[0451]
<合成例>
[0452]
(合成例1)(化合物(1)-1的合成)
[0453]
按照以下方案合成了中间体1-1。在下述方案中,参考日本特开2016-081035号公报的0176段中记载的方法,使用甲基对苯醌(p-toluquinone)来代替2-叔丁基-1,4-苯醌来进行了从甲基对苯醌至中间体1-1的合成。
[0454]
[化学式22]
[0455][0456]
接着,按照以下合成方案,合成了化合物(2)-31。参考日本专利第5376885号公报的0154~0155段中记载的方法,使用中间体1-1来代替1-(4,7-二羟基苯并[1,3]二硫醇-2-亚基(ylidene))乙酸哌啶,由此进行了从中间体1-1至化合物(2)-31的合成。
[0457]
[化学式23]
[0458][0459]
接着,将0.5g的化合物(2)-31、0.39g的碳酸钾、5ml的n,n-二甲基乙酰胺进行混合,并在室温下搅拌了5分钟。对其添加0.46g的2-碘丙烷,在90℃下加热4小时的同时进行了搅拌。反应结束后,冷却至室温之后,添加1.5ml的水并搅拌了20分钟。滤取所析出的固体之后,添加2.5ml的甲醇、2.5ml的乙腈,并在氮气氛下进行了1小时的加热还流。冷却至室温之后,在室温下搅拌1小时之后滤取固体,用2.5ml的甲醇与2.5ml的乙腈的混合溶剂清洗,由此获得了0.4g的化合物(1)-1(产率70%)。1h-nmr(cdcl3):δ6.70(s,1h),4.62(m,1h),4.42(m,1h),3.66(m,4h),2.34(s,3h),1.54(m,4h),1.4~1.2(m,16h),0.91(m,6h)
[0460]
[化学式24]
[0461][0462]
(合成例2)(化合物(1)-2~化合物(1)-8的合成)
[0463]
在合成例1中,使用所对应的烷基化剂来代替2-碘丙烷,除此以外,以与合成例1相同的方法分别合成了化合物(1)-2~化合物(1)-8。
[0464]
[化学式25]
[0465][0466]
(合成例3)(化合物(1)-9~化合物(1)-10的合成)
[0467]
在合成例1中,使用1,2-二甲基-吡唑烷-3,5-二酮来代替中间体1-2,除此以外,以与合成例1相同的方法分别合成了化合物(1)-9及化合物(1)-10。
[0468]
[化学式26]
[0469]
[0470]
(合成例4)(化合物(1)-11的合成)
[0471]
在合成例1中,使用2-叔丁基-1,4-苯醌来代替甲基对苯醌,除此以外,以与合成例1相同的方法合成了化合物(1)-11。
[0472]
[化学式27]
[0473][0474]
(合成例5)(化合物(1)-12的合成)
[0475]
在合成例1中,使用2-苯基-1,4-苯醌来代替甲基对苯醌,除此以外,以与合成例1相同的方法合成了化合物(1)-12。
[0476]
[化学式28]
[0477][0478]
(合成例6)(化合物(1)-13的合成)
[0479]
通过与合成例1相同的方法,按照下述方案合成了化合物(2)-40。
[0480]
[化学式29]
[0481][0482]
通过与合成例1相同的方法,按照下述方案合成了化合物(1)-13。
[0483]
[化学式30]
[0484]
[0485]
(合成例7)(化合物(1)-14的合成)
[0486]
参考日本专利第5376885号公报的0154~0155段中记载的方法,按照下述方案合成了化合物(1)-14。
[0487]
[化学式31]
[0488][0489]
(合成例8)(化合物(1)-15的合成)
[0490]
通过与合成例1相同的方法,按照以下方案合成了中间体15-2。在下述方案中,使用中间体15-1来代替合成例1中使用的中间体1-2,由此进行了从中间体1-1至中间体15-2的合成。另外,通过journal of the american chemical society,2009,vol.131,33,11875-11881页中记载的方法合成了中间体15-1。
[0491]
[化学式32]
[0492][0493]
通过与合成例1相同的方法,按照下述方案合成了化合物(1)-15。
[0494]
[化学式33]
[0495][0496]
(合成例9)(化合物(1)-16的合成)
[0497]
按照下述方案合成了中间体16-2。在下述方案中,使用1,4-萘醌来代替合成例1中使用的甲基对苯醌、使用中间体16-1来代替中间体1-2,由此进行了从1,4-萘醌至中间体16-2的合成。
[0498]
[化学式34]
[0499][0500]
通过与合成例1相同的方法,按照下述方案合成了化合物(1)-16。
[0501]
[化学式35]
[0502][0503]
(合成例10)(化合物(1)-37、化合物(1)-46的合成)
[0504]
按照下述方案合成了化合物(2)-22。在下述方案中,使用中间体37-1来代替合成例1中使用的中间体1-2,由此进行了从中间体1-1至化合物(2)-22的合成。
[0505]
[化学式36]
[0506][0507]
在合成例1中,使用化合物(2)-22来代替化合物(2)-31、使用所对应的烷基化剂来代替2-碘丙烷,除此以外,以与合成例1相同的方法分别合成了化合物(1)-37、化合物(1)-46。
[0508]
[化学式37]
[0509][0510]
(合成例11)(化合物(1)-47的合成)
[0511]
按照下述方案合成了化合物(2)-1。在下述方案中,使用2,3-二甲基-对苯醌来代替合成例1中使用的甲基对苯醌,由此进行了从2,3-二甲基-对苯醌至化合物(2)-1的合成。
[0512]
[化学式38]
[0513][0514]
通过与合成例1相同的方法,按照下述方案合成了化合物(1)-47。
[0515]
[化学式39]
[0516][0517]
(合成例12)(化合物(1)-48的合成)
[0518]
按照下述方案合成了化合物(2)-54。在下述方案中,使用2,3-二甲基-对苯醌来代替合成例1中使用的甲基对苯醌,由此进行了从2,3-二甲基-对苯醌至化合物(2)-54的合成。
[0519]
[化学式40]
[0520][0521]
通过与合成例1相同的方法,按照下述方案合成了化合物(1)-48。
[0522]
[化学式41]
[0523][0524]
<试验例1>
[0525]
将2mg的下述表中记载的化合物(化合物(1)-1~化合物(1)-16、化合物(1)-37、化
合物(1)-46、化合物(1)-47、化合物(1)-48、比较化合物1~4)溶解于乙酸乙酯100ml中之后,用乙酸乙酯稀释至溶液的吸光度在0.6~1.2的范围内,由此制备了试样溶液101~120。另外,作为比较化合物1~4,使用了以下结构的化合物。
[0526]
[化学式42]
[0527][0528]
通过1cm石英槽,用分光光度计uv-1800pc(shimadzu corporation制)分别测定了试样溶液101~120的吸光度。根据所获得的光谱图测定了各试样溶液的极大吸收波长(λ
max
)。将λ
max
的值记载于下述表。
[0529]
并且,按照下述式算出了在波长405nm处的摩尔吸光系数(ε
405
)。
[0530]
ε
405
=ε
max
×
(a
405
/a
max
)
[0531]
ε
405
是试样溶液在波长405nm处的摩尔吸光系数,ε
max
是试样溶液在极大吸收波长处的摩尔吸光系数,a
405
是试样溶液在波长405nm处的吸光度,a
max
是试样溶液在极大吸收波长处的吸光度。
[0532]
将ε
405
的值为3000以上的设为a,小于3000且500以上的设为b,小于500的设为c,以3个阶段进行了评价。ε
405
的值越大,表示在405nm处的吸收能力越高。将评价结果记载于下述表1的ε
405
一栏。
[0533]
并且,算出将试样溶液在波长405nm处的吸光度设为1时的波长430nm处的吸光度的值,将波长430nm处的吸光度小于0.13的设为a,将0.13以上的设为b而评价了着色。波长430nm处的吸光度的值越小,表示着色越少。将结果示于下述表1的着色一栏。
[0534]
[表1]
[0535]
试样溶液no.化合物的种类λ
max
(nm)ε
405
着色101化合物(1)-1383aa102化合物(1)-2381aa103化合物(1)-3383aa104化合物(1)-4383aa105化合物(1)-5383aa106化合物(1)-6383aa107化合物(1)-7384aa108化合物(1)-8383aa109化合物(1)-9381aa110化合物(1)-10382aa111化合物(1)-11383aa112化合物(1)-12383aa113化合物(1)-13388aa
114化合物(1)-14382aa115化合物(1)-15393aa116化合物(1)-16388aa117化合物(1)-37386aa118化合物(1)-46387aa119化合物(1)-47385aa120化合物(1)-48388aa121比较化合物1350cb122比较化合物2352ca123比较化合物3350cb124比较化合物4380ba
[0536]
如上述表所示,化合物(1)-1~(1)-16、化合物(1)-37、化合物(1)-46、化合物(1)-47、化合物(1)-48在波长405nm处的摩尔吸光系数(ε
405
)高且着色少。
[0537]
<试验例2-1>
[0538]
将下述表中记载的化合物、7.6g的氯仿及1.1g的(甲基)丙烯酸树脂(dianal br-80、mitsubishi chemical corporation,含有60质量%以上甲基丙烯酸甲酯作为单体单元,mw95000)混合而制备了树脂组合物。将所获得的树脂组合物旋涂在玻璃基板上来形成涂布膜,并将所获得的涂布膜在110℃下干燥2分钟,由此制作了树脂膜。另外,在下述表2的化合物的种类一栏中记载的化合物(1)-1、化合物(1)-2、化合物(1)-8、化合物(1)-11、化合物(1)-12、化合物(1)-13、化合物(1)-14、化合物(1)-5、化合物(1)-37、化合物(1)-46、化合物(1)-47、化合物(1)-48、比较化合物1~4分别为上述结构的化合物。
[0539]
(面状不均匀的评价)
[0540]
用光学显微镜(olympus corporation制,mx-61l),在明视场200倍下观察以上制作的树脂膜,并观察了树脂膜中是否存在不均匀。在光学显微镜下未确认到不均匀而成为均匀的膜时,判断为对成膜时的热应力的耐性优异。将面状不均匀的评价结果示于下述表2。
[0541]
a:在光学显微镜下未观察到不均匀。
[0542]
b:在光学显微镜下观察到轻微的不均匀。
[0543]
c:在光学显微镜下观察到明显的不均匀。
[0544]
(耐光性)
[0545]
关于以上制作的树脂膜,在以下条件1下进行耐光性试验,求出在极大吸收波长(λ
max
)处的吸光度的维持率,并评价了耐光性。具体而言,测定树脂膜在极大吸收波长(λ
max
)处吸光度之后,测定了在条件1下对树脂膜进行了1周的耐光性试验的耐光性试验后的树脂膜在极大吸收波长(λ
max
)处的吸光度。
[0546]
(条件1)
[0547]
装置:氙气(xenon)耐候性试验仪(suga test instruments co.,ltd.:xl75)
[0548]
照度:10klx(40w/m2)
[0549]
试验期间:1周
[0550]
环境:23℃、相对湿度50%
[0551]
根据耐光性试验前后的树脂膜在极大吸收波长(λ
max
)处的吸光度的值,利用下述式算出了吸光度的维持率(%)。按照下述式计算了维持率。
[0552]
吸光度的维持率(%)=100
×
(照射后的树脂膜在λ
max
处的吸光度)/(照射前的树脂膜在λ
max
处的吸光度)
[0553]
a:吸光度的维持率为90%以上
[0554]
b:吸光度的维持率为80%以上且低于90%
[0555]
c:吸光度的维持率低于80%
[0556]
并且,目视确认了耐光性试验后的树脂膜的着色变化程度。将评价结果示于下述表2。
[0557]
[表2]
[0558][0559]
相较于树脂膜213a~216a,树脂膜201a~212a在波长400nm附近的光吸收更大,长波长侧的紫外线的吸收性优异。并且,树脂膜201a~212a的着色少。即,树脂膜201a~212a在波长400nm附近的光吸收大且着色少。
[0560]
并且,如上述表所示,树脂膜201a~212a的面状不均匀少,而且耐光性也优异。
[0561]
并且,关于用于形成树脂膜20a1~212a的树脂组合物,通过含有上述本说明书中记载的化合物(2)(由式(2)表示的化合物),树脂组合物的保存稳定性得到提高,例如,即便使用在5℃下保管2周后的树脂组合物来形成树脂膜,也未发现化合物(1)的析出等。
[0562]
<试验例2-2>
[0563]
将下述表中记载的化合物、7.6g的氯仿及1.1g的(甲基)丙烯酸树脂(dianal br-80、mitsubishi chemical corporation,含有60质量%以上甲基丙烯酸甲酯作为单体单元,mw95000)混合而制备了树脂组合物。将所获得的树脂组合物旋涂在玻璃基板上来形成涂布膜,并将所获得的涂布膜在110℃下干燥2分钟,由此制作了树脂膜。另外,在下述表3的
化合物的种类一栏中记载的化合物中,化合物(1)-1、化合物(1)-5、化合物(1)-8分别为上述结构的化合物。并且,uv-1~uv-6是下述结构的化合物。
[0564]
[化学式43]
[0565][0566]
(面状不均匀的评价)
[0567]
关于以上制作的树脂膜,以与试验例2-1相同的方法及评价基准评价了面状不均匀。
[0568]
(耐光性2(在405nm处的吸光度的维持率))
[0569]
关于以上制作的树脂膜,在试验例2-1的条件1下进行耐光性试验,求出在波长405nm处的吸光度的维持率,并评价了耐光性2。具体而言,测定树脂膜在波长405nm处的吸光度之后,测定了在条件1下对树脂膜进行了1周的耐光性试验的耐光性试验后的树脂膜在波长405nm处的吸光度。根据耐光性试验前后的树脂膜在405nm处的吸光度的值,利用下述式算出了吸光度的维持率(%)。按照下述式计算了维持率。
[0570]
吸光度的维持率(%)=100
×
(照射后的树脂膜在波长405nm处的吸光度)/(照射前的树脂膜在波长405nm处的吸光度)
[0571]
a:吸光度的维持率为90%以上
[0572]
b:吸光度的维持率为80%以上且低于90%
[0573]
c:吸光度的维持率低于80%
[0574]
[表3]
[0575][0576]
树脂膜201b~206b在波长400nm附近的光吸收大,长波长侧的紫外线的吸收性优异。并且,耐光性试验后的405nm处的吸光度的维持率也良好,耐光性优异。
[0577]
<试验例3>
[0578]
通过以下所示的方法制作了树脂膜301。
[0579]
(1)原料的制备
[0580]
(1-1)酰化纤维素的制备
[0581]
制备了乙酰取代度2.85的酰化纤维素。添加硫酸(相对于纤维素100质量份为7.8质量份)作为催化剂,并添加各羧酸,在40℃下进行了酰化反应。之后,通过调整硫酸催化剂量、水分量及熟化时间来调整了总取代度和6位取代度。熟化温度在40℃下进行。此外,用丙酮清洗并去除了该酰化纤维素的低分子量成分。
[0582]
(1-2)糖酯化合物的制备
[0583]
通过以下方法制备了糖酯化合物。
[0584]
首先,通过国际公开第2009/003164号的0054段的例示化合物3的合成中记载的方法合成了下述结构的糖酯化合物1。并且,关于糖酯化合物2,也通过相同的方法进行了合成。
[0585]
(2)掺杂物的制备
[0586]
将下述组合物放入混合罐中,搅拌以溶解各成分,进一步在80℃下加热约180分钟之后,利用平均孔径34μm的滤纸及平均孔径10μm的烧结金属过滤器进行了过滤。
[0587]
(掺杂物的组成)
[0588]
酰化纤维素(取代度2.85)
……
100.0质量份
[0589]
糖酯1
……
7.5质量份
[0590]
糖酯2
……
2.5质量份
[0591]
紫外线吸收剂1(化合物(1)-5)
……
0.1质量份
[0592]
紫外线吸收剂2(比较化合物5)
……
0.1质量份
[0593]
二氯甲烷
……
475.3质量份
[0594]
甲醇
……
103.9质量份
[0595]
丁醇
……
4.6质量份
[0596]
掺杂物的固体成分浓度为16.0质量%,塑化剂的添加量均为相对于纤维素酯的比例,掺杂物的溶剂是二氯甲烷/甲醇/丁醇=81/18/1(质量比)。并且,膜厚均为60μm。
[0597]
以下示出具体的糖酯结构。糖酯1的添加量是7.5质量%,使用了平均取代度5.5的下述结构的糖酯。关于取代度的计算,通过hplc(高效率液相层析法)进行了测定。糖酯2的添加量是2.5质量%,化合物(1)-5的添加量是0.1质量%。
[0598]
[化学式44]
[0599][0600]
[化学式45]
[0601][0602]
如下述表所示,除了改变紫外线吸收剂1、紫外线吸收剂2的添加量以外,以与树脂膜301a的掺杂物相同的方法制备了其他各实施例及比较例的掺杂物。
[0603]
(3)流延
[0604]
利用滚筒式制膜机流延了上述掺杂物。以表层的掺杂物置于芯层的掺杂物上的方式从模具共流延芯层的掺杂物并使其凝胶化而剥离,由此使其与冷却至-10℃的金属支承体接触。另外,滚筒为不锈钢制。
[0605]
(4)干燥
[0606]
将流延而获得的网状物(膜)从滚筒剥离之后,在传送膜时,用夹具夹住网状物的两端,利用传送中的拉幅机装置在拉幅机装置内,以30~40℃干燥了20分钟。之后,将已干燥的膜装框并在140℃下进行了后干燥。另外,此处的干燥温度是指膜的膜表面温度。
[0607]
(5)卷取
[0608]
制作下述表所示的组成的膜,以判断其制造适性为目的,在上述条件下,制作了最少24卷的卷宽1280mm、卷长2600mm的卷。针对连续制造的24卷中的1卷,以100m间隔切出长
边1m的样品(宽1280mm),并进行了各测定。将所获得的酰化纤维素膜作为各实施例及比较例的树脂膜301~309。
[0609]
用分光光度计uv3600(shimadzu corporation制)分别测定了以上制作的树脂膜301a~309a的吸光度。
[0610]
并且,将在波长405nm处的吸光度除以紫外线吸收剂的添加量(相对于酰化纤维素的质量%)时的值是50以上设为a,25~50设为b,25以下设为c而评价了长波长的紫外线吸收能力。值越大,表示长波长的紫外线吸收能力越高。将结果示于下述表的长波长的紫外线吸收能力一栏。
[0611]
[表4]
[0612][0613]
用作紫外线吸收剂1的化合物(1)-5是上述结构的化合物。并且,用作紫外线吸收剂2的比较化合物5是下述结构的化合物。
[0614]
[化学式46]
[0615][0616]
相较于树脂膜307a~309a,树脂膜301a~306a在波长400nm附近的光的吸收更大,长波长侧的紫外线的吸收性优异。
[0617]
(6)偏振片的制作
[0618]
通过以下所示的方法制作了偏振片。
[0619]
(6-1)树脂膜的皂化处理
[0620]
将所制作的树脂膜303a、304a、308a在2.3mol/l的氢氧化钠水溶液中,在55℃下浸渍了3分钟。在室温(25℃)的水洗浴槽中清洗,在30℃下用0.05mol/l的硫酸进行了中和。再
次在室温的水洗浴槽中清洗,进一步用100℃的热风进行了干燥。
[0621]
(6-2)起偏器的制作
[0622]
将厚度80μm的聚乙烯醇(pva)膜在碘浓度0.05质量%的碘水溶液中,在30℃下浸渍60秒而进行染色,接着在硼酸浓度4质量%的硼酸水溶液中浸渍60秒期间,纵向拉伸至原来长度的5倍之后,在50℃下使其干燥4分钟,由此获得了厚度19μm的起偏器。
[0623]
(6-3)va(vertical alignment:垂直对齐)相位差膜的制作
[0624]
作为相位差膜,使用了下述va相位差膜1或va相位差膜2。
[0625]
(6-3-1)va相位差膜1的制作
[0626]
<环烯烃系聚合物a的合成>
[0627]
将8-甲氧基羰基-8-甲基四环[4.4.0.1
2,5
.1
7,10
]-3-十二烯72.5质量份、二环戊二烯27.5质量份、作为分子量调节剂的1-己烯5.6质量份及甲苯200质量份放入经氮取代的反应容器中,并加热至80℃。对其添加三乙基铝(0.6摩尔/l)的甲苯溶液0.18ml、甲醇改性wcl6的甲苯溶液(0.025摩尔/l)0.58ml,使其在80℃下反应3小时,由此获得了开环聚合物。接着,将所获得的开环聚合物的溶液放入高压釜中,进一步添加了甲苯200质量份。相对于单体添加量,添加2500ppm的氢化催化剂ruhcl(co)[p(c6h5)]3,将氢气压设为9-10mpa,在160~165℃下进行了3小时的反应。反应结束后,使其在大量的甲醇溶液中沉淀,由此获得了开环聚合物的氢化物(环烯烃系聚合物a)。所获得的开环聚合物的氢化物的重均分子量(mw)=119
×
103、分子量分布(mw/mn)=3.1。
[0628]
<微粒分散液的制备>
[0629]
将微粒(aerosil r812,nippon aerosil co.,ltd.制)11质量份和乙醇89质量份用溶解器搅拌混合50分钟之后,用manton-gaulin进行分散,由此制备了微粒分散液。
[0630]
<微粒添加液的制备>
[0631]
将放入了99质量份的二氯甲烷的溶解罐中添加4质量份的环烯烃系聚合物a,加热而使其完全溶解之后,充分搅拌的同时对其缓慢添加11质量份的微粒分散液,并用磨碎机进行了分散。将其用过滤器(nippon seisen co.,ltd.制,fine met nf)过滤,制备了微粒添加液。
[0632]
<va相位差膜1的制作>
[0633]
首先,向加压溶解罐中添加了二氯甲烷和甲醇。将环烯烃系聚合物a搅拌的同时放入添加有溶剂的加压溶解罐中。将其加热,搅拌的同时使其完全溶解,由此制备了主掺杂物液。向100质量份的主掺杂物液中添加了2质量份的微粒添加液,利用管内混合机(toray静止型管内混合机hi-mixer,swj)充分混合,接着使用带式流延装置,在宽2m的不锈钢带支承体上将其均匀地流延。关于所获得的网状物(膜),使溶剂蒸发至残留溶剂量成为110质量%,并从不锈钢带支承体剥离。剥离后施加拉力而拉伸,以使纵向拉伸倍率成为2%。接着,使其干燥至膜的残留溶剂量成为少于1质量%之后,进一步用拉幅机,沿与膜传送方向正交的方向,在165℃下拉伸了35%。另外,按照下述式求出了残留溶剂量。
[0634]
残留溶剂量(质量%)={(m-n)/n}
×
100
[0635]
在此,m是网状物在任意时刻的质量、n是将测定了m的网状物在120℃下干燥2小时时的质量。
[0636]
如上所述,制作了宽1.5m且在端部具有宽1cm、高8μm的滚纹的膜厚35μm、rth为
121nm的va相位差膜1。
[0637]
(6-3-2)va相位差膜2的制作
[0638]
<酰化纤维素的制作>
[0639]
通过日本特开平10-045804号公报、日本特开平08-231761号公报中记载的方法,合成酰化纤维素,并测定了其酰基取代度。具体而言,添加硫酸(相对于纤维素100质量份为7.8质量份)作为催化剂,并添加成为酰基的原料的羧酸(乙酸),在40℃下进行了酰化反应。此时,通过调整羧酸的量来调整了酰基(乙酰基)的取代度。并且,酰化后在40℃下进行了熟化。此外,用丙酮清洗并去除该酰化纤维素(乙酸纤维素)的低分子量成分,由此获得了具有各种平均酰基取代度的酰化纤维素。
[0640]
<添加剂a的合成>
[0641]
添加剂a通过与日本专利第6095766号公报中记载的方法类似的方法或以其为基准的方法进行了合成。以下示出经合成的化合物的结构式。
[0642]
[化学式47]
[0643][0644]
<添加剂b的合成>
[0645]
添加剂b通过与国际公开第2015/005398号中记载的方法类似的方法或以其为基准的方法进行了合成。以下示出经合成的化合物的结构式。
[0646]
[化学式48]
[0647][0648]
<添加剂c的合成>
[0649]
添加剂c通过与日本专利第4260332号公报中记载的方法类似的方法或以其为基准的方法进行了合成。以下示出经合成的化合物的结构式。
[0650]
[化学式49]
[0651][0652]
<芯层形成用掺杂物的制备>
[0653]
将下述组合物放入混合罐中,搅拌以溶解各成分,由此制备了芯层形成用掺杂物。
[0654]
(芯层形成用掺杂物的组成)
[0655]
乙酸纤维素(取代度2.4)
……
100.0质量份
[0656]
添加剂a
……
12.0质量份
[0657]
添加剂b
……
3.5质量份
[0658]
添加剂c
……
1.0质量份
[0659]
二氯甲烷
……
392.0质量份
[0660]
甲醇
……
58.5质量份
[0661]
<表皮层形成用掺杂物的制备>
[0662]
将下述组合物放入混合罐中,搅拌以溶解乙酸纤维素,由此制备了表皮层形成用掺杂物。
[0663]
(表皮层形成用掺杂物的组成)
[0664]
乙酸纤维素(取代度2.8)
……
100质量份
[0665]
二氯甲烷
……
440质量份
[0666]
甲醇
……
65.8质量份
[0667]
<va相位差膜2的流延>
[0668]
利用带式流延装置,将所制备的芯层形成用掺杂物及表皮层形成用掺杂物进行三层共流延,以依次层叠表皮层、芯层、表皮层。使干燥后的芯层的膜厚成为39μm、各表皮层的膜厚成为1μm。将所获得的膜(网状物)从带上剥离,夹在夹具中,在残留溶剂量相对于膜整体的质量是20~5质量%的状态时,用拉幅机在140℃下,以1.1倍的拉伸倍率进行了横向拉伸(沿宽度方向拉伸)。之后,从膜上移除夹具,使其在140℃下干燥20分钟之后,进一步用拉幅机在膜的tg(玻璃转移温度)-3℃下,以1.2倍的拉伸倍率进行横向拉伸,由此制作了va相位差膜2。所获得的va相位差膜2的膜厚为40μm。另外,“拉伸倍率(%)”是指通过下述式求出的值。
[0669]
拉伸倍率(%)=100
×
{(拉伸后的长度)-(拉伸前的长度)}/拉伸前的长度,另外,tg是通过动态粘弹性测定求出的损耗正切tanδ成为最大值的温度。关于损耗正切tanδ,利用动态粘弹性测定装置(it measurement control co.,ltd.制dva-200)针对预先在温度25℃、相对湿度60%气氛下进行了2小时以上调湿的膜试样,在下述条件下测定e”(损耗弹
性模量)和e’(储存弹性模量)并求出tanδ(=e”/e’)及其最大值,由此测定了tg。
[0670]
装置:it measurement control co.,ltd.制dva-200
[0671]
试样:5mm、长度50mm(间隙20mm)
[0672]
测定条件:拉伸模式
[0673]
测定温度:-25℃~220℃
[0674]
升温条件:5℃/分钟
[0675]
频率:1hz
[0676]
并且,按照下述式求出了残留溶剂量。
[0677]
残留溶剂量(质量%)={(m-n)/n}
×
100
[0678]
m是网状物在任意时刻的质量、n是将测定了m的网状物在120℃下干燥2小时时的质量。
[0679]
(6-4)带起偏器的va相位差膜1的制作
[0680]
<紫外线固化性粘合剂1的制备>
[0681]
利用以下所示的组成,制备了紫外线固化性粘合剂。
[0682]
(紫外线固化性粘合剂1的组成)
[0683]
celloxide 2021p(daicel corporation,多官能环氧化合物)
……
100.0质量份
[0684]
rikaresin dme-100(new japan chemical co.,ltd.,多官能环氧化合物)
……
28.6质量份
[0685]
2-乙基己基环氧丙基醚(单官能环氧化合物)
……
14.3质量份
[0686]
cpi-100p(光产酸剂,san-apro ltd.)
……
2.9质量份
[0687]
irgacure290(光产酸剂,basf japan ltd.)
……
5.7质量份
[0688]
2-异丙基噻吨酮(光产酸剂)
……
1.4质量份
[0689]
<va相位差膜1与起偏器的粘合>
[0690]
利用紫外线固化性粘合剂1,将上述va相位差膜1贴附于起偏器的一侧,5秒后从va相位差膜1侧,以200mj的强度照射紫外线,使紫外线固化性粘合剂1固化而作为带起偏器的va相位差膜1。
[0691]
(6-5-1)偏振片303b1的制造
[0692]
用聚乙烯醇系粘合剂,将经皂化处理的树脂膜303a贴附于带起偏器的va相位差膜1的起偏器侧,由此制作了偏振片303b1。
[0693]
(6-5-2)偏振片303b2的制造
[0694]
用聚乙烯醇系粘合剂,将经皂化处理的树脂膜303a贴附于起偏器的一侧,并在与贴合了树脂膜303a的表面相反的一侧的表面贴合va相位差膜2,由此制作了偏振片303b2。
[0695]
(6-6-1)液晶显示装置303c1、304c1、308c1的制造
[0696]
取出市售的液晶显示装置flexscan 19英寸彩色液晶显示器s1923-hbk(商品名,eizo corporation制)的液晶面板,剥离前侧的偏振片,取而代之,通过粘结剂(sk-2057,soken chemical&engineering co.,ltd.制)贴附了偏振片303b1的va相位差膜侧。如此,制造了液晶显示装置303c1。如下述表所示,除了改变树脂膜的种类以外,以相同的方法制造了液晶显示装置304c1、308c1。
[0697]
(6-6-2)液晶显示装置303c2、304c2、308c2的制造
[0698]
取出市售的液晶显示装置flexscan 19英寸彩色液晶显示器s1923-hbk(商品名,eizo corporation制)的液晶面板,剥离前侧的偏振片,取而代之,通过粘结剂(sk-2057,soken chemical&engineering co.,ltd.制)贴附了偏振片303b2的va相位差膜侧。如此,制造了液晶显示装置303c2。如下述表所示,除了改变树脂膜的种类以外,以相同的方法制造了液晶显示装置304c2、308c2。
[0699]
[表5]
[0700]
液晶显示装置no偏振片no树脂膜nova相位差膜no图no303c1303b1303a1图1304c1304b1304a1图1308c1308b1308a1图1303c2303b2303a2图1304c2304b2304a2图1308c2308b2308a2图1
[0701]
相较于液晶显示装置308c1及308c2,包含本发明的紫外线吸收剂的液晶显示装置303c1、303c2、304c1及304c2在长时间显示中,画质的变化也较少,因此优选。
[0702]
(7)有机电致发光显示装置的制作
[0703]
通过以下所示的方法制作了有机电致发光显示装置。
[0704]
(7-1)光学各向异性层a的制作
[0705]
(酰化纤维素溶液的制备)
[0706]
将下述组合物放入混合罐中,加热的同时搅拌以溶解各成分,由此制备了酰化纤维素溶液。
[0707]
(酰化纤维素溶液的组成)
[0708]
乙酸纤维素(乙酰化度2.86)
……
100质量份
[0709]
二氯甲烷(第1溶剂)
……
320质量份
[0710]
甲醇(第2溶剂)
……
83质量份
[0711]
1-丁醇(第3溶剂)
……
3质量份
[0712]
磷酸三苯酯
……
7.6质量份
[0713]
磷酸联苯基二苯酯
……
3.8质量份
[0714]
(消光剂分散液的制备)
[0715]
将下述组合物放入分散机,搅拌以溶解各成分,由此制备了消光剂分散液。
[0716]
(消光剂分散液的组成)
[0717]
二氧化硅粒子分散液(平均粒径16nm,aerosil r972,nippon aerosil co.,ltd.制)
……
10.0质量份
[0718]
二氯甲烷
……
72.8质量份
[0719]
甲醇
……
3.9质量份
[0720]
丁醇
……
0.5质量份
[0721]
酰化纤维素溶液
……
0.3质量份
[0722]
(紫外线吸收剂溶液的制备)
[0723]
将下述组合物放入混合罐中,加热的同时搅拌以溶解各成分,由此制备了紫外线
吸收剂溶液。
[0724]
(紫外线吸收剂溶液的组成)
[0725]
紫外线吸收剂(由式(uv-11)表示的结构的化合物)
……
10.0质量份
[0726]
紫外线吸收剂(由式(uv-12)表示的结构的化合物)
……
10.0质量份
[0727]
二氯甲烷
……
55.7质量份
[0728]
甲醇
……
10质量份
[0729]
丁醇
……
1.3质量份
[0730]
酰化纤维素溶液
……
12.9质量份
[0731]
[化学式50]
[0732][0733]
(酰化纤维素膜的制作)
[0734]
向混合有94.6质量份的酰化纤维素溶液和1.3质量份的消光剂分散液的混合液中添加紫外线吸收剂溶液,以使紫外线吸收剂(uv-1)及紫外线吸收剂(uv-2)在每100质量份的酰化纤维素中分别成为1.0质量份,加热的同时充分搅拌以溶解各成分,由此制备了掺杂物。将所获得的掺杂物增温至30℃,并经由流延模具在直径3m的滚筒即镜面不锈钢支承体上进行了流延。将镜面不锈钢支承体的表面温度设定为-5℃,涂布宽度设为1470mm。通过在滚筒上以150m3/分钟,对经流延的掺杂物膜吹送34℃的干燥风而使其干燥,在残留溶剂为150%的状态下从滚筒剥离。剥离时,沿传送方向(长边方向)进行了15%的拉伸。之后,用针板拉幅机(日本特开平04-001009号公报的图3中记载的针板拉幅机)把持膜的宽度方向(与流延方向正交的方向)的两端的同时进行传送,在宽度方向上未进行拉伸处理。此外,通过在热处理装置的辊之间传送而进一步进行干燥,由此制造了酰化纤维素膜(t1)。所制作的长条状的酰化纤维素膜(t1)的残留溶剂量为0.2%,厚度为60μm,波长550nm处的re(面内延迟)与rth(厚度方向的延迟)分别为0.8nm、40nm。
[0735]
(碱皂化处理)
[0736]
使前述酰化纤维素膜(t1)通过温度60℃的介电式加热辊,将膜表面温度升温至40℃之后,用棒涂机,以14ml/m2涂布量在膜的带面涂布了以下所示的组成的碱性溶液。之后,将涂布有碱性溶液的酰化纤维素膜在加热至110℃的noritake co.,limited制的蒸气式远红外加热器下传送了10秒。接着,同样用棒涂机,在所获得的膜上涂布了3ml/m2纯水。接着,对所获得的膜重复进行3次基于喷注式涂布机(fountain coater)的水洗和基于气刀的除水之后,将膜在70℃的干燥区传送10秒而进行干燥,由此制作了经碱皂化处理的酰化纤维素膜。
[0737]
(碱性溶液的组成)
[0738]
氢氧化钾
……
4.7质量份
[0739]
水
……
15.8质量份
[0740]
异丙醇
……
63.7质量份
[0741]
表面活性剂sf-1(c
14h29
o(ch2ch2o)
20
h)
……
1.0质量份
[0742]
丙二醇
……
14.8质量份
[0743]
(取向膜的形成)
[0744]
在酰化纤维素膜(t1)的进行了碱皂化处理的表面,用#14的线棒涂布机连续涂布了下述组成的取向膜涂布液。将涂布有取向膜涂布液的膜用60℃的热风干燥60秒,进一步用100℃的热风干燥120秒,由此形成了取向膜。所使用的改性聚乙烯醇的皂化度为88%。
[0745]
(取向膜涂布液的组成)
[0746]
下述结构的改性聚乙烯醇
……
10质量份
[0747]
水
……
308质量份
[0748]
甲醇
……
70质量份
[0749]
异丙醇
……
29质量份
[0750]
光聚合引发剂(omnirad 2959,igm resins b.v.公司制)
……
0.8质量份
[0751]
[化学式51]
[0752][0753]
(光学各向异性层a的形成)
[0754]
对以上制作的取向膜连续实施了摩擦处理。此时,长条状的膜的长边方向与传送方向为平行,将膜长边方向(传送方向)与摩擦辊的旋转轴所成的角度设为72.5
°
(若将膜长边方向(传送方向)设为90
°
,从取向膜侧观察,以膜宽度方向为基准(0
°
),将逆时针旋转方向由正值表示时,摩擦辊的旋转轴位于-17.5
°
。)换言之,摩擦辊的旋转轴的位置符合以膜长边方向为基准,逆时针旋转72.5
°
的位置。)。
[0755]
将包含下述组成的盘状液晶(dlc)化合物的光学各向异性层涂布液(a)用#5.0的线棒涂布机连续涂布于以上制作的取向膜上。将膜的传送速度(v)设为26m/分钟。为了涂布液的溶剂的干燥及盘状液晶化合物(dlc化合物)的取向熟化,用115℃的热风干燥90秒,接着用80℃的热风干燥60秒,之后,对所获得的涂膜以80℃进行uv(紫外线)照射(曝光量:70mj/cm2),由此固定了液晶化合物的取向。光学各向异性层a的厚度为2.0μm。确认到dlc化合物的圆盘面相对于膜面的平均倾斜角为90
°
,dlc化合物与膜面垂直地取向。并且,慢轴的角度与摩擦辊的旋转轴平行,若将膜长边方向(传送方向)设为90
°
(将膜宽度方向设为0
°
。从取向膜侧观察,以膜宽度方向为基准(0
°
),将逆时针方向用正值表示。),则慢轴的角度为-17.5
°
。所获得的光学各向异性层a符合λ/2板,波长550nm处的re及rth分别为re(550):238nm,rth(550):-119nm。
[0756]
(光学各向异性层涂布液(a)的组成)
[0757]
下述盘状液晶化合物(a)
……
80质量份
[0758]
下述盘状液晶化合物(b)
……
20质量份
[0759]
环氧乙烷改性三羟甲基丙烷丙烯酸酯(v#360,osaka organic chemical industry ltd制)
……
5质量份
[0760]
光聚合引发剂(omnirad 907,igm resins b.v.公司制)
……
4质量份
[0761]
下述吡啶鎓盐(a)
……
2质量份
[0762]
下述聚合物(a)
……
0.2质量份
[0763]
下述聚合物(b)
……
0.1质量份
[0764]
下述聚合物(c)
……
0.1质量份
[0765]
甲基乙基酮
……
211质量份
[0766]
[化学式52]
[0767][0768]
聚合物a:下述结构的树脂
[0769]
[化学式53]
[0770]
[0771]
聚合物b:下述结构的树脂(在结构式中,a表示90,b表示10。)
[0772]
[化学式54]
[0773][0774]
聚合物c:下述结构的树脂
[0775]
[化学式55]
[0776][0777]
(7-2)光学各向异性层b的制作
[0778]
(光学各向异性层b的形成)
[0779]
按照与以上(光学各向异性层a的制作)相同的步骤,在酰化纤维素膜(t1)上形成取向膜,对取向膜连续实施了摩擦处理。此时,长条状的膜的长边方向与传送方向为平行,将膜长边方向(传送方向)与摩擦辊的旋转轴所成的角度设为102.5
°
(若将膜长边方向(传送方向)设为90
°
,从取向膜侧观察,以膜宽度方向为基准,将逆时针旋转方向由正值表示时,摩擦辊的旋转轴位于12.5
°
。)换言之,摩擦辊的旋转轴的位置符合以膜长边方向为基准,逆时针旋转102.5
°
的位置。)。
[0780]
将包含下述组成的盘状液晶化合物的光学各向异性层涂布液(b)用#2.8的线棒涂布机连续涂布于摩擦处理后的取向膜上。将膜的传送速度(v)设为26m/分钟。为了涂布液的溶剂的干燥及盘状液晶化合物的取向熟化,用60℃的热风加热60秒,之后,对所获得的涂膜以60℃进行uv照射,由此固定了盘状液晶化合物的取向。光学各向异性层b的厚度为0.8μm。确认到盘状液晶化合物的长轴相对于膜面的平均倾斜角为90
°
,盘状液晶化合物与膜面垂直地取向。并且,慢轴的角度与摩擦辊的旋转轴正交,若将膜长边方向设为90
°
(将膜宽度方向设为0
°
。从取向膜侧观察,以膜宽度方向为基准(0
°
),将逆时针方向用正值表示。),则慢轴的角度为102.5
°
(-77.5
°
)。所获得的光学各向异性层b符合λ/4板,re(550)为118nm,rth(550)为-59nm。
[0781]
(光学各向异性层涂布液(b)的组成)
[0782]
上述盘状液晶化合物(a)
……
80质量份
[0783]
上述盘状液晶化合物(b)
……
20质量份
[0784]
环氧乙烷改性三羟甲基丙烷丙烯酸酯(v#360、osaka organic chemical industry ltd制)
……
10质量份
[0785]
光聚合引发剂(omnirad 907,igm resins b.v.公司制)
……
5质量份
[0786]
上述吡啶鎓盐(a)
……
1质量份
[0787]
上述聚合物(a)
……
0.2质量份
[0788]
上述聚合物(b)
……
0.1质量份
[0789]
上述聚合物(c)
……
0.1质量份
[0790]
甲基乙基酮
……
348质量份
[0791]
(7-3)树脂膜的皂化处理
[0792]
将以上制作的树脂膜303a、304a、308a在2.3mol/l的氢氧化钠水溶液中,在55℃下浸渍了3分钟。在室温(25℃)的水洗浴槽中清洗,在30℃下用0.05mol/l的硫酸进行了中和。再次在室温的水洗浴槽中清洗,进一步用100℃的热风进行了干燥。
[0793]
(7-4)起偏器的制作
[0794]
将厚度80μm的聚乙烯醇(pva)膜在碘浓度0.05质量%的碘水溶液中,在30℃下浸渍60秒而进行染色,接着在硼酸浓度4质量%的硼酸水溶液中浸渍60秒期间,纵向拉伸至原来长度的5倍之后,在50℃下使其干燥4分钟,由此获得了厚度19μm的起偏器。
[0795]
用聚乙烯醇系粘合剂,将以上经皂化处理的树脂膜303a贴附于以上制作的起偏器的一面,由此制作了偏振片。
[0796]
(7-5)圆偏振片303d的制造
[0797]
在以上制作的偏振片中的起偏器(无树脂膜303a)侧,涂布粘结剂(sk-2057,soken chemical&engineering co.,ltd.制)来形成粘结剂层,并贴合了以上制作的酰化纤维素膜、取向膜及具有光学各向异性层a的膜,以使粘结剂层与光学各向异性层a密接。之后,剥离酰化纤维素膜及取向膜来获得了层叠体。接着,在所获得的层叠体中的光学各向异性层a上涂布粘结剂(sk-2057,soken chemical&engineering co.,ltd.制)来形成了粘结剂层。接着,使配置有粘结剂层的层叠体与以上制作的酰化纤维素膜、取向膜及具有光学各向异性层b的膜贴合,以使粘结剂层与光学各向异性层b密接。之后,剥离了酰化纤维素膜及取向膜。通过上述步骤,制作了依次配置有起偏器、光学各向异性层a(λ/2板)及光学各向异性层b(λ/4板)的圆偏振片303d。另外,若从起偏器侧观察,以起偏器的透过轴为基准(0
°
),将逆时针方向用正值表示,则λ/2板的慢轴的角度为-17.5
°
,λ/4板的慢轴的角度为-77.5
°
。即,光学各向异性层a(λ/2板)的慢轴与起偏器的透过轴所成的角度为17.5
°
,光学各向异性层a(λ/2板)的慢轴与光学各向异性层b(λ/4板)的慢轴所成的角度为60
°
。
[0798]
(7-6)有机电致发光显示装置303e、304e、308e的制造
[0799]
从市售的有机电致发光显示装置galaxy s5(商品名,samsung公司制)剥离带圆偏振片的触控面板,进一步从触控面板剥离圆偏振片,由此分别分离出了有机电致发光显示元件、触控面板及圆偏振片。接着,将分离出的触控面板与有机电致发光显示元件再次贴合,进一步以使空气不进入的方式在触控面板上贴合以上制作的圆偏振片303e,由此制作了有机电致发光显示装置。如表3所示,除了改变树脂膜的种类以外,以相同的方法制造了液晶显示装置304e、308e。
[0800]
[表6]
[0801]
有机电致发光显示装置no圆偏振片no树脂膜no图no303e303d303a图11304e304d304a图11308e308d308a图11
[0802]
相较于有机电致发光显示装置308e,包含本发明的紫外线吸收剂的有机电致发光显示装置303e及304e在长时间显示中,画质的变化也较少,因此优选。
[0803]
<试验例4>
[0804]
通过以下所示的方法,在基材膜上形成光学膜401a,制作了剥离性层叠膜401b。
[0805]
(1)涂布液的制备
[0806]
通过以下所示的组成制备了光学膜401a形成用涂布液1。用绝对过滤精度5μm的过滤器过滤了所获得的涂布液。
[0807]
(涂布液1的组成)
[0808]
as-70(丙烯腈/苯乙烯共聚树脂,nippon steel chemical&material co.,ltd.制)
……
100.0质量份
[0809]
byron 500(聚酯树脂,toyobo co.,ltd.制)
……
0.9质量份
[0810]
sma2000p(苯乙烯/马来酸共聚物,kawahara petrochemical co.,ltd)
……
4.2质量份
[0811]
表面活性剂1
……
0.1质量份
[0812]
紫外线吸收剂(化合物(1)-5)
……
3.1质量份
[0813]
紫外线吸收剂(比较化合物5)
……
0.0质量份
[0814]
乙酸甲酯
……
255.1质量份
[0815]
乙腈
……
229.6质量份
[0816]
乙醇
……
25.5质量份
[0817]
表面活性剂1:下述结构的化合物
[0818]
[化学式56]
[0819][0820]
用作紫外线吸收剂的化合物(1)-5及比较化合物5分别为上述结构的化合物。
[0821]
如下述表所示,除了改变化合物(1)-5及比较化合物5的添加量以外,以与涂布液1相同的方法制备了涂布液2~6。
[0822]
(2)剥离性层叠膜的涂设
[0823]
将市售的聚对苯二甲酸乙二酯膜(emblet s38,膜厚38μm,短波侧的吸收端波长310nm,unitika ltd制)用作基材膜,使用涂布液1~6,制作膜厚为5μm的光学膜401a~406a,由此获得了剥离性层叠膜(膜厚43μm,短波侧的吸收端波长310nm)。具体而言,通过使用了日本特开2006-122889号公报的实施例1中记载的狭缝模具的模涂法,以传送速度30m/分钟的条件在基材膜上涂布了涂布液1,并使其在105℃下干燥了30秒。之后,将其卷取。将所获得的剥离性层叠膜作为各实施例及比较例的剥离性层叠膜401b~406b。
[0824]
用分光光度计uv3600(shimadzu corporation制),分别测定了以上制作的剥离性层叠膜401b~406b的吸光度。并且,将在波长405nm处的吸光度除以紫外线吸收剂的添加量(相对于as-70的质量%)时的值是50以上设为a,25~50设为b,25以下设为c而评价了长波长的紫外线吸收能力。值越大,表示长波长的紫外线吸收能力越高。将结果示于下述表的长波长的紫外线吸收能力一栏。
[0825]
[表7]
[0826][0827]
相较于剥离性层叠膜404b~406b,剥离性层叠膜401b~403b在波长400nm附近的光的吸收更大,长波长侧的紫外线的吸收性优异。
[0828]
(3)偏振片的制作
[0829]
通过以下所示的方法制作了偏振片。
[0830]
(3-1)偏振片保护膜的皂化处理
[0831]
将60μm的三乙酰纤维素膜(fujitac tg60,fujifilm corporation制)在2.3mol/l的氢氧化钠水溶液中,在55℃下浸渍了3分钟。在室温(25℃)的水洗浴槽中清洗,在30℃下用0.05mol/l的硫酸进行了中和。再次在室温的水洗浴槽中清洗,进一步用100℃的热风进行了干燥。
[0832]
(3-2-1)偏振片4c1的制造
[0833]
使用上述60μm的三乙酰纤维素膜来代替树脂膜303a,除此以外,以与偏振片303b1相同的方法制作了偏振片4c1。
[0834]
(3-2-2)偏振片4c2的制造
[0835]
使用上述60μm的三乙酰纤维素膜来代替树脂膜303a,除此以外,以与偏振片303b2相同的方法制作了偏振片4c2。
[0836]
(3-3-1)带剥离性层叠膜的偏振片402d1的制造
[0837]
通过紫外线固化性粘合剂1,使剥离性层叠膜402的光学膜侧与偏振片4c-1的va相位差膜侧贴合之后,以200mj的强度照射紫外线,使紫外线固化性粘合剂1固化而作为带剥离性层叠膜的偏振片402d1。
[0838]
(3-3-2)带剥离性层叠膜的偏振片402d2的制造
[0839]
通过紫外线固化性粘合剂1,使剥离性层叠膜402的光学膜侧与偏振片4c-2的va相位差膜侧贴合之后,以200mj的强度照射紫外线,使紫外线固化性粘合剂1固化而作为带剥离性层叠膜的偏振片402d2。
[0840]
(3-4)液晶显示装置402e1、405e1、402e2、405e2的制造
[0841]
剥离偏振片402d1的emblet s38,使光学膜露出之后,取出市售的液晶显示装置flexscan 19英寸彩色液晶显示器s1923-hbk(商品名,eizo corporation制)的液晶面板,剥离前侧的偏振片,取而代之,通过粘结剂(sk-2057,soken chemical&engineering co.,ltd.制)贴附了偏振片402d1的光学膜侧。如此,制造了液晶显示装置402e1。如下述表所示,除了改变带剥离性层叠膜的偏振片的种类以外,以相同的方法制造了液晶显示装置405e1、402e2、405e2。
[0842]
[表8]
[0843]
液晶显示装置no带剥离性层叠膜的偏振片no偏振片no剥离性层叠膜no图no402e1402d14c1402a图5405e1405d14c1405a图5402e2402d24c2402a图5405e2405d24c2405a图5
[0844]
相较于液晶显示装置405e1及405e2,含有本发明的紫外线吸收剂的液晶显示装置402e1及402e2在长时间显示中,画质的变化也较少,因此优选。
[0845]
<试验例5>
[0846]
通过以下所示的方法制作了粘结剂501。
[0847]
(1)涂布液的制备
[0848]
(涂布液1的组成)
[0849]
丙烯酸树脂(sk dyne-sf2147)
……
100.0质量份
[0850]
聚合性化合物(td-75)
……
0.04质量份
[0851]
硅烷偶联剂(a-50)
……
0.06质量份
[0852]
紫外线吸收剂(化合物(1)-5)
……
0.2质量份
[0853]
紫外线吸收剂(比较化合物5)
……
0.0质量份
[0854]
以下示出所使用的材料。另外,用作紫外线吸收剂的化合物(1)-5及比较化合物5分别为上述结构的化合物。
[0855]
sk dyne-sf2147:丙烯酸酯共聚物。固体成分浓度10~20质量%%、乙酸乙酯、丙烯酸丁酯溶剂(soken chemical&engineering co.,ltd.)
[0856]
td-75:二异氰酸甲苯酯的三羟甲丙烷赋予物(soken chemical&engineering co.,ltd.)
[0857]
a-50:有机硅烷(soken chemical&engineering co.,ltd.)
[0858]
如下述表所示,除了改变化合物(1)-5及比较化合物5的添加量以外,以与涂布液1相同的方法制备了涂布液2~6。
[0859]
(2)粘结剂片的制作
[0860]
在实施了脱模处理的聚对苯二甲酸乙二酯膜(fujimori kogyo co.,ltd.制,mastack as3-310,以下简称为隔膜。)的脱模处理面,用敷贴器将上述涂布液1~6涂布至干燥后的厚度成为35μm,并使其在110℃下干燥3分钟。之后贴合隔膜的脱模处理面,在温度25℃、湿度60%下调湿24小时,由此制作了粘结剂片501a~506a。
[0861]
(3)玻璃贴合粘结剂的制作
[0862]
将粘结剂片501a~506a的隔膜剥离而贴合于厚度1.1mm的eagle玻璃上,由此制作了玻璃贴合粘结剂501b~506b。用分光光度计uv3600(shimadzu corporation制),分别测定了以上制作的玻璃贴合粘结剂501b~506b的吸光度。并且,将在波长405nm处的吸光度除以紫外线吸收剂的添加量(相对于sk dyne-sf2147的质量%)时的值是50以上设为a,25~50设为b,25以下设为c而评价了长波长的紫外线吸收能力。值越大,表示长波长的紫外线吸收能力越高。将结果示于下述表的长波长的紫外线吸收能力一栏。
[0863]
[表9]
[0864][0865]
相较于剥离性层叠膜504b~506b,剥离性层叠膜501b~503b在波长400nm附近的光的吸收更大,长波长侧的紫外线的吸收性优异。
[0866]
(4)液晶显示装置502c1、505c1、502c2、505c2的制造
[0867]
取出市售的液晶显示装置flexscan 19英寸彩色液晶显示器s1923-hbk(商品名,eizo corporation制)的液晶面板,剥离背光侧的偏振片,取而代之,通过粘结剂片502a贴附了偏振片4c1的va相位差膜侧。如此,制造了液晶显示装置502c1。并且,除了改变粘结剂片的种类及偏振片的种类以外,以相同的方法制造了液晶显示装置505c1、502c2、505c2。
[0868]
[表10]
[0869]
液晶显示装置no偏振片no粘结剂片no图no502c14c1502a图8505c14c1505a图8502c24c2502a图8505c24c2505a图8
[0870]
相较于液晶显示装置505c1及505c2,含有本发明的紫外线吸收剂的液晶显示装置502c1及502c2在长时间显示中,画质的变化也较少,因此优选。
[0871]
符号说明
[0872]
1~10-液晶显示装置,11~13-有机电致发光显示装置,22、49、176-含有本发明的紫外线吸收剂的偏振片保护膜,56、75-含有本发明的紫外线吸收剂的内保护膜(相位差膜),88、107、206-含有本发明的紫外线吸收剂的光学部件(光学膜),121、138、194-含有本发明的紫外线吸收剂的粘结剂或粘合剂,145、174-含有本发明的紫外线吸收剂的功能性层,21、35、36、50、51、65、66、80、81、97、98、114、115、129、130、144、159、160、175、186、197-功能性层,23、25、27、29、31、33、38、40、42、44、46、48、53、55、57、59、61、63、68、70、72、74、76、78、83、85、87、89、91、93、95、100、102、104、106、108、110、112、117、119、123、125、127、132、134、136、140、142、147、149、151、153、155、157、162、164、166、168、170、172、177、179、181、183、188、190、192、199、201、203、205、207-粘合剂或粘结剂,24、32、39、47、54、62、69、77、84、94、101、111、118、126、133、141、148、156、163、171、178、189、200-起偏器,26、30、41、45、56、60、71、75、86、92、103、109、120、124、135、139、150、154、165、169-相位差膜,28、43、58、73、90、105、122、137、152、167-液晶单元,34、37、52、64、67、79、82、96、99、113、116、128、
131、143、146、158、161、173、187、198-偏振片保护膜,180、191、202-2/λ板,182、193、204-4/λ板,184、195、208-触控面板,185、196、209-有机电致发光元件。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1