检测环状RNA和/或所述环状RNA表达量的制剂在制备结直肠癌诊断试剂中的应用
检测环状rna和/或所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用
技术领域
1.本发明属于分子标志物技术领域,具体涉及检测环状rna和/或所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用。
背景技术:
2.结直肠癌(colorectal cancer,crc)是常见的消化系统恶性肿瘤,其死亡率位居世界疾病死亡率排行第四位,每年有90万人死于该病。crc发病率预期到2030年将增加160%,预计每年新增病例210万人次,给卫生系统以及整个社会带来严重的经济负担。早发现早治疗是提高结直肠癌治愈率的最佳途径,现有的肿瘤标志物cea、ca19-9在结直肠癌诊断中的敏感度与特异性不够高;同时,尽管现有技术中也存在以环状rna为检测标志物的相关研究,但是并未见hsa_circ_0071106和hsa_circ_0000825在结直肠癌研究中的相关报道,因而,增加结直肠癌的检测标志物,丰富结直肠癌筛查的途径对结直肠癌的预防和治疗具有重要的意义。
技术实现要素:
3.基于上述技术问题,本发明的目的在于提供检测环状rna和/或所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用,检测环状rna和/或所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用。
4.为了实现上述目的,本发明提供了环状rna和/或检测所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用,所述环状rna包括hsa_circ_0071106和/或hsa_circ_0000825;
5.所述hsa_circ_0071106的核苷酸序列如seq id no.1所示;
6.所述hsa_circ_0000825的核苷酸序列如seq id no.2所示。
7.本发明提供了一种结直肠癌的诊断试剂,包括针对环状rna hsa_circ_0071106和/或hsa_circ_0000825设计的特异性引物;
8.所述hsa_circ_0071106的特异性引物为p1和p2;所述hsa_circ_0000825的特异性引物为p3和p4;
9.所述p1的核苷酸序列如seq id no.3所示,所述p2的核苷酸序列如seq id no.4所示,所述p3的核苷酸序列如seq id no.5所示,所述p4的核苷酸序列如seq id no.6所示。
10.优选的,所述诊断试剂还包括管家基因gapdh。
11.优选的,所述管家基因gapdh的特异性引物包括p5和p6;
12.所述p5的核苷酸序列如seq id no.7所示,所述p6的核苷酸序列如seq id no.8所示。
13.本发明还提供了一种结直肠癌的诊断试剂盒,所述试剂盒包括上述技术方案中所述的诊断试剂。
14.本发明还提供了环状rna和/或检测所述环状rna表达量的制剂在制备判断结直肠癌治疗效果的试剂中的应用,所述环状rna包括hsa_circ_0071106和/或hsa_circ_0000825;
15.所述hsa_circ_0071106的核苷酸序列如seq id no.1所示;
16.所述hsa_circ_0000825的核苷酸序列如seq id no.2所示。
17.本发明还提供了一种判断结直肠癌治疗效果的试剂,所述试剂包括针对环状rnahsa_circ_0071106和/或hsa_circ_0000825设计的特异性引物;
18.所述hsa_circ_0071106的特异性引物为p1和p2;所述hsa_circ_0000825的特异性引物为p3和p4;
19.所述p1的核苷酸序列如seq id no.3所示,所述p2的核苷酸序列如seq id no.4所示,所述p3的核苷酸序列如seq id no.5所示,所述p4的核苷酸序列如seq id no.6所示。
20.有益效果:
21.本发明提供了检测环状rna和/或所述环状rna表达量的制剂在制备结直肠癌辅助诊断试剂中的应用,以所述环状rna hsa_circ_0071106和/或hsa_circ_0000825作为一种新的结直肠癌检测分子标志物,所述标志物在结直肠癌患者癌组织中特异性下调表达,尤其将所述环状rna hsa_circ_0071106和hsa_circ_0000825联合使用,可以更准确地对结直肠癌样本进行筛查;利用该分子标志物可以简单、快捷地进行结直肠癌诊断,成为结直肠癌检测诊断、病理分级、临床分期、治疗疗效判断的有效工具,具有良好的临床应用前景。
22.同时,本发明采用实时定量pcr测定所述环状rna hsa_circ_0071106和/或hsa_circ_0000825的表达量,荧光染料不需要另行设计探针即可同时检测目的环状rna和管家基因,经济、方便,对进一步研究结直肠癌相关环状rna的生物学机制具有重要意义。
附图说明
23.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍。
24.图1为正常组织和结直肠癌组织中hsa_circ_0071106和gapdh的荧光信号曲线图;
25.图2为正常组织和结直肠癌组织中hsa_circ_0000825和gapdh的荧光信号曲线图;
26.图3为荧光定量rt-pcr验证结直肠癌组织异常表达的circ rna,其中hsa_circ_0071106的表达在扩大标本验证实验中显著下调(p《0.001);
27.图4为荧光定量rt-pcr验证结直肠癌组织异常表达的circ rna,其中hsa_circ_0000825的表达在扩大标本验证实验中显著下调(p《0.001);
28.图5为检测81例结直肠癌患者癌组织及其癌旁组织hsa_circ_0071106水平,而制作的roc曲线。
29.图6为检测81例结直肠癌患者癌组织及其癌旁组织hsa_circ_0000825水平,而制作的roc曲线。
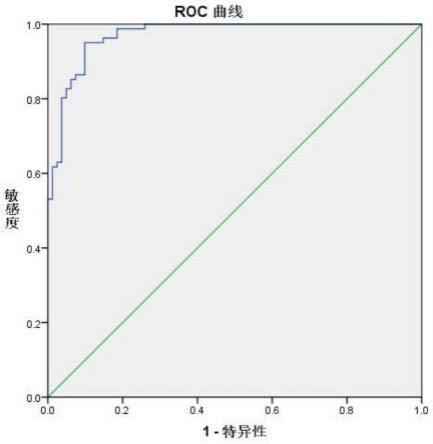
30.图7为检测81例结直肠癌患者癌组织及其癌旁组织hsa_circ_0071106和hsa_circ_0000825水平,而制作的roc曲线。
具体实施方式
31.本发明提供了环状rna和/或检测所述环状rna表达量的制剂在制备结直肠癌诊断试剂中的应用,所述环状rna包括hsa_circ_0071106和/或hsa_circ_0000825;所述hsa_circ_0071106的核苷酸序列如seq id no.1所示;所述hsa_circ_0000825的核苷酸序列如seq id no.2所示。
32.本发明所述环状rna hsa_circ_0071106在基因组上的定位为:chr4:148778703-148803083,相应的线性基因为arhgap10(nm_024605.4),所述环状rna的核苷酸序列如seq id no.1所示:5
’‑
gaagaaaaaaagaagtttgacaaagagacagaaaagaattatagtctaattgataaacatttgaatttatcagcaaaaaagaaagactcacatttacaagaggcagatatccaagtagagcagaaccggcaacacttctatgaactgtctctcgagtatgtgtgtaagctgcaggaaatccaagaaagaaagaagtttgagtttgtggaacctatgctgtcattttttcaggggatgtttaccttctatcatcagggccatgaacttgccaaagacttcaatcactacaaaatggaactacagatcaacattcagaatacacggaatcgatttgaaggaacaaggtcagaagtggaagagctcatgaacaaaatcagacagaatcccaaggaccacaaacgagcaagtcagtttacagccgaaggctacctgtatgtccaggaaaaaaggcctgctccgtttggttccagttgggtcaaacactattgcatgtatcgaaaagcagcaaagaagttcaacatgatcccatttgagcacagatctggagggaaacttggggacggagaggtgttctttttgaaagaatgtaccaagaggcatactgactccattgacagaaggttttgttttgacatagaagctgctgatcg-3’。
33.本发明所述环状rna hsa_circ_0000825在基因组上的定位为:chr18:8718421-8720494,相应的线性基因为ccdc165(nm_001378205.1),所述环状rna的核苷酸序列如seq id no.2所示:5
’‑
gatgagttagatgaactccgtgctgagatggaagagatgagagacagttatttagaggaagatgtttaccagctgcaggaacttcggcgagaactggaccgcgctaataaaaactgccgaatcctgcagtaccgtcttcggaaagccgagcagaaaagcctgaaagtggctgagacgggtcaggtggatggtgagcttattcgaagcctggagcaggacttgaaggtagccaaagatgtatctgtcagattgcaccacgaacttaagacggtggaggaaaagcgcgctaaagctgaggatgaaaacgaaactctccgacagcagatgattgaagtggaaatatccaaacaggccctccagaatgagctggagagactgaaagag-3’。
34.本发明所述环状rna hsa_circ_0071106、hsa_circ_0000825以及所述rna hsa_circ_0071106和hsa_circ_0000825的组合在结直肠癌患者的肿瘤组织中,特异性表达下调,可作为结直肠癌诊断的新型分子标志物。
35.本发明提供了一种结直肠癌的诊断试剂,包括针对环状rna hsa_circ_0071106和/或hsa_circ_0000825设计的特异性引物;所述hsa_circ_0071106的特异性引物为p1和p2;所述hsa_circ_0000825的特异性引物为p3和p4;所述p1的核苷酸序列如seq id no.3所示:5
’‑
aggcatactgactccattgaca-3’;所述p2的核苷酸序列如seq id no.4所示:5
’‑
ttttcttccgatcagcagct-3’;所述p3的核苷酸序列如seq id no.5所示:5
’‑
agaatgagctggagagactga-3’;所述p4的核苷酸序列如seq id no.6所示:5
’‑
ctcttccatctcagcacgga-3’。本发明所述hsa_circ_0071106的特异性引物为p1和p2和/或所述hsa_circ_0000825的特异性引物优选还用于检测所述环状rna的表达量。本发明所述诊断试剂中优选还包括管家基因gapdh,所述gapdh的特异性引物优选包括p5和p6,所述p5的核苷酸序列优选如seq id no.7所示:5
’‑
ggtctcctctgacttcaaca-3’;所述p6的核苷酸序列优选如seq id no.8所示:5
’‑
gtgagggtctctctcttcct-3’。
36.本发明还提供了一种结直肠癌的诊断试剂盒,所述试剂盒包括上述技术方案中所
述的诊断试剂。本发明所述诊断试剂盒中优选还包括2
×
quantinova sybr green pcr master mix。
37.本发明还提供了利用上述诊断试剂或诊断试剂盒进行结直肠癌辅助诊断的方法,所述方法包括荧光定量pcr。通过所述荧光定量pcr过程中的目的基因和管家基因的ct值,通过管家基因gapdh的表达水平来均一化circrna的水平,计算得到组织中hsa_circ_0071106以及hsa_circ_0000825的相对表达水平,并使用2
δct
公式来计算hsa_circ_0071106以及hsa_circ_0000825的pcr相对定量值,式中δ
ct1
=ct hsa_circ_0071106-ct gapdh,δ
ct2
=ct hsa_circ_0000825-ct gapdh。当样本中的hsa_circ_0071106生物标志物的pcr相对定量值δ
ct1
小于或等于6.84时,则认为是非结直肠癌样本;大于6.84时,则认为是结直肠癌样本。当样本中的hsa_circ_0000825生物标志物的pcr相对定量值δ
ct2
小于或等于7.51时,则认为是非结直肠癌样本;大于7.51时,则认为是结直肠癌样本。
38.本发明所述荧光定量pcr的体系以20μl计,优选包括2
×
quantinova sybr green pcr master mix 12μl、模板1μl、引物各1.4μl和ddh2o 4.2μl。本发明所述模板优选为结直肠正常组织或结直肠癌患者的肿瘤组织提取得到的rna经反转录后获得的cdna。本发明对所述rna的提取方法并没有特殊限定,利用本领域的常规试剂盒法提取即可。
39.本发明所述荧光定量pcr的程序优选包括:95℃预变性2min;95℃变性5s,60℃退火30s,40个循环;95℃酶变性15s;60℃退火1min;4℃保温。
40.本发明上述荧光定量pcr除用以诊断是否患有结直肠癌外,还可以用于对结直肠癌患者进行病理分级和临床分期,且具体的方法优选与上述荧光定量pcr方法相同,在此不再赘述。
41.本发明还提供了环状rna和/或检测所述环状rna表达量的制剂在制备判断结直肠癌治疗效果的试剂中的应用,所述环状rna包括hsa_circ_0071106和/或hsa_circ_0000825;所述hsa_circ_0071106的核苷酸序列如seq id no.1所示;所述hsa_circ_0000825的核苷酸序列如seq id no.2所示。本发明所述应用优选与上述相同,在此不再赘述。
42.本发明还提供了一种判断结直肠癌治疗效果的试剂,所述试剂包括针对环状rna hsa_circ_0071106和/或hsa_circ_0000825设计的特异性引物;所述hsa_circ_0071106的特异性引物为p1和p2;所述hsa_circ_0000825的特异性引物为p3和p4;所述p1的核苷酸序列如seq id no.3所示,所述p2的核苷酸序列如seq id no.4所示,所述p3的核苷酸序列如seq id no.5所示,所述p4的核苷酸序列如seq id no.6所示。本发明所述试剂优选与上述相同,在此不再赘述。
43.为了进一步说明本发明,下面结合附图和实施例对本发明提供的技术方案进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
44.实施例1
45.分别检测hsa_circ_0071106和hsa_circ_0000825在结直肠癌组织和正常结直肠组织中的表达情况
46.1、芯片分析:采用上海康成生物公司arraystar human circ rna array(6
×
7k)芯片检测结直肠癌组织和正常组织中circ rna的水平。
47.2、芯片结果:hsa_circ_0071106在结直肠癌组织和正常组织中表达量差异达8.73
倍,hsa_circ_0000825在结直肠癌组织和正常组织中的差异达8.37倍,提示hsa_circ_0071106和hsa_circ_0000825在结直肠癌中可能作为抑癌基因发挥作用。
48.实施例2
49.采集正常结直肠组织作为正常对照组,按照如下步骤进行环状rna的检测,包括以下步骤:
50.a.收集组织:结直肠癌组织和正常结直肠组织分别收集在加入了rna保存液的无菌冻存管中,不及时使用时存放在-80℃超低温冰箱中;
51.b.释放rna:称取约20mg组织放置于2ml离心管中,置于冰上加入1ml trizol。使用手持式自动匀浆机将组织充分匀浆至无固体,室温静置10min,使组织中的rna充分释放至溶液中;
52.c.氯仿提取:加入0.2ml三氯甲烷,涡旋震荡混匀,室温静置10min;4℃下,13000rpm离心10min,此时液体分层,其中上层水相中富集了rna,小心吸取上层水相至1.5ml rnase-free离心管中;
53.d.异丙醇沉淀:加入等体积异丙醇,涡旋震荡混匀,4℃下静置30min,12000rpm在4℃下离心10min,弃上清;
54.e.乙醇洗涤:加入1ml 75%的乙醇,混匀,12000rpm在4℃下离心5min,弃上清,弃尽上清,采取先倾倒,再用移液枪吸取,最后放置干燥的方法,最后加入适量rnase-free水溶解沉淀,即为组织中总rna提取液,-80℃保存备用,经检测od
260
/od
280
比值均在1.8到2.0之间,且浓度为516~1213g/ul;
55.f.rna逆转录:使用逆转录试剂盒对上述步骤e提取出的rna进行逆转录,得到cdna,保存于-20℃备用;
56.g.荧光染料法实时定量pcr检测:将上述步骤f获得的cdna配制反应体系,进行荧光定量pcr。
57.20μl荧光定量pcr体系:2
×
quantinova sybr green pcr mastermix 12μl、模板1μl、引物各1.4μl和ddh2o 4.2μl。
58.程序:95℃预变性2min;95℃变性5s,60℃退火30s,40个循环;95℃酶变性15s;60℃退火1min;4℃保温。
59.结果如图1所示,正常组织和结直肠癌组织中hsa_circ_0071106和gapdh均得到有效扩增。由公式δ
ct1
=ct hsa_circ_0071106-ct gapdh可得出正常组织的δ
ct1
=4.06;结直肠癌组织的δ
ct
=8.37,明显大于正常组织的δ
ct1
值,说明结直肠癌组织中hsa_circ_0071106表达量低于正常结直肠组织中的表达量,与基因芯片的结果应该是一致的。
60.结果如图2所示,正常组织和结直肠癌组织中hsa_circ_0000825和gapdh均得到有效扩增。由公式δ
ct2
=ct hsa_circ_0000825-ct gapdh可得出正常组织的δ
ct2
=5.34;结直肠癌组织的δ
ct
=9.38,明显大于正常组织的δ
ct2
值,说明结直肠癌组织中hsa_circ_0000825表达量低于正常结直肠组织中的表达量,与基因芯片的结果应该是一致的。
61.实施例3
62.应用hsa_circ_0071106以及hsa_circ_0000825生物标志物进行结直肠癌检测
63.1、收集组织样本;
64.2、结直肠癌组织中环状rna的提取(提取方法如同实施例2);
65.3、反转录和荧光定量pcr反应如同按照实施例2中的“反转录和荧光定量反应”进行操作;
66.4、以hsa_circ_0071106以及hsa_circ_0000825作为结直肠癌检测的生物标志物,分别分析81例结直肠癌患者癌组织与其癌旁组织中hsa_circ_0071106以及hsa_circ_0000825的表达水平。结直肠癌患者组hsa_circ_0071106以及hsa_circ_0000825的δ
ct
明显高于正常组,p《0.01,证明其hsa_circ_0071106以及hsa_circ_0000825的表达水平明显低于正常组,如图3所示。hsa_circ_0071106作为结直肠癌标志物的截断值为6.84,当样本中的hsa_circ_0071106生物标志物的pcr相对定量值δ
ct
小于或等于6.84时,则认为是非结直肠癌样本;大于6.84时,则认为是结直肠癌样本,如图4所示。hsa_circ_0000825作为结直肠癌标志物的截断值为7.51,当样本中的hsa_circ_0000825生物标志物的pcr相对定量值δ
ct
小于或等于7.51时,则认为是非结直肠癌样本;大于7.51时,则认为是结直肠癌样本。
67.检测81例结直肠癌患者结直肠癌组织及其癌旁组织hsa_circ_0071106水平,制作roc曲线,如图5所示,auc值为0.788,p《0.001。表1为hsa_circ_0071106为生物标志物进行结直肠癌诊断的结果,可得出hsa_circ_0071106作为结直肠癌标记物的灵敏度为64.2%,特异度为96.3%。
68.检测81例结直肠癌患者结直肠癌组织及其癌旁组织hsa_circ_0000825水平,制作roc曲线,如图6所示,auc值为0.963,p《0.001。表1为hsa_circ_0000825为生物标志物进行结直肠癌诊断的结果,可得出hsa_circ_0000825作为结直肠癌标记物的灵敏度为96.3%,特异度为87.7%。
69.联合检测81例结直肠癌患者结直肠癌组织及其癌旁组织hsa_circ_0071106和hsa_circ_0000825水平,制作roc曲线,如图7所示,auc值为0.970,p《0.001。表1为hsa_circ_0071106和hsa_circ_0000825为生物标志物进行结直肠癌联合诊断的结果,可得出hsa_circ_0071106和hsa_circ_0000825作为结直肠癌标记物的灵敏度为95.1%,特异度为90.1%。
70.表1 hsa_circ_0071106和/或hsa_circ_0000825为生物标志物进行结直肠癌诊断的结果
[0071][0072]
本发明roc曲线采用spss绘制得到,并直接获得表1中的灵敏度和特异度;所述约登指数=灵敏度+特异度-1,约登指数表示表示筛检方法发现真正的患者与非患者的总能力。指数越大说明筛查实验的效果越好,真实性越大。
[0073]
由上述实施例可以得出,以所述环状rna hsa_circ_0071106和/或hsa_circ_0000825作为一种新的结直肠癌检测分子标志物,所述标志物在结直肠癌患者癌组织中特异性下调表达,尤其将所述环状rna hsa_circ_0071106和hsa_circ_0000825联合使用,可以更准确地对结直肠癌样本进行筛查。
[0074]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1